Аденома гипофиза при беременности | Первый Медицинский Центр Тель-Авива
Аденома гипофиза и беременность сочетаются редко, патология часто сопровождается бесплодием. Лечение назначают с осторожностью, лишь при угрозе здоровью и жизни матери или плода. В Израиле при аденоме гипофиза у беременных применяют щадящую хирургию, медикаментозную терапию.
Причины аденомы гипофиза у беременных неизвестны. В норме у женщин, вынашивающих ребенка, орган увеличивается на 30%. Своего максимума его размеры достигают сразу после родов. Большинство врачей сходится во мнении, что аденома не связана с физиологической гипертрофией. Скорее всего, бессимптомная опухоль манифестирует в этот период.
Аденомы встречаются у 0,93 людей репродуктивного возраста на 100 000 населения. Женщин в группе в 4 раза больше, чем мужчин. Гормональные сбои часто ведут к бесплодию, что еще больше снижает количество пациенток среди беременных.
Симптомы заболевания
Симптомы зависят от типа и размеров новообразования. Чаще всего яркие проявления имеет крупная опухоль, которая сдавливает соседние структуры. Больные жалуются на головную боль, сужение поля зрения. Беременность при клинически выраженной аденоме гипофиза может заканчиваться выкидышем.
Чаще всего яркие проявления имеет крупная опухоль, которая сдавливает соседние структуры. Больные жалуются на головную боль, сужение поля зрения. Беременность при клинически выраженной аденоме гипофиза может заканчиваться выкидышем.
Макроаденома иногда становится причиной гипопитуитризма – уменьшения синтеза гормонов гипофизом. При таком состоянии возникают проблемы с зачатием, развиваются симптомы гипотиреоза (отеки, снижение температуры, быстрая утомляемость, избыток массы). Недостаток остальных гормонов не так заметен, их синтез компенсируется за счет увеличения гипофиза и активности плаценты.
Опухоль может продуцировать различные гормоны или подавлять их выработку. Чаще всего она развивается из одного вида клеток и обладает определенным типом активности.
ПролактиномаАктивная пролактинома часто диагностируется до беременности. Повышенная продукция гормона негативно влияет на овуляцию, менструальное кровотечение, что делает женщину бесплодной.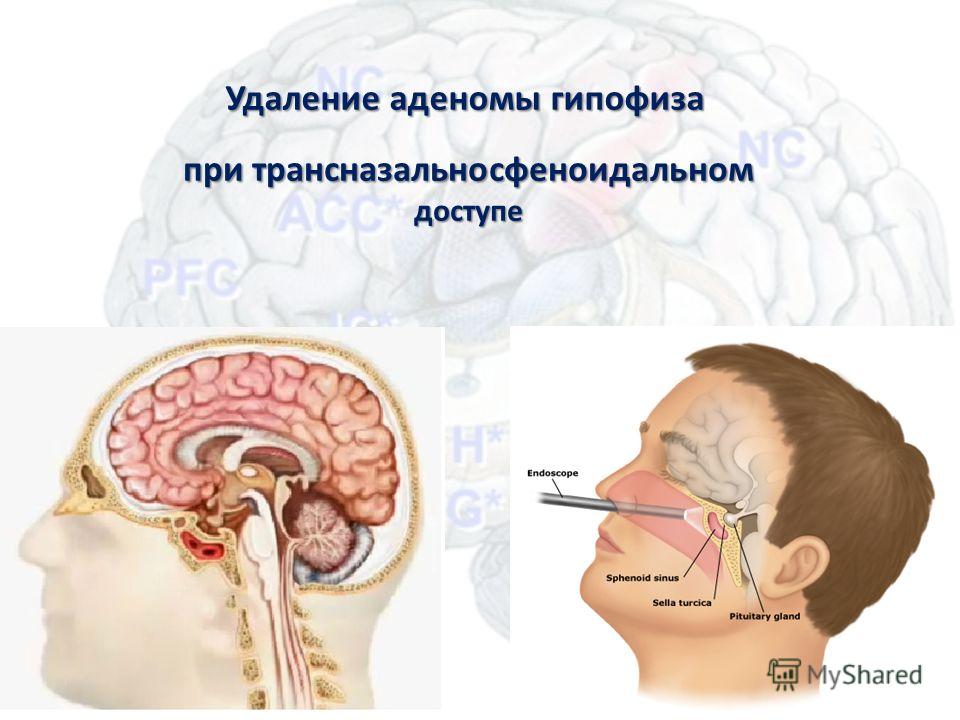 Лечение антагонистами допамина позволяет в 90% случаев возобновить репродуктивную функцию.
Лечение антагонистами допамина позволяет в 90% случаев возобновить репродуктивную функцию.
Микроаденомы, продуцирующие пролактин, носят доброкачественный характер и у будущей мамы никак себя не проявляет. Риск увеличения опухоли составляет 1,3% после приема препаратов, 23,2% при нелеченной форме, и 2,8% после радиотерапии.
СоматотропиномаЕсли опухоль не была диагностирована раньше, ее тяжело выявить во время беременности. У женщин, вынашивающих ребенка, есть легкие признаки акромегалии (укрупнение черт лица, гиперпигментация, повышение сахара в крови, боли в спине, утомляемость, гирсутизм).
При больших размерах опухоль сдавливает соседние структуры и провоцирует головную боль, нарушения зрения. Ярко выраженная акромегалия тоже становится сигналом о возможном наличии заболевания.
КортикотропиномаЗаболевание носит название болезнь Кушинга. Его бывает трудно отличить от синдрома Кушинга, вызванного гиперпродукцией адренокортикоидов в надпочечниках. При физиологической беременности АКТГ также повышается, что вызывает увеличение массы, отеки, повышение давления и сахара в крови, уменьшение толерантности к глюкозе, растяжки на животе и бедрах.
При физиологической беременности АКТГ также повышается, что вызывает увеличение массы, отеки, повышение давления и сахара в крови, уменьшение толерантности к глюкозе, растяжки на животе и бедрах.
Подозрение на аденому гипофиза у беременных появляются при устойчивой гипертензии, гипергликемии, мышечной слабости. Стрии при патологии красные или фиолетовые, а не белые, как у здоровых женщин. Истончение и сальность кожных покровов, акне, гирсутизм говорят о повышении уровня тестостерона.
Увеличение выработки АКТГ несет опасность для матери и плода. Приблизительно 25% беременностей заканчиваются выкидышами или мертворождением. Отслоение плаценты на разных сроках наблюдается в 60% случаев. У 87% пациенток есть гипертензия, у 61% — признаки диабета, у 16% — преэклампсия.
ТиреотропиномаТакая форма недуга встречается крайне редко. У пациенток отмечают резкое похудение, повышение давления, иногда температуры, тремор рук, перепады настроения. Часто беременность заканчивается выкидышами. После благополучного родоразрешения не все матери могут кормить ребенка.
После благополучного родоразрешения не все матери могут кормить ребенка.
Диагностика опухоли
Для диагностики аденомы гипофиза применяют две группы методов:
- Инструментальные (КТ, МРТ, рентгенография)
- Лабораторные (определение уровня гормонов)
При беременности информативность и возможность проведения обследований ограничена. Рентгенография противопоказана, их вред значительно превосходит пользу. КТ проводят в крайних случаях. МРТ показана при аденоме гипофиза с яркими симптомами, но гадолиний при этом не используют.
В ходе лабораторной диагностики определяют следующие гормоны:
- Пролактин. Природное повышение уровня гормона начинается с 5-8 недели. Поэтому тест на его определение не информативный.
- Соматотропин. Этот гормон продуцируется как гипофизом, так и плацентой. Важное значение имеет определение соматотропина в динамике. Гипофиз выделяет его порциями, а плацента постоянно. Поэтому при аденоме повышение уровня будет пульсирующим.

- АКТГ во время беременности частично продуцируется плацентой, его уровень всегда повышен. Косвенным подтверждением болезни Кушинга может служить отсутствие суточных колебаний кортизола при его определении в крови или моче.
Лечение заболевания
Лечение аденомы гипофиза бывает консервативным и хирургическим. Радиотерапия гамма-нож при беременности не используются, из-за негативного влияния на плод. Часть женщин начинают терапию еще до зачатия, в связи с бесплодием. Микроаденома и беременность могут протекать без нарушений и поэтому коррекции не требуют.
Консервативная терапияКонсервативная терапия аденомы гипофиза направлена на коррекцию уровня гормонов и приостановку роста новообразования. При выборе препаратов учитывают гормональную активность опухоли, стараются обеспечить максимальную безопасность для плода.
У пациенток с пролактиномой применяют агонисты дофамина – бромокриптин или карбеголин. При соматотропиноме и кортикотропиноме показано только симптоматическое лечение. Пациенткам с гиперпродукцией тиреотропного гормона в первом триместре назначают пропилтиоурацил, а во втором и третьем – метимазол. Эти препараты подавляют синтез ТТГ в гипофизе.
Пациенткам с гиперпродукцией тиреотропного гормона в первом триместре назначают пропилтиоурацил, а во втором и третьем – метимазол. Эти препараты подавляют синтез ТТГ в гипофизе.
При гипопитуитризме корректируют заместительную терапию, в соответствии с уровнем гормонов. В первую очередь это касается тироксина при гипотиреозе. Если пациентки до беременности принимали гонадотропин или эстрогены, их отменяют. Применение глюкокортикоидов остается спорным, так как нет доказательств об их безопасности для плода.
Хирургическое лечениеПри аденоме гипофиза у беременных проводят транссфеноидальную резекцию. При этой процедуре все инструменты вводятся через ноздри. Она позволяет удалить опухоль с минимальным влиянием на здоровье беременной и плода.
Операция показана только при макроаденоме с явными клиническими симптомами. У пациенток с болезнью Кушинга она проводится на любом сроке, опасной для жизни матери и плода. Во всех других случаях лечение откладывают до рождения ребенка.
Аденома гипофиза при беременности – нечастое заболевание. Но в Первом Медицинском центре Тель-Авива есть опыт его лечения. Врачи постоянно следят за научными исследованиями и публикациями.
При всех назначениях медики стараются действовать максимально осторожно, чтобы не навредить матери и будущему ребенку. Во многих случаях предпочитают наблюдать за пациентками и начинать терапию только в тяжелых случаях.
Проходя лечение аденомы гипофиза в Израиле, вы получите ряд преимуществ:
- Опытный персонал
- Качественную диагностику на современном оборудовании
- Безопасные и эффективные схемы лечения
- Комфортные условия пребывания в стационаре
- Разумные цены
Лечением аденомы гипофиза занимаются врачи хирурги и эндокринологи. Обследование и терапия беременных женщин всегда идет под контролем акушера-гинеколога. При необходимости подключаются смежные специалисты. Выбрать доктора вам поможет координатор, он будет сопровождать на всех этапах пребывания в клинике.
Выбрать доктора вам поможет координатор, он будет сопровождать на всех этапах пребывания в клинике.
беременность при аденоме гипофиза — 25 рекомендаций на Babyblog.ru
Щитовидка — это главный производитель гормонов, которые влияют на все процессы в нашем организме: на вес, настроение, работоспособность, самочувствие и т. д. При этом, по наблюдениям врачей, люди склонны забывать о щитовидной железе, а симптомы, которые указывают на проблемы именно в этом органе, списывать на усталость, наследственность или другие заболевания, теряя при этом драгоценное время и усугубляя последствия.
Нарушениями в работе «щитовидки» страдает до трети населения планеты, при этом большую часть заболеваний этого органа можно предотвратить и вылечить — если вовремя диагностировать и начать лечение.
Щитовидная железа находится в средней трети шеи между кадыком и грудиной и имеет форму бабочки.
Первые симптомы
Регулярно делайте как минимум визуальный осмотр щитовидной железы — в идеале её не должно быть видно вообще.
О проблемах с этим органом могут говорить разные симптомы, например быстрое, в течение короткого периода времени, похудание или, наоборот, резкий набор веса при обычном питании.
Также стоит обратить внимание на потливость, дрожание пальцев рук, увеличение глазных яблок (пучеглазие), раздражительность, плаксивость — это симптомы гипертиреоза, повышенной функции щитовидной железы. Если вы заметили эти признаки, не откладывайте визит к врачу — как и в случае с гипотиреозом.
Гипертиреоз
Гипертиреоз — распространённое гормональное заболевание, вызванное повышением функции щитовидной железы. Она переходит в состояние чрезмерной активности, увеличивается в размерах и вырабатывает большое количество тиреоидных гормонов (Т3 — трийодтиронина и Т4 — тироксина), отравляющих организм. Другое название этого состояния — тиреотоксикоз.
Гипертиреоз является одним из главных проявлений диффузного токсического зоба, тиреотоксической аденомы, отдельных форм аутоиммунного тиреоидита.
Основные симптомы гипертиреоза — учащённое сердцебиение, повышенная потливость, постоянная нервозность, раздражительность, тревожность. Также наблюдаются частая смена настроения, плаксивость, быстрая утомляемость, общая слабость, подавленность, плохой сон. Возможны повышение температуры, непереносимость громких звуков и яркого света, сухость кожи, дрожание рук (тремор).
20 — 50 лет — возраст, когда гипертиреоз возникает чаще всего, при этом гипертиреоз встречается у женщин почти в 10 раз чаще, чем у мужчин. Виной тому — гормональные колебания, которые происходят в критические дни, во время беременности, при менопаузе. Специалисты рекомендуют женщинам регулярно бывать у эндокринолога и делать УЗИ щитовидной железы.
до 30 лет — раз в пять лет,
30 — 45 лет
после 45 лет — раз в год.
Особенно важна диагностика гипотиреоза у беременных женщин.
В 70-80% случаев развитие гипертиреоза происходит по причине диффузного токсического зоба — увеличения щитовидной железы в результате аутоиммунного нарушения.
Гипотиреоз
Гипотиреоз — это эндокринное заболевание, при котором щитовидная железа вырабатывает недостаточное количество гормонов — тироксина и трийодтиронина, что и приводит к замедлению обмена веществ в организме.
Медики различают первичный и вторичный гипотиреоз. При первичном снижение выработки гормонов связано с повреждением самой щитовидной железы в результате травм, лучевого воздействия, поражения инфекциями, атаки собственной иммунной системы. Также причиной может стать недостаточное поступление в организм йода. Поражение щитовидной железы является причиной 99% случаев гипотиреоза.
Оставшийся 1% приходится на вторичный гипотиреоз, он бывает следствием поражения гипофиза или гипоталамуса. Гипофиз — это железа, расположенная в основании головного мозга, она вырабатывает тиреотропный гормон (ТТГ), который регулирует работу щитовидной железы. А гипоталамус — это отдел промежуточного мозга, под контролем которого находятся и гипофиз, и щитовидная железа.
А гипоталамус — это отдел промежуточного мозга, под контролем которого находятся и гипофиз, и щитовидная железа.
Наиболее опасен гипотиреоз для маленьких детей, поскольку без своевременного лечения он грозит малышам многочисленными и необратимыми осложнениями. Если ребёнка с врождённым гипотиреозом не лечить до двух лет, потом даже хорошо проведённое лечение вряд ли предотвратит умственную отсталость. Согласно статистике, врождённый гипотиреоз встречается у 1-2 из 5000 новорождённых. Девочки страдают им в два раза чаще, чем мальчики.

Лечение гипотиреоза и гипертиреоза
Заболевание требует усиленное лечение уже на ранних стадиях, соблюдение диеты и режима дня, посещение врача, прием препаратов.
На сегодняшний дней одним из самых эффективным способов лечения считается прием препаратов на основе корня растения Лапчатка Белая, который содержит в себе огромное количество полезных веществ, и главное из них — альбинин.
На Российском рынке наиболее эффективным препаратом, в который входит экстракт корня Лапчатки Белой, считается Эндонорм. Однако, надо отметить, что Эндонорм оказывает наибольший фармакологический эффект на начальных стадиях заболеваний, а при запущенных формах рекомендован пожизненный прием тироксина (Эутирокса, Л-Тироксина). Именно поэтому, при появлении симптомов заболеваний важно своевременное обращение к эндокринологу.
Дети
У подростков нередко встречается зоб (увеличение размеров щитовидной железы) без нарушения выработки гормонов.
Аденома гипофиза:Патогенез аденомы гипофиза,Симптомы аденомы гипофиза,Диагностика аденомы гипофиза
Патогенез аденомы гипофиза
 Также есть концепция первичного поражения гипофиза, которое прямо влияет на развитие аденомы.
Также есть концепция первичного поражения гипофиза, которое прямо влияет на развитие аденомы.Большая часть аденом – опухоли, не имеющие морфологических признаков злокачественных. Тем не менее, они предрасположены к прорастанию и дальнейшему сдавливанию близко расположенных к гипофизу структур головного мозга. Это может проявляться в виде эндокринных, неврологических, зрительных нарушений. Также аденома гипофиза может сопровождаться рядом осложнений – кровоизиляниями в опухоль (апоплексией), кистозным перерождением. Также есть неподтвержденная теория об излишне долгом приема оральных контрацептивов.
Аденома гипофиза может быть гормонально неактивной (клетки, из которой она состоит, гормонов не продуцируют) или же гормонально активной. По размерам аденомы гипофиза разделяют на микроаденомы (1мм-2см в диаметре) и макроаденомы (больше 2см).
Виды аденом:
- аденома соматотропинпродуцирующая, продуцирующая гормон роста: аденома соматотропная; соматотропинома;
- аденома пролактинсекретирующая: пролактиновая аденома; пролактинома;
- аденома аденокортикопинпродуцирующая: кортикотропная аденома; кортикотропинома;
- аденома тиротропинпродуцирующая: тиреотропная аденома; тиротропинома;
- аденома фоллтропинпродуцирующая (лютропинпродуцирующая, гонадотропная).
 Продуцирует гонадотропные гормоны.
Продуцирует гонадотропные гормоны.
Симптомы аденомы гипофиза
В целом аденома гипофиза симптомы имеет неоднозначные. Клинические проявления аденом гормонально-активного типа — это эндокринно-обменный синдром, рентгенологические и офтальмоневрологические симптомы. Выраженный эндокринно-обменный синдром свидетельствует об избыточном уровне гормона гипофиза и степени поражения ткани, которая окружает опухоль.
Офтальмоневрологические симптомы: первичная атрофия зрительного нерва, изменение поля зрения и другие проявления. Интенсивность этих симптомов напрямую зависит от роста опухоли. Если процесс усиливается, к симптомам добавляются головные боли, сосредоточенные в лобной, глазничной, височной областях. Боли тупые, не сопровождаются тошнотой, не меняются при смене положения тела. Анальгетики чаще всего не снижают боль. Если рост опухоли продолжается в сторону верхней области, повреждаются гипоталамические структуры. Рост книзу провоцирует ощущения заложенного носа, постоянное течение из носа цереброспинальной жидкости.
Усиление головной боли вместе с офтальмоневрологическими симптомами происходит резко. Это связано в большинстве случаев с ускорением увеличения опухоли (к примеру, при беременности) или с кровоизлиянием в опухоль. Это тяжелое, но не смертельное осложнение. Кровоизлияния характерны для аденомы гипофиза и в некоторых случаях приводят к спонтанному излечению аденомы гипофиза гормонально-активного типа.
При рентгенологическом исследовании к основным симптомам аденомы гипофиза относят изменение размера и формы турецкого седла, истончение и деструкцию образующих его костных структур. В случае проведения компьютерной томографии можно визуализировать и непосредственно опухоль.
В отдельных случаях аденома пролактинома головного мозга гормоналньо-активной формы имеет специфическую симптоматику. У женщин опухоль может проявляться как синдром галактореи аменореи. Треть женщин с опухолями имеет умеренное ожирение, себорею волосистой части головы, снижение либидо, аноргазмию. Основное эндокринное проявление опухоли у мужчин – импотенция или снижение либидо.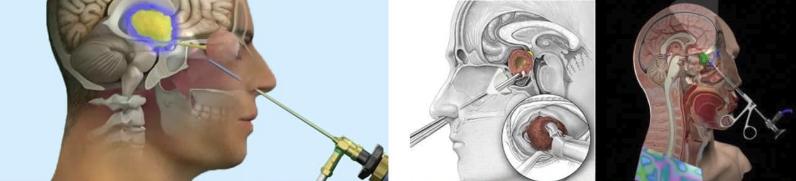
Соматотропинома проявляется клинически как синдром акромелагии либо гигантизма у детей. Кроме характерных для этого заболевания изменений скелета и мягких тканей возможно развитие ожирения и появление симптомов сахарного диабета, часто увеличивается щитовидная железа (ее функции при этом не нарушаются). Часто отмечается появление папиллом, бородавок, увеличение сальности кожи, сильное потоотделение, снижение работоспособности.
Кортикотропиномы – редко встречающиеся аденомы гипофиза. Современные данные свидетельствуют, что при болезни Иценко Кушинга почти всегда обнаруживаются кортикотропиномы. Кортикотропиномы чаще всего склонны к метастазированию (по сравнению с аденомами гипофиза других типов). Офтальмоневрологические симптомы при кортикотропиномах чаще всего не проявляется, так как диагностика этих опухолей почти всегда происходит на ранних этапах. Один из показателей наличия опухоли – эндокринное психическое расстройство.
Тиреотропиномы и гонадотропиномы – редко встречающиеся аденомы гипофиза. Их проявления зависят от того, проявляются они как первичные опухоли или развились из-за длительного поражения железы-мишени.
Их проявления зависят от того, проявляются они как первичные опухоли или развились из-за длительного поражения железы-мишени.
Аденома гипофиза и беременность
Беременность и аденома – несовместимые понятия (при пролактиносекретирующих аденомах гипофиза, при которых не было проведено адекватное лечение). Опухоль секретирует большим количеством пролактина, из-за чего забеременеть женщина не сможет. Однако есть случаи, когда аденома гипофиза начинает развиваться в процессе беременности. Что касается других типов аденом гипофиза у женщин – если концентрация пролакетина в крови находится в пределах нормы, никаких помех для зачатия ребенка нет. Если заболевание выявлено, на протяжении всей беременности женщине рекомендуется наблюдаться не только у
Диагностика аденомы гипофиза
Главный метод диагностики аденомы гипофиза – клинико-биохимическое исследование, а также краниография (рентгенологическое исследование). Кроме того, используют компьютерную томографию, радиоиммунологический метод, ЯМР-томографию. В первую очередь проводится именно краниография в 2 проекциях, а также томография области турецкого седла, позволяющая выявить признаки внутриселлярного объемного процесса, который провоцирует изменения в костных структурах (остеопороз, деструкцию спинки турецкого седла). Характерная особенность – двухконтурность дна в турецком седле. Наличие опухоли, ее структуру, размеры и направление разрастания позволяет определить компьютерная томография (с контрастным усилением). Радиоиммунологическое обследование позволяет определить концентрацию гипофизарных гормонов в сыворотке крови. Это специфичный и высокочувствительный метод определения аденомы гипофиза.
В первую очередь проводится именно краниография в 2 проекциях, а также томография области турецкого седла, позволяющая выявить признаки внутриселлярного объемного процесса, который провоцирует изменения в костных структурах (остеопороз, деструкцию спинки турецкого седла). Характерная особенность – двухконтурность дна в турецком седле. Наличие опухоли, ее структуру, размеры и направление разрастания позволяет определить компьютерная томография (с контрастным усилением). Радиоиммунологическое обследование позволяет определить концентрацию гипофизарных гормонов в сыворотке крови. Это специфичный и высокочувствительный метод определения аденомы гипофиза.
В любом случае диагностику аденомы гипофиза нужно проводить комплексно. Подозрения на наличие заболевание должны вызвать офтальмоневрологические нарушения и эндокринно-обменный синдром. Больные аденомой гипофиза характеризируются выраженной эмоциональностью, поэтому доктор должен знакомить их с результатами обследования тактично, уведомив о трудностях диагностического поиска, вероятности гипердиагностики, доброкачественном течении большинства аденом и медленном их росте.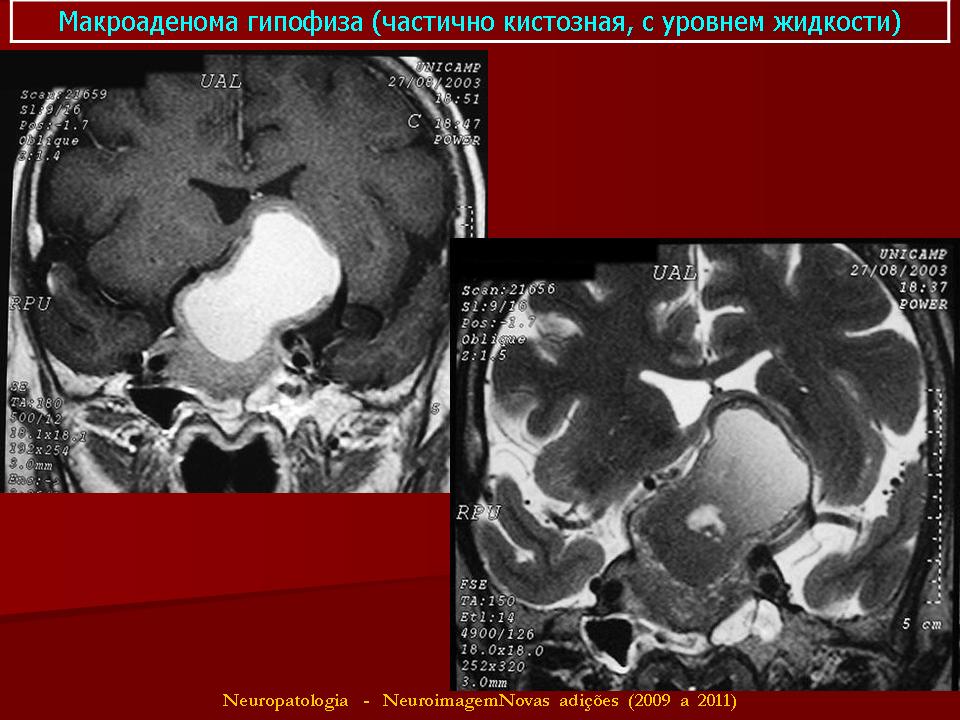
Первоначально доктор должен убедиться, что эндокринно-обменный синдром – это не итог приема антидепрессантов, нейролептиков и других лекарственных средств, а также нервно-рефлекторных воздействий (наличия контрацептива внутри матки, частой самопальпации груди и т.п.). Также нужно определить степень концентрации в крови тропных гормонов гипофиза.
Если концентрация сильно увеличена, а рентгенологическое обследование указывает на признаки аденомы гипофиза, диагноз можно подтверждать. При невысокой концентрации гормонов гипофиза, но при этом наличии признаков объемного образования на рентгенограмме в области турецкого седла можно использовать дополнительные методики обследования: компьютерную томографию, церебральную ангиографию, ЯМР-томографию и другие.
Чтобы выявить аномальную реакцию аденоматозной ткани на фармакологическое воздействие обычно применяют специальные фармакологические нагрузочные пробы. При наличии подозрения на аденому гипофиза пациента нужно направить на обследование к офтальмологу. Обследование полей зрения и остроты, исследование глазного дна позволяет обнаружить зрительные нарушения, в некоторых случаях – поражение глазодвигательного нерва.
Обследование полей зрения и остроты, исследование глазного дна позволяет обнаружить зрительные нарушения, в некоторых случаях – поражение глазодвигательного нерва.
Дифференциальный диагноз характерен для гормонально-неактивных опухолей, расположенных в области турецкого седла, опухолей негипофизарной локализации, продуцирующих пептидные гормоны, гипоталамо-гипофизарной недостаточности неопухолевого генеза. Дифференцируют аденому гипофиза с синдромом пустого турецкого седла, для которого присуще также развитие офтальмоневрологического синдрома.
Лечение аденомы гипофиза
Если у пациента подтверждена аденома гипофиза, лечение может быть медикаментозным, радиохирургическим и нейрохирургическим. Медикаментозное лечение проводят с помощью препарата парлодела (бромокриптина). Также применяют методы лучевого лечения: дистанционную лучевую терапию, гамма-терапию, протонную терапию, радиохирургию. Радиохирургическая методика заключается в введении в аденому радиоактивных веществ. Особенно эффективны лучевые методы лечения аденомы гипофиза при небольших опухолях.
Особенно эффективны лучевые методы лечения аденомы гипофиза при небольших опухолях.
Нейрохирургическое лечение проводят при нарушении зрения, а также при осложненных аденомах (при кровоизлиянии в аденому, при образовании кисты в области аденомы). Также сейчас выполняют операции с применением транссфеноидального хирургического подхода. При небольших аденомах такое лечение дает преимущественно хорошие результаты.
Общий прогноз на выздоровление – 85% положительных случаев. Естественно, все зависит от размеров опухоли, а также того, насколько рано она была диагностирована. Чтобы последствия аденомы гипофиза не были тяжелыми, нужно вовремя диагностировать заболевание и провести удаление аденомы гипофиза. Для этого важно обратиться к опытному врачу-эндокринологу или нейрохирургу, который проведет комплексное обследование пациента и выберет оптимальный способ лечения.
Аденома Гипофиза. Гиперпролактенимия. Бесплодие.
Вопрос
Женщина, 33 полных лет. Аденома гипофиза — обнаружена в сентябре 2005. МРТ РАМН (Зенкова Т.) С тех пор на достинексе в разных дозах. В начале помогло. ПРолактин с 2500 упал до 600 ед. Потом снова постепенно начал подниматься. Половая жизнь с 28 лет. Беременность- 0. (Основная жалоба — на отсутствие беременности, которую врачи связывают с аденомой и гиперпролактенимией). На сегодняшний день картина следующая.
Аденома гипофиза — обнаружена в сентябре 2005. МРТ РАМН (Зенкова Т.) С тех пор на достинексе в разных дозах. В начале помогло. ПРолактин с 2500 упал до 600 ед. Потом снова постепенно начал подниматься. Половая жизнь с 28 лет. Беременность- 0. (Основная жалоба — на отсутствие беременности, которую врачи связывают с аденомой и гиперпролактенимией). На сегодняшний день картина следующая.
МРТ 2012 (апрель, РАМН ЭНЦ) — Очаговых и диффузных изменений сигнала, поступающего от больших полушарий ГМ, мозжечка и стволов структур не определяется. Срединные образования не смещены. Желудочк. система не расширена и не деформирована. Субарахноидальные пространства не расширены. Гипофиз имеет размеры- ветикальн.5 мм, поперечный 16 мм, переднезадний 11 мм. Стр-ра аденогипофиза неоднородна- в правой части аденогипофиза на границе с кавернозным синусом определяется образование неправильной формы размерами 3,5Х6Х5 мм, умеренно гипоинтенсивное на Т1 взвешенных изображениях, при контрастном усилении характеризуется сниженным (по сравнению с тканью аденогипофиза) накоплением контрастного вещества..png) Медиальная стенка правого кавернозного синуса деформирована. Воронка отклонена влево. Карниовертебральн переход, стволов стр-ры без особенностей. В обл среднего уха и сосцевидного отростка справа отмечаются зоны неоднородно повышенного МР-сигнала на Т2взвешан изображ-х (МР признаки воспалительных изменений).
Медиальная стенка правого кавернозного синуса деформирована. Воронка отклонена влево. Карниовертебральн переход, стволов стр-ры без особенностей. В обл среднего уха и сосцевидного отростка справа отмечаются зоны неоднородно повышенного МР-сигнала на Т2взвешан изображ-х (МР признаки воспалительных изменений).
Закл.- МР картина ЭНДОСЕЛЛЯРНОЙ АДЕНОМЫ СРАСЕЛЛЯРНОМУ РАСПРОСТРАНЕНИЮ. МР- КАРТИНА ВОСПАЛИТЕЛЬНЫХ ИЗМЕНЕНИЙ В ОБЛАСТИ СРЕДНЕГО УХА С ВОВЛЕЧЕНИЕМ В ПРОЦЕСС СОСЦЕВИДНОГО ОТРОСТКА СПРАВА. ( Если необходимо,то данные всех прежних 2005, 2006, 2009 МРТ пришлю).
Выписка из гинекологии (сентябрь 2012). Менсис с 13 лет, регулярные, умеренные, длительностью в 5-7 дней, через 26 дней (теперь уже через 24! дня). Половая жизнь с 28 лет. Замужем. Беременность — 0. Патологии со стороны органов и систем не выявлено. Оволосение по женскому типу. Наружные половые органы развиты правильно. Влагалище нерожавшей. Шейка матки конической формы. Матка в anteversio flexio, чувствительная при пальпации. Придатки болезненные. Выделения слизистые, скудные. Диагноз- Бесплодие — 1, Хронический метроэндометрит. Хронический двусторонний аднексит. Аденома гипофиза.
Придатки болезненные. Выделения слизистые, скудные. Диагноз- Бесплодие — 1, Хронический метроэндометрит. Хронический двусторонний аднексит. Аденома гипофиза.
К.справка эндокринолога- Щитовидная железа 1 степени, эутиреоз. Лакторея+. ТОны сердца ясные, ритм не нарушен. АД — 110.70. Над легкими везикулярное дыхание… Рекомендовано обследование в отделении нейроэндокринологии ФГУЭНЦ с целью уточнения дальнейшей тактики лечения.
Свои жалобы: Головные боли, очень быстрая утомляемость,перепады в настроении, чувствительность. плаксивость, постоянная тошнота, сонливость, выделения из молочных желез, снижение памяти, увеличение веса (было 48-49кг. стало — 60-63кг). Цифры пролактина с 2005 г.
Сентябрь 05. 2400,00
Ноябрь 05. 1083,30
Декабрь 05. 609,60
Март 06. 773,40
Июнь 06. 543,60
Август 06. 566,00
Ноябрь 06. 1000,00
Февраль 07. 977,30
Март 07. 900,00
Май 2007. 940,00
Июль 07. 1200,00
Август 07. 1050,00
Ноябрь 07. 2000,00
Март 08. 1700,00
1700,00
Апрель 08. 1960,00
Август 08. 3458,90
Декабрь 08. 2252,60
Февраль 09. 3637,80
Март 09. 1700,00
Май 09. 1442,00
Июнь 09. 1622,00
Июль 09. 1540,00
Август 09. 1101,00
Октябрь 09. 1460,00
Февраль 10. 1015
Май начало 10 1123,00
ИЮЛЬ 10. 1160,60
………………..
Декабрь конец 10 1182,00
………………
Август начало 11 1309,00
Октябрь 11. 639,80
Ноябрь11. 1442,00
Декабрь 11. 1354,00
Февраль 12. 1546,00
Апрель 12. 1569,00
Май 12. 1455,00
июнь 12. 1480,00
июль 12. 1902,00
Папилома на соске левой груди начала кровить, расти, давать резкую боль и жгучее ощущение в левую руку. Затем часть отошла и начало вытекать кровянисто-желтая жидкость, похожая на гной.
ПРием Достинекса с 2005 года увеличен с 0,5 тб в неделю до 6 тб. в неделю и снова снижен до 5 тб. в неделю,так как тошнота была не прекращающаяся.
УЗИ желчного пузыря и поджелудочной железы — ж.п. не увеличен, форма — 83Х31 мм, стенка не утолщена, содержимое взвесь, осадок; подж. ж. головка не увеличена, до 25 мм, тело 17 мм, контуры ровные,структура однородна, эхогенность умеренно повышена. Закл- Признаки холецистита, диффузные изменения поджелудочной железы.
ж. головка не увеличена, до 25 мм, тело 17 мм, контуры ровные,структура однородна, эхогенность умеренно повышена. Закл- Признаки холецистита, диффузные изменения поджелудочной железы.
Помогите, пожалуйста, понять является ли моя аденома гипофиза и гиперпролактенимия причиной моего бесплодия. Если да, то как мне это лечить или оперировать и где? Я очень очень хочу малыша. Спасибо Вам огромное заранее!
Аденома гипофиза
Аденома гипофиза представляет собой доброкачественное образование в передней доле гипофиза. Основная опасность этого недуга состоит в следующем:
- нарушение гормонального баланса: опухоль может как продуцировать излишки гормонов, так и сокращать их выработку гипофизом, что приводит к эндокринным проблемам;
- давление на гипофиз и другие структуры мозга: провоцирует головные боли, нарушение зрения и движения глаз, вызывает эпилепсию.
При подозрении на аденому гипофиза головного мозга важно как можно скорее пройти обследование.
 В клинике «МедикПро» в Калуге работает грамотный врач-эндокринолог, способный выявить недуг уже на ранней стадии и своевременно предпринять меры по его устранению.
В клинике «МедикПро» в Калуге работает грамотный врач-эндокринолог, способный выявить недуг уже на ранней стадии и своевременно предпринять меры по его устранению.Причины и симптомы аденомы гипофиза
Наследственных факторов, вызывающих склонность к появлению аденомы гипофиза не обнаружено, но есть ряд причин, способствующих возникновению недуга:
- травмы головы;
- воздействия токсинов и ядов;
- инфекционные заболевания мозга;
- воспалительные заболевания мозга;
- патологии во время беременности или родовые травмы;
- длительный приём оральных контрацептивов.
В большинстве случаев выявляется аденома гипофиза головного мозга у женщин и мужчин в равной степени в возрасте от 30 до 40 лет. В редких случаях диагностируется в более раннем возрасте.
Развитие заболевания сопровождается следующими признаками:
- частые головные боли неизвестного происхождения, головокружения;
- нарушение остроты зрения, двоение в глазах;
- слабость, повышенная утомляемость;
- нарушение сна;
- сухая кожа с шелушением;
- снижение аппетита, тошнота;
- набор веса при сбалансированном питании;
- снижение либидо;
- нарушение менструального цикла у женщин;
- снижение половой функции у мужчин, вплоть до импотенции.

Аналогичные симптомы могут сопровождать ряд других заболеваний, поэтому крайне важна грамотная диагностика.
Диагностика аденомы гипофиза мозга
На первом осмотре пациента собирается анамнез и симптоматика, назначается офтальмологический осмотр, а также ряд инструментальных исследований:
- рентгенография;
- МРТ;
- КТ;
- ангиография сосудов головного мозга.
Рентгенография позволяет наиболее точно диагностировать наличие аденомы гипофиза у женщин и мужчин любых возрастов. МРТ и КТ применяются для определения размеров и границ, а также исключения распространения клеток опухоли на здоровые ткани гипофиза.
Кроме того, назначается общий, биохимический, радиоиммунологический анализ крови, а также определение уровня половых, тиреоидных, глюкокортикоидных гормонов.
На основании полученных данных диагностируется заболевание и назначается компетентное лечение.

Лечение аденомы гипофиза
В определённых случаях можно вылечить аденому гипофиза консервативным способом. Это зависит от типа, размеров и гормональной активности опухоли. Если образование не сдавливает гипофиз, а состояние пациента не требует незамедлительного хирургического вмешательства, пациенту назначаются:
- медикаменты, нормализующие выработку гормонов и стабилизирующие гормональный фон;
- препараты-антагонисты в соответствии с типом опухоли.
Лечение может продолжаться от нескольких месяцев до нескольких лет. На протяжении всего периода терапии необходимо регулярно проходить обследование и наблюдаться у лечащего врача. При необходимости дозировка и типы препаратов корректируются.
Удаление аденомы гипофиза необходимо в тех случаях, если диагностируются гормонально зависимые, сдавливающие гипофиз новообразования. Для определения правильного лечения важно пройти полноценную квалифицированную диагностику. Для этого запишитесь на приём в нашу клинику.
Для этого запишитесь на приём в нашу клинику.
Мы всегда рады помочь Вам и приглашаем в медицинский центр «МЕДИКПРО»!
Будьте здоровы!
Записаться на прием к врачу-эндокринологу вы можете по телефону: 8 (4842) 27-72-50.
Пролактинома и беременность — Вопрос эндокринологу
Если вы не нашли нужной информации среди ответов на этот вопрос, или же ваша проблема немного отличается от представленной, попробуйте задать дополнительный вопрос врачу на этой же странице, если он будет по теме основного вопроса. Вы также можете задать новый вопрос, и через некоторое время наши врачи на него ответят. Это бесплатно. Также можете поискать нужную информацию в похожих вопросах на этой странице или через страницу поиска по сайту. Мы будем очень благодарны, если Вы порекомендуете нас своим друзьям в социальных сетях.Медпортал 03online.com осуществляет медконсультации в режиме переписки с врачами на сайте. Здесь вы получаете ответы от реальных практикующих специалистов в своей области. В настоящий момент на сайте можно получить консультацию по 74 направлениям: специалиста COVID-19, аллерголога, анестезиолога-реаниматолога, венеролога, гастроэнтеролога, гематолога, генетика, гепатолога, гериатра, гинеколога, гинеколога-эндокринолога, гомеопата, дерматолога, детского гастроэнтеролога, детского гинеколога, детского дерматолога, детского инфекциониста, детского кардиолога, детского лора, детского невролога, детского нефролога, детского онколога, детского офтальмолога, детского психолога, детского пульмонолога, детского ревматолога, детского уролога, детского хирурга, детского эндокринолога, дефектолога, диетолога, иммунолога, инфекциониста, кардиолога, клинического психолога, косметолога, липидолога, логопеда, лора, маммолога, медицинского юриста, нарколога, невропатолога, нейрохирурга, неонатолога, нефролога, нутрициолога, онколога, онкоуролога, ортопеда-травматолога, офтальмолога, паразитолога, педиатра, пластического хирурга, подолога, проктолога, психиатра, психолога, пульмонолога, ревматолога, рентгенолога, репродуктолога, сексолога-андролога, стоматолога, трихолога, уролога, фармацевта, физиотерапевта, фитотерапевта, флеболога, фтизиатра, хирурга, эндокринолога.
В настоящий момент на сайте можно получить консультацию по 74 направлениям: специалиста COVID-19, аллерголога, анестезиолога-реаниматолога, венеролога, гастроэнтеролога, гематолога, генетика, гепатолога, гериатра, гинеколога, гинеколога-эндокринолога, гомеопата, дерматолога, детского гастроэнтеролога, детского гинеколога, детского дерматолога, детского инфекциониста, детского кардиолога, детского лора, детского невролога, детского нефролога, детского онколога, детского офтальмолога, детского психолога, детского пульмонолога, детского ревматолога, детского уролога, детского хирурга, детского эндокринолога, дефектолога, диетолога, иммунолога, инфекциониста, кардиолога, клинического психолога, косметолога, липидолога, логопеда, лора, маммолога, медицинского юриста, нарколога, невропатолога, нейрохирурга, неонатолога, нефролога, нутрициолога, онколога, онкоуролога, ортопеда-травматолога, офтальмолога, паразитолога, педиатра, пластического хирурга, подолога, проктолога, психиатра, психолога, пульмонолога, ревматолога, рентгенолога, репродуктолога, сексолога-андролога, стоматолога, трихолога, уролога, фармацевта, физиотерапевта, фитотерапевта, флеболога, фтизиатра, хирурга, эндокринолога.
Мы отвечаем на 97.46% вопросов.
Оставайтесь с нами и будьте здоровы!
Беременность с микроаденомой гипофиза и запоздалый отчет – мальчик Федор 6/08/2014, г. Минск: ru_perinatal — LiveJournal
Вчера мой сынИтак, 6 августа в 3-ем роддоме Минска на сроке 40 недель и 3 дня родился наш сын, 3.630, 53 см, 8/9 Апгар, роды со стимуляцией, о чем я ни разу не пожалела, под катом — много букв про беременность с микроаденомой, быстрые роды со стимуляцией и разные советы новобранцам.
Беременность моя хоть и не была запланированной – чего уж тут лукавить – протекала очень легко, не считая адового токсикоза вначале. О том что мы ждем ребенка мы узнали в Тае на 5 день долгожданного отпуска. До этого на УЗИ (предположительно в день зачатия) мне сказали что да, задержка у Вас из-за того, что овуляции нет и не предвидится, а вот какая-то киста на яичнике, приходите через месяц)) Надо сказать что я к тому моменту полтора года снижала пролактин достинексом, имея микроаденому гипофиза, цикл был длинным и нестабильным, овуляция не всегда появлялась, поэтому я не очень удивилась такому результату УЗИ.
 Зато я очень удивилась, когда меня полечили тайские врачи от отравления, а на следующий день, когда легче не стало – по совету мудрой мамы купила тест, и увидела там две полоски))) оставшиеся десять дней отпуска я лежала как зайчик под кондиционером, тошнила в мусорку, есть могла только бананы и чипсы.. А уж какие запахи на улице в Тайланде лучше не вспоминать тем у кого токсикоз))
Зато я очень удивилась, когда меня полечили тайские врачи от отравления, а на следующий день, когда легче не стало – по совету мудрой мамы купила тест, и увидела там две полоски))) оставшиеся десять дней отпуска я лежала как зайчик под кондиционером, тошнила в мусорку, есть могла только бананы и чипсы.. А уж какие запахи на улице в Тайланде лучше не вспоминать тем у кого токсикоз))Дома все было полегче, к 12 неделям отпустило совсем. Дальше я исправно сдавала анализы, ходила на УЗИ, вкусно кушала, смотрела кино, выбирала малышу приданное, гуляла, общалась с друзьями – мне повезло, что на работу ходить не нужно было и я смогла насладиться этим чудесным периодом сполна. Все проходило идеально, не считая ОРЗ на 33 неделе с температурой, но за недельку я его победила))) Достинекс, который я пила до беременности, я заменила на бромокрептин, после 20 недели получив консультацию другого врача и поныв тут потихоньку снизила дозу и отменила его вовсе. Сейчас с молоком все более чем хорошо) Анализы на пролактин собираюсь сдавать после окончания ГВ.
 Таким образом беременность с микроаденомой в моем случае ничем не отличалась от самой обычной))
Таким образом беременность с микроаденомой в моем случае ничем не отличалась от самой обычной))Рожать я собиралась в 3 роддоме, который в Минске не очень популярен, но у меня была весомая причина – гражданская жена моего отца работает там) Поэтому после 38 недели я стала приходить на осмотры, КТГ и УЗИ, которые все хором говорили, что все прекрасно и замечательно. Но ближе к 40 неделе меня стали торопить, а я стала упираться, что очень хочу ЕР и все такое. Шейка была мягкая, голова была низко, я пыталась договориться с сыном как могла, но ничего не помогало… 5 августа на сроке 40+2 мне было предложено залечь 6-го в роддом и попытаться ускорить процесс. Все складывалось удачно – дежурство нужного врача и хорошей акушерки, личное присутствие моей родственницы… Я сделала марш-бросок по парку в раздумьях и сказала, что утром едем))
Примерно в 7.30 я была в приемном, меня посмотрели «с пристрастием», дальше сделали клизму, я приняла душ и мы поднялись в предродовую. У меня была отдельная двухместная, в соседней – 4 места, сначала было пусто, потом оттуда стали доноситься стоны) Не знаю, что со мной сделали внизу, но примерно к 10 я стала ощущать потягивания живота как при месячных. К 11 они стали посильнее, но я все еще могла ходить по отделению и вести светские беседы) к 12 я уже не могла слушать музыку, вся была в себе – а на кресле открытие было 3 см. Боль становилась все сильнее и сильнее и к 14 раскрытие было 4 см, а я уже стала спрашивать про обезболивание.. Меня предупредили что можем сделать эпидурал – но тогда возможно я что-то не почувствую когда надо будет тужиться. Тут надо сделать лирическое отступление и сказать, что у нас эпидуралка далеко не так распространена как в России, и опыта у анестезиологов тоже не очень много – поэтому я решила от нее отказаться. Но шейка открывалась плохо, поэтому мне поставили окситоцин и промедол. Между схватками я проваливалась в сонное состояние. Бороться с болью мне помогало только дыхание – вдох и длинный выдох, как будто задуваешь свечу. Ходить я не могла, стоять тоже, я могла только лежать на боку, и на каждую схватку собираться и дышать, дышать, дышать…. При этом на мне как водится постоянно висело КТГ, и акушерка периодически меня ворочала, чтобы не терять сердцебиение…Прошло время, меня посмотрели, раскрытие было 8 см, но было сказано ходить или лежать на спине – чтобы дать ребенку правильно вставиться.
К 11 они стали посильнее, но я все еще могла ходить по отделению и вести светские беседы) к 12 я уже не могла слушать музыку, вся была в себе – а на кресле открытие было 3 см. Боль становилась все сильнее и сильнее и к 14 раскрытие было 4 см, а я уже стала спрашивать про обезболивание.. Меня предупредили что можем сделать эпидурал – но тогда возможно я что-то не почувствую когда надо будет тужиться. Тут надо сделать лирическое отступление и сказать, что у нас эпидуралка далеко не так распространена как в России, и опыта у анестезиологов тоже не очень много – поэтому я решила от нее отказаться. Но шейка открывалась плохо, поэтому мне поставили окситоцин и промедол. Между схватками я проваливалась в сонное состояние. Бороться с болью мне помогало только дыхание – вдох и длинный выдох, как будто задуваешь свечу. Ходить я не могла, стоять тоже, я могла только лежать на боку, и на каждую схватку собираться и дышать, дышать, дышать…. При этом на мне как водится постоянно висело КТГ, и акушерка периодически меня ворочала, чтобы не терять сердцебиение…Прошло время, меня посмотрели, раскрытие было 8 см, но было сказано ходить или лежать на спине – чтобы дать ребенку правильно вставиться. Я встала, на схватку упиралась руками в кровать, и пыталась ходить – и вскоре почувствовала, как меня подтуживает. На кресле мои ощущения подтвердились и мы пошли в родзал…
Я встала, на схватку упиралась руками в кровать, и пыталась ходить – и вскоре почувствовала, как меня подтуживает. На кресле мои ощущения подтвердились и мы пошли в родзал…
Тут меня уложили и сразу набежала куча народу)) Сначала лежишь одна в предродовой, умираешь – а тут такой аншлаг! И врачи, и акушерки, и неонатолог, и детская медсестра, я почувствовала себя звездой)) Меня проинструктировали, что «вот эти ручки ломаешь на себя, ногами упираешься тут и на схватку — глубокий вдох и тужишься так сильно, как можешь, и так три раза». Но я уже не чувствовала схваток, и тогда мне подсказали, когда тужиться. Если честно, вся эта самая главная часть – в тумане в моих воспоминаниях) Я старалась как могла, и на выдохе орала конечно, но мне казалось, что ничего не происходит… После первой «тройки» родилась голова, и мне сказали, что осталось немного) И действительно — еще немного – и я почувствовала облегчение.. Нет, не так – ОБЛЕГЧЕНИЕ. Я поняла, что вся титаническая работа закончилась… Посмотрела в окно – оказывается впервые за много дней ужасной жары шел дождь, по небу бежали огромные темные облака… Мальчик мой родился в 16. 25, но был немного сонный из-за промедола и закричал не сразу – и это были самые страшные 30 секунд в моей жизни… А дальше – счастье знакомства – мне положили его на живот, и я заплакала, а он успокоился… Потом малыша забрали, мне наложили пару стежков – ни разрывов, ни разрезов не было, только ссадина на губе. Дальше все стандартно – два часа в коридоре, потом меня перевезли в одноместную палату. А потом мне принесли моего малыша и мы стали знакомиться и прилаживаться к моей не очень удобной груди… Но это все уже начало совершенно другой истории)))
25, но был немного сонный из-за промедола и закричал не сразу – и это были самые страшные 30 секунд в моей жизни… А дальше – счастье знакомства – мне положили его на живот, и я заплакала, а он успокоился… Потом малыша забрали, мне наложили пару стежков – ни разрывов, ни разрезов не было, только ссадина на губе. Дальше все стандартно – два часа в коридоре, потом меня перевезли в одноместную палату. А потом мне принесли моего малыша и мы стали знакомиться и прилаживаться к моей не очень удобной груди… Но это все уже начало совершенно другой истории)))
В целом я довольна, что получилось, так как получилось, не так страшна стимуляция, как ее малюют, зато все прошло под присмотром нужных людей, что было для меня важно. И еще я поняла, что партнерские роды — не для всех, я вот лично даже не знаю, зачем мне там нужен был бы муж. Я настолько была сосредоточена на своих ощущениях, что мне кажется могла бы и стукнуть, если бы кто-то мне мешал)) Помочь он мне бы никак не смог, нервничал бы а курить нельзя, единственное — было бы здорово, если бы ребенок провел время после родов с ним, а не в детском, пока я лежала в коридоре.
Про роддом могу более обстоятельно рассказать в личке интересующимся белорускам) В целом мне все понравилось, были нюансы конечно, но пока в нашей стране глобально что-то не поменяется в родовспоможении – эти нюансы есть везде.
А теперь советы – как водится, это все глубоко мое личное мнение, но может кому-то будет полезно)) Самый главный – сначала кажется, что роды – это очень важно, к ним готовишься, переживаешь и так далее… Но они быстро проходят, а на руках остается прекрасный младенец без инструкции! Поэтому я бы советовала больше читать про уход за маленьким – хотя в любом случае придется сто раз бегать за советами в малыши)))
Также очень советую покупать одежду 2в1 – для беременных и для кормления грудью, если Вы конечно собираетесь кормить. Потому что я потратилась два раза на специальный гардероб.
Еще я пожалела, что сразу не купила молокоотсос и термонакладки для груди – когда просыпаешься с адовой болью от лактостаза, отправлять кого-то в магазин за этими супер-важными вещами особо нет возможности. Прикладывать термонакладку вместо горячего полотенца/пакета с замороженными овощами гораздо удобнее)) В крайнем случае всегда можно продать на вторичке.
Прикладывать термонакладку вместо горячего полотенца/пакета с замороженными овощами гораздо удобнее)) В крайнем случае всегда можно продать на вторичке.
Слинг! Это вещь, лучше тоже иметь сразу)
Всем спасибо за внимание!
Лечение опухолей гипофиза во время беременности
Бронштейн, доктор медицинских наук, Эндокринология 6-е изд. Том. 1 гл. 18 (под редакцией DeGroot, LJ & Jameson, JL) 333–357 (Elsevier, Philadelphia, 2010).
Google Scholar
Клибански А. Клиническая практика. пролактиномы. Н. англ. Дж. Мед. 362 , 1219–1226 (2010).
КАС пабмед Google Scholar
Шарма Дж.В. и др. . Исход беременности при опухолях гипофиза. Арх. Гинекол. Обст. 280 , 401–404 (2009).
ПабМед Google Scholar
Бронштейн, М. Д. Пролактиномы и беременность. Гипофиз 8 , 31–38 (2005).
Д. Пролактиномы и беременность. Гипофиз 8 , 31–38 (2005).
ПабМед Google Scholar
Мелмед, С. и Клейнберг, Д. в Williams Textbook of Endocrinology 11th edn Ch.8 (ред. Кроненберг, Х.М., Мелмед, С., Полонский, К.С. и Ларсен, П.Р.), 255–261 (Elsevier, 2007).
Google Scholar
Окафор, У. В., Онвуекве, И. О. и Эзегвуи, Х. У. Лечение аденомы гипофиза с эффектом массы во время беременности: клинический случай. Cases J. 2 , 6350 (2009).
КАС пабмед ПабМед Центральный Google Scholar
Караджа, З., Танриверди Ф., Унлухизарци К. и Келестимур Ф. Беременность и нарушения гипофиза. евро. Дж. Эндокринол. 162 , 453–475 (2010).
КАС пабмед Google Scholar
Molitch, M. E. Нарушения гипофиза во время беременности. Эндокринол. Метаб. клин. Север Ам. 35 , 99–116 (2006).
E. Нарушения гипофиза во время беременности. Эндокринол. Метаб. клин. Север Ам. 35 , 99–116 (2006).
ПабМед Google Scholar
Мусолино, Н.RC & Paraiba, DB в Clínica Médica 1st edn Vol. 5 гл. 8 (ред. Martins, MA и др. .) 96–107 (Manole, 2009).
Google Scholar
Casanueva, F. F. и др. . Рекомендации Гипофизарного общества по диагностике и лечению пролактином. клин. Эндокринол. (Oxf. ) 65 , 265–273 (2006).
Google Scholar
Гиллам, М.П., Молич М.Э., Ломбарди Г. и Колао А. Достижения в лечении пролактином. Эндокр. Ред. 27 , 485–534 (2006).
КАС пабмед Google Scholar
Colao, A. Опухоли гипофиза: пролактинома. Лучшая практика. Рез. клин. Эндокринол. Метаб. 23 , 575–596 (2009).
Метаб. 23 , 575–596 (2009).
КАС пабмед Google Scholar
Карс, М., Деккерс, О.М., Перейра, А.М. и Ромейн, Дж.А. Обновление пролактиномы. Нет. Дж. Мед. 68 , 104–112 (2010).
КАС пабмед Google Scholar
Gemzell, C. & Wang, C.F. Исход беременности у женщин с аденомой гипофиза. Фертил. Стерильно. 31 , 363–372 (1979).
КАС пабмед Google Scholar
Молич М.E. Беременность и женщина с гиперпролактинемией. Н. англ. Дж. Мед. 312 , 1364–1370 (1985).
КАС пабмед Google Scholar
Musolino, N.R.C. & Bronstein, MD в Опухоли гипофиза при беременности 2nd edn Ch. 4 (изд. Бронштейн, доктор медицины) 91–108 (Kluwer Academic Publishers, 2001).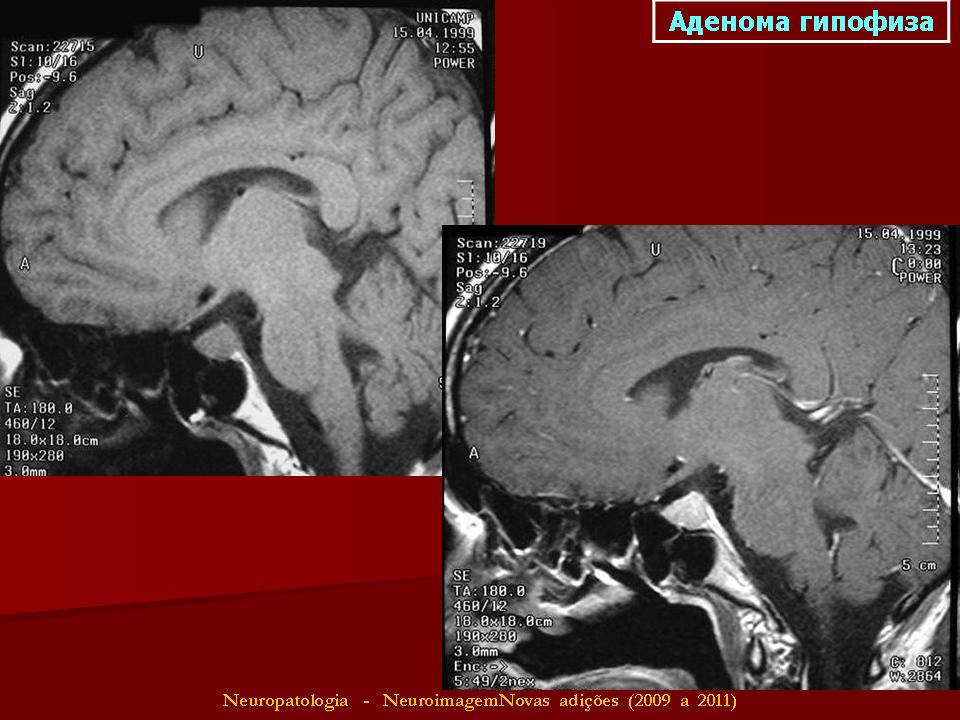
Google Scholar
Молич М.E. Пролактиномы и беременность. клин. Эндокринол. (Oxf.) 73 , 147–148 (2010).
Google Scholar
Lebbe, M., Hubinnt, C., Bernard, P. & Maiter, D. Исход 100 беременностей, начатых на фоне лечения каберголином у женщин с гиперпролактинемией. клин. Эндокринол. (Oxf.) 73 , 236–242 (2010).
КАС Google Scholar
Холмгрен, У., Бергстранд Г., Хагенфельдт К. и Вернер С. Женщины с пролактиномой — влияние беременности и лактации на уровень пролактина в сыворотке и на рост опухоли. Акта Эндокринол. 111 , 452–459 (1986).
КАС пабмед Google Scholar
Роберт Э., Мусатти Л., Писцителли Г. и Феррари С. И. Исход беременности после лечения производным спорыньи, каберголином. Репрод. Токсикол. 10 , 333–337 (1996).
Репрод. Токсикол. 10 , 333–337 (1996).
КАС пабмед Google Scholar
Krupp, P. & Monka, C. Бромокриптин при беременности: аспекты безопасности. Клин. Wochenschr. 65 , 823–827 (1987).
КАС пабмед Google Scholar
Риччи, Э. и др. . Исход беременности после лечения каберголином в первые недели гестации. Репрод. Токсикол. 16 , 791–793 (2002).
КАС пабмед Google Scholar
Колао, А. и др. . Исходы беременности после лечения каберголином: расширенные результаты 12-летнего обсервационного исследования. клин. Эндокринол. (Оксф.) 68 , 66–71 (2008).
КАС Google Scholar
Оно, М. и др. .Индивидуальная терапия высокими дозами каберголина при гиперпролактинемическом бесплодии у женщин с микро- и макропролактиномами. Дж. Клин. Эндокринол. Метаб. 95 , 2672–2679 (2010).
Дж. Клин. Эндокринол. Метаб. 95 , 2672–2679 (2010).
КАС пабмед Google Scholar
Webster, J. Сравнительный обзор профилей переносимости агонистов допамина при лечении гиперпролактинемии и торможении лактации. Безвредный для наркотиков. 14 , 228–238 (1996).
КАС пабмед Google Scholar
Манчини Т., Казануева Ф. Ф. и Джустина А. Гиперпролактинемия и пролактиномы. Эндокринол. Метаб. клин. Север Ам. 37 , 67–99 (2008).
КАС пабмед Google Scholar
Расмуссен С., Берг Т., Ниллиус С. Дж. и Уайд Л. Возобновление менструации и нормализация пролактина у женщин с гиперпролактинемией и беременностью, вызванной бромкриптином. Фертил. Стерильно. 44 , 31–34 (1985).
КАС пабмед Google Scholar
Берг Т. , Ниллиус С. Дж. и Уайд Л. Клиническое течение и исход беременности у женщин с аменореей, гиперпролактинемией и опухолями гипофиза. руб. Мед. J. 1 , 875–880 (1978).
, Ниллиус С. Дж. и Уайд Л. Клиническое течение и исход беременности у женщин с аменореей, гиперпролактинемией и опухолями гипофиза. руб. Мед. J. 1 , 875–880 (1978).
КАС пабмед ПабМед Центральный Google Scholar
Крозиньяни, П.G. и др. . Долгосрочные эффекты времени, лечения и беременности у 176 женщин с гиперпролактинемией. евро. Дж. Обст. Гинекол. Воспр. биол. 44 , 175–180 (1992).
КАС пабмед Google Scholar
Badawy, S.Z., Marziale, J.C., Rosenbaum, A.E., Chang, J.K. & Joy, S.E. Долгосрочные эффекты беременности и лечения бромокриптином на пролактиномы — ценность радиологических исследований. Ранняя беременность 3 , 306–311 (1997).
КАС пабмед Google Scholar
Ямада М. и др. . Спонтанная беременность после беременности, вызванной лечением у женщин с гиперпролактинемией. евро. Дж. Обст. Гинекол. Воспр. биол. 35 , 125–129 (1990).
евро. Дж. Обст. Гинекол. Воспр. биол. 35 , 125–129 (1990).
КАС пабмед Google Scholar
Кристин-Мэтр, С., Делемер Б., Турейн П. и Янг Дж. Пролактинома и эстрогены: беременность, контрацепция и заместительная гормональная терапия. Энн. Эндокринол. (Париж) 68 , 106–112 (2007).
Google Scholar
Пейон, Ф. и др. . Секреция и синтез пролактина в краткосрочной и долгосрочной органной культуре опухолей гипофиза у пациентов с акромегалией. Акта Эндокринол. 87 , 701–715 (1978).
КАС пабмед Google Scholar
Фриман, Р. и др. . Связанное с беременностью подострое кровотечение в пролактиному, приводящее к несахарному диабету. Фертил. Стерильно. 58 , 427–429 (1992).
КАС пабмед Google Scholar
Фриман М. Е., Каньицка Б., Лерант А. и Надь Г. Пролактин: структура, функция и регуляция секреции. Физиол. Ред. 80 , 1523–1631 (2000 г.).
Е., Каньицка Б., Лерант А. и Надь Г. Пролактин: структура, функция и регуляция секреции. Физиол. Ред. 80 , 1523–1631 (2000 г.).
КАС пабмед Google Scholar
George, D.L., Phillips, J.A. 3 rd , Francke, U. & Seeburg, P.H. Гены гормона роста и хорионического соматомаммотропина находятся на длинном плече хромосомы 17 человека в области q21–qter. Гул. Жене. 57 , 138–141 (1981).
КАС пабмед Google Scholar
Маклауд, Дж.Н., Ли, А.К., Либхабер, С.А. и Кук, Н.Е. Контроль развития и альтернативный сплайсинг плацентарно экспрессируемых транскриптов из кластера генов гормона роста человека. Дж. Биол. хим. 267 , 14219–14226 (1992).
КАС пабмед Google Scholar
Чен, Э. Ю. и др. . Нуклеотидная последовательность локуса гормона роста человека, биология и эволюция. Genomics 4 , 479–497 (1989).
Genomics 4 , 479–497 (1989).
КАС пабмед Google Scholar
Swenne, I., Hill, DJ, Strain, AJ & Milner, RD Влияние плацентарного лактогена и гормона роста человека на выработку инсулина и соматомедина C/инсулиноподобного фактора роста I поджелудочной железой плода человека в ткани культура. Дж. Эндокринол. 113 , 297–303 (1987).
КАС пабмед Google Scholar
Франкен, Ф. и др. . Физиология гормонов роста (ГР) у беременных и частичная характеристика плацентарного варианта ГР. Дж. Клин. Эндокринол. Метаб. 66 , 1171–1180 (1988).
КАС пабмед Google Scholar
Эрикссон, Л., Франкен, Ф., Эден, С., Хеннен, Г. и фон Шульц, Б. Профили гормона роста в сыворотке крови за 24 часа во время беременности — отсутствие пульсации для секреции плацентарного варианта . руб. Дж. Обст. Гинеколь. 9 6 , 949 (1989).
руб. Дж. Обст. Гинеколь. 9 6 , 949 (1989).
Google Scholar
Эрикссон Л., Эден С., Фрёландер Н., Бенгтссон Б. А. и фон Шульц Б. Непрерывная 24-часовая секреция гормона роста на поздних сроках беременности. Регулятор материнского метаболизма? Acta Obstet. Гинекол. Сканд. 67 , 543–547 (1988).
КАС пабмед Google Scholar
Макинтайр, Х.D. и др. . Плацентарный гормон роста (GH), GH-связывающий белок и ось инсулиноподобного фактора роста при нормальной беременности, задержке роста и диабетической беременности: корреляция с ростом плода. Дж. Клин. Эндокринол. Метаб. 85 , 1143–1150 (2000).
КАС пабмед Google Scholar
Кофриз, А. и др. . Плацентарный гормон роста как потенциальный регулятор материнского IGF-1 во время беременности человека. утра. Дж. Физиол. 258 (часть 1), E1014–E1019 (1990).
утра. Дж. Физиол. 258 (часть 1), E1014–E1019 (1990).
КАС пабмед Google Scholar
Caufriez, A., Frankenne, F., Hennen, G. & Copinschi, G. Регулирование материнского IGF-1 плацентарным GH при нормальной и аномальной беременности человека. утра. Дж. Физиол. 265 (часть 1), E572–E577 (1993).
КАС пабмед Google Scholar
Алсат Э., Гибурденш Дж., Лутон Д., Франкен Ф. и Эвейн-Брион Д. Плацентарный гормон роста человека. утра. Дж. Обст. Гинекол. 177 , 1526 (1997).
КАС пабмед Google Scholar
Daughaday, W. H., Trivedi, B., Winn, H. N. & Yan, H. Гиперсоматотропизм у беременных женщин, измеренный с помощью анализа радиорецепторов печени человека. Дж. Клин. Эндокринол. Метаб. 70 , 215–221 (1990).
КАС пабмед Google Scholar
Мирлесс, В. и др. . Уровень плацентарного гормона роста при нормальной беременности и при беременности с задержкой внутриутробного развития. Педиатр. Рез. 34 , 439–442 (1993).
и др. . Уровень плацентарного гормона роста при нормальной беременности и при беременности с задержкой внутриутробного развития. Педиатр. Рез. 34 , 439–442 (1993).
КАС пабмед Google Scholar
Кальцас, Г. А. и др. . Нарушение менструального цикла у женщин с акромегалией. Дж. Клин. Эндокринол. Метаб. 84 , 2731–2735 (1999).
КАС пабмед Google Scholar
Кацнельсон Л. и др. . Гипогонадизм у больных акромегалией: данные многоцентрового пилотного исследования регистра акромегалии. клин. Эндокринол. (Oxf.) 54 , 183–188 (2001).
КАС Google Scholar
Кальцас Г.А. и др. . Поликистоз яичников и фенотип синдрома поликистозных яичников у женщин с активной акромегалией. клин. Эндокринол. (Оксф.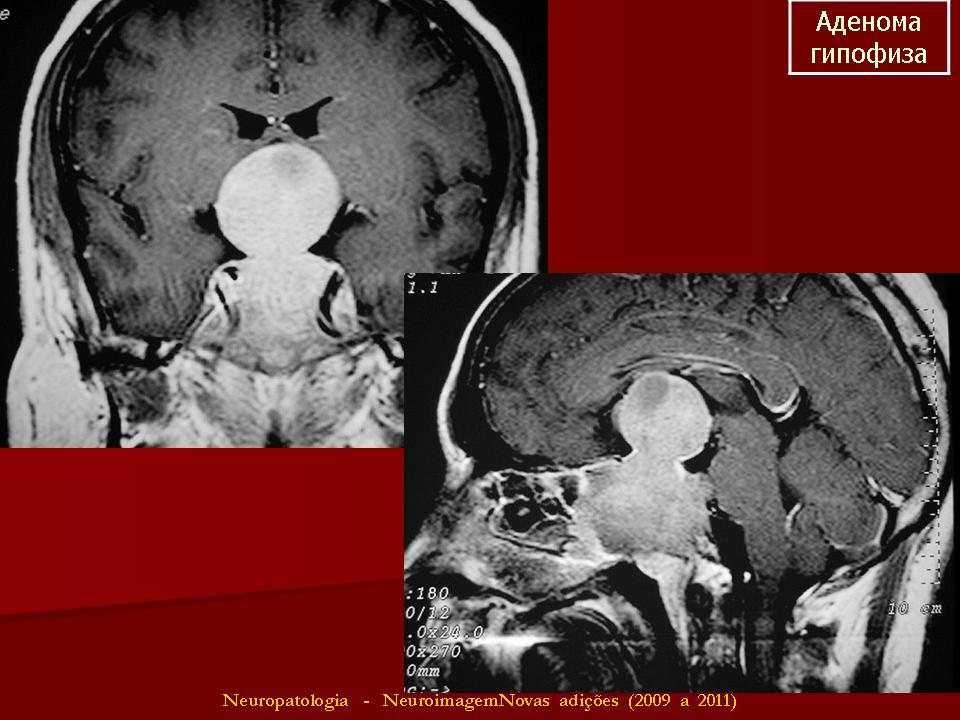 ). 67 , 917–922 (2007).
). 67 , 917–922 (2007).
КАС пабмед Google Scholar
Гринберг М., Саленаве С., Янг Дж. и Чансон П. Функция женских половых желез до и после лечения акромегалии. Дж. Клин. Эндокринол. Метаб. 95 , 4518–4525 (2010).
КАС пабмед Google Scholar
Jamnongjit, M., Gill, A. & Hammes, S. R. Передача сигналов рецептора эпидермального фактора роста необходима для нормального стероидогенеза яичников и созревания ооцитов. Проц. Натл акад. науч. США 102 , 16257–16261 (2005 г.).
КАС пабмед Google Scholar
Карон П. и др. .Акромегалия и беременность: ретроспективное многоцентровое исследование 59 беременностей у 46 женщин. Дж. Клин. Эндокринол. Метаб. 95 , 4680–4687 (2010).
КАС пабмед Google Scholar
Beckers, A.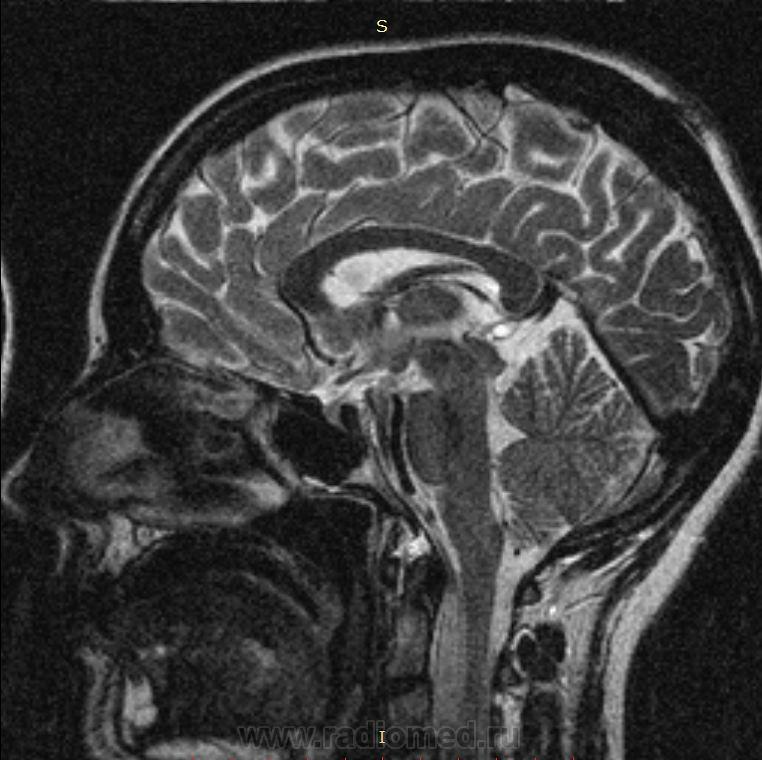 , Stevenaert, A., Foidart, JM, Hennen, G. & Frankenne, F. Плацентарная и гипофизарная секреция гормона роста во время беременности у женщин с акромегалией. Дж. Клин. Эндокринол. Метаб. 71 , 725–731 (1990).
, Stevenaert, A., Foidart, JM, Hennen, G. & Frankenne, F. Плацентарная и гипофизарная секреция гормона роста во время беременности у женщин с акромегалией. Дж. Клин. Эндокринол. Метаб. 71 , 725–731 (1990).
КАС пабмед Google Scholar
Serri, O. & Lanoie, G. Успешная беременность у женщины с акромегалией, получавшей октреотид пролонгированного действия. Эндокринолог 13 , 17–19 (2003).
Google Scholar
Лау С.Л., МакГрат С., Эвейн-Брион Д. и Смит Р. Клиническое и биохимическое улучшение при акромегалии во время беременности. Дж. Эндокринол. Вкладывать деньги. 31 , 255–261 (2008).
КАС пабмед Google Scholar
Бетеа Д., Вальдес Сосин Х., Хансен И., Стивенарт А. и Беккерс А. Акромегалия и беременность [французский]. Энн. Эндокринол.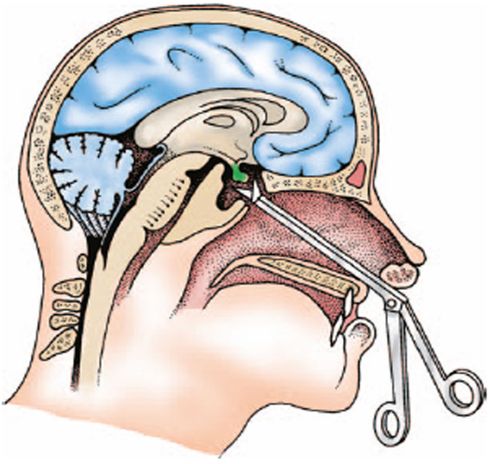 (Париж) 63 , 457–463 (2002).
(Париж) 63 , 457–463 (2002).
Google Scholar
Лунарди П., Риццо А., Миссори П.& Fraioli, B. Апоплексия гипофиза у женщины с акромегалией, оперированной во время беременности трансфеноидальным доступом. Междунар. Дж. Гинекол. Обст. 34 , 71–74 (1991).
КАС пабмед Google Scholar
Атмака А., Дагделен С. и Эрбас Т. Наблюдение за беременными женщинами с акромегалией: различные проявления и исходы. Экспл. клин. Эндокринол. Диабет 114 , 135–139 (2006).
КАС пабмед Google Scholar
Cozzi, R., Attanasio, R. & Barausse, M. Беременность при акромегалии: опыт одного центра. евро. Дж. Эндокринол. 155 (2), 279–284 (2006).
КАС пабмед Google Scholar
Леунг, К.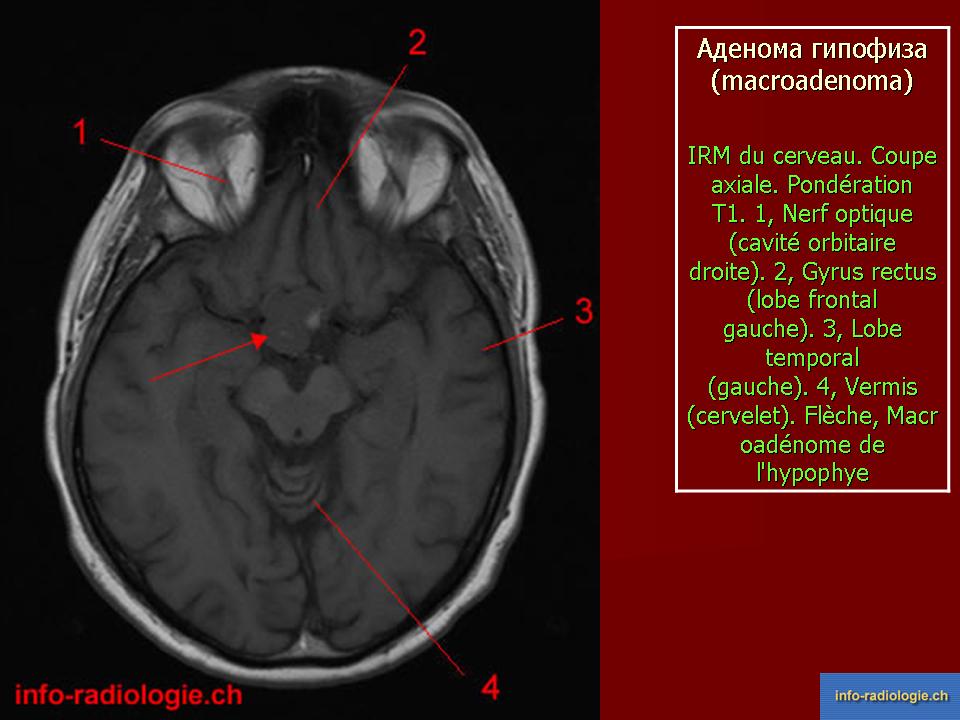 К., Йоханнссон, Г., Леонг, Г. М. и Хо, К. К. Эстрогеновая регуляция действия гормона роста. Эндокр. Ред. 25 , 693–721 (2004).
К., Йоханнссон, Г., Леонг, Г. М. и Хо, К. К. Эстрогеновая регуляция действия гормона роста. Эндокр. Ред. 25 , 693–721 (2004).
КАС пабмед Google Scholar
Обуоби К. и др. . Синдром МакКьюна-Олбрайта: динамика гормона роста при беременности. Дж. Клин. Эндокринол. Метаб. 86 , 2456–2458 (2001).
КАС пабмед Google Scholar
Герман-Бонерт В., Селиверстов М.& Melmed, S. Беременность при акромегалии: успешный терапевтический результат. Дж. Клин. Эндокринол. Метаб. 83 , 727–731 (1998).
КАС пабмед Google Scholar
Абелов, В. А., Рупп, Дж. Дж. и Пашкис, К. Е. Акромегалия и беременность. Дж. Клин. Эндокринол. Метаб. 14 , 32–44 (1954).
КАС пабмед Google Scholar
Куреши А. и др. . ЭКО/ИКСИ у женщины с активной акромегалией: успешный результат лечения пегвисомантом. Дж. Ассист. Воспр. Жене. 23 , 439–442 (2006).
и др. . ЭКО/ИКСИ у женщины с активной акромегалией: успешный результат лечения пегвисомантом. Дж. Ассист. Воспр. Жене. 23 , 439–442 (2006).
ПабМед ПабМед Центральный Google Scholar
Гювен С. и др. . Случай акромегалии при беременности: сочетанная трансфеноидальная аденомэктомия и кесарево сечение. Дж. Матерн. Фетальная неонатальная мед. 19 , 69–71 (2006).
ПабМед Google Scholar
Shnider, S.M. & Levinson, G. in Anesthesia for Obstetrics 4th edn Vol. 2 гл. 29 (изд. Миллер, Р. Д.) 509–528 (Lippincott Williams & Wilkins, 2002).
Google Scholar
Caron, P., Gerbeau, C. & Pradayrol, L. Передача октреотида от матери к плоду. Н. англ. Дж. Мед. 333 , 601–602 (1995).
КАС пабмед Google Scholar
Caron, P. , Gerbeau, C., Pradayrol, L., Cimonetta, C. & Bayard, F. Успешная беременность у бесплодной женщины с тиреотропин-секретирующей макроаденомой, получавшей лечение аналогом соматостатина (октреотид). Дж. Клин. Эндокринол. Метаб. 81 , 1164–1168 (1996).
, Gerbeau, C., Pradayrol, L., Cimonetta, C. & Bayard, F. Успешная беременность у бесплодной женщины с тиреотропин-секретирующей макроаденомой, получавшей лечение аналогом соматостатина (октреотид). Дж. Клин. Эндокринол. Метаб. 81 , 1164–1168 (1996).
КАС пабмед Google Scholar
Карон, П. и др. . Экспрессия рецептора соматостатина SST4 в плаценте человека и отсутствие влияния октреотида на концентрацию плацентарного гормона роста человека во время беременности. Дж. Клин. Эндокринол. Метаб. 82 , 3771–3776 (1997).
КАС пабмед Google Scholar
Маффеи, П. и др. . Эффекты воздействия октреотида во время беременности при акромегалии. клин. Эндокринол. (Оксф.) 72 , 668–677 (2010).
КАС Google Scholar
Цаликян, Э. , Фоли, Т. П. младший и Беккер, Д. Дж. Характеристика специфического связывания соматостатина в плазматических мембранах плаценты человека. Педиатр. Рез. 18 , 953–957 (1984).
, Фоли, Т. П. младший и Беккер, Д. Дж. Характеристика специфического связывания соматостатина в плазматических мембранах плаценты человека. Педиатр. Рез. 18 , 953–957 (1984).
КАС пабмед Google Scholar
Фасснахт, М., Капеллер, Б., Арльт, В., Steck, T. & Allolio, B. Лечение октреотидом LAR на протяжении всей беременности у женщин с акромегалией. клин. Эндокринол. (Oxf.) 5 5 , 411–415 (2001).
Google Scholar
Бигацци, М. и др. . Беременность у женщины с акромегалией во время лечения бромокриптином: влияние на гормон роста и пролактин в материнском, плодном и амниотическом отделах. Дж. Клин. Эндокринол.Метаб. 48 , 9–12 (1979).
КАС пабмед Google Scholar
Аоно Т., Шиодзи Т., Коно М., Уэда Г. и Курачи К. Беременность после индуцированной 2-бром-альфа-эргокриптином (CB-154) овуляции у пациентки с акромегалией с галактореей и аменореей. Фертил. Стерильно. 27 , 341–344 (1976).
Фертил. Стерильно. 27 , 341–344 (1976).
КАС пабмед Google Scholar
Эсперсен Т.и Дитцель, Дж. Беременность и роды при терапии бромокриптином. Ланцет 2 , 985–986 (1977).
КАС пабмед Google Scholar
Любошицки Р., Дикштейн Г. и Барзилай Д. Беременность, индуцированная бромкриптином, у пациентки с акромегалией. JAMA 244 , 584–586 (1980).
КАС пабмед Google Scholar
Хисано, М. и др. . Акромегалия у женщины впервые диагностирована во время беременности. Арх. Гинекол. Обст. 274 , 171–173 (2005).
ПабМед Google Scholar
Брайан С.Р., Бидлингмайер М., Вайнрайч М.П., Вайнцимер С.А. и Инзукки С.Е. Лечение акромегалии пегвисомантом во время беременности: влияние на мать и плод. Дж. Клин. Эндокринол. Метаб. 92 , 3374–3377 (2007).
Дж. Клин. Эндокринол. Метаб. 92 , 3374–3377 (2007).
КАС пабмед Google Scholar
Вилар Л., Фрейташ Мда. C., Lima, LH, Lyra, R. & Kater, CE Синдром Кушинга при беременности: обзор. Арк. Бюстгальтеры. Эндокринол. Метабол. 51 , 1293–1302 (2007).
ПабМед Google Scholar
Hunt, A.B. & McConahey, W.M. Беременность, связанная с заболеванием надпочечников. утра. Дж. Обст. Гинекол. 66 , 970–987 (1953).
КАС пабмед Google Scholar
Buescher, M.A., McClamrock, H.D. & Adashi, E.Y. Синдром Кушинга при беременности. Акушерство. Гинекол. 79 , 130–137 (1992).
КАС пабмед Google Scholar
Пикард, Дж., Йохен, А.Л., Садур, К.Н. и Хофельдт, Ф.Д. Синдром Кушинга при беременности. Акушерство. Гинекол. Surv. 45 , 87–93 (1990).
Акушерство. Гинекол. Surv. 45 , 87–93 (1990).
КАС пабмед Google Scholar
Клибански, А., Стивен, А. Э., Грин, М. Ф., Блейк, М. А. и Ву, К. Л. История болезни Массачусетской больницы общего профиля. Дело 36–2006. Беременная 35 лет с впервые выявленной артериальной гипертензией. Н. англ. Дж. Мед. 355 , 2237–2245 (2006).
КАС пабмед Google Scholar
Кохаде, К. и др. . Эктопический синдром Кушинга вследствие феохромоцитомы: новый послеродовой случай и обзор литературы. Гинекол. Эндокринол. 25 , 624–627 (2009).
ПабМед Google Scholar
Чуй, М. Х. и др. . Отчет о клиническом случае: избыточная экспрессия надпочечниковых рецепторов ЛГ/ХГЧ и амплификация гена, вызывающая индуцированный беременностью синдром Кушинга.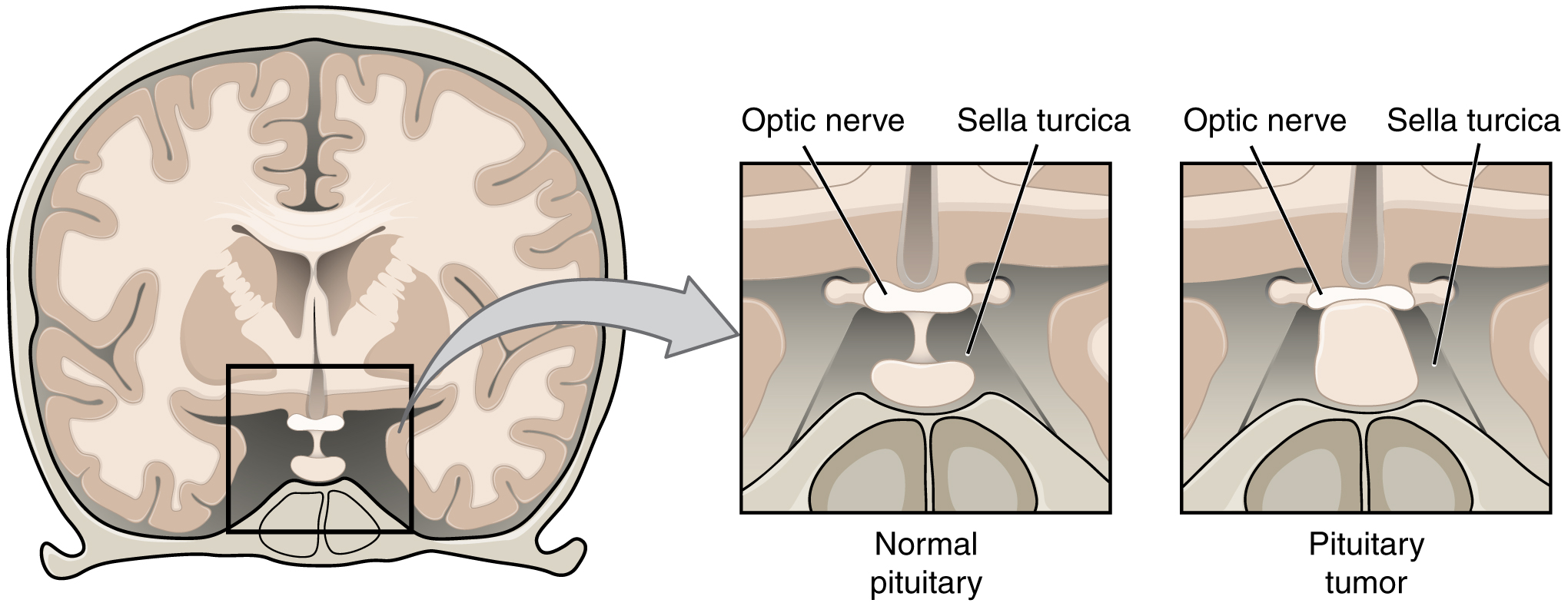 Эндокр. Патол. 20 , 256–261 (2009).
Эндокр. Патол. 20 , 256–261 (2009).
ПабМед Google Scholar
Арон Д. К., Шналль А. М. и Шилер Л. Р. Синдром Кушинга и беременность. утра. Дж. Обст. Гинекол. 162 , 244–252 (1990).
КАС пабмед Google Scholar
Линдсей, Дж. Р., Джонклаас, Дж., Олдфилд, Э. Х. и Ниман, Л. К. Синдром Кушинга во время беременности: личный опыт и обзор литературы. Дж. Клин. Эндокринол. Метаб. 90 , 3077–3083 (2005).
КАС пабмед Google Scholar
Линдси, Дж. Р. и Ниман, Л. К. Гипоталамо-гипофизарно-надпочечниковая ось во время беременности: проблемы выявления и лечения заболеваний. Эндокр. Ред. 26 , 775–799 (2005).
КАС пабмед Google Scholar
Бронштейн М.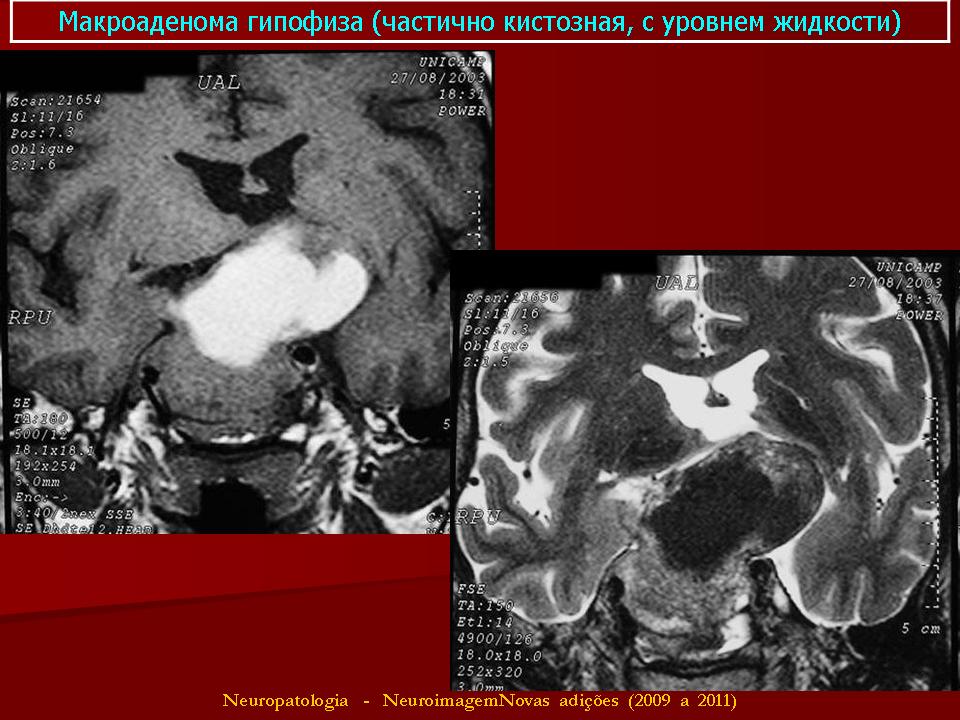 Д., Сальгадо, Л. Р. и де Кастро Мусолино, Н. Р. Медикаментозное лечение аденомы гипофиза: особый случай ведения беременной женщины. Гипофиз 5 , 99–107 (2002).
Д., Сальгадо, Л. Р. и де Кастро Мусолино, Н. Р. Медикаментозное лечение аденомы гипофиза: особый случай ведения беременной женщины. Гипофиз 5 , 99–107 (2002).
КАС пабмед Google Scholar
Кабесон, К., Бруно, О.Д., Коэн, М., Гарсия, С. и Гутман, Р.А. Двойная беременность у пациентки с болезнью Кушинга. Фертил. Стерильно. 72 , 371–372 (1999).
ПабМед Google Scholar
Росс, Р. Дж. и др. . Диагностика и селективное лечение болезни Кушинга при беременности методом транссфеноидальной хирургии. евро. Дж. Эндокринол. 132 , 722–726 (1995).
КАС пабмед Google Scholar
Меллор, А., Харви, Р. Д., Поберескин, Л. Х. и Снейд, Дж. Р. Болезнь Кушинга лечится транссфеноидальной селективной аденомэктомией в середине беременности. руб. Дж. Анаст. 80 , 850–852 (1998).
руб. Дж. Анаст. 80 , 850–852 (1998).
КАС пабмед Google Scholar
Lo, C.Y., Lo, C.M. & Lam, K.Y. Синдром Кушинга, вторичный по отношению к аденоме надпочечников во время беременности. Хирург. Эндоск. 16 , 219–220 (2002).
КАС пабмед Google Scholar
Бертанья, X., Гинья, Л., Груссен, Л.& Bertherat, J. Болезнь Кушинга. Лучшая практика. Рез. клин. Эндокринол. Метаб. 23 , 607–623 (2009).
КАС пабмед Google Scholar
Коннелл, Дж. М. и др. . Беременность, осложненная синдромом Кушинга: потенциальная опасность терапии метирапоном (клинический случай). руб. Дж. Обст. Гинеколь. 92 , 1192–1195 (1985).
КАС пабмед Google Scholar
Хана, В. , Докупилова М., Марек Дж. и Плавка Р. Рецидивирующий АКТГ-независимый синдром Кушинга при многоплодной беременности и его лечение метирапоном. клин. Эндокринол. (Оксф.). 54 , 277–281 (2001).
, Докупилова М., Марек Дж. и Плавка Р. Рецидивирующий АКТГ-независимый синдром Кушинга при многоплодной беременности и его лечение метирапоном. клин. Эндокринол. (Оксф.). 54 , 277–281 (2001).
ПабМед Google Scholar
Уоллес К., Тот Э. Л., Леванчук Р. З. и Симиноски К. Синдром Кушинга, вызванный беременностью, при многоплодной беременности. Дж. Клин. Эндокринол. Метаб. 81 , 15–21 (1996).
КАС пабмед Google Scholar
Амадо, Дж. А. и др. . Успешное лечение кетоконазолом синдрома Кушинга при беременности. Аспирантура. Мед. J. 66 , 221–223 (1990).
КАС пабмед ПабМед Центральный Google Scholar
Berwaerts, J., Verhelst, J., Mahler, C. & Abs, R. Синдром Кушинга при беременности, лечение кетоконазолом: клинический случай и обзор литературы. Гинекол. Эндокринол. 1 3 , 175–182 (1999).
Гинекол. Эндокринол. 1 3 , 175–182 (1999).
Google Scholar
Serafini, P., Motta, E.L.A. & White, J.S. в Опухоли гипофиза при беременности 2nd edn Ch. 4 (изд. Бронштейн, доктор медицины) 173–194 (Kluwer Academic Publishers, 2001).
Google Scholar
Масдинг, М. Г., Лиз, П. Д., Гон-Кейн, М. Л. и Сандеман, Д.D. Сдавление поля зрения несекретирующей опухолью гипофиза во время беременности. J. R. Soc. Мед. 96 , 27–28 (2003).
КАС пабмед ПабМед Центральный Google Scholar
Caron, P., Gerbeau, C., Pradayrol, L., Simonetta, C. & Bayard, F. Успешная беременность у бесплодной женщины с тиреотропин-секретирующей макроаденомой, получавшей лечение аналогом соматостатина (октреотид). Дж. Клин. Эндокринол.Метаб. 81 , 1164–1168 (1996).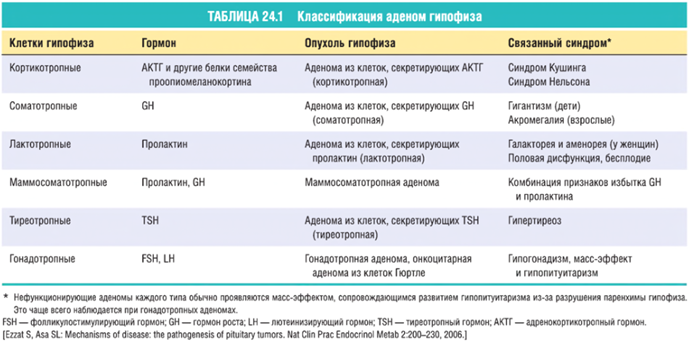
КАС пабмед Google Scholar
Блэкхерст, Г. и др. . Лечение макроаденомы гипофиза, секретирующей тиреотропин, октреотидом при беременности двойней. клин. Эндокринол. (Oxf.) 57 , 401–404 (2002).
КАС Google Scholar
Чайамнуай С., Мостер М., Кац, М. Р. и Ким, Ю. Н. Успешное лечение беременной женщины с аденомой гипофиза, секретирующей ТТГ, с помощью хирургического и медикаментозного лечения. Гипофиз 6 , 109–113 (2003).
ПабМед Google Scholar
Гонсалес, Дж. Г. и др. . Рост гипофиза во время нормальной беременности: исследование in vivo с использованием магнитно-резонансной томографии. утра. Дж. Мед. 85 , 217–220 (1988).
КАС пабмед Google Scholar
Глезер А. и др. . Макропролактин человека проявляет низкую биологическую активность через свой гомологичный рецептор в новом чувствительном биологическом анализе. Дж. Клин. Эндокринол. Метаб. 91 , 1048–1055 (2006).
и др. . Макропролактин человека проявляет низкую биологическую активность через свой гомологичный рецептор в новом чувствительном биологическом анализе. Дж. Клин. Эндокринол. Метаб. 91 , 1048–1055 (2006).
КАС пабмед Google Scholar
Лечение пролактином во время беременности
Front Endocrinol (Лозанна).2015 г.; 6: 85.
, 1, 2, * , 1, , 2 , 3 , 1 , 1 , 1, 2 и 1Mussa Hussain Almalki
1 Центр ожирения, эндокринной системы и обмена веществ, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия
2 Медицинский колледж, Медицинский городок короля Фахда, Университет медицинских наук имени короля Сауда бин Абдулазиза, Эр-Рияд, Саудовская Аравия
Saad Alzahrani
1 Центр ожирения, эндокринной системы и метаболизма, Медицинский центр короля Фахда, Эр-Рияд, Саудовская Аравия
2 Медицинский колледж, Медицинский городок короля Фахда, Университет медицинских наук имени короля Сауда бин Абдулазиза , Эр-Рияд, Саудовская Аравия
Fahad Alshahrani
3 Медицинский колледж, Медицинский город короля Абдулазиза, Университет медицинских наук имени короля Сауда бин Абдулазиза, Эр-Рияд, Саудовская Аравия
Safia Alsherbeni
1 Центр ожирения, эндокринной системы и обмена веществ, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия
Охуд Альмохариб
1 Центр ожирения, эндокринной системы и обмена веществ, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия 99106 Naji Aljohani
1 Центр ожирения, эндокринной системы и метаболизма, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия
2 Медицинский колледж, Медицинский городок короля Фахда, Университет медицинских наук имени короля Сауда бин Абдулазиза, Эр-Рияд, Саудовская Аравия Arabia
Abdurahman Almagamsi
1 Центр ожирения, эндокринной системы и метаболизма, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия
1 Центр ожирения, эндокринной системы и метаболизма, Медицинский городок короля Фахада, Саудовская Аравия, Эр-Рияд 906
2 Медицинский колледж, Медицинский городок имени короля Фахда, Университет медицинских наук имени короля Сауда бин Абдель Азиза, Эр-Рияд, Саудовская Аравия
3 903 67 Медицинский колледж, Медицинский город короля Абдулазиза, Университет медицинских наук имени короля Сауда бин Абдулазиза, Эр-Рияд, Саудовская Аравия
Под редакцией: Корин Бадиу, Медицинский и фармацевтический университет Кэрол Давила, Румыния
Рецензент: Акира Симацу, Национальная больница организация Киотский медицинский центр, Япония; Хиденори Фукуока, университетская больница Кобе, Япония; Jacqueline Trouillas, Университет Лиона 1, Франция,
. oohay@iklam2m
oohay@iklam2mСпециализированный раздел: Эта статья была отправлена в Pituitary Endocrinology, раздел журнала Frontiers in Endocrinology
Поступила в редакцию 7 марта 2015 г.; Принято 10 мая 2015 года.
Copyright © 2015 Алмалки, Альзахрани, Альшахрани, Альшербени, Альмохариб, Алджохани и Алмагамси.Это статья с открытым доступом, распространяемая на условиях лицензии Creative Commons Attribution License (CC BY). Использование, распространение или воспроизведение на других форумах разрешено при условии указания автора(ов) или лицензиара оригинала и ссылки на оригинальную публикацию в этом журнале в соответствии с общепринятой академической практикой.Запрещается использование, распространение или воспроизведение без соблюдения этих условий.
Эта статья была процитирована другими статьями в PMC.Abstract
Пролактиномы являются наиболее распространенными функциональными доброкачественными опухолями гипофиза, обусловленными микро- или макроаденомами гипофиза.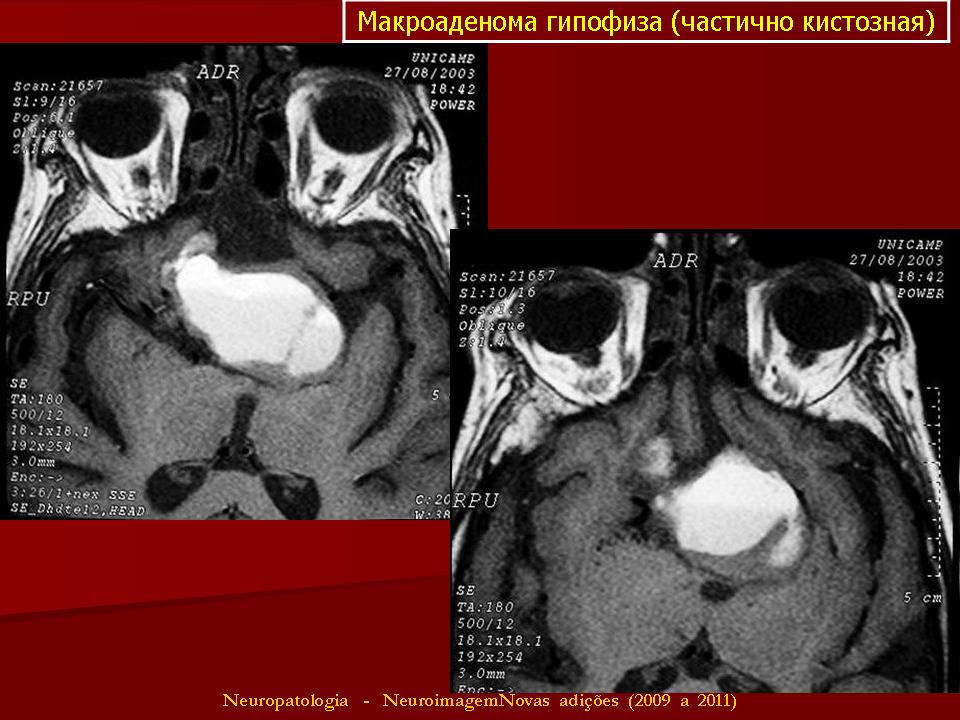 У большинства больных наблюдается бесплодие и дисфункция гонад. Агонисты дофамина (ДА) (бромокриптин или каберголин) являются препаратами выбора, которые могут нормализовать уровень пролактина, уменьшить размер опухоли и восстановить овуляцию и фертильность.Каберголин обычно предпочтительнее бромокриптина из-за его более высокой эффективности и переносимости. Лечение пролактином во время беременности может быть сложной задачей. Во время беременности гипофиз подвергается глобальной гиперплазии из-за прогрессирующего повышения уровня эстрогенов в сыворотке крови, что может привести к увеличению объема опухоли с потенциальным эффектом массы и потерей зрения. Риск роста опухоли может возникать у 3% пациентов с микроаденомами, у 32% пациентов с ранее не оперированными макроаденомами и 4.8% пациентов с макроаденомами с предшествующим абляционным лечением. Хотя оба препарата кажутся безопасными во время беременности, данные о воздействии DA на плод во время беременности при применении бромокриптина намного превышают таковые при применении каберголина без связи с повышенным риском невынашивания беременности и преждевременных родов.
У большинства больных наблюдается бесплодие и дисфункция гонад. Агонисты дофамина (ДА) (бромокриптин или каберголин) являются препаратами выбора, которые могут нормализовать уровень пролактина, уменьшить размер опухоли и восстановить овуляцию и фертильность.Каберголин обычно предпочтительнее бромокриптина из-за его более высокой эффективности и переносимости. Лечение пролактином во время беременности может быть сложной задачей. Во время беременности гипофиз подвергается глобальной гиперплазии из-за прогрессирующего повышения уровня эстрогенов в сыворотке крови, что может привести к увеличению объема опухоли с потенциальным эффектом массы и потерей зрения. Риск роста опухоли может возникать у 3% пациентов с микроаденомами, у 32% пациентов с ранее не оперированными макроаденомами и 4.8% пациентов с макроаденомами с предшествующим абляционным лечением. Хотя оба препарата кажутся безопасными во время беременности, данные о воздействии DA на плод во время беременности при применении бромокриптина намного превышают таковые при применении каберголина без связи с повышенным риском невынашивания беременности и преждевременных родов.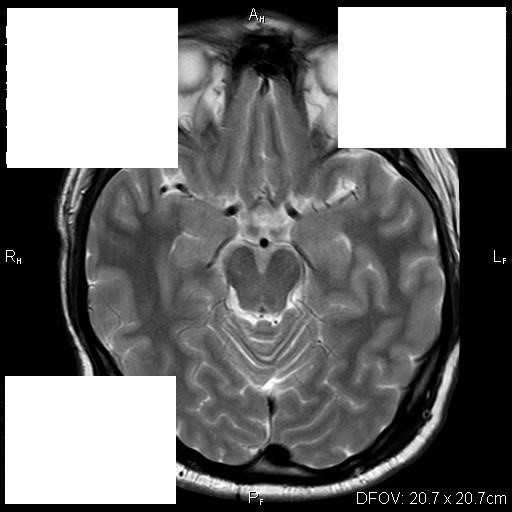 Рекомендуется прекратить использование DA сразу же после подтверждения беременности, за исключением женщин с инвазивными макропролактиномами или симптомами сдавления. В этом обзоре описывается терапевтический подход к пролактиноме во время беременности с акцентом на безопасность доступной терапии DA.
Рекомендуется прекратить использование DA сразу же после подтверждения беременности, за исключением женщин с инвазивными макропролактиномами или симптомами сдавления. В этом обзоре описывается терапевтический подход к пролактиноме во время беременности с акцентом на безопасность доступной терапии DA.
Ключевые слова: пролактин, опухоль гипофиза, агонист дофамина, беременность и исход около 40% всех аденом гипофиза (1). Производство и высвобождение пролактина опосредовано тоническим ингибированием дофамином, секретируемым гипоталамусом. Молочная железа является основной тканью-мишенью для пролактина, но рецепторы пролактина были обнаружены в нескольких тканях, включая печень, яичники, яички и предстательную железу (2).Основное действие пролактина заключается в инициации и поддержании лактации, но он может действовать как фактор роста, нейротрансмиттер или иммунорегулятор через аутокринные или паракринные механизмы (3).
Пролактиномы являются одной из причин гиперпролактинемии, состояния, при котором 90% составляют межселлярные аденомы и 10% — макроаденомы (≥10 мм) (4). Пролактиномы встречаются с распространенностью 60–100 случаев на миллион (1). Чаще встречается у женщин, особенно в репродуктивном периоде.Самый высокий уровень заболеваемости был обнаружен у женщин в возрасте от 25 до 34 лет: 23,9/100 000 человеко-лет (4). У женщин пролактиномы обычно представляют собой микроаденомы (<10 мм) с высоким уровнем пролактина, что приводит к аменорее, галакторее и бесплодию. Мужчины с пролактиномами часто имеют симптомы масс-эффекта, такие как головная боль и потеря зрения, а иногда и гипогонадизм и бесплодие. Потеря костной массы может возникать как долгосрочное последствие гиперпролактинемии как у мужчин, так и у женщин.
Пролактиномы встречаются с распространенностью 60–100 случаев на миллион (1). Чаще встречается у женщин, особенно в репродуктивном периоде.Самый высокий уровень заболеваемости был обнаружен у женщин в возрасте от 25 до 34 лет: 23,9/100 000 человеко-лет (4). У женщин пролактиномы обычно представляют собой микроаденомы (<10 мм) с высоким уровнем пролактина, что приводит к аменорее, галакторее и бесплодию. Мужчины с пролактиномами часто имеют симптомы масс-эффекта, такие как головная боль и потеря зрения, а иногда и гипогонадизм и бесплодие. Потеря костной массы может возникать как долгосрочное последствие гиперпролактинемии как у мужчин, так и у женщин.
Агонисты дофамина (ДА) все чаще используются в качестве средств выбора для лечения пролактином, поскольку они нормализуют уровень пролактина и приводят к уменьшению размеров опухоли. Хирургия в настоящее время зарезервирована для резистентности или непереносимости DA, в то время как лучевая терапия используется только в случаях хирургической неудачи или резистентности к DA.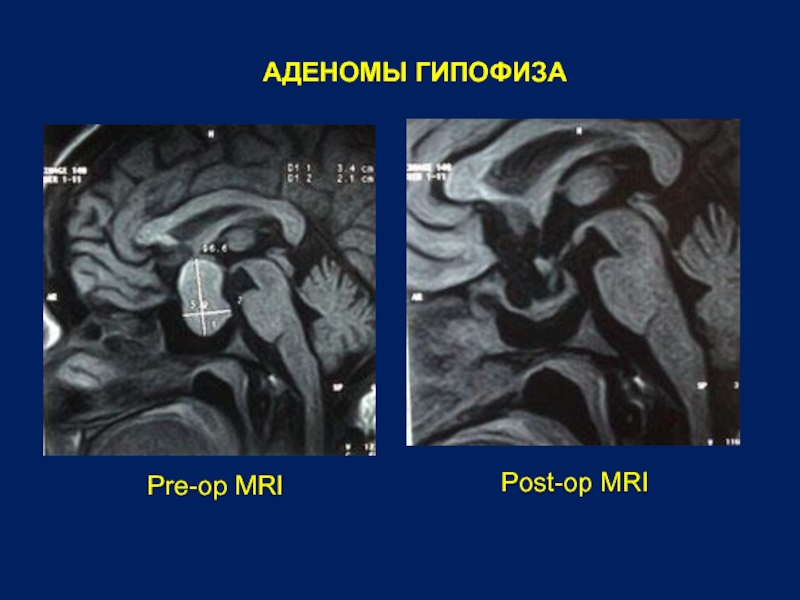
Во время беременности гипофиз подвергается глобальной гиперплазии из-за прогрессирующего повышения уровня эстрогенов в сыворотке крови, что может привести к увеличению объема опухоли с потенциальным эффектом массы и потерей зрения, что представляет собой серьезную проблему для эндокринологов.
Пролактинома во время беременности
Опухолевые клетки у пациентов с пролактиномами экспрессируют рецепторы эстрогена; в результате повышенного уровня эстрогена во время беременности (5) может наблюдаться значительное увеличение объема пролактиномы с прогрессирующим повышением уровня пролактина в сыворотке вследствие гиперплазии лактотрофных клеток (6). Основной проблемой является возможное увеличение опухоли во время беременности. Установлено, что риск увеличения опухоли во время беременности зависит от размера опухоли. Имеющиеся в литературе данные указывают на то, что, хотя увеличение опухоли составляет всего 3% для микропролактином, оно достигает 32% для макропролактином, которые ранее не оперировались (7).
Магнитно-резонансная томография (МРТ) должна быть проведена до зачатия, чтобы задокументировать размер опухоли и служить базой для сравнения с МРТ, проведенной во время беременности. Кроме того, МРТ помогает отличить кровоизлияние в опухоль от простого увеличения опухоли во время беременности (8).
Хотя было обнаружено, что пролактиномы поддаются медикаментозному лечению во время беременности, особенно с помощью DA, таких как бромокриптин, недостаточно данных о безопасности, чтобы рекомендовать рутинное использование этих препаратов во время беременности.Клинические рекомендации общества эндокринологов по ведению и лечению пролактином рекомендуют прекращение приема DA вскоре после подтверждения беременности, за исключением женщин с инвазивными макропролактиномами (5).
Бромокриптин является производным эрголина, агонистом дофаминовых D2-рецепторов с агонистическими и антагонистическими свойствами в отношении D1-рецепторов. Обычно требуется многократный прием в течение дня из-за короткого периода полувыведения (9–11). У женщин, принимающих бромокриптин на ранних сроках беременности, частота абортов, внематочной беременности или врожденных пороков развития не выше, чем в общей популяции (12).В исследовании 2587 беременных женщин, из которых у 2437 был повышен риск самопроизвольного аборта, врожденных аномалий или многоплодной беременности и не влиял на постнатальное развитие (13). В других исследованиях среди 6329 пациенток, получавших бромокриптин на ранних сроках беременности, риск самопроизвольных абортов составил 9,9%, что не выше, чем в общей популяции (10,9%) (7, 14). Более того, при длительном наблюдении до 9 лет детей, рожденных от матерей, принимавших бромокриптин, не было выявлено неблагоприятного влияния на исходы плода с точки зрения физического развития, а также не выявлено нарушений психомоторного развития [5].5 лет (1–20 лет) наблюдения (15).
У женщин, принимающих бромокриптин на ранних сроках беременности, частота абортов, внематочной беременности или врожденных пороков развития не выше, чем в общей популяции (12).В исследовании 2587 беременных женщин, из которых у 2437 был повышен риск самопроизвольного аборта, врожденных аномалий или многоплодной беременности и не влиял на постнатальное развитие (13). В других исследованиях среди 6329 пациенток, получавших бромокриптин на ранних сроках беременности, риск самопроизвольных абортов составил 9,9%, что не выше, чем в общей популяции (10,9%) (7, 14). Более того, при длительном наблюдении до 9 лет детей, рожденных от матерей, принимавших бромокриптин, не было выявлено неблагоприятного влияния на исходы плода с точки зрения физического развития, а также не выявлено нарушений психомоторного развития [5].5 лет (1–20 лет) наблюдения (15).
Кроме того, оптимальный результат был обнаружен при непрерывном применении бромокриптина на протяжении всей беременности примерно в 100 случаях (16).
Каберголин является дофаминовым производным эрголина с более высокой аффинностью и селективностью в отношении дофаминовых рецепторов D2. Он имеет большую продолжительность действия, что позволяет применять его один или два раза в неделю с лучшей переносимостью и соблюдением пациентом режима лечения (17–20). Более того, частота наступления беременности у бесплодных женщин с пролактиномой выше при применении каберголина, чем при применении бромокриптина (21).
Такие же результаты были получены у женщин, принимавших каберголин до и во время беременности (22, 23). В одном отчете было описано более 800 таких беременностей (24) (из которых примерно 350 были связаны с облучением в течение первых недель беременности) без существенной разницы в частоте самопроизвольных абортов, преждевременных родов, многоплодной беременности или пороков развития новорожденных. 25, 26).
В ретроспективном исследовании 103 беременностей у 90 женщин с гиперпролактинемией и последующем наблюдении за 61 ребенком не было выявлено значительных отклонений, связанных ни с дозами каберголина, ни со временем воздействия (27). Данные 12-летнего наблюдения за детьми, рожденными от матерей, получавших каберголин, не выявили влияния на их постнатальное развитие, такого как физические проблемы или задержка психомоторного развития (28). В соответствии с предыдущими исследованиями результаты метаанализа не показали значительного увеличения риска выкидышей или пороков развития плода при использовании DA (29).
Данные 12-летнего наблюдения за детьми, рожденными от матерей, получавших каберголин, не выявили влияния на их постнатальное развитие, такого как физические проблемы или задержка психомоторного развития (28). В соответствии с предыдущими исследованиями результаты метаанализа не показали значительного увеличения риска выкидышей или пороков развития плода при использовании DA (29).
Хинаголид – это DA, не являющийся спорыньей, с селективным агонистом рецептора допамина-2 и длительным эффектом снижения уровня пролактина. Его обычно принимают один раз в день, и он лучше переносится и имеет удобный график дозирования, чем бромокриптин (13, 30, 31).Он имеет ограниченную безопасность по сравнению с бромокриптином. В обзоре 176 беременностей, при которых применялся хинаголид (в среднем 37 дней), самопроизвольный аборт произошел в 14% случаев, у 1 были преждевременные роды и у 1 была внематочная беременность (13). В другом небольшом исследовании девяти беременностей было два случая лечения двумя хинаголидами без осложнений (31).
У женщин, принимавших хинаголид, было зарегистрировано более 200 беременностей, при этом не было выявлено явных неблагоприятных эффектов на течение беременности или развитие плода (32).
Следовательно, каждая женщина с пролактиномой должна быть осведомлена о естественном течении пролактиномы и должна обсудить свои планы зачатия со своим врачом, чтобы пройти тщательное обследование перед беременностью.
Определение подходящего варианта лечения является индивидуальным выбором, зависящим в основном от размера опухоли. Предлагаемый терапевтический подход показан на рисунке (33). Исходы пролактином после беременности широко обсуждались с различными результатами.Недавнее исследование показало нормализацию уровня пролактина более чем на 40% без медикаментозного лечения при среднем периоде наблюдения 22 месяца после родов и прекращения лактации (34).
Подход к лечению пролактином во время беременности .
Лечение микропролактином во время беременности
Микропролактиномы у небеременных женщин обычно имеют доброкачественное течение. Риск значительного бессимптомного роста опухоли во время беременности составляет 4,5% (35), а симптоматического роста опухоли <2% (36).Риск развития новых неврологических осложнений (головные боли, сдавление зрительного нерва и др.) колеблется от 1,6 до 5,5% (37). Пролактин имеет тенденцию к увеличению во время беременности; следовательно, он не отражает достоверно увеличение размера опухоли и бесполезен для клинической оценки.
Риск значительного бессимптомного роста опухоли во время беременности составляет 4,5% (35), а симптоматического роста опухоли <2% (36).Риск развития новых неврологических осложнений (головные боли, сдавление зрительного нерва и др.) колеблется от 1,6 до 5,5% (37). Пролактин имеет тенденцию к увеличению во время беременности; следовательно, он не отражает достоверно увеличение размера опухоли и бесполезен для клинической оценки.
В связи с очень низким риском увеличения микропролактиномы во время беременности имеются убедительные данные, подтверждающие необходимость прекращения лечения ДА после подтверждения беременности. Пациентке следует сообщить, что риск увеличения аденомы во время беременности очень мал, и при появлении симптомов медикаментозное лечение, скорее всего, будет эффективным.
При появлении необычных симптомов, таких как сильная головная боль или нарушение зрения, пациенту следует обратиться для срочного обследования, чтобы исключить возможность увеличения опухоли. Серийное определение пролактина не требуется из-за высокой изменчивости пролактина во время беременности (38).
Серийное определение пролактина не требуется из-за высокой изменчивости пролактина во время беременности (38).
Во время постановки диагноза пациентка должна пройти базовое официальное тестирование поля зрения и проходить клиническое наблюдение каждые 2–3 месяца во время беременности (33), но серийные МРТ-исследования или тестирование поля зрения во время беременности не требуются.Однако нет данных, подтверждающих вред для плода ни от МРТ, ни от гадолиния (8).
Если у пациента появляются симптомы нарушения зрения или прогрессирующие головные боли, следует выполнить МРТ без гадолиния (не КТ) для оценки изменений размера опухоли (39).
Если очевиден значительный рост опухоли, следует немедленно возобновить прием DA бромокриптина (36), поскольку в таких случаях он является препаратом первого выбора.
У женщин, у которых симптомы не проявляются на протяжении всей беременности, следует измерить уровень пролактина в сыворотке через 2 месяца после родов или прекращения кормления грудью, и, если он аналогичен значению до лечения, следует возобновить прием препарата (40). Точно так же женщинам, желающим кормить грудью, следует провести МРТ, чтобы убедиться в стабильности опухоли в течение 4–6 недель после родов (37), поскольку ДА снижают уровень ПРЛ в сыворотке, что впоследствии ухудшает лактацию.
Точно так же женщинам, желающим кормить грудью, следует провести МРТ, чтобы убедиться в стабильности опухоли в течение 4–6 недель после родов (37), поскольку ДА снижают уровень ПРЛ в сыворотке, что впоследствии ухудшает лактацию.
Лечение макропролактином во время беременности
У женщин макропролактиномы встречаются реже, чем микропролактиномы. При макропролактиноме симптоматическое увеличение опухоли наблюдается в 20–30% случаев (41). Сообщалось, что риск клинически значимого увеличения опухоли падает с более чем 30% до <5%, если пациентка подвергается лучевой терапии или хирургическому вмешательству до беременности (25).
Беременные женщины с большими опухолями и женщины с экстраселлярным распространением, которые прекратили прием бромокриптина, подвержены риску роста опухоли, поэтому в каждом триместре необходимо проводить официальное исследование поля зрения. Так же, как и при микропролактиномах, нет необходимости измерять уровень пролактина в сыворотке на протяжении всей беременности, потому что уровни неравномерно увеличиваются во время беременности и не коррелируют с увеличением опухоли (8, 25).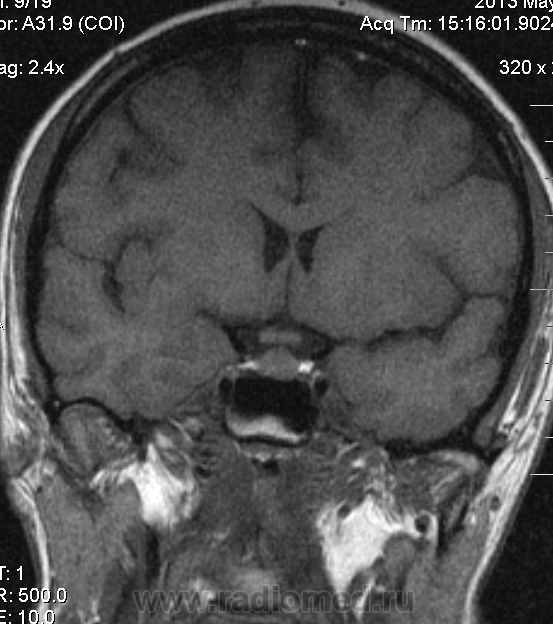 Кроме того, в этих случаях лечение должно быть индивидуализированным, так как данные, сравнивающие различные стратегии лечения, отсутствуют.
Кроме того, в этих случаях лечение должно быть индивидуализированным, так как данные, сравнивающие различные стратегии лечения, отсутствуют.
Пациентка должна быть проинформирована об относительно более высоком риске увеличения опухоли, необходимости нормализации уровня пролактина и важности лечения до зачатия.
В случае интраселлярных и небольших макропролактином, которые не прилегают к перекресту зрительных нервов, прием ДА следует прекратить при подтверждении беременности.
Пациент должен быть проинформирован о симптомах и необходимости срочного обследования при их появлении. В каждом триместре следует проводить тщательный клинический мониторинг с формальным исследованием поля зрения.Если пациент жалуется на головную боль или изменение зрения, следует провести МРТ. Если результаты МРТ подтверждают увеличение опухоли, женщине следует повторно назначить DA (5).
Бромокриптин считается препаратом первого выбора, и он обычно уменьшает размер аденомы и устраняет симптомы (42). Каберголин можно рассмотреть, если аденома не реагирует на бромокриптин (43).
Каберголин можно рассмотреть, если аденома не реагирует на бромокриптин (43).
Если увеличенная опухоль не отвечает на терапию каберголином, альтернативы включают транссфеноидальную операцию во втором триместре или родоразрешение, если беременность находится на достаточном сроке (16, 25, 41).
Пациентам с большими макропролактиномами и пациентам с экстраселлярным распространением настоятельно не рекомендуется забеременеть до тех пор, пока не будет проведена радикальная терапия. Терапию с хирургическим уменьшением объема можно рассмотреть до беременности, поскольку было показано, что хирургическое вмешательство или лучевая терапия снижают риск симптоматического увеличения опухоли (25), но в этих случаях существует высокий риск гипопитуитаризма. Однако операция по удалению опухоли менее предпочтительна, поскольку медикаментозная терапия во время беременности, вероятно, менее вредна, чем операция (41).Женщины с пролактиномами, устойчивыми к DA, обычно бесплодны. Таким образом, беременность в этих случаях является неожиданной, если они не подвергаются стимуляции яичников гонадотропинами или ГнРГ. Более того, беременность не рекомендуется женщинам с большими макропролактиномами, резистентными к лекарственным препаратам, и они не должны забеременеть, даже если опухоль является интраселлярной, до тех пор, пока размер не будет уменьшен с помощью транссфеноидальной хирургии.
Более того, беременность не рекомендуется женщинам с большими макропролактиномами, резистентными к лекарственным препаратам, и они не должны забеременеть, даже если опухоль является интраселлярной, до тех пор, пока размер не будет уменьшен с помощью транссфеноидальной хирургии.
Хирургическое вмешательство возможно в случаях, когда опухоль не уменьшилась во время медикаментозного лечения DA или у тех, у кого развился рост опухоли во время предыдущей беременности (44).
Влияние беременности и кормления грудью на уровень пролактина, объем опухоли и частоту ремиссий
В современной литературе показано, что беременность вызывает ремиссию гиперпролактинемии у двух третей женщин после прекращения приема ДА. В одном исследовании было обнаружено, что беременность вызывает ремиссию в 76% случаев неопухолевой гиперпролактинемии (NTHP), в 70% случаев микропролактином и в 64% случаев макропролактином с более высокой частотой рецидивов среди пациентов с макропролактиномами и пациентов с микропролактиномами с видимой опухолью на МРТ. на момент прекращения лечения (45).
на момент прекращения лечения (45).
В недавнем исследовании полная ремиссия была обнаружена у 100% пациентов с НТГП, у 66% пациентов с микропролактиномами и у 70% пациентов с макропролактиномами (46). Основные механизмы неясны, но обычно связывают с аутоинфарктом опухоли (46).
С другой стороны, нет данных, позволяющих предположить, что грудное вскармливание связано с повышенной выработкой пролактина или риском увеличения опухоли (28, 46). Таким образом, женщины могли нормально кормить грудью и возобновлять ДА после прекращения лактации.
Заключение
Лечение пролактиномы во время беременности является сложной задачей. Клинические испытания, подчеркивающие результаты медикаментозной терапии по сравнению с другими видами лечения, немногочисленны; поэтому пациент лечится на индивидуальной основе. Исход микроаденомы превосходный, что позволяет пациентам безопасно прекратить прием DA при тщательном клиническом наблюдении; с другой стороны, макроаденому необходимо лечить до зачатия, так как риск увеличения опухоли относительно высок.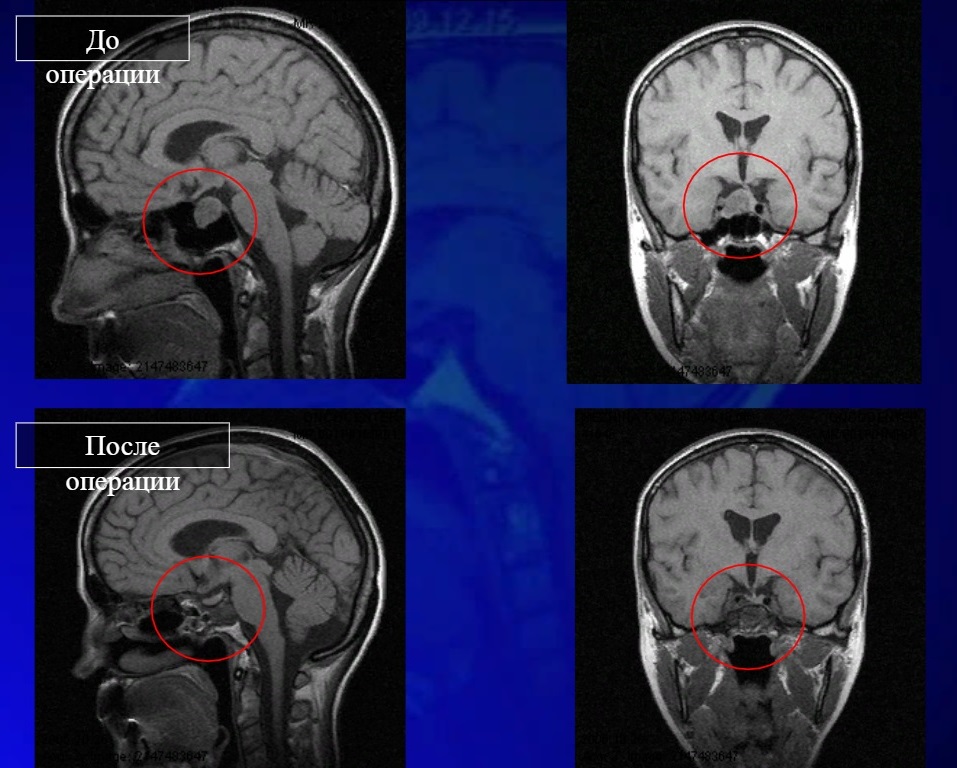
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Ссылки
1. Ciccarelli A, Daly AF, Beckers A. Эпидемиология пролактином. Гипофиз (2005) 8(1):3–6.10.1007/s11102-005-5079-0 [PubMed] [CrossRef] [Google Scholar]2. Индер В.Дж. Гиперпролактинемия – дифференциальный диагноз, обследование и лечение. Eur Endocr Rev (2006): 76–1002. [Google Академия]3. Карс М., Деккерс О.М., Перейра А.М., Ромейн Я.А. Обновление в пролактиномах. Neth J Med (2010) 68 (3): 104–12. [PubMed] [Google Scholar]4. Молич М.Е. пролактинома. гипофиз. Кембридж, Индиана: Наука Блэквелла; (1995).п. 433–77. [Google Академия]5. Мелмед С., Казануева Ф.Ф., Хоффман А.Р., Клейнберг Д.Л., Монтори В.М., Шлехте Дж.А. и соавт. Диагностика и лечение гиперпролактинемии: руководство по клинической практике эндокринологического общества. J Clin Endocrinol Metab (2011) 96(2):273–88. 10.1210/jc.2010-1692 [PubMed] [CrossRef] [Google Scholar]6. Пишон М.Ф., Брессион Д., Пейон Ф., Милгром Э. Рецепторы эстрогена в аденомах гипофиза человека. J Clin Endocrinol Metab (1980) 51(4):897–902.10.1210/jcem-51-4-897 [PubMed] [CrossRef] [Google Scholar]7.Гиллам М.П., Молич М.Е., Ломбарди Г., Колао А.
Достижения в лечении пролактином. Endocr Rev (2006) 27(5):485–534.10.1210/er.2005-9998 [PubMed] [CrossRef] [Google Scholar]8. Молич М.Е. Эндокринология при беременности: ведение беременной с пролактиномой. Eur J Endocrinol (2015) 172(5):R205–13.10.1530/EJE-14-0848 [PubMed] [CrossRef] [Google Scholar]9. Мах П.М., Вебстер Дж.
Гиперпролактинемия: этиология, диагностика и лечение. Semin Reprod Med (2002) 20(4):365–74.10.1055/s-2002-36709 [PubMed] [CrossRef] [Google Scholar]10.Биллер БМ. Гиперпролактинемия. Int J Fertil Womens Med (1999) 44 (2): 74–7. [PubMed] [Google Scholar] 11. Банковский Б.Дж., Закур Х.А.
Терапия агонистами допамина при гиперпролактинемии. Clin Obstet Gynecol (2003) 46(2):349–62.
10.1210/jc.2010-1692 [PubMed] [CrossRef] [Google Scholar]6. Пишон М.Ф., Брессион Д., Пейон Ф., Милгром Э. Рецепторы эстрогена в аденомах гипофиза человека. J Clin Endocrinol Metab (1980) 51(4):897–902.10.1210/jcem-51-4-897 [PubMed] [CrossRef] [Google Scholar]7.Гиллам М.П., Молич М.Е., Ломбарди Г., Колао А.
Достижения в лечении пролактином. Endocr Rev (2006) 27(5):485–534.10.1210/er.2005-9998 [PubMed] [CrossRef] [Google Scholar]8. Молич М.Е. Эндокринология при беременности: ведение беременной с пролактиномой. Eur J Endocrinol (2015) 172(5):R205–13.10.1530/EJE-14-0848 [PubMed] [CrossRef] [Google Scholar]9. Мах П.М., Вебстер Дж.
Гиперпролактинемия: этиология, диагностика и лечение. Semin Reprod Med (2002) 20(4):365–74.10.1055/s-2002-36709 [PubMed] [CrossRef] [Google Scholar]10.Биллер БМ. Гиперпролактинемия. Int J Fertil Womens Med (1999) 44 (2): 74–7. [PubMed] [Google Scholar] 11. Банковский Б.Дж., Закур Х.А.
Терапия агонистами допамина при гиперпролактинемии. Clin Obstet Gynecol (2003) 46(2):349–62. 10.1097/00003081-200306000-00013 [PubMed] [CrossRef] [Google Scholar]12. Krupp P, Monka C. Бромокриптин при беременности: аспекты безопасности. Klin Wochenschr (1987) 65(17):823–7.10.1007/BF01727477 [PubMed] [CrossRef] [Google Scholar]13. Вебстер Дж. Сравнительный обзор профилей переносимости агонистов допамина при лечении гиперпролактинемии и подавлении лактации.Безопасность лекарств (1996) 14(4):228–38.10.2165/00002018-199614040-00003 [PubMed] [CrossRef] [Google Scholar]14. Нюбо Андерсен А.М., Вольфарт Дж., Кристенс П., Олсен Дж., Мелби М. Возраст матери и потеря плода: исследование связи регистров на основе популяции. BMJ (2000) 320(7251):1708–12.10.1136/bmj.320.7251.1708 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]15. Шибли-Рахал А., Шлехте Дж.
Гиперпролактинемия и бесплодие. Endocrinol Metab Clin North Am (2011) 40(4):837–46.10.1016/j.ecl.2011.08.008 [PubMed] [CrossRef] [Google Scholar]16.Хрисулиду А., Будина М., Каравитаки Н., Били Э., Васс Дж.
Гипофизарные нарушения при беременности.
10.1097/00003081-200306000-00013 [PubMed] [CrossRef] [Google Scholar]12. Krupp P, Monka C. Бромокриптин при беременности: аспекты безопасности. Klin Wochenschr (1987) 65(17):823–7.10.1007/BF01727477 [PubMed] [CrossRef] [Google Scholar]13. Вебстер Дж. Сравнительный обзор профилей переносимости агонистов допамина при лечении гиперпролактинемии и подавлении лактации.Безопасность лекарств (1996) 14(4):228–38.10.2165/00002018-199614040-00003 [PubMed] [CrossRef] [Google Scholar]14. Нюбо Андерсен А.М., Вольфарт Дж., Кристенс П., Олсен Дж., Мелби М. Возраст матери и потеря плода: исследование связи регистров на основе популяции. BMJ (2000) 320(7251):1708–12.10.1136/bmj.320.7251.1708 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]15. Шибли-Рахал А., Шлехте Дж.
Гиперпролактинемия и бесплодие. Endocrinol Metab Clin North Am (2011) 40(4):837–46.10.1016/j.ecl.2011.08.008 [PubMed] [CrossRef] [Google Scholar]16.Хрисулиду А., Будина М., Каравитаки Н., Били Э., Васс Дж.
Гипофизарные нарушения при беременности.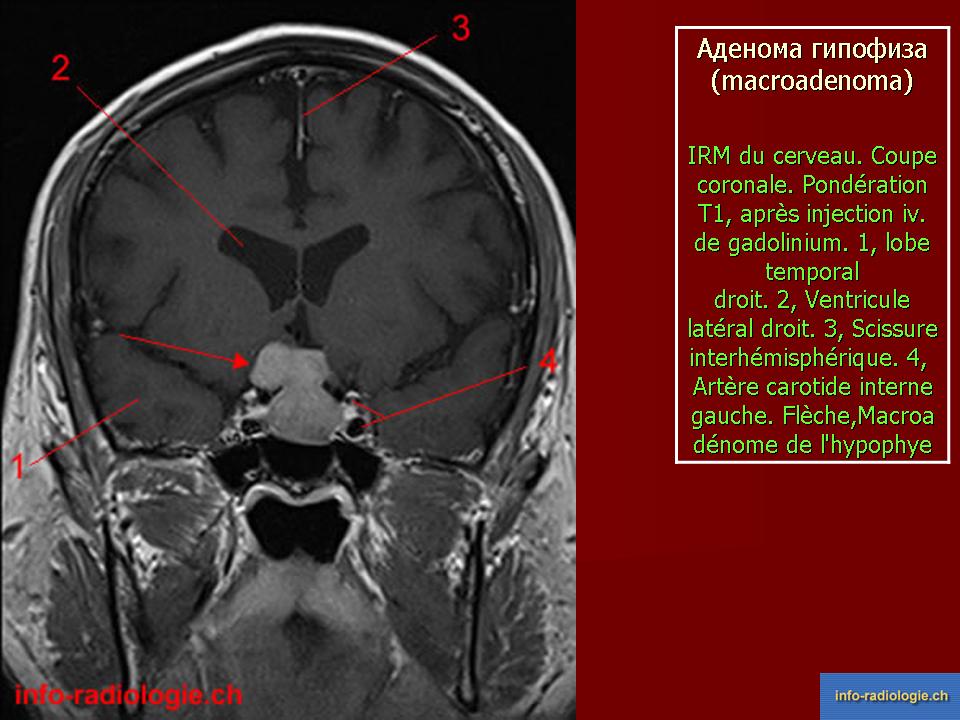 Гормоны (2015) 14(1):70–80.10.14310/horm.2002.1575 [PubMed] [CrossRef] [Google Scholar]17. Колао А., Ди Сарно А., Сарнаккиаро Ф., Фероне Д., Ди Ренцо Г., Мерола Б. и др.
Пролактиномы, резистентные к стандартным агонистам дофамина, реагируют на длительное лечение каберголином. J Clin Endocrinol Metab (1997) 82(3):876–83.10.1210/jcem.82.8.4178-3 [PubMed] [CrossRef] [Google Scholar]18. Verhelst J, Abs R, Maiter D, van den Bruel A, Vandeweghe M, Velkeniers B, et al.Каберголин в лечении гиперпролактинемии: исследование 455 пациентов. J Clin Endocrinol Metab (1999) 84(7):2518–22.10.1210/jcem.84.7.5810 [PubMed] [CrossRef] [Google Scholar]20. Лю Дж.К., Кэдвелл В.Т.
Современное лечение пролактином. Neurosurg Focus (2004) 16(4):E2.10.3171/foc.2004.16.4.3 [PubMed] [CrossRef] [Google Scholar]21. Оно М., Мики Н., Амано К., Кавамата Т., Секи Т., Макино Р. и др.
Индивидуальная терапия высокими дозами каберголина при гиперпролактинемическом бесплодии у женщин с микро- и макропролактиномами.J Clin Endocrinol Metab (2010) 95(6):2672–9.
Гормоны (2015) 14(1):70–80.10.14310/horm.2002.1575 [PubMed] [CrossRef] [Google Scholar]17. Колао А., Ди Сарно А., Сарнаккиаро Ф., Фероне Д., Ди Ренцо Г., Мерола Б. и др.
Пролактиномы, резистентные к стандартным агонистам дофамина, реагируют на длительное лечение каберголином. J Clin Endocrinol Metab (1997) 82(3):876–83.10.1210/jcem.82.8.4178-3 [PubMed] [CrossRef] [Google Scholar]18. Verhelst J, Abs R, Maiter D, van den Bruel A, Vandeweghe M, Velkeniers B, et al.Каберголин в лечении гиперпролактинемии: исследование 455 пациентов. J Clin Endocrinol Metab (1999) 84(7):2518–22.10.1210/jcem.84.7.5810 [PubMed] [CrossRef] [Google Scholar]20. Лю Дж.К., Кэдвелл В.Т.
Современное лечение пролактином. Neurosurg Focus (2004) 16(4):E2.10.3171/foc.2004.16.4.3 [PubMed] [CrossRef] [Google Scholar]21. Оно М., Мики Н., Амано К., Кавамата Т., Секи Т., Макино Р. и др.
Индивидуальная терапия высокими дозами каберголина при гиперпролактинемическом бесплодии у женщин с микро- и макропролактиномами.J Clin Endocrinol Metab (2010) 95(6):2672–9. 10.1210/jc.2009-2605 [PubMed] [CrossRef] [Google Scholar]22. Чиккарелли Э., Гроттоли С., Раззор П., Гайя Д., Бертанья А., Чирилло С. и др.
Длительное лечение каберголином, новым производным эрголина длительного действия, при идиопатической или опухолевой гиперпролактинемии и исходах медикаментозной беременности. J Endocrinol Invest (1997) 20(9):547–51.10.1007/BF03348017 [PubMed] [CrossRef] [Google Scholar]23. Джонс Дж., Башир Т., Олни Дж., Уитли Т.
Лечение каберголином крупной макропролактиномы на протяжении всей беременности.J Obstet Gynaecol (1997) 17(4):375–6.10.1080/01443619750112916 [PubMed] [CrossRef] [Google Scholar]24. Молич М.Е.
Пролактинома при беременности. Best Pract Res Clin Endocrinol Metab (2011) 25(6):885–96.10.1016/j.beem.2011.05.011 [PubMed] [CrossRef] [Google Scholar]25. Мусолино Н.Р., Бронштейн М.Д.
Пролактиномы и беременность. Издательство Kluwer Academic Publishers; (2001). п. 91–108. [Google Академия] 26. Риччи Э., Параццини Ф., Мотта Т., Феррари С.И., Колао А., Клавенна А.
10.1210/jc.2009-2605 [PubMed] [CrossRef] [Google Scholar]22. Чиккарелли Э., Гроттоли С., Раззор П., Гайя Д., Бертанья А., Чирилло С. и др.
Длительное лечение каберголином, новым производным эрголина длительного действия, при идиопатической или опухолевой гиперпролактинемии и исходах медикаментозной беременности. J Endocrinol Invest (1997) 20(9):547–51.10.1007/BF03348017 [PubMed] [CrossRef] [Google Scholar]23. Джонс Дж., Башир Т., Олни Дж., Уитли Т.
Лечение каберголином крупной макропролактиномы на протяжении всей беременности.J Obstet Gynaecol (1997) 17(4):375–6.10.1080/01443619750112916 [PubMed] [CrossRef] [Google Scholar]24. Молич М.Е.
Пролактинома при беременности. Best Pract Res Clin Endocrinol Metab (2011) 25(6):885–96.10.1016/j.beem.2011.05.011 [PubMed] [CrossRef] [Google Scholar]25. Мусолино Н.Р., Бронштейн М.Д.
Пролактиномы и беременность. Издательство Kluwer Academic Publishers; (2001). п. 91–108. [Google Академия] 26. Риччи Э., Параццини Ф., Мотта Т., Феррари С.И., Колао А., Клавенна А. и др.
Исход беременности после лечения каберголином в первые недели гестации.Reprod Toxicol (2002) 16(6):791–3.10.1016/S0890-6238(02)00055-2 [PubMed] [CrossRef] [Google Scholar]27. Сталлдекер Г., Маллеа-Гил М.С., Гительман М., Альфьери А., Балларино М.С., Боэро Л. и др.
Влияние каберголина на беременность и развитие эмбриона и плода: ретроспективное исследование 103 беременностей и обзор литературы. Pituitary (2010) 13(4):345–50.10.1007/s11102-010-0243-6 [PubMed] [CrossRef] [Google Scholar]28. Леббе М., Хубинонт С., Бернард П., Майтер Д. Исход 100 беременностей, начатых при лечении каберголином у женщин с гиперпролактинемией.Clin Endocrinol (2010) 73(2):236–42.10.1111/j.1365-2265.2010.03808.x [PubMed] [CrossRef] [Google Scholar]29. Ван А.Т., Муллан Р.Дж., Лейн М.А., Хазем А., Прасад С., Гатайя Н.В. и др.
Лечение гиперпролактинемии: систематический обзор и метаанализ. Syst Rev (2012) 1:33.10.1186/2046-4053-1-33 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]30. Дюранто Л., Шансон П.
и др.
Исход беременности после лечения каберголином в первые недели гестации.Reprod Toxicol (2002) 16(6):791–3.10.1016/S0890-6238(02)00055-2 [PubMed] [CrossRef] [Google Scholar]27. Сталлдекер Г., Маллеа-Гил М.С., Гительман М., Альфьери А., Балларино М.С., Боэро Л. и др.
Влияние каберголина на беременность и развитие эмбриона и плода: ретроспективное исследование 103 беременностей и обзор литературы. Pituitary (2010) 13(4):345–50.10.1007/s11102-010-0243-6 [PubMed] [CrossRef] [Google Scholar]28. Леббе М., Хубинонт С., Бернард П., Майтер Д. Исход 100 беременностей, начатых при лечении каберголином у женщин с гиперпролактинемией.Clin Endocrinol (2010) 73(2):236–42.10.1111/j.1365-2265.2010.03808.x [PubMed] [CrossRef] [Google Scholar]29. Ван А.Т., Муллан Р.Дж., Лейн М.А., Хазем А., Прасад С., Гатайя Н.В. и др.
Лечение гиперпролактинемии: систематический обзор и метаанализ. Syst Rev (2012) 1:33.10.1186/2046-4053-1-33 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]30. Дюранто Л., Шансон П. , Лавуанн А., Хорле С., Любецки Дж., Кун Дж.М. Влияние нового дофаминергического агониста CV 205-502 на уровни пролактина в плазме и размер опухоли при резистентных к бромокриптину пролактиномах.Clin Endocrinol (1991) 34(1):25–9.10.1111/j.1365-2265.1991.tb01731.x [PubMed] [CrossRef] [Google Scholar]31. Morange I, Barlier A, Pellegrini I, Brue T, Enjalbert A, Jaquet P. Пролактиномы, устойчивые к бромокриптину: долгосрочная эффективность хинаголида и исход беременности. Eur J Endocrinol (1996) 135(4):413–20.10.1530/eje.0.1350413 [PubMed] [CrossRef] [Google Scholar]32. Вебстер Дж.
Клиническое лечение пролактином. Baillieres Best Pract Res Clin Endocrinol Metab (1999) 13(3):395–408.10.1053/beem.1999.0030 [PubMed] [CrossRef] [Google Scholar]34. Domingue ME, Devuyst F, Alexopoulou O, Corvilain B, Maiter D. Исход пролактиномы после беременности и кормления грудью: исследование 73 пациентов. Clin Endocrinol (2014) 80(5):642–8.10.1111/cen.12370 [PubMed] [CrossRef] [Google Scholar]35. Молич М.Е.
Беременность и женщина с гиперпролактинемией.
, Лавуанн А., Хорле С., Любецки Дж., Кун Дж.М. Влияние нового дофаминергического агониста CV 205-502 на уровни пролактина в плазме и размер опухоли при резистентных к бромокриптину пролактиномах.Clin Endocrinol (1991) 34(1):25–9.10.1111/j.1365-2265.1991.tb01731.x [PubMed] [CrossRef] [Google Scholar]31. Morange I, Barlier A, Pellegrini I, Brue T, Enjalbert A, Jaquet P. Пролактиномы, устойчивые к бромокриптину: долгосрочная эффективность хинаголида и исход беременности. Eur J Endocrinol (1996) 135(4):413–20.10.1530/eje.0.1350413 [PubMed] [CrossRef] [Google Scholar]32. Вебстер Дж.
Клиническое лечение пролактином. Baillieres Best Pract Res Clin Endocrinol Metab (1999) 13(3):395–408.10.1053/beem.1999.0030 [PubMed] [CrossRef] [Google Scholar]34. Domingue ME, Devuyst F, Alexopoulou O, Corvilain B, Maiter D. Исход пролактиномы после беременности и кормления грудью: исследование 73 пациентов. Clin Endocrinol (2014) 80(5):642–8.10.1111/cen.12370 [PubMed] [CrossRef] [Google Scholar]35. Молич М.Е.
Беременность и женщина с гиперпролактинемией. N Engl J Med (1985) 312(21):1364–70.10.1056/NEJM198505233122106 [PubMed] [CrossRef] [Google Scholar]36. Куперсмит М.Дж., Розенберг С., Клейнберг Д. Потеря зрения у беременных с аденомами гипофиза.Ann Intern Med (1994) 121(7):473–7.10.7326/0003-4819-121-7-199410010-00001 [PubMed] [CrossRef] [Google Scholar]37. Гемзелл С., Ван С.Ф.
Исход беременности у женщин с аденомой гипофиза. Фертил Стерил (1979) 31 (4): 363–72. [PubMed] [Google Scholar] 38. Шлехте Я.А.
Клиническая практика. пролактинома. N Engl J Med (2003) 349(21):2035–41.10.1056/NEJMcp025334 [PubMed] [CrossRef] [Google Scholar]39. Шлехте Я.А. Длительное лечение пролактином. J Clin Endocrinol Metab (2007) 92(8):2861–5.10.1210/jc.2007-0836 [PubMed] [CrossRef] [Google Scholar]40. Лавэй Б.А., Мир С.А. Беременность и гипофизарные заболевания: проблемы диагностики и лечения. Indian J Endocrinol Metab (2013) 17(6):996–1004.10.4103/2230-8210.122608 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]41. Молич М.Е.
Лечение пролактином во время беременности.
N Engl J Med (1985) 312(21):1364–70.10.1056/NEJM198505233122106 [PubMed] [CrossRef] [Google Scholar]36. Куперсмит М.Дж., Розенберг С., Клейнберг Д. Потеря зрения у беременных с аденомами гипофиза.Ann Intern Med (1994) 121(7):473–7.10.7326/0003-4819-121-7-199410010-00001 [PubMed] [CrossRef] [Google Scholar]37. Гемзелл С., Ван С.Ф.
Исход беременности у женщин с аденомой гипофиза. Фертил Стерил (1979) 31 (4): 363–72. [PubMed] [Google Scholar] 38. Шлехте Я.А.
Клиническая практика. пролактинома. N Engl J Med (2003) 349(21):2035–41.10.1056/NEJMcp025334 [PubMed] [CrossRef] [Google Scholar]39. Шлехте Я.А. Длительное лечение пролактином. J Clin Endocrinol Metab (2007) 92(8):2861–5.10.1210/jc.2007-0836 [PubMed] [CrossRef] [Google Scholar]40. Лавэй Б.А., Мир С.А. Беременность и гипофизарные заболевания: проблемы диагностики и лечения. Indian J Endocrinol Metab (2013) 17(6):996–1004.10.4103/2230-8210.122608 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]41. Молич М.Е.
Лечение пролактином во время беременности.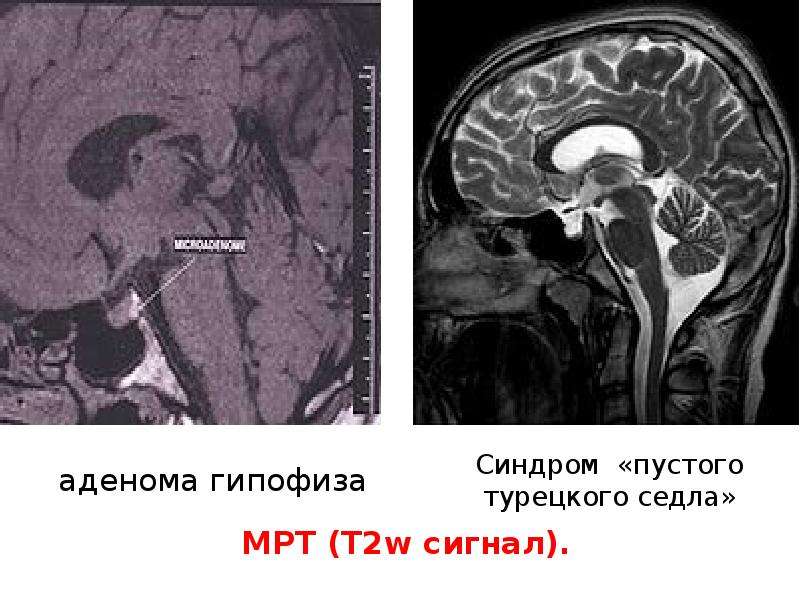 J Reprod Med (1999) 44 (12 Suppl): 1121–6. [PubMed] [Google Scholar]42. ван Роон Э., ван дер Вийвер Дж. К., Герретсен Г., Хекстер Р. Е., Ваттендорф Р. А. Быстрая регрессия супраселлярной пролактиномы после лечения бромокриптином во время беременности.Фертил Стерил (1981) 36 (2): 173–7. [PubMed] [Google Scholar]43. Лю С, Тиррелл Дж.Б. Успешное лечение крупной макропролактиномы каберголином во время беременности. Pituitary (2001) 4(3):179–85.10.1023/A:10153180 [PubMed] [CrossRef] [Google Scholar]44. Бронштейн М.Д., Сальгадо Л.Р., де Кастро Мусолино Н.Р. Медикаментозное лечение аденом гипофиза: частный случай ведения беременной. Pituitary (2002) 5(2):99–107.10.1023/A:1022364514971 [PubMed] [CrossRef] [Google Scholar]45. Колао А., Ди Сарно А., Каппабьянка П., Ди Сомма К., Пивонелло Р., Ломбарди Г.Прекращение длительной терапии каберголином по поводу опухолевой и неопухолевой гиперпролактинемии. N Engl J Med (2003) 349(21):2023–33.10.1056/NEJMoa022657 [PubMed] [CrossRef] [Google Scholar]46.
J Reprod Med (1999) 44 (12 Suppl): 1121–6. [PubMed] [Google Scholar]42. ван Роон Э., ван дер Вийвер Дж. К., Герретсен Г., Хекстер Р. Е., Ваттендорф Р. А. Быстрая регрессия супраселлярной пролактиномы после лечения бромокриптином во время беременности.Фертил Стерил (1981) 36 (2): 173–7. [PubMed] [Google Scholar]43. Лю С, Тиррелл Дж.Б. Успешное лечение крупной макропролактиномы каберголином во время беременности. Pituitary (2001) 4(3):179–85.10.1023/A:10153180 [PubMed] [CrossRef] [Google Scholar]44. Бронштейн М.Д., Сальгадо Л.Р., де Кастро Мусолино Н.Р. Медикаментозное лечение аденом гипофиза: частный случай ведения беременной. Pituitary (2002) 5(2):99–107.10.1023/A:1022364514971 [PubMed] [CrossRef] [Google Scholar]45. Колао А., Ди Сарно А., Каппабьянка П., Ди Сомма К., Пивонелло Р., Ломбарди Г.Прекращение длительной терапии каберголином по поводу опухолевой и неопухолевой гиперпролактинемии. N Engl J Med (2003) 349(21):2023–33.10.1056/NEJMoa022657 [PubMed] [CrossRef] [Google Scholar]46. Ауриемма Р.С., Пероне И., Ди Сарно А., Грассо Л.Ф., Герра Э., Гаспери М. и др.
Результаты одноцентрового обсервационного 10-летнего обзорного исследования рецидивов гиперпролактинемии после беременности и лактации. J Clin Endocrinol Metab (2013) 98(1):372–9.10.1210/jc.2012-3039 [PubMed] [CrossRef] [Google Scholar]
Ауриемма Р.С., Пероне И., Ди Сарно А., Грассо Л.Ф., Герра Э., Гаспери М. и др.
Результаты одноцентрового обсервационного 10-летнего обзорного исследования рецидивов гиперпролактинемии после беременности и лактации. J Clin Endocrinol Metab (2013) 98(1):372–9.10.1210/jc.2012-3039 [PubMed] [CrossRef] [Google Scholar]Управление пролактиномами во время беременности
Front Endocrinol (Лозанна).2015 г.; 6: 85.
, 1, 2, * , 1, , 2 , 3 , 1 , 1 , 1, 2 и 1Mussa Hussain Almalki
1 Центр ожирения, эндокринной системы и обмена веществ, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия
2 Медицинский колледж, Медицинский городок короля Фахда, Университет медицинских наук имени короля Сауда бин Абдулазиза, Эр-Рияд, Саудовская Аравия
Saad Alzahrani
1 Центр ожирения, эндокринной системы и метаболизма, Медицинский центр короля Фахда, Эр-Рияд, Саудовская Аравия
2 Медицинский колледж, Медицинский городок короля Фахда, Университет медицинских наук имени короля Сауда бин Абдулазиза , Эр-Рияд, Саудовская Аравия
Fahad Alshahrani
3 Медицинский колледж, Медицинский город короля Абдулазиза, Университет медицинских наук имени короля Сауда бин Абдулазиза, Эр-Рияд, Саудовская Аравия
Safia Alsherbeni
1 Центр ожирения, эндокринной системы и обмена веществ, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия
Охуд Альмохариб
1 Центр ожирения, эндокринной системы и обмена веществ, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия 99106 Naji Aljohani
1 Центр ожирения, эндокринной системы и метаболизма, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия
2 Медицинский колледж, Медицинский городок короля Фахда, Университет медицинских наук имени короля Сауда бин Абдулазиза, Эр-Рияд, Саудовская Аравия Arabia
Abdurahman Almagamsi
1 Центр ожирения, эндокринной системы и метаболизма, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия
1 Центр ожирения, эндокринной системы и метаболизма, Медицинский городок короля Фахада, Саудовская Аравия, Эр-Рияд 906
2 Медицинский колледж, Медицинский городок имени короля Фахда, Университет медицинских наук имени короля Сауда бин Абдель Азиза, Эр-Рияд, Саудовская Аравия
3 903 67 Медицинский колледж, Медицинский город короля Абдулазиза, Университет медицинских наук имени короля Сауда бин Абдулазиза, Эр-Рияд, Саудовская Аравия
Под редакцией: Корин Бадиу, Медицинский и фармацевтический университет Кэрол Давила, Румыния
Рецензент: Акира Симацу, Национальная больница организация Киотский медицинский центр, Япония; Хиденори Фукуока, университетская больница Кобе, Япония; Jacqueline Trouillas, Университет Лиона 1, Франция,
. oohay@iklam2m
oohay@iklam2mСпециализированный раздел: Эта статья была отправлена в Pituitary Endocrinology, раздел журнала Frontiers in Endocrinology
Поступила в редакцию 7 марта 2015 г.; Принято 10 мая 2015 года.
Copyright © 2015 Алмалки, Альзахрани, Альшахрани, Альшербени, Альмохариб, Алджохани и Алмагамси.Это статья с открытым доступом, распространяемая на условиях лицензии Creative Commons Attribution License (CC BY). Использование, распространение или воспроизведение на других форумах разрешено при условии указания автора(ов) или лицензиара оригинала и ссылки на оригинальную публикацию в этом журнале в соответствии с общепринятой академической практикой.Запрещается использование, распространение или воспроизведение без соблюдения этих условий.
Эта статья была процитирована другими статьями в PMC.Abstract
Пролактиномы являются наиболее распространенными функциональными доброкачественными опухолями гипофиза, обусловленными микро- или макроаденомами гипофиза. У большинства больных наблюдается бесплодие и дисфункция гонад. Агонисты дофамина (ДА) (бромокриптин или каберголин) являются препаратами выбора, которые могут нормализовать уровень пролактина, уменьшить размер опухоли и восстановить овуляцию и фертильность.Каберголин обычно предпочтительнее бромокриптина из-за его более высокой эффективности и переносимости. Лечение пролактином во время беременности может быть сложной задачей. Во время беременности гипофиз подвергается глобальной гиперплазии из-за прогрессирующего повышения уровня эстрогенов в сыворотке крови, что может привести к увеличению объема опухоли с потенциальным эффектом массы и потерей зрения. Риск роста опухоли может возникать у 3% пациентов с микроаденомами, у 32% пациентов с ранее не оперированными макроаденомами и 4.8% пациентов с макроаденомами с предшествующим абляционным лечением. Хотя оба препарата кажутся безопасными во время беременности, данные о воздействии DA на плод во время беременности при применении бромокриптина намного превышают таковые при применении каберголина без связи с повышенным риском невынашивания беременности и преждевременных родов.
У большинства больных наблюдается бесплодие и дисфункция гонад. Агонисты дофамина (ДА) (бромокриптин или каберголин) являются препаратами выбора, которые могут нормализовать уровень пролактина, уменьшить размер опухоли и восстановить овуляцию и фертильность.Каберголин обычно предпочтительнее бромокриптина из-за его более высокой эффективности и переносимости. Лечение пролактином во время беременности может быть сложной задачей. Во время беременности гипофиз подвергается глобальной гиперплазии из-за прогрессирующего повышения уровня эстрогенов в сыворотке крови, что может привести к увеличению объема опухоли с потенциальным эффектом массы и потерей зрения. Риск роста опухоли может возникать у 3% пациентов с микроаденомами, у 32% пациентов с ранее не оперированными макроаденомами и 4.8% пациентов с макроаденомами с предшествующим абляционным лечением. Хотя оба препарата кажутся безопасными во время беременности, данные о воздействии DA на плод во время беременности при применении бромокриптина намного превышают таковые при применении каберголина без связи с повышенным риском невынашивания беременности и преждевременных родов. Рекомендуется прекратить использование DA сразу же после подтверждения беременности, за исключением женщин с инвазивными макропролактиномами или симптомами сдавления. В этом обзоре описывается терапевтический подход к пролактиноме во время беременности с акцентом на безопасность доступной терапии DA.
Рекомендуется прекратить использование DA сразу же после подтверждения беременности, за исключением женщин с инвазивными макропролактиномами или симптомами сдавления. В этом обзоре описывается терапевтический подход к пролактиноме во время беременности с акцентом на безопасность доступной терапии DA.
Ключевые слова: пролактин, опухоль гипофиза, агонист дофамина, беременность и исход около 40% всех аденом гипофиза (1). Производство и высвобождение пролактина опосредовано тоническим ингибированием дофамином, секретируемым гипоталамусом. Молочная железа является основной тканью-мишенью для пролактина, но рецепторы пролактина были обнаружены в нескольких тканях, включая печень, яичники, яички и предстательную железу (2).Основное действие пролактина заключается в инициации и поддержании лактации, но он может действовать как фактор роста, нейротрансмиттер или иммунорегулятор через аутокринные или паракринные механизмы (3).
Пролактиномы являются одной из причин гиперпролактинемии, состояния, при котором 90% составляют межселлярные аденомы и 10% — макроаденомы (≥10 мм) (4).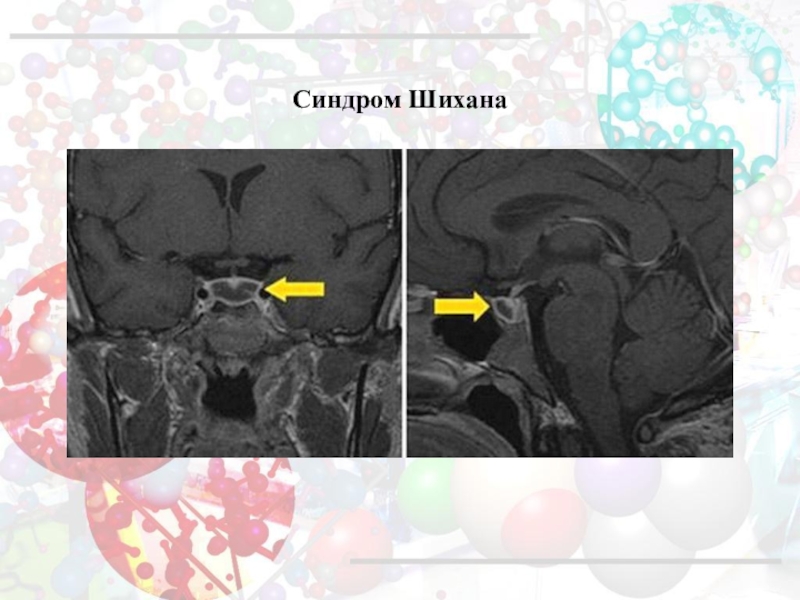 Пролактиномы встречаются с распространенностью 60–100 случаев на миллион (1). Чаще встречается у женщин, особенно в репродуктивном периоде.Самый высокий уровень заболеваемости был обнаружен у женщин в возрасте от 25 до 34 лет: 23,9/100 000 человеко-лет (4). У женщин пролактиномы обычно представляют собой микроаденомы (<10 мм) с высоким уровнем пролактина, что приводит к аменорее, галакторее и бесплодию. Мужчины с пролактиномами часто имеют симптомы масс-эффекта, такие как головная боль и потеря зрения, а иногда и гипогонадизм и бесплодие. Потеря костной массы может возникать как долгосрочное последствие гиперпролактинемии как у мужчин, так и у женщин.
Пролактиномы встречаются с распространенностью 60–100 случаев на миллион (1). Чаще встречается у женщин, особенно в репродуктивном периоде.Самый высокий уровень заболеваемости был обнаружен у женщин в возрасте от 25 до 34 лет: 23,9/100 000 человеко-лет (4). У женщин пролактиномы обычно представляют собой микроаденомы (<10 мм) с высоким уровнем пролактина, что приводит к аменорее, галакторее и бесплодию. Мужчины с пролактиномами часто имеют симптомы масс-эффекта, такие как головная боль и потеря зрения, а иногда и гипогонадизм и бесплодие. Потеря костной массы может возникать как долгосрочное последствие гиперпролактинемии как у мужчин, так и у женщин.
Агонисты дофамина (ДА) все чаще используются в качестве средств выбора для лечения пролактином, поскольку они нормализуют уровень пролактина и приводят к уменьшению размеров опухоли. Хирургия в настоящее время зарезервирована для резистентности или непереносимости DA, в то время как лучевая терапия используется только в случаях хирургической неудачи или резистентности к DA.
Во время беременности гипофиз подвергается глобальной гиперплазии из-за прогрессирующего повышения уровня эстрогенов в сыворотке крови, что может привести к увеличению объема опухоли с потенциальным эффектом массы и потерей зрения, что представляет собой серьезную проблему для эндокринологов.
Пролактинома во время беременности
Опухолевые клетки у пациентов с пролактиномами экспрессируют рецепторы эстрогена; в результате повышенного уровня эстрогена во время беременности (5) может наблюдаться значительное увеличение объема пролактиномы с прогрессирующим повышением уровня пролактина в сыворотке вследствие гиперплазии лактотрофных клеток (6). Основной проблемой является возможное увеличение опухоли во время беременности. Установлено, что риск увеличения опухоли во время беременности зависит от размера опухоли. Имеющиеся в литературе данные указывают на то, что, хотя увеличение опухоли составляет всего 3% для микропролактином, оно достигает 32% для макропролактином, которые ранее не оперировались (7).
Магнитно-резонансная томография (МРТ) должна быть проведена до зачатия, чтобы задокументировать размер опухоли и служить базой для сравнения с МРТ, проведенной во время беременности. Кроме того, МРТ помогает отличить кровоизлияние в опухоль от простого увеличения опухоли во время беременности (8).
Хотя было обнаружено, что пролактиномы поддаются медикаментозному лечению во время беременности, особенно с помощью DA, таких как бромокриптин, недостаточно данных о безопасности, чтобы рекомендовать рутинное использование этих препаратов во время беременности.Клинические рекомендации общества эндокринологов по ведению и лечению пролактином рекомендуют прекращение приема DA вскоре после подтверждения беременности, за исключением женщин с инвазивными макропролактиномами (5).
Бромокриптин является производным эрголина, агонистом дофаминовых D2-рецепторов с агонистическими и антагонистическими свойствами в отношении D1-рецепторов. Обычно требуется многократный прием в течение дня из-за короткого периода полувыведения (9–11). У женщин, принимающих бромокриптин на ранних сроках беременности, частота абортов, внематочной беременности или врожденных пороков развития не выше, чем в общей популяции (12).В исследовании 2587 беременных женщин, из которых у 2437 был повышен риск самопроизвольного аборта, врожденных аномалий или многоплодной беременности и не влиял на постнатальное развитие (13). В других исследованиях среди 6329 пациенток, получавших бромокриптин на ранних сроках беременности, риск самопроизвольных абортов составил 9,9%, что не выше, чем в общей популяции (10,9%) (7, 14). Более того, при длительном наблюдении до 9 лет детей, рожденных от матерей, принимавших бромокриптин, не было выявлено неблагоприятного влияния на исходы плода с точки зрения физического развития, а также не выявлено нарушений психомоторного развития [5].5 лет (1–20 лет) наблюдения (15).
У женщин, принимающих бромокриптин на ранних сроках беременности, частота абортов, внематочной беременности или врожденных пороков развития не выше, чем в общей популяции (12).В исследовании 2587 беременных женщин, из которых у 2437 был повышен риск самопроизвольного аборта, врожденных аномалий или многоплодной беременности и не влиял на постнатальное развитие (13). В других исследованиях среди 6329 пациенток, получавших бромокриптин на ранних сроках беременности, риск самопроизвольных абортов составил 9,9%, что не выше, чем в общей популяции (10,9%) (7, 14). Более того, при длительном наблюдении до 9 лет детей, рожденных от матерей, принимавших бромокриптин, не было выявлено неблагоприятного влияния на исходы плода с точки зрения физического развития, а также не выявлено нарушений психомоторного развития [5].5 лет (1–20 лет) наблюдения (15).
Кроме того, оптимальный результат был обнаружен при непрерывном применении бромокриптина на протяжении всей беременности примерно в 100 случаях (16).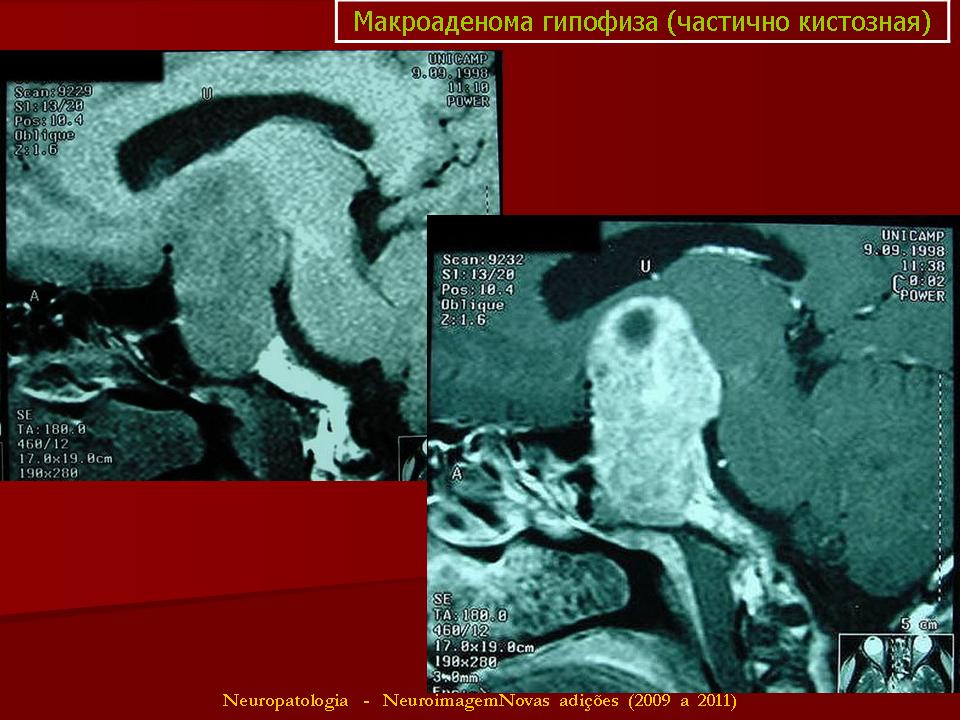
Каберголин является дофаминовым производным эрголина с более высокой аффинностью и селективностью в отношении дофаминовых рецепторов D2. Он имеет большую продолжительность действия, что позволяет применять его один или два раза в неделю с лучшей переносимостью и соблюдением пациентом режима лечения (17–20). Более того, частота наступления беременности у бесплодных женщин с пролактиномой выше при применении каберголина, чем при применении бромокриптина (21).
Такие же результаты были получены у женщин, принимавших каберголин до и во время беременности (22, 23). В одном отчете было описано более 800 таких беременностей (24) (из которых примерно 350 были связаны с облучением в течение первых недель беременности) без существенной разницы в частоте самопроизвольных абортов, преждевременных родов, многоплодной беременности или пороков развития новорожденных. 25, 26).
В ретроспективном исследовании 103 беременностей у 90 женщин с гиперпролактинемией и последующем наблюдении за 61 ребенком не было выявлено значительных отклонений, связанных ни с дозами каберголина, ни со временем воздействия (27). Данные 12-летнего наблюдения за детьми, рожденными от матерей, получавших каберголин, не выявили влияния на их постнатальное развитие, такого как физические проблемы или задержка психомоторного развития (28). В соответствии с предыдущими исследованиями результаты метаанализа не показали значительного увеличения риска выкидышей или пороков развития плода при использовании DA (29).
Данные 12-летнего наблюдения за детьми, рожденными от матерей, получавших каберголин, не выявили влияния на их постнатальное развитие, такого как физические проблемы или задержка психомоторного развития (28). В соответствии с предыдущими исследованиями результаты метаанализа не показали значительного увеличения риска выкидышей или пороков развития плода при использовании DA (29).
Хинаголид – это DA, не являющийся спорыньей, с селективным агонистом рецептора допамина-2 и длительным эффектом снижения уровня пролактина. Его обычно принимают один раз в день, и он лучше переносится и имеет удобный график дозирования, чем бромокриптин (13, 30, 31).Он имеет ограниченную безопасность по сравнению с бромокриптином. В обзоре 176 беременностей, при которых применялся хинаголид (в среднем 37 дней), самопроизвольный аборт произошел в 14% случаев, у 1 были преждевременные роды и у 1 была внематочная беременность (13). В другом небольшом исследовании девяти беременностей было два случая лечения двумя хинаголидами без осложнений (31).
У женщин, принимавших хинаголид, было зарегистрировано более 200 беременностей, при этом не было выявлено явных неблагоприятных эффектов на течение беременности или развитие плода (32).
Следовательно, каждая женщина с пролактиномой должна быть осведомлена о естественном течении пролактиномы и должна обсудить свои планы зачатия со своим врачом, чтобы пройти тщательное обследование перед беременностью.
Определение подходящего варианта лечения является индивидуальным выбором, зависящим в основном от размера опухоли. Предлагаемый терапевтический подход показан на рисунке (33). Исходы пролактином после беременности широко обсуждались с различными результатами.Недавнее исследование показало нормализацию уровня пролактина более чем на 40% без медикаментозного лечения при среднем периоде наблюдения 22 месяца после родов и прекращения лактации (34).
Подход к лечению пролактином во время беременности .
Лечение микропролактином во время беременности
Микропролактиномы у небеременных женщин обычно имеют доброкачественное течение. Риск значительного бессимптомного роста опухоли во время беременности составляет 4,5% (35), а симптоматического роста опухоли <2% (36).Риск развития новых неврологических осложнений (головные боли, сдавление зрительного нерва и др.) колеблется от 1,6 до 5,5% (37). Пролактин имеет тенденцию к увеличению во время беременности; следовательно, он не отражает достоверно увеличение размера опухоли и бесполезен для клинической оценки.
Риск значительного бессимптомного роста опухоли во время беременности составляет 4,5% (35), а симптоматического роста опухоли <2% (36).Риск развития новых неврологических осложнений (головные боли, сдавление зрительного нерва и др.) колеблется от 1,6 до 5,5% (37). Пролактин имеет тенденцию к увеличению во время беременности; следовательно, он не отражает достоверно увеличение размера опухоли и бесполезен для клинической оценки.
В связи с очень низким риском увеличения микропролактиномы во время беременности имеются убедительные данные, подтверждающие необходимость прекращения лечения ДА после подтверждения беременности. Пациентке следует сообщить, что риск увеличения аденомы во время беременности очень мал, и при появлении симптомов медикаментозное лечение, скорее всего, будет эффективным.
При появлении необычных симптомов, таких как сильная головная боль или нарушение зрения, пациенту следует обратиться для срочного обследования, чтобы исключить возможность увеличения опухоли. Серийное определение пролактина не требуется из-за высокой изменчивости пролактина во время беременности (38).
Серийное определение пролактина не требуется из-за высокой изменчивости пролактина во время беременности (38).
Во время постановки диагноза пациентка должна пройти базовое официальное тестирование поля зрения и проходить клиническое наблюдение каждые 2–3 месяца во время беременности (33), но серийные МРТ-исследования или тестирование поля зрения во время беременности не требуются.Однако нет данных, подтверждающих вред для плода ни от МРТ, ни от гадолиния (8).
Если у пациента появляются симптомы нарушения зрения или прогрессирующие головные боли, следует выполнить МРТ без гадолиния (не КТ) для оценки изменений размера опухоли (39).
Если очевиден значительный рост опухоли, следует немедленно возобновить прием DA бромокриптина (36), поскольку в таких случаях он является препаратом первого выбора.
У женщин, у которых симптомы не проявляются на протяжении всей беременности, следует измерить уровень пролактина в сыворотке через 2 месяца после родов или прекращения кормления грудью, и, если он аналогичен значению до лечения, следует возобновить прием препарата (40). Точно так же женщинам, желающим кормить грудью, следует провести МРТ, чтобы убедиться в стабильности опухоли в течение 4–6 недель после родов (37), поскольку ДА снижают уровень ПРЛ в сыворотке, что впоследствии ухудшает лактацию.
Точно так же женщинам, желающим кормить грудью, следует провести МРТ, чтобы убедиться в стабильности опухоли в течение 4–6 недель после родов (37), поскольку ДА снижают уровень ПРЛ в сыворотке, что впоследствии ухудшает лактацию.
Лечение макропролактином во время беременности
У женщин макропролактиномы встречаются реже, чем микропролактиномы. При макропролактиноме симптоматическое увеличение опухоли наблюдается в 20–30% случаев (41). Сообщалось, что риск клинически значимого увеличения опухоли падает с более чем 30% до <5%, если пациентка подвергается лучевой терапии или хирургическому вмешательству до беременности (25).
Беременные женщины с большими опухолями и женщины с экстраселлярным распространением, которые прекратили прием бромокриптина, подвержены риску роста опухоли, поэтому в каждом триместре необходимо проводить официальное исследование поля зрения. Так же, как и при микропролактиномах, нет необходимости измерять уровень пролактина в сыворотке на протяжении всей беременности, потому что уровни неравномерно увеличиваются во время беременности и не коррелируют с увеличением опухоли (8, 25). Кроме того, в этих случаях лечение должно быть индивидуализированным, так как данные, сравнивающие различные стратегии лечения, отсутствуют.
Кроме того, в этих случаях лечение должно быть индивидуализированным, так как данные, сравнивающие различные стратегии лечения, отсутствуют.
Пациентка должна быть проинформирована об относительно более высоком риске увеличения опухоли, необходимости нормализации уровня пролактина и важности лечения до зачатия.
В случае интраселлярных и небольших макропролактином, которые не прилегают к перекресту зрительных нервов, прием ДА следует прекратить при подтверждении беременности.
Пациент должен быть проинформирован о симптомах и необходимости срочного обследования при их появлении. В каждом триместре следует проводить тщательный клинический мониторинг с формальным исследованием поля зрения.Если пациент жалуется на головную боль или изменение зрения, следует провести МРТ. Если результаты МРТ подтверждают увеличение опухоли, женщине следует повторно назначить DA (5).
Бромокриптин считается препаратом первого выбора, и он обычно уменьшает размер аденомы и устраняет симптомы (42). Каберголин можно рассмотреть, если аденома не реагирует на бромокриптин (43).
Каберголин можно рассмотреть, если аденома не реагирует на бромокриптин (43).
Если увеличенная опухоль не отвечает на терапию каберголином, альтернативы включают транссфеноидальную операцию во втором триместре или родоразрешение, если беременность находится на достаточном сроке (16, 25, 41).
Пациентам с большими макропролактиномами и пациентам с экстраселлярным распространением настоятельно не рекомендуется забеременеть до тех пор, пока не будет проведена радикальная терапия. Терапию с хирургическим уменьшением объема можно рассмотреть до беременности, поскольку было показано, что хирургическое вмешательство или лучевая терапия снижают риск симптоматического увеличения опухоли (25), но в этих случаях существует высокий риск гипопитуитаризма. Однако операция по удалению опухоли менее предпочтительна, поскольку медикаментозная терапия во время беременности, вероятно, менее вредна, чем операция (41).Женщины с пролактиномами, устойчивыми к DA, обычно бесплодны. Таким образом, беременность в этих случаях является неожиданной, если они не подвергаются стимуляции яичников гонадотропинами или ГнРГ. Более того, беременность не рекомендуется женщинам с большими макропролактиномами, резистентными к лекарственным препаратам, и они не должны забеременеть, даже если опухоль является интраселлярной, до тех пор, пока размер не будет уменьшен с помощью транссфеноидальной хирургии.
Более того, беременность не рекомендуется женщинам с большими макропролактиномами, резистентными к лекарственным препаратам, и они не должны забеременеть, даже если опухоль является интраселлярной, до тех пор, пока размер не будет уменьшен с помощью транссфеноидальной хирургии.
Хирургическое вмешательство возможно в случаях, когда опухоль не уменьшилась во время медикаментозного лечения DA или у тех, у кого развился рост опухоли во время предыдущей беременности (44).
Влияние беременности и кормления грудью на уровень пролактина, объем опухоли и частоту ремиссий
В современной литературе показано, что беременность вызывает ремиссию гиперпролактинемии у двух третей женщин после прекращения приема ДА. В одном исследовании было обнаружено, что беременность вызывает ремиссию в 76% случаев неопухолевой гиперпролактинемии (NTHP), в 70% случаев микропролактином и в 64% случаев макропролактином с более высокой частотой рецидивов среди пациентов с макропролактиномами и пациентов с микропролактиномами с видимой опухолью на МРТ.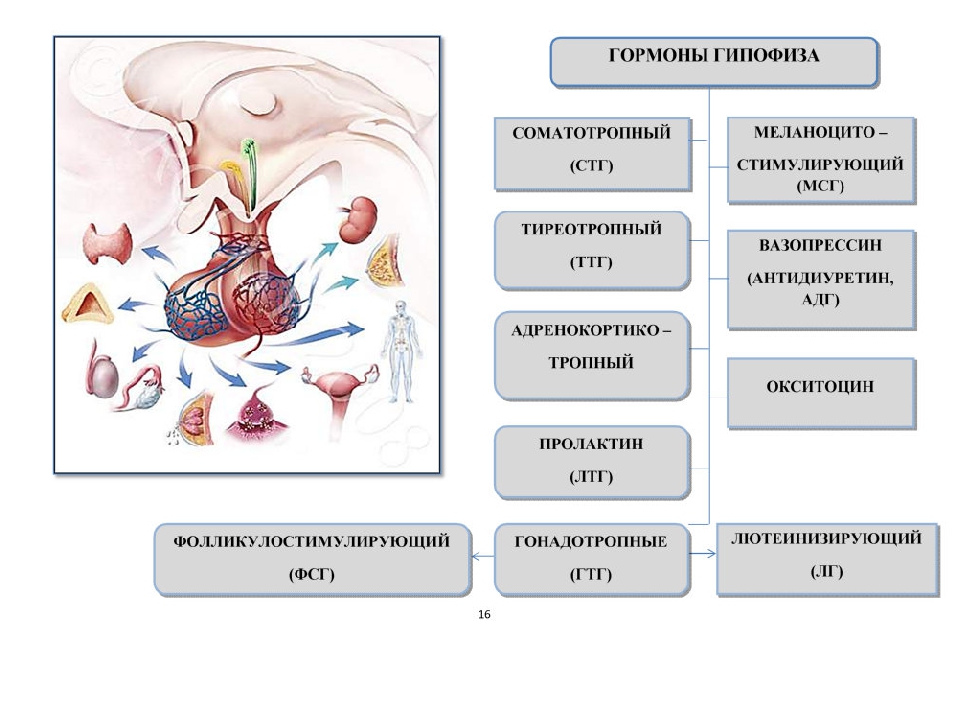 на момент прекращения лечения (45).
на момент прекращения лечения (45).
В недавнем исследовании полная ремиссия была обнаружена у 100% пациентов с НТГП, у 66% пациентов с микропролактиномами и у 70% пациентов с макропролактиномами (46). Основные механизмы неясны, но обычно связывают с аутоинфарктом опухоли (46).
С другой стороны, нет данных, позволяющих предположить, что грудное вскармливание связано с повышенной выработкой пролактина или риском увеличения опухоли (28, 46). Таким образом, женщины могли нормально кормить грудью и возобновлять ДА после прекращения лактации.
Заключение
Лечение пролактиномы во время беременности является сложной задачей. Клинические испытания, подчеркивающие результаты медикаментозной терапии по сравнению с другими видами лечения, немногочисленны; поэтому пациент лечится на индивидуальной основе. Исход микроаденомы превосходный, что позволяет пациентам безопасно прекратить прием DA при тщательном клиническом наблюдении; с другой стороны, макроаденому необходимо лечить до зачатия, так как риск увеличения опухоли относительно высок.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Ссылки
1. Ciccarelli A, Daly AF, Beckers A. Эпидемиология пролактином. Гипофиз (2005) 8(1):3–6.10.1007/s11102-005-5079-0 [PubMed] [CrossRef] [Google Scholar]2. Индер В.Дж. Гиперпролактинемия – дифференциальный диагноз, обследование и лечение. Eur Endocr Rev (2006): 76–1002. [Google Академия]3. Карс М., Деккерс О.М., Перейра А.М., Ромейн Я.А. Обновление в пролактиномах. Neth J Med (2010) 68 (3): 104–12. [PubMed] [Google Scholar]4. Молич М.Е. пролактинома. гипофиз. Кембридж, Индиана: Наука Блэквелла; (1995).п. 433–77. [Google Академия]5. Мелмед С., Казануева Ф.Ф., Хоффман А.Р., Клейнберг Д.Л., Монтори В.М., Шлехте Дж.А. и соавт. Диагностика и лечение гиперпролактинемии: руководство по клинической практике эндокринологического общества. J Clin Endocrinol Metab (2011) 96(2):273–88.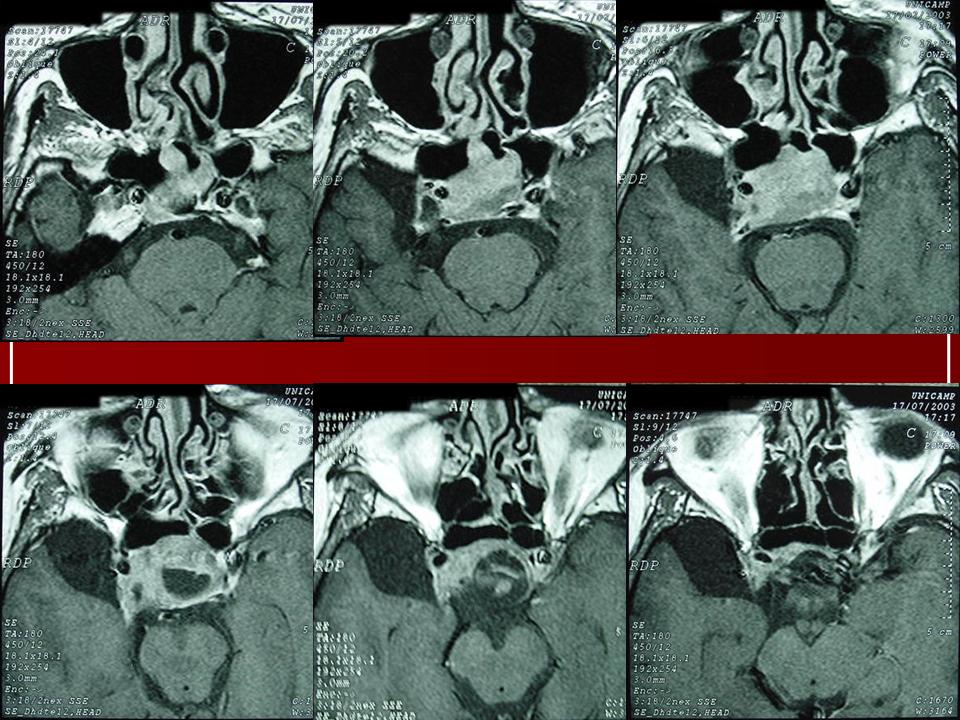 10.1210/jc.2010-1692 [PubMed] [CrossRef] [Google Scholar]6. Пишон М.Ф., Брессион Д., Пейон Ф., Милгром Э. Рецепторы эстрогена в аденомах гипофиза человека. J Clin Endocrinol Metab (1980) 51(4):897–902.10.1210/jcem-51-4-897 [PubMed] [CrossRef] [Google Scholar]7.Гиллам М.П., Молич М.Е., Ломбарди Г., Колао А.
Достижения в лечении пролактином. Endocr Rev (2006) 27(5):485–534.10.1210/er.2005-9998 [PubMed] [CrossRef] [Google Scholar]8. Молич М.Е. Эндокринология при беременности: ведение беременной с пролактиномой. Eur J Endocrinol (2015) 172(5):R205–13.10.1530/EJE-14-0848 [PubMed] [CrossRef] [Google Scholar]9. Мах П.М., Вебстер Дж.
Гиперпролактинемия: этиология, диагностика и лечение. Semin Reprod Med (2002) 20(4):365–74.10.1055/s-2002-36709 [PubMed] [CrossRef] [Google Scholar]10.Биллер БМ. Гиперпролактинемия. Int J Fertil Womens Med (1999) 44 (2): 74–7. [PubMed] [Google Scholar] 11. Банковский Б.Дж., Закур Х.А.
Терапия агонистами допамина при гиперпролактинемии. Clin Obstet Gynecol (2003) 46(2):349–62.
10.1210/jc.2010-1692 [PubMed] [CrossRef] [Google Scholar]6. Пишон М.Ф., Брессион Д., Пейон Ф., Милгром Э. Рецепторы эстрогена в аденомах гипофиза человека. J Clin Endocrinol Metab (1980) 51(4):897–902.10.1210/jcem-51-4-897 [PubMed] [CrossRef] [Google Scholar]7.Гиллам М.П., Молич М.Е., Ломбарди Г., Колао А.
Достижения в лечении пролактином. Endocr Rev (2006) 27(5):485–534.10.1210/er.2005-9998 [PubMed] [CrossRef] [Google Scholar]8. Молич М.Е. Эндокринология при беременности: ведение беременной с пролактиномой. Eur J Endocrinol (2015) 172(5):R205–13.10.1530/EJE-14-0848 [PubMed] [CrossRef] [Google Scholar]9. Мах П.М., Вебстер Дж.
Гиперпролактинемия: этиология, диагностика и лечение. Semin Reprod Med (2002) 20(4):365–74.10.1055/s-2002-36709 [PubMed] [CrossRef] [Google Scholar]10.Биллер БМ. Гиперпролактинемия. Int J Fertil Womens Med (1999) 44 (2): 74–7. [PubMed] [Google Scholar] 11. Банковский Б.Дж., Закур Х.А.
Терапия агонистами допамина при гиперпролактинемии. Clin Obstet Gynecol (2003) 46(2):349–62. 10.1097/00003081-200306000-00013 [PubMed] [CrossRef] [Google Scholar]12. Krupp P, Monka C. Бромокриптин при беременности: аспекты безопасности. Klin Wochenschr (1987) 65(17):823–7.10.1007/BF01727477 [PubMed] [CrossRef] [Google Scholar]13. Вебстер Дж. Сравнительный обзор профилей переносимости агонистов допамина при лечении гиперпролактинемии и подавлении лактации.Безопасность лекарств (1996) 14(4):228–38.10.2165/00002018-199614040-00003 [PubMed] [CrossRef] [Google Scholar]14. Нюбо Андерсен А.М., Вольфарт Дж., Кристенс П., Олсен Дж., Мелби М. Возраст матери и потеря плода: исследование связи регистров на основе популяции. BMJ (2000) 320(7251):1708–12.10.1136/bmj.320.7251.1708 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]15. Шибли-Рахал А., Шлехте Дж.
Гиперпролактинемия и бесплодие. Endocrinol Metab Clin North Am (2011) 40(4):837–46.10.1016/j.ecl.2011.08.008 [PubMed] [CrossRef] [Google Scholar]16.Хрисулиду А., Будина М., Каравитаки Н., Били Э., Васс Дж.
Гипофизарные нарушения при беременности.
10.1097/00003081-200306000-00013 [PubMed] [CrossRef] [Google Scholar]12. Krupp P, Monka C. Бромокриптин при беременности: аспекты безопасности. Klin Wochenschr (1987) 65(17):823–7.10.1007/BF01727477 [PubMed] [CrossRef] [Google Scholar]13. Вебстер Дж. Сравнительный обзор профилей переносимости агонистов допамина при лечении гиперпролактинемии и подавлении лактации.Безопасность лекарств (1996) 14(4):228–38.10.2165/00002018-199614040-00003 [PubMed] [CrossRef] [Google Scholar]14. Нюбо Андерсен А.М., Вольфарт Дж., Кристенс П., Олсен Дж., Мелби М. Возраст матери и потеря плода: исследование связи регистров на основе популяции. BMJ (2000) 320(7251):1708–12.10.1136/bmj.320.7251.1708 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]15. Шибли-Рахал А., Шлехте Дж.
Гиперпролактинемия и бесплодие. Endocrinol Metab Clin North Am (2011) 40(4):837–46.10.1016/j.ecl.2011.08.008 [PubMed] [CrossRef] [Google Scholar]16.Хрисулиду А., Будина М., Каравитаки Н., Били Э., Васс Дж.
Гипофизарные нарушения при беременности. Гормоны (2015) 14(1):70–80.10.14310/horm.2002.1575 [PubMed] [CrossRef] [Google Scholar]17. Колао А., Ди Сарно А., Сарнаккиаро Ф., Фероне Д., Ди Ренцо Г., Мерола Б. и др.
Пролактиномы, резистентные к стандартным агонистам дофамина, реагируют на длительное лечение каберголином. J Clin Endocrinol Metab (1997) 82(3):876–83.10.1210/jcem.82.8.4178-3 [PubMed] [CrossRef] [Google Scholar]18. Verhelst J, Abs R, Maiter D, van den Bruel A, Vandeweghe M, Velkeniers B, et al.Каберголин в лечении гиперпролактинемии: исследование 455 пациентов. J Clin Endocrinol Metab (1999) 84(7):2518–22.10.1210/jcem.84.7.5810 [PubMed] [CrossRef] [Google Scholar]20. Лю Дж.К., Кэдвелл В.Т.
Современное лечение пролактином. Neurosurg Focus (2004) 16(4):E2.10.3171/foc.2004.16.4.3 [PubMed] [CrossRef] [Google Scholar]21. Оно М., Мики Н., Амано К., Кавамата Т., Секи Т., Макино Р. и др.
Индивидуальная терапия высокими дозами каберголина при гиперпролактинемическом бесплодии у женщин с микро- и макропролактиномами.J Clin Endocrinol Metab (2010) 95(6):2672–9.
Гормоны (2015) 14(1):70–80.10.14310/horm.2002.1575 [PubMed] [CrossRef] [Google Scholar]17. Колао А., Ди Сарно А., Сарнаккиаро Ф., Фероне Д., Ди Ренцо Г., Мерола Б. и др.
Пролактиномы, резистентные к стандартным агонистам дофамина, реагируют на длительное лечение каберголином. J Clin Endocrinol Metab (1997) 82(3):876–83.10.1210/jcem.82.8.4178-3 [PubMed] [CrossRef] [Google Scholar]18. Verhelst J, Abs R, Maiter D, van den Bruel A, Vandeweghe M, Velkeniers B, et al.Каберголин в лечении гиперпролактинемии: исследование 455 пациентов. J Clin Endocrinol Metab (1999) 84(7):2518–22.10.1210/jcem.84.7.5810 [PubMed] [CrossRef] [Google Scholar]20. Лю Дж.К., Кэдвелл В.Т.
Современное лечение пролактином. Neurosurg Focus (2004) 16(4):E2.10.3171/foc.2004.16.4.3 [PubMed] [CrossRef] [Google Scholar]21. Оно М., Мики Н., Амано К., Кавамата Т., Секи Т., Макино Р. и др.
Индивидуальная терапия высокими дозами каберголина при гиперпролактинемическом бесплодии у женщин с микро- и макропролактиномами.J Clin Endocrinol Metab (2010) 95(6):2672–9. 10.1210/jc.2009-2605 [PubMed] [CrossRef] [Google Scholar]22. Чиккарелли Э., Гроттоли С., Раззор П., Гайя Д., Бертанья А., Чирилло С. и др.
Длительное лечение каберголином, новым производным эрголина длительного действия, при идиопатической или опухолевой гиперпролактинемии и исходах медикаментозной беременности. J Endocrinol Invest (1997) 20(9):547–51.10.1007/BF03348017 [PubMed] [CrossRef] [Google Scholar]23. Джонс Дж., Башир Т., Олни Дж., Уитли Т.
Лечение каберголином крупной макропролактиномы на протяжении всей беременности.J Obstet Gynaecol (1997) 17(4):375–6.10.1080/01443619750112916 [PubMed] [CrossRef] [Google Scholar]24. Молич М.Е.
Пролактинома при беременности. Best Pract Res Clin Endocrinol Metab (2011) 25(6):885–96.10.1016/j.beem.2011.05.011 [PubMed] [CrossRef] [Google Scholar]25. Мусолино Н.Р., Бронштейн М.Д.
Пролактиномы и беременность. Издательство Kluwer Academic Publishers; (2001). п. 91–108. [Google Академия] 26. Риччи Э., Параццини Ф., Мотта Т., Феррари С.И., Колао А., Клавенна А.
10.1210/jc.2009-2605 [PubMed] [CrossRef] [Google Scholar]22. Чиккарелли Э., Гроттоли С., Раззор П., Гайя Д., Бертанья А., Чирилло С. и др.
Длительное лечение каберголином, новым производным эрголина длительного действия, при идиопатической или опухолевой гиперпролактинемии и исходах медикаментозной беременности. J Endocrinol Invest (1997) 20(9):547–51.10.1007/BF03348017 [PubMed] [CrossRef] [Google Scholar]23. Джонс Дж., Башир Т., Олни Дж., Уитли Т.
Лечение каберголином крупной макропролактиномы на протяжении всей беременности.J Obstet Gynaecol (1997) 17(4):375–6.10.1080/01443619750112916 [PubMed] [CrossRef] [Google Scholar]24. Молич М.Е.
Пролактинома при беременности. Best Pract Res Clin Endocrinol Metab (2011) 25(6):885–96.10.1016/j.beem.2011.05.011 [PubMed] [CrossRef] [Google Scholar]25. Мусолино Н.Р., Бронштейн М.Д.
Пролактиномы и беременность. Издательство Kluwer Academic Publishers; (2001). п. 91–108. [Google Академия] 26. Риччи Э., Параццини Ф., Мотта Т., Феррари С.И., Колао А., Клавенна А. и др.
Исход беременности после лечения каберголином в первые недели гестации.Reprod Toxicol (2002) 16(6):791–3.10.1016/S0890-6238(02)00055-2 [PubMed] [CrossRef] [Google Scholar]27. Сталлдекер Г., Маллеа-Гил М.С., Гительман М., Альфьери А., Балларино М.С., Боэро Л. и др.
Влияние каберголина на беременность и развитие эмбриона и плода: ретроспективное исследование 103 беременностей и обзор литературы. Pituitary (2010) 13(4):345–50.10.1007/s11102-010-0243-6 [PubMed] [CrossRef] [Google Scholar]28. Леббе М., Хубинонт С., Бернард П., Майтер Д. Исход 100 беременностей, начатых при лечении каберголином у женщин с гиперпролактинемией.Clin Endocrinol (2010) 73(2):236–42.10.1111/j.1365-2265.2010.03808.x [PubMed] [CrossRef] [Google Scholar]29. Ван А.Т., Муллан Р.Дж., Лейн М.А., Хазем А., Прасад С., Гатайя Н.В. и др.
Лечение гиперпролактинемии: систематический обзор и метаанализ. Syst Rev (2012) 1:33.10.1186/2046-4053-1-33 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]30. Дюранто Л., Шансон П.
и др.
Исход беременности после лечения каберголином в первые недели гестации.Reprod Toxicol (2002) 16(6):791–3.10.1016/S0890-6238(02)00055-2 [PubMed] [CrossRef] [Google Scholar]27. Сталлдекер Г., Маллеа-Гил М.С., Гительман М., Альфьери А., Балларино М.С., Боэро Л. и др.
Влияние каберголина на беременность и развитие эмбриона и плода: ретроспективное исследование 103 беременностей и обзор литературы. Pituitary (2010) 13(4):345–50.10.1007/s11102-010-0243-6 [PubMed] [CrossRef] [Google Scholar]28. Леббе М., Хубинонт С., Бернард П., Майтер Д. Исход 100 беременностей, начатых при лечении каберголином у женщин с гиперпролактинемией.Clin Endocrinol (2010) 73(2):236–42.10.1111/j.1365-2265.2010.03808.x [PubMed] [CrossRef] [Google Scholar]29. Ван А.Т., Муллан Р.Дж., Лейн М.А., Хазем А., Прасад С., Гатайя Н.В. и др.
Лечение гиперпролактинемии: систематический обзор и метаанализ. Syst Rev (2012) 1:33.10.1186/2046-4053-1-33 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]30. Дюранто Л., Шансон П. , Лавуанн А., Хорле С., Любецки Дж., Кун Дж.М. Влияние нового дофаминергического агониста CV 205-502 на уровни пролактина в плазме и размер опухоли при резистентных к бромокриптину пролактиномах.Clin Endocrinol (1991) 34(1):25–9.10.1111/j.1365-2265.1991.tb01731.x [PubMed] [CrossRef] [Google Scholar]31. Morange I, Barlier A, Pellegrini I, Brue T, Enjalbert A, Jaquet P. Пролактиномы, устойчивые к бромокриптину: долгосрочная эффективность хинаголида и исход беременности. Eur J Endocrinol (1996) 135(4):413–20.10.1530/eje.0.1350413 [PubMed] [CrossRef] [Google Scholar]32. Вебстер Дж.
Клиническое лечение пролактином. Baillieres Best Pract Res Clin Endocrinol Metab (1999) 13(3):395–408.10.1053/beem.1999.0030 [PubMed] [CrossRef] [Google Scholar]34. Domingue ME, Devuyst F, Alexopoulou O, Corvilain B, Maiter D. Исход пролактиномы после беременности и кормления грудью: исследование 73 пациентов. Clin Endocrinol (2014) 80(5):642–8.10.1111/cen.12370 [PubMed] [CrossRef] [Google Scholar]35. Молич М.Е.
Беременность и женщина с гиперпролактинемией. N Engl J Med (1985) 312(21):1364–70.10.1056/NEJM198505233122106 [PubMed] [CrossRef] [Google Scholar]36. Куперсмит М.Дж., Розенберг С., Клейнберг Д. Потеря зрения у беременных с аденомами гипофиза.Ann Intern Med (1994) 121(7):473–7.10.7326/0003-4819-121-7-199410010-00001 [PubMed] [CrossRef] [Google Scholar]37. Гемзелл С., Ван С.Ф.
Исход беременности у женщин с аденомой гипофиза. Фертил Стерил (1979) 31 (4): 363–72. [PubMed] [Google Scholar] 38. Шлехте Я.А.
Клиническая практика. пролактинома. N Engl J Med (2003) 349(21):2035–41.10.1056/NEJMcp025334 [PubMed] [CrossRef] [Google Scholar]39. Шлехте Я.А. Длительное лечение пролактином. J Clin Endocrinol Metab (2007) 92(8):2861–5.10.1210/jc.2007-0836 [PubMed] [CrossRef] [Google Scholar]40. Лавэй Б.А., Мир С.А. Беременность и гипофизарные заболевания: проблемы диагностики и лечения. Indian J Endocrinol Metab (2013) 17(6):996–1004.10.4103/2230-8210.122608 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]41. Молич М.Е.
Лечение пролактином во время беременности. J Reprod Med (1999) 44 (12 Suppl): 1121–6. [PubMed] [Google Scholar]42. ван Роон Э., ван дер Вийвер Дж. К., Герретсен Г., Хекстер Р. Е., Ваттендорф Р. А. Быстрая регрессия супраселлярной пролактиномы после лечения бромокриптином во время беременности.Фертил Стерил (1981) 36 (2): 173–7. [PubMed] [Google Scholar]43. Лю С, Тиррелл Дж.Б. Успешное лечение крупной макропролактиномы каберголином во время беременности. Pituitary (2001) 4(3):179–85.10.1023/A:10153180 [PubMed] [CrossRef] [Google Scholar]44. Бронштейн М.Д., Сальгадо Л.Р., де Кастро Мусолино Н.Р. Медикаментозное лечение аденом гипофиза: частный случай ведения беременной. Pituitary (2002) 5(2):99–107.10.1023/A:1022364514971 [PubMed] [CrossRef] [Google Scholar]45. Колао А., Ди Сарно А., Каппабьянка П., Ди Сомма К., Пивонелло Р., Ломбарди Г.Прекращение длительной терапии каберголином по поводу опухолевой и неопухолевой гиперпролактинемии. N Engl J Med (2003) 349(21):2023–33.10.1056/NEJMoa022657 [PubMed] [CrossRef] [Google Scholar]46. Ауриемма Р.С., Пероне И., Ди Сарно А., Грассо Л.Ф., Герра Э., Гаспери М. и др.
Результаты одноцентрового обсервационного 10-летнего обзорного исследования рецидивов гиперпролактинемии после беременности и лактации. J Clin Endocrinol Metab (2013) 98(1):372–9.10.1210/jc.2012-3039 [PubMed] [CrossRef] [Google Scholar]
, Лавуанн А., Хорле С., Любецки Дж., Кун Дж.М. Влияние нового дофаминергического агониста CV 205-502 на уровни пролактина в плазме и размер опухоли при резистентных к бромокриптину пролактиномах.Clin Endocrinol (1991) 34(1):25–9.10.1111/j.1365-2265.1991.tb01731.x [PubMed] [CrossRef] [Google Scholar]31. Morange I, Barlier A, Pellegrini I, Brue T, Enjalbert A, Jaquet P. Пролактиномы, устойчивые к бромокриптину: долгосрочная эффективность хинаголида и исход беременности. Eur J Endocrinol (1996) 135(4):413–20.10.1530/eje.0.1350413 [PubMed] [CrossRef] [Google Scholar]32. Вебстер Дж.
Клиническое лечение пролактином. Baillieres Best Pract Res Clin Endocrinol Metab (1999) 13(3):395–408.10.1053/beem.1999.0030 [PubMed] [CrossRef] [Google Scholar]34. Domingue ME, Devuyst F, Alexopoulou O, Corvilain B, Maiter D. Исход пролактиномы после беременности и кормления грудью: исследование 73 пациентов. Clin Endocrinol (2014) 80(5):642–8.10.1111/cen.12370 [PubMed] [CrossRef] [Google Scholar]35. Молич М.Е.
Беременность и женщина с гиперпролактинемией. N Engl J Med (1985) 312(21):1364–70.10.1056/NEJM198505233122106 [PubMed] [CrossRef] [Google Scholar]36. Куперсмит М.Дж., Розенберг С., Клейнберг Д. Потеря зрения у беременных с аденомами гипофиза.Ann Intern Med (1994) 121(7):473–7.10.7326/0003-4819-121-7-199410010-00001 [PubMed] [CrossRef] [Google Scholar]37. Гемзелл С., Ван С.Ф.
Исход беременности у женщин с аденомой гипофиза. Фертил Стерил (1979) 31 (4): 363–72. [PubMed] [Google Scholar] 38. Шлехте Я.А.
Клиническая практика. пролактинома. N Engl J Med (2003) 349(21):2035–41.10.1056/NEJMcp025334 [PubMed] [CrossRef] [Google Scholar]39. Шлехте Я.А. Длительное лечение пролактином. J Clin Endocrinol Metab (2007) 92(8):2861–5.10.1210/jc.2007-0836 [PubMed] [CrossRef] [Google Scholar]40. Лавэй Б.А., Мир С.А. Беременность и гипофизарные заболевания: проблемы диагностики и лечения. Indian J Endocrinol Metab (2013) 17(6):996–1004.10.4103/2230-8210.122608 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]41. Молич М.Е.
Лечение пролактином во время беременности. J Reprod Med (1999) 44 (12 Suppl): 1121–6. [PubMed] [Google Scholar]42. ван Роон Э., ван дер Вийвер Дж. К., Герретсен Г., Хекстер Р. Е., Ваттендорф Р. А. Быстрая регрессия супраселлярной пролактиномы после лечения бромокриптином во время беременности.Фертил Стерил (1981) 36 (2): 173–7. [PubMed] [Google Scholar]43. Лю С, Тиррелл Дж.Б. Успешное лечение крупной макропролактиномы каберголином во время беременности. Pituitary (2001) 4(3):179–85.10.1023/A:10153180 [PubMed] [CrossRef] [Google Scholar]44. Бронштейн М.Д., Сальгадо Л.Р., де Кастро Мусолино Н.Р. Медикаментозное лечение аденом гипофиза: частный случай ведения беременной. Pituitary (2002) 5(2):99–107.10.1023/A:1022364514971 [PubMed] [CrossRef] [Google Scholar]45. Колао А., Ди Сарно А., Каппабьянка П., Ди Сомма К., Пивонелло Р., Ломбарди Г.Прекращение длительной терапии каберголином по поводу опухолевой и неопухолевой гиперпролактинемии. N Engl J Med (2003) 349(21):2023–33.10.1056/NEJMoa022657 [PubMed] [CrossRef] [Google Scholar]46. Ауриемма Р.С., Пероне И., Ди Сарно А., Грассо Л.Ф., Герра Э., Гаспери М. и др.
Результаты одноцентрового обсервационного 10-летнего обзорного исследования рецидивов гиперпролактинемии после беременности и лактации. J Clin Endocrinol Metab (2013) 98(1):372–9.10.1210/jc.2012-3039 [PubMed] [CrossRef] [Google Scholar]Управление пролактиномами во время беременности
Front Endocrinol (Лозанна).2015 г.; 6: 85.
, 1, 2, * , 1, , 2 , 3 , 1 , 1 , 1, 2 и 1Mussa Hussain Almalki
1 Центр ожирения, эндокринной системы и обмена веществ, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия
2 Медицинский колледж, Медицинский городок короля Фахда, Университет медицинских наук имени короля Сауда бин Абдулазиза, Эр-Рияд, Саудовская Аравия
Saad Alzahrani
1 Центр ожирения, эндокринной системы и метаболизма, Медицинский центр короля Фахда, Эр-Рияд, Саудовская Аравия
2 Медицинский колледж, Медицинский городок короля Фахда, Университет медицинских наук имени короля Сауда бин Абдулазиза , Эр-Рияд, Саудовская Аравия
Fahad Alshahrani
3 Медицинский колледж, Медицинский город короля Абдулазиза, Университет медицинских наук имени короля Сауда бин Абдулазиза, Эр-Рияд, Саудовская Аравия
Safia Alsherbeni
1 Центр ожирения, эндокринной системы и обмена веществ, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия
Охуд Альмохариб
1 Центр ожирения, эндокринной системы и обмена веществ, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия 99106 Naji Aljohani
1 Центр ожирения, эндокринной системы и метаболизма, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия
2 Медицинский колледж, Медицинский городок короля Фахда, Университет медицинских наук имени короля Сауда бин Абдулазиза, Эр-Рияд, Саудовская Аравия Arabia
Abdurahman Almagamsi
1 Центр ожирения, эндокринной системы и метаболизма, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия
1 Центр ожирения, эндокринной системы и метаболизма, Медицинский городок короля Фахада, Саудовская Аравия, Эр-Рияд 906
2 Медицинский колледж, Медицинский городок имени короля Фахда, Университет медицинских наук имени короля Сауда бин Абдель Азиза, Эр-Рияд, Саудовская Аравия
3 903 67 Медицинский колледж, Медицинский город короля Абдулазиза, Университет медицинских наук имени короля Сауда бин Абдулазиза, Эр-Рияд, Саудовская Аравия
Под редакцией: Корин Бадиу, Медицинский и фармацевтический университет Кэрол Давила, Румыния
Рецензент: Акира Симацу, Национальная больница организация Киотский медицинский центр, Япония; Хиденори Фукуока, университетская больница Кобе, Япония; Jacqueline Trouillas, Университет Лиона 1, Франция,
.oohay@iklam2mСпециализированный раздел: Эта статья была отправлена в Pituitary Endocrinology, раздел журнала Frontiers in Endocrinology
Поступила в редакцию 7 марта 2015 г.; Принято 10 мая 2015 года.
Copyright © 2015 Алмалки, Альзахрани, Альшахрани, Альшербени, Альмохариб, Алджохани и Алмагамси.Это статья с открытым доступом, распространяемая на условиях лицензии Creative Commons Attribution License (CC BY). Использование, распространение или воспроизведение на других форумах разрешено при условии указания автора(ов) или лицензиара оригинала и ссылки на оригинальную публикацию в этом журнале в соответствии с общепринятой академической практикой.Запрещается использование, распространение или воспроизведение без соблюдения этих условий.
Эта статья была процитирована другими статьями в PMC.Abstract
Пролактиномы являются наиболее распространенными функциональными доброкачественными опухолями гипофиза, обусловленными микро- или макроаденомами гипофиза. У большинства больных наблюдается бесплодие и дисфункция гонад. Агонисты дофамина (ДА) (бромокриптин или каберголин) являются препаратами выбора, которые могут нормализовать уровень пролактина, уменьшить размер опухоли и восстановить овуляцию и фертильность.Каберголин обычно предпочтительнее бромокриптина из-за его более высокой эффективности и переносимости. Лечение пролактином во время беременности может быть сложной задачей. Во время беременности гипофиз подвергается глобальной гиперплазии из-за прогрессирующего повышения уровня эстрогенов в сыворотке крови, что может привести к увеличению объема опухоли с потенциальным эффектом массы и потерей зрения. Риск роста опухоли может возникать у 3% пациентов с микроаденомами, у 32% пациентов с ранее не оперированными макроаденомами и 4.8% пациентов с макроаденомами с предшествующим абляционным лечением. Хотя оба препарата кажутся безопасными во время беременности, данные о воздействии DA на плод во время беременности при применении бромокриптина намного превышают таковые при применении каберголина без связи с повышенным риском невынашивания беременности и преждевременных родов. Рекомендуется прекратить использование DA сразу же после подтверждения беременности, за исключением женщин с инвазивными макропролактиномами или симптомами сдавления. В этом обзоре описывается терапевтический подход к пролактиноме во время беременности с акцентом на безопасность доступной терапии DA.
Ключевые слова: пролактин, опухоль гипофиза, агонист дофамина, беременность и исход около 40% всех аденом гипофиза (1). Производство и высвобождение пролактина опосредовано тоническим ингибированием дофамином, секретируемым гипоталамусом. Молочная железа является основной тканью-мишенью для пролактина, но рецепторы пролактина были обнаружены в нескольких тканях, включая печень, яичники, яички и предстательную железу (2).Основное действие пролактина заключается в инициации и поддержании лактации, но он может действовать как фактор роста, нейротрансмиттер или иммунорегулятор через аутокринные или паракринные механизмы (3).
Пролактиномы являются одной из причин гиперпролактинемии, состояния, при котором 90% составляют межселлярные аденомы и 10% — макроаденомы (≥10 мм) (4). Пролактиномы встречаются с распространенностью 60–100 случаев на миллион (1). Чаще встречается у женщин, особенно в репродуктивном периоде.Самый высокий уровень заболеваемости был обнаружен у женщин в возрасте от 25 до 34 лет: 23,9/100 000 человеко-лет (4). У женщин пролактиномы обычно представляют собой микроаденомы (<10 мм) с высоким уровнем пролактина, что приводит к аменорее, галакторее и бесплодию. Мужчины с пролактиномами часто имеют симптомы масс-эффекта, такие как головная боль и потеря зрения, а иногда и гипогонадизм и бесплодие. Потеря костной массы может возникать как долгосрочное последствие гиперпролактинемии как у мужчин, так и у женщин.
Агонисты дофамина (ДА) все чаще используются в качестве средств выбора для лечения пролактином, поскольку они нормализуют уровень пролактина и приводят к уменьшению размеров опухоли. Хирургия в настоящее время зарезервирована для резистентности или непереносимости DA, в то время как лучевая терапия используется только в случаях хирургической неудачи или резистентности к DA.
Во время беременности гипофиз подвергается глобальной гиперплазии из-за прогрессирующего повышения уровня эстрогенов в сыворотке крови, что может привести к увеличению объема опухоли с потенциальным эффектом массы и потерей зрения, что представляет собой серьезную проблему для эндокринологов.
Пролактинома во время беременности
Опухолевые клетки у пациентов с пролактиномами экспрессируют рецепторы эстрогена; в результате повышенного уровня эстрогена во время беременности (5) может наблюдаться значительное увеличение объема пролактиномы с прогрессирующим повышением уровня пролактина в сыворотке вследствие гиперплазии лактотрофных клеток (6). Основной проблемой является возможное увеличение опухоли во время беременности. Установлено, что риск увеличения опухоли во время беременности зависит от размера опухоли. Имеющиеся в литературе данные указывают на то, что, хотя увеличение опухоли составляет всего 3% для микропролактином, оно достигает 32% для макропролактином, которые ранее не оперировались (7).
Магнитно-резонансная томография (МРТ) должна быть проведена до зачатия, чтобы задокументировать размер опухоли и служить базой для сравнения с МРТ, проведенной во время беременности. Кроме того, МРТ помогает отличить кровоизлияние в опухоль от простого увеличения опухоли во время беременности (8).
Хотя было обнаружено, что пролактиномы поддаются медикаментозному лечению во время беременности, особенно с помощью DA, таких как бромокриптин, недостаточно данных о безопасности, чтобы рекомендовать рутинное использование этих препаратов во время беременности.Клинические рекомендации общества эндокринологов по ведению и лечению пролактином рекомендуют прекращение приема DA вскоре после подтверждения беременности, за исключением женщин с инвазивными макропролактиномами (5).
Бромокриптин является производным эрголина, агонистом дофаминовых D2-рецепторов с агонистическими и антагонистическими свойствами в отношении D1-рецепторов. Обычно требуется многократный прием в течение дня из-за короткого периода полувыведения (9–11). У женщин, принимающих бромокриптин на ранних сроках беременности, частота абортов, внематочной беременности или врожденных пороков развития не выше, чем в общей популяции (12).В исследовании 2587 беременных женщин, из которых у 2437 был повышен риск самопроизвольного аборта, врожденных аномалий или многоплодной беременности и не влиял на постнатальное развитие (13). В других исследованиях среди 6329 пациенток, получавших бромокриптин на ранних сроках беременности, риск самопроизвольных абортов составил 9,9%, что не выше, чем в общей популяции (10,9%) (7, 14). Более того, при длительном наблюдении до 9 лет детей, рожденных от матерей, принимавших бромокриптин, не было выявлено неблагоприятного влияния на исходы плода с точки зрения физического развития, а также не выявлено нарушений психомоторного развития [5].5 лет (1–20 лет) наблюдения (15).
Кроме того, оптимальный результат был обнаружен при непрерывном применении бромокриптина на протяжении всей беременности примерно в 100 случаях (16).
Каберголин является дофаминовым производным эрголина с более высокой аффинностью и селективностью в отношении дофаминовых рецепторов D2. Он имеет большую продолжительность действия, что позволяет применять его один или два раза в неделю с лучшей переносимостью и соблюдением пациентом режима лечения (17–20). Более того, частота наступления беременности у бесплодных женщин с пролактиномой выше при применении каберголина, чем при применении бромокриптина (21).
Такие же результаты были получены у женщин, принимавших каберголин до и во время беременности (22, 23). В одном отчете было описано более 800 таких беременностей (24) (из которых примерно 350 были связаны с облучением в течение первых недель беременности) без существенной разницы в частоте самопроизвольных абортов, преждевременных родов, многоплодной беременности или пороков развития новорожденных. 25, 26).
В ретроспективном исследовании 103 беременностей у 90 женщин с гиперпролактинемией и последующем наблюдении за 61 ребенком не было выявлено значительных отклонений, связанных ни с дозами каберголина, ни со временем воздействия (27).Данные 12-летнего наблюдения за детьми, рожденными от матерей, получавших каберголин, не выявили влияния на их постнатальное развитие, такого как физические проблемы или задержка психомоторного развития (28). В соответствии с предыдущими исследованиями результаты метаанализа не показали значительного увеличения риска выкидышей или пороков развития плода при использовании DA (29).
Хинаголид – это DA, не являющийся спорыньей, с селективным агонистом рецептора допамина-2 и длительным эффектом снижения уровня пролактина. Его обычно принимают один раз в день, и он лучше переносится и имеет удобный график дозирования, чем бромокриптин (13, 30, 31).Он имеет ограниченную безопасность по сравнению с бромокриптином. В обзоре 176 беременностей, при которых применялся хинаголид (в среднем 37 дней), самопроизвольный аборт произошел в 14% случаев, у 1 были преждевременные роды и у 1 была внематочная беременность (13). В другом небольшом исследовании девяти беременностей было два случая лечения двумя хинаголидами без осложнений (31).
У женщин, принимавших хинаголид, было зарегистрировано более 200 беременностей, при этом не было выявлено явных неблагоприятных эффектов на течение беременности или развитие плода (32).
Следовательно, каждая женщина с пролактиномой должна быть осведомлена о естественном течении пролактиномы и должна обсудить свои планы зачатия со своим врачом, чтобы пройти тщательное обследование перед беременностью.
Определение подходящего варианта лечения является индивидуальным выбором, зависящим в основном от размера опухоли. Предлагаемый терапевтический подход показан на рисунке (33). Исходы пролактином после беременности широко обсуждались с различными результатами.Недавнее исследование показало нормализацию уровня пролактина более чем на 40% без медикаментозного лечения при среднем периоде наблюдения 22 месяца после родов и прекращения лактации (34).
Подход к лечению пролактином во время беременности .
Лечение микропролактином во время беременности
Микропролактиномы у небеременных женщин обычно имеют доброкачественное течение. Риск значительного бессимптомного роста опухоли во время беременности составляет 4,5% (35), а симптоматического роста опухоли <2% (36).Риск развития новых неврологических осложнений (головные боли, сдавление зрительного нерва и др.) колеблется от 1,6 до 5,5% (37). Пролактин имеет тенденцию к увеличению во время беременности; следовательно, он не отражает достоверно увеличение размера опухоли и бесполезен для клинической оценки.
В связи с очень низким риском увеличения микропролактиномы во время беременности имеются убедительные данные, подтверждающие необходимость прекращения лечения ДА после подтверждения беременности. Пациентке следует сообщить, что риск увеличения аденомы во время беременности очень мал, и при появлении симптомов медикаментозное лечение, скорее всего, будет эффективным.
При появлении необычных симптомов, таких как сильная головная боль или нарушение зрения, пациенту следует обратиться для срочного обследования, чтобы исключить возможность увеличения опухоли. Серийное определение пролактина не требуется из-за высокой изменчивости пролактина во время беременности (38).
Во время постановки диагноза пациентка должна пройти базовое официальное тестирование поля зрения и проходить клиническое наблюдение каждые 2–3 месяца во время беременности (33), но серийные МРТ-исследования или тестирование поля зрения во время беременности не требуются.Однако нет данных, подтверждающих вред для плода ни от МРТ, ни от гадолиния (8).
Если у пациента появляются симптомы нарушения зрения или прогрессирующие головные боли, следует выполнить МРТ без гадолиния (не КТ) для оценки изменений размера опухоли (39).
Если очевиден значительный рост опухоли, следует немедленно возобновить прием DA бромокриптина (36), поскольку в таких случаях он является препаратом первого выбора.
У женщин, у которых симптомы не проявляются на протяжении всей беременности, следует измерить уровень пролактина в сыворотке через 2 месяца после родов или прекращения кормления грудью, и, если он аналогичен значению до лечения, следует возобновить прием препарата (40).Точно так же женщинам, желающим кормить грудью, следует провести МРТ, чтобы убедиться в стабильности опухоли в течение 4–6 недель после родов (37), поскольку ДА снижают уровень ПРЛ в сыворотке, что впоследствии ухудшает лактацию.
Лечение макропролактином во время беременности
У женщин макропролактиномы встречаются реже, чем микропролактиномы. При макропролактиноме симптоматическое увеличение опухоли наблюдается в 20–30% случаев (41). Сообщалось, что риск клинически значимого увеличения опухоли падает с более чем 30% до <5%, если пациентка подвергается лучевой терапии или хирургическому вмешательству до беременности (25).
Беременные женщины с большими опухолями и женщины с экстраселлярным распространением, которые прекратили прием бромокриптина, подвержены риску роста опухоли, поэтому в каждом триместре необходимо проводить официальное исследование поля зрения. Так же, как и при микропролактиномах, нет необходимости измерять уровень пролактина в сыворотке на протяжении всей беременности, потому что уровни неравномерно увеличиваются во время беременности и не коррелируют с увеличением опухоли (8, 25). Кроме того, в этих случаях лечение должно быть индивидуализированным, так как данные, сравнивающие различные стратегии лечения, отсутствуют.
Пациентка должна быть проинформирована об относительно более высоком риске увеличения опухоли, необходимости нормализации уровня пролактина и важности лечения до зачатия.
В случае интраселлярных и небольших макропролактином, которые не прилегают к перекресту зрительных нервов, прием ДА следует прекратить при подтверждении беременности.
Пациент должен быть проинформирован о симптомах и необходимости срочного обследования при их появлении. В каждом триместре следует проводить тщательный клинический мониторинг с формальным исследованием поля зрения.Если пациент жалуется на головную боль или изменение зрения, следует провести МРТ. Если результаты МРТ подтверждают увеличение опухоли, женщине следует повторно назначить DA (5).
Бромокриптин считается препаратом первого выбора, и он обычно уменьшает размер аденомы и устраняет симптомы (42). Каберголин можно рассмотреть, если аденома не реагирует на бромокриптин (43).
Если увеличенная опухоль не отвечает на терапию каберголином, альтернативы включают транссфеноидальную операцию во втором триместре или родоразрешение, если беременность находится на достаточном сроке (16, 25, 41).
Пациентам с большими макропролактиномами и пациентам с экстраселлярным распространением настоятельно не рекомендуется забеременеть до тех пор, пока не будет проведена радикальная терапия. Терапию с хирургическим уменьшением объема можно рассмотреть до беременности, поскольку было показано, что хирургическое вмешательство или лучевая терапия снижают риск симптоматического увеличения опухоли (25), но в этих случаях существует высокий риск гипопитуитаризма. Однако операция по удалению опухоли менее предпочтительна, поскольку медикаментозная терапия во время беременности, вероятно, менее вредна, чем операция (41).Женщины с пролактиномами, устойчивыми к DA, обычно бесплодны. Таким образом, беременность в этих случаях является неожиданной, если они не подвергаются стимуляции яичников гонадотропинами или ГнРГ. Более того, беременность не рекомендуется женщинам с большими макропролактиномами, резистентными к лекарственным препаратам, и они не должны забеременеть, даже если опухоль является интраселлярной, до тех пор, пока размер не будет уменьшен с помощью транссфеноидальной хирургии.
Хирургическое вмешательство возможно в случаях, когда опухоль не уменьшилась во время медикаментозного лечения DA или у тех, у кого развился рост опухоли во время предыдущей беременности (44).
Влияние беременности и кормления грудью на уровень пролактина, объем опухоли и частоту ремиссий
В современной литературе показано, что беременность вызывает ремиссию гиперпролактинемии у двух третей женщин после прекращения приема ДА. В одном исследовании было обнаружено, что беременность вызывает ремиссию в 76% случаев неопухолевой гиперпролактинемии (NTHP), в 70% случаев микропролактином и в 64% случаев макропролактином с более высокой частотой рецидивов среди пациентов с макропролактиномами и пациентов с микропролактиномами с видимой опухолью на МРТ. на момент прекращения лечения (45).
В недавнем исследовании полная ремиссия была обнаружена у 100% пациентов с НТГП, у 66% пациентов с микропролактиномами и у 70% пациентов с макропролактиномами (46). Основные механизмы неясны, но обычно связывают с аутоинфарктом опухоли (46).
С другой стороны, нет данных, позволяющих предположить, что грудное вскармливание связано с повышенной выработкой пролактина или риском увеличения опухоли (28, 46). Таким образом, женщины могли нормально кормить грудью и возобновлять ДА после прекращения лактации.
Заключение
Лечение пролактиномы во время беременности является сложной задачей. Клинические испытания, подчеркивающие результаты медикаментозной терапии по сравнению с другими видами лечения, немногочисленны; поэтому пациент лечится на индивидуальной основе. Исход микроаденомы превосходный, что позволяет пациентам безопасно прекратить прием DA при тщательном клиническом наблюдении; с другой стороны, макроаденому необходимо лечить до зачатия, так как риск увеличения опухоли относительно высок.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Ссылки
1. Ciccarelli A, Daly AF, Beckers A. Эпидемиология пролактином. Гипофиз (2005) 8(1):3–6.10.1007/s11102-005-5079-0 [PubMed] [CrossRef] [Google Scholar]2. Индер В.Дж. Гиперпролактинемия – дифференциальный диагноз, обследование и лечение. Eur Endocr Rev (2006): 76–1002. [Google Академия]3. Карс М., Деккерс О.М., Перейра А.М., Ромейн Я.А. Обновление в пролактиномах. Neth J Med (2010) 68 (3): 104–12. [PubMed] [Google Scholar]4. Молич М.Е. пролактинома. гипофиз. Кембридж, Индиана: Наука Блэквелла; (1995).п. 433–77. [Google Академия]5. Мелмед С., Казануева Ф.Ф., Хоффман А.Р., Клейнберг Д.Л., Монтори В.М., Шлехте Дж.А. и соавт. Диагностика и лечение гиперпролактинемии: руководство по клинической практике эндокринологического общества. J Clin Endocrinol Metab (2011) 96(2):273–88.10.1210/jc.2010-1692 [PubMed] [CrossRef] [Google Scholar]6. Пишон М.Ф., Брессион Д., Пейон Ф., Милгром Э. Рецепторы эстрогена в аденомах гипофиза человека. J Clin Endocrinol Metab (1980) 51(4):897–902.10.1210/jcem-51-4-897 [PubMed] [CrossRef] [Google Scholar]7.Гиллам М.П., Молич М.Е., Ломбарди Г., Колао А. Достижения в лечении пролактином. Endocr Rev (2006) 27(5):485–534.10.1210/er.2005-9998 [PubMed] [CrossRef] [Google Scholar]8. Молич М.Е. Эндокринология при беременности: ведение беременной с пролактиномой. Eur J Endocrinol (2015) 172(5):R205–13.10.1530/EJE-14-0848 [PubMed] [CrossRef] [Google Scholar]9. Мах П.М., Вебстер Дж. Гиперпролактинемия: этиология, диагностика и лечение. Semin Reprod Med (2002) 20(4):365–74.10.1055/s-2002-36709 [PubMed] [CrossRef] [Google Scholar]10.Биллер БМ. Гиперпролактинемия. Int J Fertil Womens Med (1999) 44 (2): 74–7. [PubMed] [Google Scholar] 11. Банковский Б.Дж., Закур Х.А. Терапия агонистами допамина при гиперпролактинемии. Clin Obstet Gynecol (2003) 46(2):349–62.10.1097/00003081-200306000-00013 [PubMed] [CrossRef] [Google Scholar]12. Krupp P, Monka C. Бромокриптин при беременности: аспекты безопасности. Klin Wochenschr (1987) 65(17):823–7.10.1007/BF01727477 [PubMed] [CrossRef] [Google Scholar]13. Вебстер Дж. Сравнительный обзор профилей переносимости агонистов допамина при лечении гиперпролактинемии и подавлении лактации.Безопасность лекарств (1996) 14(4):228–38.10.2165/00002018-199614040-00003 [PubMed] [CrossRef] [Google Scholar]14. Нюбо Андерсен А.М., Вольфарт Дж., Кристенс П., Олсен Дж., Мелби М. Возраст матери и потеря плода: исследование связи регистров на основе популяции. BMJ (2000) 320(7251):1708–12.10.1136/bmj.320.7251.1708 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]15. Шибли-Рахал А., Шлехте Дж. Гиперпролактинемия и бесплодие. Endocrinol Metab Clin North Am (2011) 40(4):837–46.10.1016/j.ecl.2011.08.008 [PubMed] [CrossRef] [Google Scholar]16.Хрисулиду А., Будина М., Каравитаки Н., Били Э., Васс Дж. Гипофизарные нарушения при беременности. Гормоны (2015) 14(1):70–80.10.14310/horm.2002.1575 [PubMed] [CrossRef] [Google Scholar]17. Колао А., Ди Сарно А., Сарнаккиаро Ф., Фероне Д., Ди Ренцо Г., Мерола Б. и др. Пролактиномы, резистентные к стандартным агонистам дофамина, реагируют на длительное лечение каберголином. J Clin Endocrinol Metab (1997) 82(3):876–83.10.1210/jcem.82.8.4178-3 [PubMed] [CrossRef] [Google Scholar]18. Verhelst J, Abs R, Maiter D, van den Bruel A, Vandeweghe M, Velkeniers B, et al.Каберголин в лечении гиперпролактинемии: исследование 455 пациентов. J Clin Endocrinol Metab (1999) 84(7):2518–22.10.1210/jcem.84.7.5810 [PubMed] [CrossRef] [Google Scholar]20. Лю Дж.К., Кэдвелл В.Т. Современное лечение пролактином. Neurosurg Focus (2004) 16(4):E2.10.3171/foc.2004.16.4.3 [PubMed] [CrossRef] [Google Scholar]21. Оно М., Мики Н., Амано К., Кавамата Т., Секи Т., Макино Р. и др. Индивидуальная терапия высокими дозами каберголина при гиперпролактинемическом бесплодии у женщин с микро- и макропролактиномами.J Clin Endocrinol Metab (2010) 95(6):2672–9.10.1210/jc.2009-2605 [PubMed] [CrossRef] [Google Scholar]22. Чиккарелли Э., Гроттоли С., Раззор П., Гайя Д., Бертанья А., Чирилло С. и др. Длительное лечение каберголином, новым производным эрголина длительного действия, при идиопатической или опухолевой гиперпролактинемии и исходах медикаментозной беременности. J Endocrinol Invest (1997) 20(9):547–51.10.1007/BF03348017 [PubMed] [CrossRef] [Google Scholar]23. Джонс Дж., Башир Т., Олни Дж., Уитли Т. Лечение каберголином крупной макропролактиномы на протяжении всей беременности.J Obstet Gynaecol (1997) 17(4):375–6.10.1080/01443619750112916 [PubMed] [CrossRef] [Google Scholar]24. Молич М.Е. Пролактинома при беременности. Best Pract Res Clin Endocrinol Metab (2011) 25(6):885–96.10.1016/j.beem.2011.05.011 [PubMed] [CrossRef] [Google Scholar]25. Мусолино Н.Р., Бронштейн М.Д. Пролактиномы и беременность. Издательство Kluwer Academic Publishers; (2001). п. 91–108. [Google Академия] 26. Риччи Э., Параццини Ф., Мотта Т., Феррари С.И., Колао А., Клавенна А. и др. Исход беременности после лечения каберголином в первые недели гестации.Reprod Toxicol (2002) 16(6):791–3.10.1016/S0890-6238(02)00055-2 [PubMed] [CrossRef] [Google Scholar]27. Сталлдекер Г., Маллеа-Гил М.С., Гительман М., Альфьери А., Балларино М.С., Боэро Л. и др. Влияние каберголина на беременность и развитие эмбриона и плода: ретроспективное исследование 103 беременностей и обзор литературы. Pituitary (2010) 13(4):345–50.10.1007/s11102-010-0243-6 [PubMed] [CrossRef] [Google Scholar]28. Леббе М., Хубинонт С., Бернард П., Майтер Д. Исход 100 беременностей, начатых при лечении каберголином у женщин с гиперпролактинемией.Clin Endocrinol (2010) 73(2):236–42.10.1111/j.1365-2265.2010.03808.x [PubMed] [CrossRef] [Google Scholar]29. Ван А.Т., Муллан Р.Дж., Лейн М.А., Хазем А., Прасад С., Гатайя Н.В. и др. Лечение гиперпролактинемии: систематический обзор и метаанализ. Syst Rev (2012) 1:33.10.1186/2046-4053-1-33 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]30. Дюранто Л., Шансон П., Лавуанн А., Хорле С., Любецки Дж., Кун Дж.М. Влияние нового дофаминергического агониста CV 205-502 на уровни пролактина в плазме и размер опухоли при резистентных к бромокриптину пролактиномах.Clin Endocrinol (1991) 34(1):25–9.10.1111/j.1365-2265.1991.tb01731.x [PubMed] [CrossRef] [Google Scholar]31. Morange I, Barlier A, Pellegrini I, Brue T, Enjalbert A, Jaquet P. Пролактиномы, устойчивые к бромокриптину: долгосрочная эффективность хинаголида и исход беременности. Eur J Endocrinol (1996) 135(4):413–20.10.1530/eje.0.1350413 [PubMed] [CrossRef] [Google Scholar]32. Вебстер Дж. Клиническое лечение пролактином. Baillieres Best Pract Res Clin Endocrinol Metab (1999) 13(3):395–408.10.1053/beem.1999.0030 [PubMed] [CrossRef] [Google Scholar]34. Domingue ME, Devuyst F, Alexopoulou O, Corvilain B, Maiter D. Исход пролактиномы после беременности и кормления грудью: исследование 73 пациентов. Clin Endocrinol (2014) 80(5):642–8.10.1111/cen.12370 [PubMed] [CrossRef] [Google Scholar]35. Молич М.Е. Беременность и женщина с гиперпролактинемией. N Engl J Med (1985) 312(21):1364–70.10.1056/NEJM198505233122106 [PubMed] [CrossRef] [Google Scholar]36. Куперсмит М.Дж., Розенберг С., Клейнберг Д. Потеря зрения у беременных с аденомами гипофиза.Ann Intern Med (1994) 121(7):473–7.10.7326/0003-4819-121-7-199410010-00001 [PubMed] [CrossRef] [Google Scholar]37. Гемзелл С., Ван С.Ф. Исход беременности у женщин с аденомой гипофиза. Фертил Стерил (1979) 31 (4): 363–72. [PubMed] [Google Scholar] 38. Шлехте Я.А. Клиническая практика. пролактинома. N Engl J Med (2003) 349(21):2035–41.10.1056/NEJMcp025334 [PubMed] [CrossRef] [Google Scholar]39. Шлехте Я.А. Длительное лечение пролактином. J Clin Endocrinol Metab (2007) 92(8):2861–5.10.1210/jc.2007-0836 [PubMed] [CrossRef] [Google Scholar]40. Лавэй Б.А., Мир С.А. Беременность и гипофизарные заболевания: проблемы диагностики и лечения. Indian J Endocrinol Metab (2013) 17(6):996–1004.10.4103/2230-8210.122608 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]41. Молич М.Е. Лечение пролактином во время беременности. J Reprod Med (1999) 44 (12 Suppl): 1121–6. [PubMed] [Google Scholar]42. ван Роон Э., ван дер Вийвер Дж. К., Герретсен Г., Хекстер Р. Е., Ваттендорф Р. А. Быстрая регрессия супраселлярной пролактиномы после лечения бромокриптином во время беременности.Фертил Стерил (1981) 36 (2): 173–7. [PubMed] [Google Scholar]43. Лю С, Тиррелл Дж.Б. Успешное лечение крупной макропролактиномы каберголином во время беременности. Pituitary (2001) 4(3):179–85.10.1023/A:10153180 [PubMed] [CrossRef] [Google Scholar]44. Бронштейн М.Д., Сальгадо Л.Р., де Кастро Мусолино Н.Р. Медикаментозное лечение аденом гипофиза: частный случай ведения беременной. Pituitary (2002) 5(2):99–107.10.1023/A:1022364514971 [PubMed] [CrossRef] [Google Scholar]45. Колао А., Ди Сарно А., Каппабьянка П., Ди Сомма К., Пивонелло Р., Ломбарди Г.Прекращение длительной терапии каберголином по поводу опухолевой и неопухолевой гиперпролактинемии. N Engl J Med (2003) 349(21):2023–33.10.1056/NEJMoa022657 [PubMed] [CrossRef] [Google Scholar]46. Ауриемма Р.С., Пероне И., Ди Сарно А., Грассо Л.Ф., Герра Э., Гаспери М. и др. Результаты одноцентрового обсервационного 10-летнего обзорного исследования рецидивов гиперпролактинемии после беременности и лактации. J Clin Endocrinol Metab (2013) 98(1):372–9.10.1210/jc.2012-3039 [PubMed] [CrossRef] [Google Scholar]Управление пролактиномами во время беременности
Front Endocrinol (Лозанна).2015 г.; 6: 85.
, 1, 2, * , 1, , 2 , 3 , 1 , 1 , 1, 2 и 1Mussa Hussain Almalki
1 Центр ожирения, эндокринной системы и обмена веществ, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия
2 Медицинский колледж, Медицинский городок короля Фахда, Университет медицинских наук имени короля Сауда бин Абдулазиза, Эр-Рияд, Саудовская Аравия
Saad Alzahrani
1 Центр ожирения, эндокринной системы и метаболизма, Медицинский центр короля Фахда, Эр-Рияд, Саудовская Аравия
2 Медицинский колледж, Медицинский городок короля Фахда, Университет медицинских наук имени короля Сауда бин Абдулазиза , Эр-Рияд, Саудовская Аравия
Fahad Alshahrani
3 Медицинский колледж, Медицинский город короля Абдулазиза, Университет медицинских наук имени короля Сауда бин Абдулазиза, Эр-Рияд, Саудовская Аравия
Safia Alsherbeni
1 Центр ожирения, эндокринной системы и обмена веществ, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия
Охуд Альмохариб
1 Центр ожирения, эндокринной системы и обмена веществ, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия 99106 Naji Aljohani
1 Центр ожирения, эндокринной системы и метаболизма, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия
2 Медицинский колледж, Медицинский городок короля Фахда, Университет медицинских наук имени короля Сауда бин Абдулазиза, Эр-Рияд, Саудовская Аравия Arabia
Abdurahman Almagamsi
1 Центр ожирения, эндокринной системы и метаболизма, Медицинский городок короля Фахда, Эр-Рияд, Саудовская Аравия
1 Центр ожирения, эндокринной системы и метаболизма, Медицинский городок короля Фахада, Саудовская Аравия, Эр-Рияд 906
2 Медицинский колледж, Медицинский городок имени короля Фахда, Университет медицинских наук имени короля Сауда бин Абдель Азиза, Эр-Рияд, Саудовская Аравия
3 903 67 Медицинский колледж, Медицинский город короля Абдулазиза, Университет медицинских наук имени короля Сауда бин Абдулазиза, Эр-Рияд, Саудовская Аравия
Под редакцией: Корин Бадиу, Медицинский и фармацевтический университет Кэрол Давила, Румыния
Рецензент: Акира Симацу, Национальная больница организация Киотский медицинский центр, Япония; Хиденори Фукуока, университетская больница Кобе, Япония; Jacqueline Trouillas, Университет Лиона 1, Франция,
.oohay@iklam2mСпециализированный раздел: Эта статья была отправлена в Pituitary Endocrinology, раздел журнала Frontiers in Endocrinology
Поступила в редакцию 7 марта 2015 г.; Принято 10 мая 2015 года.
Copyright © 2015 Алмалки, Альзахрани, Альшахрани, Альшербени, Альмохариб, Алджохани и Алмагамси.Это статья с открытым доступом, распространяемая на условиях лицензии Creative Commons Attribution License (CC BY). Использование, распространение или воспроизведение на других форумах разрешено при условии указания автора(ов) или лицензиара оригинала и ссылки на оригинальную публикацию в этом журнале в соответствии с общепринятой академической практикой.Запрещается использование, распространение или воспроизведение без соблюдения этих условий.
Эта статья была процитирована другими статьями в PMC.Abstract
Пролактиномы являются наиболее распространенными функциональными доброкачественными опухолями гипофиза, обусловленными микро- или макроаденомами гипофиза. У большинства больных наблюдается бесплодие и дисфункция гонад. Агонисты дофамина (ДА) (бромокриптин или каберголин) являются препаратами выбора, которые могут нормализовать уровень пролактина, уменьшить размер опухоли и восстановить овуляцию и фертильность.Каберголин обычно предпочтительнее бромокриптина из-за его более высокой эффективности и переносимости. Лечение пролактином во время беременности может быть сложной задачей. Во время беременности гипофиз подвергается глобальной гиперплазии из-за прогрессирующего повышения уровня эстрогенов в сыворотке крови, что может привести к увеличению объема опухоли с потенциальным эффектом массы и потерей зрения. Риск роста опухоли может возникать у 3% пациентов с микроаденомами, у 32% пациентов с ранее не оперированными макроаденомами и 4.8% пациентов с макроаденомами с предшествующим абляционным лечением. Хотя оба препарата кажутся безопасными во время беременности, данные о воздействии DA на плод во время беременности при применении бромокриптина намного превышают таковые при применении каберголина без связи с повышенным риском невынашивания беременности и преждевременных родов. Рекомендуется прекратить использование DA сразу же после подтверждения беременности, за исключением женщин с инвазивными макропролактиномами или симптомами сдавления. В этом обзоре описывается терапевтический подход к пролактиноме во время беременности с акцентом на безопасность доступной терапии DA.
Ключевые слова: пролактин, опухоль гипофиза, агонист дофамина, беременность и исход около 40% всех аденом гипофиза (1). Производство и высвобождение пролактина опосредовано тоническим ингибированием дофамином, секретируемым гипоталамусом. Молочная железа является основной тканью-мишенью для пролактина, но рецепторы пролактина были обнаружены в нескольких тканях, включая печень, яичники, яички и предстательную железу (2).Основное действие пролактина заключается в инициации и поддержании лактации, но он может действовать как фактор роста, нейротрансмиттер или иммунорегулятор через аутокринные или паракринные механизмы (3).
Пролактиномы являются одной из причин гиперпролактинемии, состояния, при котором 90% составляют межселлярные аденомы и 10% — макроаденомы (≥10 мм) (4). Пролактиномы встречаются с распространенностью 60–100 случаев на миллион (1). Чаще встречается у женщин, особенно в репродуктивном периоде.Самый высокий уровень заболеваемости был обнаружен у женщин в возрасте от 25 до 34 лет: 23,9/100 000 человеко-лет (4). У женщин пролактиномы обычно представляют собой микроаденомы (<10 мм) с высоким уровнем пролактина, что приводит к аменорее, галакторее и бесплодию. Мужчины с пролактиномами часто имеют симптомы масс-эффекта, такие как головная боль и потеря зрения, а иногда и гипогонадизм и бесплодие. Потеря костной массы может возникать как долгосрочное последствие гиперпролактинемии как у мужчин, так и у женщин.
Агонисты дофамина (ДА) все чаще используются в качестве средств выбора для лечения пролактином, поскольку они нормализуют уровень пролактина и приводят к уменьшению размеров опухоли. Хирургия в настоящее время зарезервирована для резистентности или непереносимости DA, в то время как лучевая терапия используется только в случаях хирургической неудачи или резистентности к DA.
Во время беременности гипофиз подвергается глобальной гиперплазии из-за прогрессирующего повышения уровня эстрогенов в сыворотке крови, что может привести к увеличению объема опухоли с потенциальным эффектом массы и потерей зрения, что представляет собой серьезную проблему для эндокринологов.
Пролактинома во время беременности
Опухолевые клетки у пациентов с пролактиномами экспрессируют рецепторы эстрогена; в результате повышенного уровня эстрогена во время беременности (5) может наблюдаться значительное увеличение объема пролактиномы с прогрессирующим повышением уровня пролактина в сыворотке вследствие гиперплазии лактотрофных клеток (6). Основной проблемой является возможное увеличение опухоли во время беременности. Установлено, что риск увеличения опухоли во время беременности зависит от размера опухоли. Имеющиеся в литературе данные указывают на то, что, хотя увеличение опухоли составляет всего 3% для микропролактином, оно достигает 32% для макропролактином, которые ранее не оперировались (7).
Магнитно-резонансная томография (МРТ) должна быть проведена до зачатия, чтобы задокументировать размер опухоли и служить базой для сравнения с МРТ, проведенной во время беременности. Кроме того, МРТ помогает отличить кровоизлияние в опухоль от простого увеличения опухоли во время беременности (8).
Хотя было обнаружено, что пролактиномы поддаются медикаментозному лечению во время беременности, особенно с помощью DA, таких как бромокриптин, недостаточно данных о безопасности, чтобы рекомендовать рутинное использование этих препаратов во время беременности.Клинические рекомендации общества эндокринологов по ведению и лечению пролактином рекомендуют прекращение приема DA вскоре после подтверждения беременности, за исключением женщин с инвазивными макропролактиномами (5).
Бромокриптин является производным эрголина, агонистом дофаминовых D2-рецепторов с агонистическими и антагонистическими свойствами в отношении D1-рецепторов. Обычно требуется многократный прием в течение дня из-за короткого периода полувыведения (9–11). У женщин, принимающих бромокриптин на ранних сроках беременности, частота абортов, внематочной беременности или врожденных пороков развития не выше, чем в общей популяции (12).В исследовании 2587 беременных женщин, из которых у 2437 был повышен риск самопроизвольного аборта, врожденных аномалий или многоплодной беременности и не влиял на постнатальное развитие (13). В других исследованиях среди 6329 пациенток, получавших бромокриптин на ранних сроках беременности, риск самопроизвольных абортов составил 9,9%, что не выше, чем в общей популяции (10,9%) (7, 14). Более того, при длительном наблюдении до 9 лет детей, рожденных от матерей, принимавших бромокриптин, не было выявлено неблагоприятного влияния на исходы плода с точки зрения физического развития, а также не выявлено нарушений психомоторного развития [5].5 лет (1–20 лет) наблюдения (15).
Кроме того, оптимальный результат был обнаружен при непрерывном применении бромокриптина на протяжении всей беременности примерно в 100 случаях (16).
Каберголин является дофаминовым производным эрголина с более высокой аффинностью и селективностью в отношении дофаминовых рецепторов D2. Он имеет большую продолжительность действия, что позволяет применять его один или два раза в неделю с лучшей переносимостью и соблюдением пациентом режима лечения (17–20). Более того, частота наступления беременности у бесплодных женщин с пролактиномой выше при применении каберголина, чем при применении бромокриптина (21).
Такие же результаты были получены у женщин, принимавших каберголин до и во время беременности (22, 23). В одном отчете было описано более 800 таких беременностей (24) (из которых примерно 350 были связаны с облучением в течение первых недель беременности) без существенной разницы в частоте самопроизвольных абортов, преждевременных родов, многоплодной беременности или пороков развития новорожденных. 25, 26).
В ретроспективном исследовании 103 беременностей у 90 женщин с гиперпролактинемией и последующем наблюдении за 61 ребенком не было выявлено значительных отклонений, связанных ни с дозами каберголина, ни со временем воздействия (27).Данные 12-летнего наблюдения за детьми, рожденными от матерей, получавших каберголин, не выявили влияния на их постнатальное развитие, такого как физические проблемы или задержка психомоторного развития (28). В соответствии с предыдущими исследованиями результаты метаанализа не показали значительного увеличения риска выкидышей или пороков развития плода при использовании DA (29).
Хинаголид – это DA, не являющийся спорыньей, с селективным агонистом рецептора допамина-2 и длительным эффектом снижения уровня пролактина. Его обычно принимают один раз в день, и он лучше переносится и имеет удобный график дозирования, чем бромокриптин (13, 30, 31).Он имеет ограниченную безопасность по сравнению с бромокриптином. В обзоре 176 беременностей, при которых применялся хинаголид (в среднем 37 дней), самопроизвольный аборт произошел в 14% случаев, у 1 были преждевременные роды и у 1 была внематочная беременность (13). В другом небольшом исследовании девяти беременностей было два случая лечения двумя хинаголидами без осложнений (31).
У женщин, принимавших хинаголид, было зарегистрировано более 200 беременностей, при этом не было выявлено явных неблагоприятных эффектов на течение беременности или развитие плода (32).
Следовательно, каждая женщина с пролактиномой должна быть осведомлена о естественном течении пролактиномы и должна обсудить свои планы зачатия со своим врачом, чтобы пройти тщательное обследование перед беременностью.
Определение подходящего варианта лечения является индивидуальным выбором, зависящим в основном от размера опухоли. Предлагаемый терапевтический подход показан на рисунке (33). Исходы пролактином после беременности широко обсуждались с различными результатами.Недавнее исследование показало нормализацию уровня пролактина более чем на 40% без медикаментозного лечения при среднем периоде наблюдения 22 месяца после родов и прекращения лактации (34).
Подход к лечению пролактином во время беременности .
Лечение микропролактином во время беременности
Микропролактиномы у небеременных женщин обычно имеют доброкачественное течение. Риск значительного бессимптомного роста опухоли во время беременности составляет 4,5% (35), а симптоматического роста опухоли <2% (36).Риск развития новых неврологических осложнений (головные боли, сдавление зрительного нерва и др.) колеблется от 1,6 до 5,5% (37). Пролактин имеет тенденцию к увеличению во время беременности; следовательно, он не отражает достоверно увеличение размера опухоли и бесполезен для клинической оценки.
В связи с очень низким риском увеличения микропролактиномы во время беременности имеются убедительные данные, подтверждающие необходимость прекращения лечения ДА после подтверждения беременности. Пациентке следует сообщить, что риск увеличения аденомы во время беременности очень мал, и при появлении симптомов медикаментозное лечение, скорее всего, будет эффективным.
При появлении необычных симптомов, таких как сильная головная боль или нарушение зрения, пациенту следует обратиться для срочного обследования, чтобы исключить возможность увеличения опухоли. Серийное определение пролактина не требуется из-за высокой изменчивости пролактина во время беременности (38).
Во время постановки диагноза пациентка должна пройти базовое официальное тестирование поля зрения и проходить клиническое наблюдение каждые 2–3 месяца во время беременности (33), но серийные МРТ-исследования или тестирование поля зрения во время беременности не требуются.Однако нет данных, подтверждающих вред для плода ни от МРТ, ни от гадолиния (8).
Если у пациента появляются симптомы нарушения зрения или прогрессирующие головные боли, следует выполнить МРТ без гадолиния (не КТ) для оценки изменений размера опухоли (39).
Если очевиден значительный рост опухоли, следует немедленно возобновить прием DA бромокриптина (36), поскольку в таких случаях он является препаратом первого выбора.
У женщин, у которых симптомы не проявляются на протяжении всей беременности, следует измерить уровень пролактина в сыворотке через 2 месяца после родов или прекращения кормления грудью, и, если он аналогичен значению до лечения, следует возобновить прием препарата (40).Точно так же женщинам, желающим кормить грудью, следует провести МРТ, чтобы убедиться в стабильности опухоли в течение 4–6 недель после родов (37), поскольку ДА снижают уровень ПРЛ в сыворотке, что впоследствии ухудшает лактацию.
Лечение макропролактином во время беременности
У женщин макропролактиномы встречаются реже, чем микропролактиномы. При макропролактиноме симптоматическое увеличение опухоли наблюдается в 20–30% случаев (41). Сообщалось, что риск клинически значимого увеличения опухоли падает с более чем 30% до <5%, если пациентка подвергается лучевой терапии или хирургическому вмешательству до беременности (25).
Беременные женщины с большими опухолями и женщины с экстраселлярным распространением, которые прекратили прием бромокриптина, подвержены риску роста опухоли, поэтому в каждом триместре необходимо проводить официальное исследование поля зрения. Так же, как и при микропролактиномах, нет необходимости измерять уровень пролактина в сыворотке на протяжении всей беременности, потому что уровни неравномерно увеличиваются во время беременности и не коррелируют с увеличением опухоли (8, 25). Кроме того, в этих случаях лечение должно быть индивидуализированным, так как данные, сравнивающие различные стратегии лечения, отсутствуют.
Пациентка должна быть проинформирована об относительно более высоком риске увеличения опухоли, необходимости нормализации уровня пролактина и важности лечения до зачатия.
В случае интраселлярных и небольших макропролактином, которые не прилегают к перекресту зрительных нервов, прием ДА следует прекратить при подтверждении беременности.
Пациент должен быть проинформирован о симптомах и необходимости срочного обследования при их появлении. В каждом триместре следует проводить тщательный клинический мониторинг с формальным исследованием поля зрения.Если пациент жалуется на головную боль или изменение зрения, следует провести МРТ. Если результаты МРТ подтверждают увеличение опухоли, женщине следует повторно назначить DA (5).
Бромокриптин считается препаратом первого выбора, и он обычно уменьшает размер аденомы и устраняет симптомы (42). Каберголин можно рассмотреть, если аденома не реагирует на бромокриптин (43).
Если увеличенная опухоль не отвечает на терапию каберголином, альтернативы включают транссфеноидальную операцию во втором триместре или родоразрешение, если беременность находится на достаточном сроке (16, 25, 41).
Пациентам с большими макропролактиномами и пациентам с экстраселлярным распространением настоятельно не рекомендуется забеременеть до тех пор, пока не будет проведена радикальная терапия. Терапию с хирургическим уменьшением объема можно рассмотреть до беременности, поскольку было показано, что хирургическое вмешательство или лучевая терапия снижают риск симптоматического увеличения опухоли (25), но в этих случаях существует высокий риск гипопитуитаризма. Однако операция по удалению опухоли менее предпочтительна, поскольку медикаментозная терапия во время беременности, вероятно, менее вредна, чем операция (41).Женщины с пролактиномами, устойчивыми к DA, обычно бесплодны. Таким образом, беременность в этих случаях является неожиданной, если они не подвергаются стимуляции яичников гонадотропинами или ГнРГ. Более того, беременность не рекомендуется женщинам с большими макропролактиномами, резистентными к лекарственным препаратам, и они не должны забеременеть, даже если опухоль является интраселлярной, до тех пор, пока размер не будет уменьшен с помощью транссфеноидальной хирургии.
Хирургическое вмешательство возможно в случаях, когда опухоль не уменьшилась во время медикаментозного лечения DA или у тех, у кого развился рост опухоли во время предыдущей беременности (44).
Влияние беременности и кормления грудью на уровень пролактина, объем опухоли и частоту ремиссий
В современной литературе показано, что беременность вызывает ремиссию гиперпролактинемии у двух третей женщин после прекращения приема ДА. В одном исследовании было обнаружено, что беременность вызывает ремиссию в 76% случаев неопухолевой гиперпролактинемии (NTHP), в 70% случаев микропролактином и в 64% случаев макропролактином с более высокой частотой рецидивов среди пациентов с макропролактиномами и пациентов с микропролактиномами с видимой опухолью на МРТ. на момент прекращения лечения (45).
В недавнем исследовании полная ремиссия была обнаружена у 100% пациентов с НТГП, у 66% пациентов с микропролактиномами и у 70% пациентов с макропролактиномами (46). Основные механизмы неясны, но обычно связывают с аутоинфарктом опухоли (46).
С другой стороны, нет данных, позволяющих предположить, что грудное вскармливание связано с повышенной выработкой пролактина или риском увеличения опухоли (28, 46). Таким образом, женщины могли нормально кормить грудью и возобновлять ДА после прекращения лактации.
Заключение
Лечение пролактиномы во время беременности является сложной задачей. Клинические испытания, подчеркивающие результаты медикаментозной терапии по сравнению с другими видами лечения, немногочисленны; поэтому пациент лечится на индивидуальной основе. Исход микроаденомы превосходный, что позволяет пациентам безопасно прекратить прием DA при тщательном клиническом наблюдении; с другой стороны, макроаденому необходимо лечить до зачатия, так как риск увеличения опухоли относительно высок.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Ссылки
1. Ciccarelli A, Daly AF, Beckers A. Эпидемиология пролактином. Гипофиз (2005) 8(1):3–6.10.1007/s11102-005-5079-0 [PubMed] [CrossRef] [Google Scholar]2. Индер В.Дж. Гиперпролактинемия – дифференциальный диагноз, обследование и лечение. Eur Endocr Rev (2006): 76–1002. [Google Академия]3. Карс М., Деккерс О.М., Перейра А.М., Ромейн Я.А. Обновление в пролактиномах. Neth J Med (2010) 68 (3): 104–12. [PubMed] [Google Scholar]4. Молич М.Е. пролактинома. гипофиз. Кембридж, Индиана: Наука Блэквелла; (1995).п. 433–77. [Google Академия]5. Мелмед С., Казануева Ф.Ф., Хоффман А.Р., Клейнберг Д.Л., Монтори В.М., Шлехте Дж.А. и соавт. Диагностика и лечение гиперпролактинемии: руководство по клинической практике эндокринологического общества. J Clin Endocrinol Metab (2011) 96(2):273–88.10.1210/jc.2010-1692 [PubMed] [CrossRef] [Google Scholar]6. Пишон М.Ф., Брессион Д., Пейон Ф., Милгром Э. Рецепторы эстрогена в аденомах гипофиза человека. J Clin Endocrinol Metab (1980) 51(4):897–902.10.1210/jcem-51-4-897 [PubMed] [CrossRef] [Google Scholar]7.Гиллам М.П., Молич М.Е., Ломбарди Г., Колао А. Достижения в лечении пролактином. Endocr Rev (2006) 27(5):485–534.10.1210/er.2005-9998 [PubMed] [CrossRef] [Google Scholar]8. Молич М.Е. Эндокринология при беременности: ведение беременной с пролактиномой. Eur J Endocrinol (2015) 172(5):R205–13.10.1530/EJE-14-0848 [PubMed] [CrossRef] [Google Scholar]9. Мах П.М., Вебстер Дж. Гиперпролактинемия: этиология, диагностика и лечение. Semin Reprod Med (2002) 20(4):365–74.10.1055/s-2002-36709 [PubMed] [CrossRef] [Google Scholar]10.Биллер БМ. Гиперпролактинемия. Int J Fertil Womens Med (1999) 44 (2): 74–7. [PubMed] [Google Scholar] 11. Банковский Б.Дж., Закур Х.А. Терапия агонистами допамина при гиперпролактинемии. Clin Obstet Gynecol (2003) 46(2):349–62.10.1097/00003081-200306000-00013 [PubMed] [CrossRef] [Google Scholar]12. Krupp P, Monka C. Бромокриптин при беременности: аспекты безопасности. Klin Wochenschr (1987) 65(17):823–7.10.1007/BF01727477 [PubMed] [CrossRef] [Google Scholar]13. Вебстер Дж. Сравнительный обзор профилей переносимости агонистов допамина при лечении гиперпролактинемии и подавлении лактации.Безопасность лекарств (1996) 14(4):228–38.10.2165/00002018-199614040-00003 [PubMed] [CrossRef] [Google Scholar]14. Нюбо Андерсен А.М., Вольфарт Дж., Кристенс П., Олсен Дж., Мелби М. Возраст матери и потеря плода: исследование связи регистров на основе популяции. BMJ (2000) 320(7251):1708–12.10.1136/bmj.320.7251.1708 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]15. Шибли-Рахал А., Шлехте Дж. Гиперпролактинемия и бесплодие. Endocrinol Metab Clin North Am (2011) 40(4):837–46.10.1016/j.ecl.2011.08.008 [PubMed] [CrossRef] [Google Scholar]16.Хрисулиду А., Будина М., Каравитаки Н., Били Э., Васс Дж. Гипофизарные нарушения при беременности. Гормоны (2015) 14(1):70–80.10.14310/horm.2002.1575 [PubMed] [CrossRef] [Google Scholar]17. Колао А., Ди Сарно А., Сарнаккиаро Ф., Фероне Д., Ди Ренцо Г., Мерола Б. и др. Пролактиномы, резистентные к стандартным агонистам дофамина, реагируют на длительное лечение каберголином. J Clin Endocrinol Metab (1997) 82(3):876–83.10.1210/jcem.82.8.4178-3 [PubMed] [CrossRef] [Google Scholar]18. Verhelst J, Abs R, Maiter D, van den Bruel A, Vandeweghe M, Velkeniers B, et al.Каберголин в лечении гиперпролактинемии: исследование 455 пациентов. J Clin Endocrinol Metab (1999) 84(7):2518–22.10.1210/jcem.84.7.5810 [PubMed] [CrossRef] [Google Scholar]20. Лю Дж.К., Кэдвелл В.Т. Современное лечение пролактином. Neurosurg Focus (2004) 16(4):E2.10.3171/foc.2004.16.4.3 [PubMed] [CrossRef] [Google Scholar]21. Оно М., Мики Н., Амано К., Кавамата Т., Секи Т., Макино Р. и др. Индивидуальная терапия высокими дозами каберголина при гиперпролактинемическом бесплодии у женщин с микро- и макропролактиномами.J Clin Endocrinol Metab (2010) 95(6):2672–9.10.1210/jc.2009-2605 [PubMed] [CrossRef] [Google Scholar]22. Чиккарелли Э., Гроттоли С., Раззор П., Гайя Д., Бертанья А., Чирилло С. и др. Длительное лечение каберголином, новым производным эрголина длительного действия, при идиопатической или опухолевой гиперпролактинемии и исходах медикаментозной беременности. J Endocrinol Invest (1997) 20(9):547–51.10.1007/BF03348017 [PubMed] [CrossRef] [Google Scholar]23. Джонс Дж., Башир Т., Олни Дж., Уитли Т. Лечение каберголином крупной макропролактиномы на протяжении всей беременности.J Obstet Gynaecol (1997) 17(4):375–6.10.1080/01443619750112916 [PubMed] [CrossRef] [Google Scholar]24. Молич М.Е. Пролактинома при беременности. Best Pract Res Clin Endocrinol Metab (2011) 25(6):885–96.10.1016/j.beem.2011.05.011 [PubMed] [CrossRef] [Google Scholar]25. Мусолино Н.Р., Бронштейн М.Д. Пролактиномы и беременность. Издательство Kluwer Academic Publishers; (2001). п. 91–108. [Google Академия] 26. Риччи Э., Параццини Ф., Мотта Т., Феррари С.И., Колао А., Клавенна А. и др. Исход беременности после лечения каберголином в первые недели гестации.Reprod Toxicol (2002) 16(6):791–3.10.1016/S0890-6238(02)00055-2 [PubMed] [CrossRef] [Google Scholar]27. Сталлдекер Г., Маллеа-Гил М.С., Гительман М., Альфьери А., Балларино М.С., Боэро Л. и др. Влияние каберголина на беременность и развитие эмбриона и плода: ретроспективное исследование 103 беременностей и обзор литературы. Pituitary (2010) 13(4):345–50.10.1007/s11102-010-0243-6 [PubMed] [CrossRef] [Google Scholar]28. Леббе М., Хубинонт С., Бернард П., Майтер Д. Исход 100 беременностей, начатых при лечении каберголином у женщин с гиперпролактинемией.Clin Endocrinol (2010) 73(2):236–42.10.1111/j.1365-2265.2010.03808.x [PubMed] [CrossRef] [Google Scholar]29. Ван А.Т., Муллан Р.Дж., Лейн М.А., Хазем А., Прасад С., Гатайя Н.В. и др. Лечение гиперпролактинемии: систематический обзор и метаанализ. Syst Rev (2012) 1:33.10.1186/2046-4053-1-33 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]30. Дюранто Л., Шансон П., Лавуанн А., Хорле С., Любецки Дж., Кун Дж.М. Влияние нового дофаминергического агониста CV 205-502 на уровни пролактина в плазме и размер опухоли при резистентных к бромокриптину пролактиномах.Clin Endocrinol (1991) 34(1):25–9.10.1111/j.1365-2265.1991.tb01731.x [PubMed] [CrossRef] [Google Scholar]31. Morange I, Barlier A, Pellegrini I, Brue T, Enjalbert A, Jaquet P. Пролактиномы, устойчивые к бромокриптину: долгосрочная эффективность хинаголида и исход беременности. Eur J Endocrinol (1996) 135(4):413–20.10.1530/eje.0.1350413 [PubMed] [CrossRef] [Google Scholar]32. Вебстер Дж. Клиническое лечение пролактином. Baillieres Best Pract Res Clin Endocrinol Metab (1999) 13(3):395–408.10.1053/beem.1999.0030 [PubMed] [CrossRef] [Google Scholar]34. Domingue ME, Devuyst F, Alexopoulou O, Corvilain B, Maiter D. Исход пролактиномы после беременности и кормления грудью: исследование 73 пациентов. Clin Endocrinol (2014) 80(5):642–8.10.1111/cen.12370 [PubMed] [CrossRef] [Google Scholar]35. Молич М.Е. Беременность и женщина с гиперпролактинемией. N Engl J Med (1985) 312(21):1364–70.10.1056/NEJM198505233122106 [PubMed] [CrossRef] [Google Scholar]36. Куперсмит М.Дж., Розенберг С., Клейнберг Д. Потеря зрения у беременных с аденомами гипофиза.Ann Intern Med (1994) 121(7):473–7.10.7326/0003-4819-121-7-199410010-00001 [PubMed] [CrossRef] [Google Scholar]37. Гемзелл С., Ван С.Ф. Исход беременности у женщин с аденомой гипофиза. Фертил Стерил (1979) 31 (4): 363–72. [PubMed] [Google Scholar] 38. Шлехте Я.А. Клиническая практика. пролактинома. N Engl J Med (2003) 349(21):2035–41.10.1056/NEJMcp025334 [PubMed] [CrossRef] [Google Scholar]39. Шлехте Я.А. Длительное лечение пролактином. J Clin Endocrinol Metab (2007) 92(8):2861–5.10.1210/jc.2007-0836 [PubMed] [CrossRef] [Google Scholar]40. Лавэй Б.А., Мир С.А. Беременность и гипофизарные заболевания: проблемы диагностики и лечения. Indian J Endocrinol Metab (2013) 17(6):996–1004.10.4103/2230-8210.122608 [бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]41. Молич М.Е. Лечение пролактином во время беременности. J Reprod Med (1999) 44 (12 Suppl): 1121–6. [PubMed] [Google Scholar]42. ван Роон Э., ван дер Вийвер Дж. К., Герретсен Г., Хекстер Р. Е., Ваттендорф Р. А. Быстрая регрессия супраселлярной пролактиномы после лечения бромокриптином во время беременности.Фертил Стерил (1981) 36 (2): 173–7. [PubMed] [Google Scholar]43. Лю С, Тиррелл Дж.Б. Успешное лечение крупной макропролактиномы каберголином во время беременности. Pituitary (2001) 4(3):179–85.10.1023/A:10153180 [PubMed] [CrossRef] [Google Scholar]44. Бронштейн М.Д., Сальгадо Л.Р., де Кастро Мусолино Н.Р. Медикаментозное лечение аденом гипофиза: частный случай ведения беременной. Pituitary (2002) 5(2):99–107.10.1023/A:1022364514971 [PubMed] [CrossRef] [Google Scholar]45. Колао А., Ди Сарно А., Каппабьянка П., Ди Сомма К., Пивонелло Р., Ломбарди Г.Прекращение длительной терапии каберголином по поводу опухолевой и неопухолевой гиперпролактинемии. N Engl J Med (2003) 349(21):2023–33.10.1056/NEJMoa022657 [PubMed] [CrossRef] [Google Scholar]46. Ауриемма Р.С., Пероне И., Ди Сарно А., Грассо Л.Ф., Герра Э., Гаспери М. и др. Результаты одноцентрового обсервационного 10-летнего обзорного исследования рецидивов гиперпролактинемии после беременности и лактации. J Clin Endocrinol Metab (2013) 98(1):372–9.10.1210/jc.2012-3039 [PubMed] [CrossRef] [Google Scholar]Беременность способствует развитию опухолей гипофиза за счет увеличения скорости клеточного цикла
Введение
Опухоли гипофиза в основном представляют собой аденомы и возникают в гипофиз (1).Они состоят трех категорий в зависимости от их биологических функций: Доброкачественные опухоли, инвазивные опухоли и карциномы (2). Рак гипофиза относится к злокачественным тип опухоли, встречающийся только в 0,1–0,2% случаев опухоли гипофиза (3). Карциномы гипофиза бывают только диагностируется при наличии метастазов внутри или вне нервной системы. наблюдается (1). Поскольку гипофиз железы близко к мозгу, инвазивные аденомы гипофиза могут проникать черепной кости и привести к побочным эффектам (4). Они могут вызывать усиление внутричерепного давление и различные виды головной боли (5,6).
Опухоли гипофиза делятся на секретирующие и несекретирующие опухоли, причем большинство опухолей являются секретирующий тип (7). Они производят обильное количество гормонов, и секреция гормонов может вызвать несколько форм гиперпитуитаризма (8). У беременных женщин избыток гормона секреция может вызвать заболеваемость матери или плода (9). Наблюдение за ростом опухоли и гормонами уровень в крови беременных помогает плоду расти быть здоровым и быть успешно доставленным (10).
Для этих беременных женщин с опухолями гипофиза: опухоли гипофиза могут выделять гормоны, влияющие на здоровье мать и плод; кроме того, беременность может также способствовать развитию опухоли рост (11). Беременные секретируют различные виды гормонов, в том числе прогестерон и человеческий плацентарный лактоген (12), который может способствуют росту опухоли (13,14). Наблюдение за размером опухоли также необходим для самого роста опухоли, так как беременность может способствовать прогрессирование опухоли гипофиза (11). Однако остается открытым вопрос о том, как беременность влияет на рост опухоли гипофиза. не понятно.Было показано, что нейротрофический фактор головного мозга (BDNF) выявляется на повышенном уровне у беременных самок по сравнению с небеременными женщинами (15). BDNF связан с раком легких прогноз (16). Однако в лучшую сторону насколько нам известно, еще не сообщалось, является ли BDNF участвует в эффекте, который беременность проявляет в индукции рост опухолевых клеток гипофиза. В настоящем исследовании установлено, что беременность модели мышей. Время возникновения опухоли и масса опухоли были определяли, а уровни BDNF у беременных или контрольных мышей были измерены.Кроме того, влияние BDNF на пролиферацию исследовали опухолевые клетки гипофиза. Как BDNF влияет на рост опухолевых клеток рост исследовали с помощью клеточного цикла анализ распределения. Результаты настоящего исследования выявили способствовала ли беременность росту опухоли гипофиза у мышей модели и определил лежащий в основе молекулярный механизм того, как беременность влияет на рост опухоли гипофиза. Результаты Настоящее исследование показывает, что может быть полезно контролировать Влияние беременности на опухоли гипофиза и терапия гипофиза опухоли.
Материалы и методы
Эксперименты на животных
Всего было отобрано 16 самок голых мышей в возрасте 8 недель. приобретены в Шанхайском центре лабораторных животных (Шанхай, Китай). Все мыши содержатся в условиях отсутствия специфических патогенов (SPF). помещение и кормят стерилизованной пищей и водой. Средний вес мышей было 30 г. Всех мышей случайным образом разделили на 2 группы по 8 мышей в каждой группе, пронумерованные идентификаторами. Каждой мыши подкожно вводили 5×106 AtT-20. клетки.Через 7 дней одну группу мышей скрещивали с мышами-самцами, тогда как другая группа была воспитана в тех же условиях, что и беременных мышей (в помещении для животных SPF и кормят стерилизованным кормом и вода). Самок мышей проверяли на наличие пессариев в утром, чтобы указать на возможность ее беременности, а мыши с пессарии были выбраны для последующих экспериментов. Беременность самок мышей проверяли через 14 дней после спаривания. В общей сложности Для спаривания было использовано 17 самок мышей, а также 8 беременных мышей. наконец, использовали в группе беременных, и 8 самок мышей, которые были неспаренные использовались в качестве контроля.Возникновение опухолей было проверяли каждые 3 дня после инъекции опухолевых клеток. Мыши были эвтаназии через 28 дней после инъекции опухоли. Опухоли были выделяют и взвешивают. Орбитальную кровь мышей собирали в 14-й день для анализа ELISA. Все эксперименты на животных были одобрены Институциональный совет по животным Шаньдунской дорожной больницы (Шаньдун, Китай) и проводится в соответствии с требованиями общественного здравоохранения США. Политика обслуживания по гуманному уходу и использованию лабораторных животных (17).
Определение уровней BDNF
Уровень BDNF в сыворотке крови мышей определяли с помощью Набор BDNF ELISA (R&D Systems, Inc., Миннеаполис, Миннесота, США; Кот. нет. DBNT00), содержащий детекцию, конъюгированную с пероксидазой хрена антитела, а также буферы для разведения и промывки в соответствии с протокол производителя. Образцы крови и стандартные белки были приготовлены до эксперимента (18). Разбавитель для анализа (100 мкл) добавляли к в каждую лунку 96-луночного планшета с последующим добавлением 50 мкл образцы крови от беременных мышей или небеременных мышей и инкубация при комнатной температуре в течение 2 часов. Всего обнаружение 100 мкл В каждую лунку добавляли антитело, разведенное в разбавителе реагента. и инкубируют при комнатной температуре в течение 1 часа.Аликвоты по 100 мкл рабочий раствор Стрептавидина-HRP инкубировали при комнатной температуре. температуры в течение 20 мин после инкубации антител и промывания 3 раз с промывочным буфером. Затем добавляли раствор субстрата. в течение 30 мин при комнатной температуре в темноте с последующей остановкой со стоп-раствором из набора ELISA (R&D Systems, Inc.). Поглощение при 450 нм оценивали и рассчитывали на основе стандартная кривая.
Культура клеток
Клетки опухоли гипофиза мыши AtT-20 были приобретены из банка клеток Шанхайского института биологических наук (Шанхай, Китай).Клетки поддерживали в среде RPMI-1640. (Thermo Fisher Scientific, Inc., Уолтем, Массачусетс) с 10% бычьего эмбриона сыворотка (Thermo Fisher Scientific, Inc.), дополненная 100 мкг/мл стрептомицин и пенициллин 100 ЕД/мл. Клетки были разделены на соотношении 1:3, когда они достигают 90–100% слияния и культивируются при 37°C во влажной атмосфере с 5% CO2.
Обнаружение клеточной пролиферации
Клетки AtT-20 были обработаны трипсином и разделены на 96-луночные планшеты по 3×103 клеток/лунку. Клетки были обработаны 50 нг/мл BDNF.Клетки выдерживали при 37°С в течение 2, 4 и 6 дней соответственно. Жизнеспособность клеток измеряли при указанные дни (2, 4 и 6 дни) с помощью набора для подсчета клеток-8 (CCK-8; Институт биотехнологии Beyotime, Хаймен, Китай), согласно протоколу производителя. Реактив CCK-8 (10 мкл) добавляли непосредственно в каждую лунку. Клетки инкубировали в течение 4 ч при 37°С. Жизнеспособность клеток измеряли при 450 нм. То кривую пролиферации строили по поглощению клеток при день 0 в качестве контроля.
Обнаружение клеточного цикла
Клетки AtT-20 были разделены на 6-луночные чашки в 3×105 клеток/лунку. Клетки обрабатывали 50 нг/мл BDNF при 37°С в течение 2 дней. Через 2 дня лечения клетки культуры трипсинизировали до одноклеточной суспензии и фиксировали 70% этанолом при 4°С в течение 30 мин. Клетки центрифугировали при 300×g при комнатной температуре в течение 5 мин и три раза промывали PBS. раз. Затем клетки инкубировали с 50 мкг/мл РНКазы А. (Sigma-Aldrich; Merck KGaA) на водяной бане при 37°C в течение 30 мин и окрашено 50 мкг/мл йодида пропидия (Sigma-Aldrich; Merck KGaA) при комнатной температуре в темноте в течение 30 мин.Клетки были отфильтрованы и подвергнуты проточной цитометрии для обнаружения клеточного цикла. То образцы были обнаружены с помощью LSR II (BD Biosciences, Franklin Lakes, Нью-Джерси, США) и проанализированы с использованием программного обеспечения FlowJo версии 8 (Tree Star, Inc., Ашленд, штат Орегон, США).
Статистический анализ
Все данные представлены как среднее ± стандарт отклонение (SD) или среднее ± SD. Независимые эксперименты были выступал трижды. Сравнения между группами были проанализированы с использованием t-критерия Стьюдента и программного обеспечения R версии 3.2.2 (https://www.r-project.org/). P<0,05 считалось указать на статистически значимую разницу между группы.
Результаты
Беременность способствует развитию опухоли из клеток AtT20 рост
Чтобы проверить, способствует ли беременность прогрессированию опухолей гипофиза, клетки опухоли гипофиза AtT-20 были подкожно вводили 8 мышам в каждой группе, и мышам спарились через 7 дней. Беременность мышей проверяли 14 дней после спаривания и опухоли собирали через 28 дней после опухолевых клеток инъекции (рис.1А). Беременность была Обнаружено, что он способствует росту опухоли у голых мышей. Возникновение опухоли в беременных мышей ранее сравнивали с контрольными мышами (таблица I). Опухоли увеличивались в беременных мышей по сравнению с неспаренными мышами (рис. 1В).
Таблица I.Время возникновения опухоли. |
Таблица I.
Время возникновения опухоли.
| Время, дни | Контрольная группа, n | Беременная группа, N |
|---|---|---|
| 7 | 0/8 | 0/8 |
| 10 | 0/8 | 0/8 |
| 14 | 2/8 | 6/8 |
| 17 | 6/8 | 8/8 |
| 21 | 8/8 | 8/8 |
| 24 | 8/8 | 8/8 |
| 28 | 8/8 | 8/8 |
Производство BDNF увеличено в беременные обнаженные мыши
Чтобы проверить, проявляли ли беременные мыши повышенный уровень BDNF, определяли уровень BDNF в сыворотке крови с помощью набора ИФА.Установлено, что беременные мыши проявляют повышенный уровень BDNF по сравнению с контрольными мышами (рис. 2).
BDNF способствует росту клеток AtT-20
Чтобы проверить, способен ли BDNF стимулировать опухоль рост, уровни BDNF клеток AtT-20 анализировали in vitro. Клетки AtT-20 обрабатывали BDNF или без него, а клетки жизнеспособность определяли через 2, 4 и 6 дней после BDNF. лечение. BDNF увеличил скорость пролиферации клеток AtT-20 (рис. 3).
BDNF изменяет клеточный цикл AtT20 распределение
Чтобы выяснить, как BDNF регулирует рост клеток AtT-20, исследовали клеточный цикл клеток AtT-20.Было установлено, что Обработка BDNF была способна изменить распределение клеточного цикла Клетки АтТ-20. Уменьшение количества клеток фазы G0/G1 присутствовало в Клетки, обработанные BDNF (рис. 4). Как ячейки в фазе G0 находятся в состоянии покоя клетки (19), обработка BDNF может способствовать Клетки AtT-20 вступают в клеточный цикл и пролиферируют. БДНФ лечение увеличивает скорость клеточного цикла.
Обсуждение
Опухоли гипофиза в основном являются доброкачественными опухолями и редко метастазируют в другие органы (4).Только 0,1–0,2% классифицируются как карциномы (1). Опухоли гипофиза исходят из гипофиза (1). Большинство опухолей гипофиза секретируют чрезмерные гормоны (11). То повышенный уровень гормонов может иметь определенные побочные эффекты на пациентов, особенно беременных женщин (11).
Не только опухоли гипофиза выделяют гормоны; беременность может также способствовать секреции большого количества гормоны (13). Опухоли гипофиза являются гормоносекретирующие опухоли, а также на них влияет гормоны, выделяемые во время беременности.Опухоли гипофиза неупорядочены беременностью (20,21). Однако как беременность влияет рост опухоли гипофиза изучен недостаточно.
Сообщается, чтоBDNF связан с беременность (22). Повышенный уровень BDNF были обнаружены в крови беременных женщин. (9). Чтобы определить, является ли BDNF причиной того, что беременность способствует росту опухоли гипофиза, мышь модель была создана в настоящем исследовании. Подкожный ксенотрансплантат был установлен на голых самках мышей с опухолью гипофиза AtT-20. клетки.Самок мышей скрещивали с самцами, и опухоль время возникновения, массу опухоли и уровень BDNF в крови. обнаружено. Повышенный уровень BDNF выявлен у беременных мышей по сравнению с контрольными мышами (рис. 2). Опухоли возникали раньше у беременных мышей по сравнению с контрольные мыши (таблица I). В сравнении с контрольными мышами опухоли росли быстрее у беременных мышей. и более крупные опухоли развились в конце эксперимента (Рисунок 1). Это указывало на то, что BDNF может быть связано со стимулированием роста опухоли гипофиза.Подтвердить В соответствии с этой гипотезой клетки AtT-20 обрабатывали BDNF в vitro и измеряли скорость пролиферации клеток. Повышенная способность к пролиферации была выявлена у обработанных BDNF клетки (рис. 3). Поскольку пролиферация заметно связаны с клеточным циклом (23), чтобы выяснить, как BDNF влияет на скорость пролиферации клеток AtT-20, распределение клеточного цикла Клетки, обработанные BDNF, и контрольные клетки были обнаружены. BDNF изменил распределение клеток AtT-20 по клеточному циклу. Пониженное соотношение G0/G1 клетки и увеличенное количество клеток S-фазы были идентифицированы в эксперименты (рис.4). Клетки в G0 фазы находятся в состоянии покоя (19). BDNF уменьшил эту субпопуляцию и увеличилось количество клеток в S-фазе. Это указывало на то, что BDNF запускал покоящиеся клетки для включения в клеточный цикл. После обработки BDNF пролиферировало больше клеток. Это может привести к более раннему возникновению опухолей и более крупных опухолей в мышей.
В настоящем исследовании было установлено, что BDNF изменяет распределение клеток AtT-20 по клеточному циклу. Номер количество покоящихся клеток уменьшалось при обработке BDNF.Покой — это связаны с раковыми стволовыми клетками, субпопуляцией раковых клеток которые имеют решающее значение для прогрессирования опухоли (24–26). опухоль стволовые клетки были зарегистрированы в основном в состоянии покоя (27,28). Дифференцировка опухолевых стволовых клеток может привести к потере состояния покоя (29,30). То существование стволовых клеток опухоли гипофиза общепризнано. (31,32). Экспрессия BDNF связана с нейронные стволовые клетки (33). это возможно, что лечение BDNF увеличивает скорость опухоли гипофиза самообновление стволовых клеток, способствующее вступлению клеток в клеточный цикл для роста опухоли.
Результаты настоящего исследования показали, что беременность может способствовать росту опухоли гипофиза в модели мышей. BDNF играет решающую роль в стимулировании прогрессирования опухоли путем увеличение скорости клеточного цикла, что приводит к росту опухолевых клеток гипофиза in vitro и in vivo. То результаты настоящего исследования позволяют предположить, что мониторинг влияния беременности при опухолях гипофиза может быть полезным для терапии опухоли гипофиза.
Каталожные номера
1 | Эззат С., Аса С.Л., Коулвелл В.Т., Барр С.Е., Dodge WE, Vance ML и McCutcheon IE: «Распространенность заболеваний гипофиза». аденомы: систематический обзор.Рак. 101: 613–619. 2004. Просмотр статьи : Академия Google |
2 | Каравитаки Н. Распространенность и заболеваемость аденомы гипофиза. Энн Эндокринол (Париж). 73:79–80. 2012. Просмотр статьи : Академия Google |
3 | Heaney AP: Клинический обзор: гипофиз карцинома: сложная диагностика и лечение. Дж. Клин Эндокринол Метаб. 96:3649–3660. 2011. Просмотр статьи : Google Scholar |
4 | Шайтхауэр Б.В., Ковач К.Т., Лоуз Э.Р. младший и Рэндалл Р.В.: Патология инвазивных опухолей гипофиза с особыми ссылка на функциональную классификацию.Дж Нейрохирург. 65:733–744. 1986. Просмотр статьи : Google Scholar |
5 | Леви М.Дж., Матару М.С., Миран К., Пауэлл М. и Goadsby PJ: Клинические характеристики головной боли у больных с опухолями гипофиза. Головной мозг. 128:1921–1930. 2005. Просмотр статьи : Академия Google |
6 | Милош П., Хавелиус У. и Хиндфельт Б.: Кластерная головная боль у больного с аденомой гипофиза. С Обзор литературы.Головная боль. 36:184–188. 1996. Просмотр статьи : Google Scholar |
7 | Кирк Л.Ф.-младший, Хэш Р.Б., Катнер Х.П. и Джонс Т: Болезнь Кушинга: Клиника и диагностика оценка. Ам семейный врач. 62 (1119–1127): 1133–1134. 2000. |
8 | Кумар В., Аббас А., Фаусто Н. и Астер Дж.: Роббинс и Котран, патологические основы болезни. 9-й. Эльзевир Медицинских наук. ISBN 9780323296397 (электронная книга). |
9 | Lee NM и Saha S: Тошнота и рвота беременность. Гастроэнтерол Клин Норт Ам. 40:309–334, vii. 2011. Просмотр статьи : Академия Google |
10 | Шарма Дж. Б., Рой К. К., Моханрадж П., Кумар С., Кармакар Д. и Баруа Дж. Исход беременности при опухолях гипофиза. Арка Гинекол Обст. 280:401–404. 2009. Просмотр статьи: Google Scholar |
11 | Молич М.Е.: Опухоли гипофиза и беременность.Гормон роста IGF Res. 13: Приложение А. S38–S44. 2003. Просмотр статьи : Академия Google |
12 | Кумар П. и Магон Н.: Гормоны в беременность. Медицина Нигера J. 53: 179–183. 2012. Просмотр статьи : Google Scholar |
13 | Караджа З., Танриверди Ф., Унлухизарчи К. и Келестимур Ф. Беременность и нарушения функции гипофиза. Евр Дж Эндокринол. 162: 453–475. 2010. Просмотр статьи : Google Scholar |
14 | Молич М.Е.: Гипофизарные нарушения во время беременность.Эндокринол Метаб Клин Норт Ам. 35:99–116, vi. 2006. Просмотр статьи : Академия Google |
15 | Миршокрай П., Хассанпур Х., Рахнама А. и Foster WG: Экспрессия генов BDNF и его рецепторов, TrkB и p75 в матке и яйцеводе беременных и небеременных маток. Рез Ветеринарная наука. 95:164–168. 2013. Просмотр статьи : Google Scholar |
16 | Окамура К., Харада Т., Ван С., Иджичи К., Фуруяма К., Кога Т., Окамото Т., Такаяма К., Яно Т. и Наканиши Ю.: Экспрессия TrkB и BDNF связана с плохим прогнозом при немелкоклеточный рак легкого.Рак легких. 78:100–106. 2012. Просмотр статьи : Академия Google |
17 | Национальные институты здравоохранения США: Благополучие лабораторных животных: политика службы здравоохранения в отношении уход за лабораторными животными и их использование учреждениями-наградителями; уведомление. Реестр ФРС. 50:19584–19585. 1985. |
18 | Ма Х, Го Дж, Ся Дж, Ню С, Шэнь С, Сун Х и Zheng Y: Приготовление и применение кроличьего антимышиного Setd8 поликлональные антитела.Си Бао Ю Фен Цзы Мянь И Сюэ За Чжи. 33:246–251. 2017 г. (на китайском языке). |
19 | Томура М., Сакауэ-Савано А., Мори Ю., Такасе-Уцуги М., Хата А., Отава К., Канагава О. и Мияваки А.: В отличие от покоящейся фазы G0 с митотическим клеточным циклом в иммунная система мыши. ПЛОС Один. 8:e738012013. Просмотр статьи : Академия Google |
20 | Прагер Д. и Браунштейн Г.Д.: Гипофиз нарушения во время беременности.Эндокринол Метаб Клин Норт Ам. 24:1–14. 1995. |
21 | Надер С.: Гипофизарные нарушения и беременность. Семин Перинатол. 14:24–33. 1990. |
22 | Фунг Дж., Гелай Б., Чжун К.И., Рондон М.Б., Санчес С.Э., Барриос Ю.В., Хевнер К., Цю С. и Уильямс М.А.: Ассоциация со сниженным нейротрофическим фактором головного мозга в сыворотке крови (BDNF) концентрации на ранних сроках беременности с дородовым депрессия.БМС Психиатрия. 15:432015. Просмотр статьи : Академия Google |
23 | Эван Г.И. и Вусден К.Х. Распространение, клеточный цикл и апоптоз при раке. Природа. 411: 342–348. 2001. Просмотр статьи : Академия Google |
24 | Beck B и Blanpain C: Разгадка рака потенциал стволовых клеток. Нат Рев Рак. 13: 727–738. 2013. Просмотр статьи : Google Scholar |
25 | Нгуен Л.В., Ваннер Р., Диркс П. и Ивз К.Дж.: Раковые стволовые клетки: развивающаяся концепция.Нат Рев Рак. 12:133–143. 2012. |
26 | Дин М.: Раковые стволовые клетки: последствия для определения причины рака и резистентности к терапии. Дисков Мед. 5: 278–282. 2005. |
27 | Ян И, Сюй Х, Хуан В, Дин М, Сяо Дж, Yang D, Li H, Liu XY и Chu L: Борьба с раком легких, похожим на ствол клетки с геном TRAIL, вооруженные онколитическим аденовирусом. J Cell Mol Med. 19:915–923. 2015. Просмотр статьи : Google Scholar |
28 | Мартин В., Санчес-Санчес А.М., Эррера Ф., Гомес-Мансано С., Фуэйо Х., Альварес-Вега М.А., Антолин И. и Родригес C: Индуцированное мелатонином метилирование промотора ABCG2/BCRP в качестве новый механизм преодоления множественной лекарственной устойчивости опухоли головного мозга стволовые клетки.Бр Дж Рак. 108:2005–2012. 2013. Просмотр статьи : Google Scholar |
29 | Ли Н, Ян И, Дин М, Хуан В, Ли Х, Е Дж, Xiao J, Zha X и Xu H: Стабильная трансфекция GFP облегчила Характеристика стволовых клеток рака легкого. Мол Биотехнолог. 56:1079–1088. 2014. Просмотр статьи : Google Scholar |
30 | Чен К., Хуан Ю. Х. и Чен Д. Л.: Понимание и нацеливание на раковые стволовые клетки: терапевтические последствия и вызовы.Акта Фармакол Син. 34:732–740. 2013. Просмотр статьи : Академия Google |
31 | Андониаду CL, Мацусима Д., Гарави Мусави С.Н., Синьор М., Макинтош А.И., Шеффер М., Гастон-Массуэ C, Mollard P, Jacques TS, Le Tissier P и др.: Sox2(+) стволовые клетки/клетки-предшественники в поддерживающем органе гипофиза взрослой мыши гомеостаза и обладают опухолеиндуцирующим потенциалом. Клеточная стволовая клетка. 13:433–445. 2013. Просмотр статьи : Google Scholar |
32 | Tunici P и Yu JS: Ствол аденомы гипофиза клетки.Методы Мол Биол. 568:195–201. 2009. Просмотр статьи: Google Scholar |
33 | Chen SQ, Cai Q, Shen YY, Cai XY и Lei HY: Комбинированное использование NGF/BDNF/bFGF способствует пролиферации и дифференцировка нейральных стволовых клеток in vitro. Int J Dev Neurosci. 38:74–78. 2014. Просмотр статьи : Google Scholar |
Успешная беременность у женщины с крупной пролактиномой после апоплексии опухоли гипофиза
Апоплексия гипофиза — редкое состояние, которое в тяжелых случаях может привести к смерти пациентки и во многих случаях приводит к гипопитуитаризму.Мы сообщаем о случае апоплексии при большой пролактиноме, приведшей к синдрому пустого турецкого седла с последующим успешным наступлением беременности. Наш пациент — 32-летняя женщина с историей макропролактиномы в течение примерно 17 лет, которая поступила в нашу больницу с историей сильной головной боли, снижения уровня сознания, лихорадки, тошноты, рвоты и диплопии продолжительностью 12 часов. Магнитно-резонансная томография при поступлении показала увеличение размеров аденомы гипофиза с малозаметными кровоизлияниями.Больной был госпитализирован в отделение реанимации и лечился консервативно. Состояние больного улучшилось в течение нескольких дней. Через несколько месяцев у нее начались регулярные менструации. Магнитно-резонансная томография гипофиза через 1,5 года выявила синдром пустого турецкого седла, и примерно через год она забеременела. При разрешении аденомы гипофиза после развившейся гипофизарной апоплексии и продолжении приема каберголина у пациентки наступила благополучная беременность без рецидива аденомы после родов и грудного вскармливания.
1. Введение
Апоплексия опухоли гипофиза относится к клиническому синдрому, состоящему из признаков и симптомов, возникающих при быстром распространении содержимого турецкого седла [1]. Обычно это результат кровоизлияния или инфаркта ранее существовавшей аденомы гипофиза [1]. Риск значительно выше при макроаденомах, чем при микроаденомах [1, 2]. Гипофизарная апоплексия обычно проявляется сильной головной болью, офтальмоплегией, нарушениями зрения и зрачков, угнетением чувствительности [3].Иногда кровоизлияние протекает бессимптомно и может встречаться до 25% аденом [4]. Приблизительно у 80% пациентов при поступлении развивается дефицит одного или нескольких гормонов передней доли гипофиза [5]. Редко сообщалось о разрешении гиперсекреторных состояний после апоплексии у пациентов с акромегалией [6], синдроме Кушинга [7], пролактиномах [6, 8] и разрешении опухоли при нефункционирующих аденомах [9]. Факторы, повышающие риск апоплексии опухоли гипофиза, включают травму головы, артериальную гипотензию, прием антикоагулянтов, хирургическое вмешательство, динамическое исследование гипофиза, облучение и артериальную гипертензию в анамнезе [1, 4].Сообщалось, что агонисты дофамина являются предрасполагающим фактором при применении бромокриптина в большей степени, чем каберголина [10, 11].
Мы сообщаем об этом случае из-за разрешения большой пролактиномы с апоплексией опухоли гипофиза, но это произошло не сразу после апоплексии, а примерно через 1,5 года. Наш пациент также продолжал принимать каберголин, что могло быть дополнительным фактором в разрешении аденомы. Пациентка смогла забеременеть без каких-либо осложнений во время беременности и продолжила рассасывание аденомы после родов и грудного вскармливания.
2. История болезни
32-летняя женщина поступила в отделение неотложной помощи в мае 2008 г. с 12-часовой историей сильной головной боли, лихорадки, тошноты, рвоты и диплопии. Ее прошлый анамнез показал, что она принимала и прекращала лечение макропролактиномы в течение приблизительно 17 лет. Пациента госпитализировали в отделение интенсивной терапии, где ему вводили внутривенно стероиды, антибиотики из-за инфекции мочевыводящих путей и другие поддерживающие меры. Анамнез показал, что у пациентки были нормальные менструации в течение примерно одного года после полового созревания, а затем у нее развилась аменорея.Позже пациентка вышла замуж и прошла обследование на бесплодие, которое показало, что у нее макропролактинома. Ей назначили бромокриптин, но без улучшения. В августе 2000 года она уехала за границу для дальнейшего лечения. В отчете о магнитно-резонансной томографии (МРТ) было выявлено интраселлярное поражение диаметром см, которое инфильтрировало левый кавернозный синус, покрывая левый кавернозный синус и внутреннюю сонную артерию. В то время ее уровень пролактина составлял 179 нг/мл (1,39–24,2 нг/мл). Пациентке было рекомендовано продолжать прием бромокриптина.
Состояние пациентки продолжало ухудшаться с усилением головных болей и аменореи при уровне пролактина около 200 нг/мл (1,39–24,2 нг/мл). Повторные МРТ в течение следующего года не выявили существенного изменения размеров аденомы.
Еще через 5 лет в апреле 2005 г. пациентка снова выехала за границу, и ей посоветовали операцию, так как она не ответила на лечение, и она перенесла транссфеноидальную операцию, но без особого успеха, а повторная МРТ после операции не показала изменений в размеры аденомы гипофиза (рис. 1).В последующий период пациент продолжал принимать и прекращать прием бромокриптина.
Состояние пациента не улучшилось, поэтому в апреле 2007 года пациент снова выехал за границу для дальнейшего лечения. Обследование показало, что уровень пролактина увеличился до 9400 нг/мл (1,39–24,2 нг/мл), а оставшаяся функция гипофиза была в пределах нормы, за исключением подавления ЛГ и ФСГ. МРТ показала увеличение размеров макроаденомы до см. Аденома полностью инфильтрировала левый кавернозный синус, а левая внутренняя сонная артерия была полностью окружена опухолью.Опухоль достигла зрительного канала, но без компрессии перекреста зрительных нервов. Эндокринолог и нейрохирург, наблюдавшие пациентку в то время, начали ей 0,5 мг каберголина два раза в неделю и постепенно увеличивали дозу до максимальной 4,5 мг в неделю.
Контрольная МРТ через 6 месяцев в декабре 2007 г. показала уменьшение размеров пролактиномы, которая уменьшилась до см, уровень пролактина на тот момент составил 261 нг/мл (1,39–24,2 нг/мл), а состояние улучшилось.В апреле 2008 г. ее уровень пролактина составлял 125 нг/мл (1,39–24,2 нг/мл), а тест поля зрения оказался нормальным.
В мае 2008 г., примерно через 13 месяцев после начала приема каберголина, у нее развился гипофизарный апоплексический удар. Состояние больного стабилизировалось на фоне внутривенного введения стероидов и других поддерживающих мероприятий. На МРТ при поступлении выявлено увеличение размеров селлярной и супраселлярной масс см. Отмечалось слабое линейное гиперинтенсивное поражение в верхней части поражения, свидетельствующее о тонком кровоизлиянии, и было увеличение размера по сравнению с предыдущей МРТ, сделанной 5 месяцами ранее в декабре 2007 года.Состояние больной улучшилось на фоне консервативного лечения, в анализе крови в стационаре выявлены нормальные показатели функции щитовидной железы, пролактин снизился до 17,3 нг/мл (1,39–24,2 нг/мл), ЛГ 4,6 мМЕ/мл (1–18 мМЕ/мл). , и ФСГ 4,2 мкЕд/мл (4-13,0 мкЕд/мл), эстрадиол был 7,21 мкг/мл (20-150 мкг/мл), и ее кортизол не проверяли до начала приема стероидов. Больная выписана из стационара через 5 дней в удовлетворительном состоянии.
Осмотр поля зрения после выписки показал дефект левого носового поля, которого раньше не было.Терапия пациентки была снижена, и анализ ее крови показал нормальный уровень кортизола и нормальные тесты функции щитовидной железы, пролактин был 23,2 нг/мл (1,39–24,2 нг/мл), а эстрадиол увеличился до 39 мкг/мл (20–20–24,2 нг/мл). 150 пг/мл). Ее доза каберголина была снижена при выписке из больницы до 2,5 мг в неделю. Через два месяца после выписки из стационара в июле 2008 г. повторная МРТ показала значительное уменьшение размеров аденомы до см с признаками старого кровоизлияния. Через 3 мес после гипофизарной апоплексии у больной начались регулярные менструации.Сообщалось, что повторное поле зрения было нормальным. В последующие месяцы уровень пролактина оставался низким на уровне примерно 2–3 нг/мл (1,39–24,2 нг/мл), а доза каберголина постепенно снижалась до 1 мг еженедельно. Повторная МРТ в апреле 2009 года показала небольшое уменьшение размера аденомы по сравнению с предыдущей МРТ, и размер аденомы составил см.
Примерно через 1,5 года после гипофизарной апоплексии больная обратилась с вопросом о возможности беременности.От повторной операции пациентка отказалась, с пациенткой обсудили риск увеличения размеров аденомы во время беременности и, если это произойдет, ей может понадобиться срочная операция во время беременности. В то время пациентка не принимала никаких противозачаточных средств, но не лечилась, чтобы попытаться зачать ребенка. МРТ была назначена в ноябре 2009 года, но пациентка представила отчет только примерно через год, когда она заподозрила, что беременна.Тест на беременность был положительным, а МРТ, сделанная годом ранее, показала наличие синдрома пустого турецкого седла (рис. 2(а)). Уровень пролактина был очень низким, поэтому было принято решение прекратить прием каберголина и вести консервативное наблюдение за больным.
Беременность протекала без осложнений, с умеренным повышением уровня пролактина по мере течения беременности (табл. 1) и примерно на 24-й неделе беременности пациентка стала жаловаться на легкие головные боли, поле зрения было упорядочено и выявило небольшое левый носовой дефект, и пациентка отказалась от МРТ, поэтому ей был начат бромокриптин 2.5 мг ежедневно. Поле зрения, повторенное через месяц, показало аналогичные результаты, и доза бромокриптина постепенно увеличивалась ежемесячно до тех пор, пока пациент не стал принимать 7,5 мг в день. Дальнейших жалоб во время беременности пациентка не предъявляла, а в сроке 38 недель ей было выполнено плановое кесарево сечение, родила здорового ребенка.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||
Пациент пожелал кормить грудью своего ребенка после доставки так ее и не перезапустили на каберголине.Ей сделали повторную МРТ через 5 недель после родов в августе 2011 г., которая снова была зарегистрирована как синдром пустого турецкого седла (рис. 2(b)). Она продолжала кормить ребенка грудью, и через несколько месяцев после родов у нее снова начался менструальный цикл. Она не принимала никакого лечения до 1 года и 8 месяцев после родов, когда решила прекратить грудное вскармливание. МРТ была повторена в апреле 2013 года, но все еще показывала синдром пустого турецкого седла, а ее пролактин в то время составлял 97,7 нг/мл (1,39–24,2 нг/мл), поэтому ей назначили короткий курс каберголина, чтобы помочь ей прекратить грудное вскармливание. .Во время последующего наблюдения, если уровень пролактина быстро нормализуется, мы рассмотрим возможность продолжения лечения без лечения, но если уровень пролактина останется слегка повышенным, мы будем продолжать принимать каберголин, поскольку в это время она хочет снова забеременеть.
3. Обсуждение
У нашей пациентки после апоплексии опухоли гипофиза было разрешение макропролактиномы с нормализацией уровня пролактина. Пока она находилась под наблюдением в конце второго триместра из-за усиливающихся головных болей и небольшого дефекта зрения, было решено возобновить ее прием агониста дофамина.Она начала лечение бромокриптином из-за более длительного периода безопасности по сравнению с каберголином, хотя некоторые исследования не показали повышенного риска при использовании каберголина во время беременности [12, 13]. У нашей пациентки после апоплексического удара уровень пролактина нормализовался, а уровень пролактина снизился до 2-3 нг/дл и оставался на этом уровне примерно 2,5 года, пока она не забеременела. Аденома гипофиза рассасывалась медленнее, ее последующие МРТ в течение примерно 1 года продолжали показывать аденому, а затем МРТ сделали 1.Через 5 лет выявили синдром пустого турецкого седла. Случаи, которые показали разрешение аденом, показали гораздо более быстрое уменьшение размера аденомы в течение нескольких месяцев [8, 9]. Приблизительно у 22,9% пациенток с макроаденомой во время беременности отмечается увеличение размера аденомы [13].


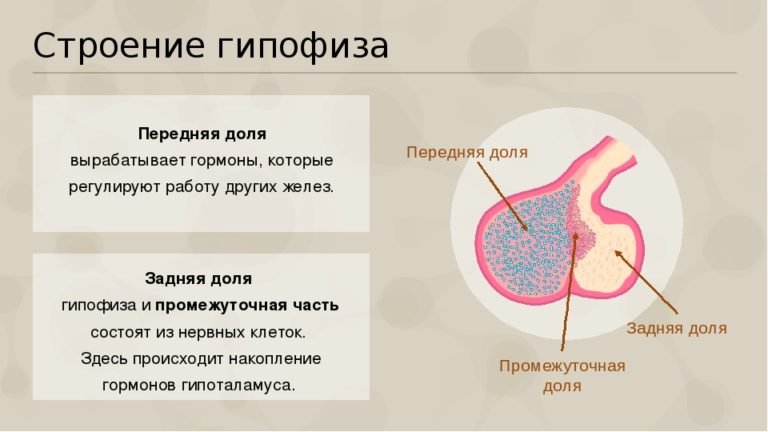 Продуцирует гонадотропные гормоны.
Продуцирует гонадотропные гормоны.