Генитальный микоплазмоз: пути заражения, симптомы, диагностика и лечение
Заболевания мочеполовой сферы, вызываемые такими простейшими, как микоплазмы и уреаплазмы, называются микоплазмозами. В нормальном состоянии человек является естественным хозяином для многих видов микоплазм.
Микоплазмы (микоплазмы и уреаплазмы) – это простейшие микроорганизмы, лишенные клеточной стенки, что делает их слабоуязвимыми при лечении обычными антибактериальными препаратами. Микоплазмы входят в состав естественной микрофлоры влагалища с детского возраста.
В подростковом периоде жизни девочек частота выявления микоплазм в посеве из половых органов колеблется от 8–10% до 50%.
Частота колонизациии уреаплазмами составляет по данным различных авторов, от 2,5 до 33%, а у девочек с наличием в анамнезе половых контактов – от 30 до 75%.
Уреаплазмы и микоплазмы редко существуют в виде моноинфекции (то есть, когда высеивается только один вид простейших).
Микоплазмоз, пути заражения
Основной путь инфицирования микоплазмой и уреаплазмой у взрослых — половой. Инфицирование детей происходит главным образом во время родов, при патологически протекающей беременности, в редких случаях — возможен контактно-бытовой путь заражения.
Наиболее опасно внутриутробное инфицирование, которое приводит к развитию врожденной инфекции: пневмонии, увеитов (воспаление сетчатки), поражению мочевой системы плода и новорожденного.
Генитальный уреаплазмоз, проявления

Клиническими проявлениями вульвита и вагинита, вызванных уреаплазменной инфекцией, являются: гиперемия наружных половых органов, отечность вульвы и влагалища. Вагинальные выделения, как правило, жидкие, появляются при физическом напряжении, дефекации, мочеиспускании, ходьбе, поднятии тяжестей. Зуд половых органов при изолированной уреаплазменной инфекции выражен слабо. Могут наблюдаться кровянистые выделения при мочеиспускании. В дальнейшем беспокоят сухость слизистой оболочки, расчесы, могут появиться синехии (сращение) больших и малых половых губ.
Воспалительный процесс во влагалищном сегменте шейки матки (цервицит) при остром течении заболевания характеризуется слизисто-гнойными выделениями, при хроническом течении – выделения чаще слизистые, жидкие, периодически усиливающиеся на фоне развития сопутствующих и простудных заболеваний.
Проявления хронического эндометрита часто характеризуются кровянистыми выделениями в период между месячными, болями в животе, а также диареей, тошнотой, рвотой.
Микоплазмоз, диагностика и лечение
В настоящее время главным методом диагностики генитальной микоплазменной и уреаплазменной инфекции является посев отделяемого из половых органов на специальные диагностические среды с последующим выделением микоплазм на культуре клеток. Этот метод за его высокую эффективность и информативность называют принятым в медицине термином – «золотой стандарт» диагностики микоплазмоза.
Выявление большинства видов микоплазм в посеве не является обязательным показанием к лечению. По современным данным, при выявлении у девочек воспалительных заболеваний, таких как уретрит, эндометриоз и другие заболевания матки и придатков, возбудителями которых могут быть данные микоплазмы и уреаплазмы при обнаружении их в результате посева, должна проводиться специфическая антибактериальная терапия.
У взрослых женщин ситуация несколько иная: при наличии хронических урогенитальных заболеваний, таких как угроза прерывания беременности, токсикоз, многоводие следует провести обследование на наличие микоплазменной инфекции как самой женщины, так и ее новорожденного ребенка, а в случае выявления микоплазмоза или уреаплазмоза, принять необходимые меры по ее лечению.
В целом же, обнаружение генитальных микоплазм при отсутствии жалоб и патологических изменений, как правило, расценивают как носительство мико- и/или уреаплазм. При этом сохраняется риск повторного инфицирования на фоне развития других инфекций, например, герпетической, снижения иммунитета, вызванного стрессом, вредными привычками, нехваткой витаминов. Кроме того, у взрослых женщин, ведущих активную половую жизнь, сохраняется возможность инфицирования половых партнеров.
Важно помнить, что для качественной профилактики повторного инфицирования и предотвращения осложнений уреа- и микоплазмоза необходимо проходить обследование и лечение обоих половых партнеров, включающее обязательное бактериологическое исследование мазка из половых органов через 3 и 6 месяцев после курса проведенного лечения.
причины, распространенные симптомы и лечение
Возбудители инфекции
Представители класса микоплазм являются мельчайшими свободноживущими микроорганизмами, обладающими уникальным строением. Отсутствие клеточной стенки сближает эти инфекционные агенты с вирусами, однако в научной среде микоплазмы все же считаются бактериями. Также к уникальным биологическим свойствам этих микроорганизмов можно отнести способность сохранять жизнедеятельность в бесклеточной среде и отсутствие ядра. Микоплазмы не окрашиваются по Граму и не идентифицируются с помощью светового микроскопа.
Отсутствие жесткой клеточной стенки объясняет многочисленные защитные свойства микоплазм. Эти бактерии невосприимчивы ко многим противомикробным препаратам, включая бета-лактамные антибиотики. Условно патогенные представители микоплазм обитают в слизистых оболочках разных анатомических областей, включая мочеполовой и дыхательный тракты. Активное распространение этих микроорганизмов в подслизистую оболочку и кровоток наблюдается только при иммунодепрессивных состояниях.
Представители микоплазм и ассоциированные с ними заболевания:
- Mycoplasma pneumoniae – хорошо изученный инфекционный агент, вызывающий атипичную пневмонию;
- Ureaplasma urealyticum и Ureaplasma parvum ответственны за возникновение неспецифического уретрита и других воспалительных процессов в мочеполовой системе;
- Mycoplasma hominis и Mycoplasma genitalium также поражают органы выделительной и репродуктивной систем;
- Mycoplasma incognitos могут провоцировать развитие диссеминированной инфекции.
Также ученым известны отдельные представители этого бактериального класса, способные вызывать воспалительные процессы у ВИЧ-инфицированных людей. Дальнейшее изучение микоплазм поможет врачам улучшить методы лечения этих заболеваний.
Способы заражения
При рассмотрении этиологии микоплазмоза необходимо учитывать, что многие условно патогенные представители этих бактерий могут присутствовать в слизистых оболочках человека без клинических проявлений. Распространенность носительства инфекции варьируется от 8% до 16%. Исключительно патогенные виды микоплазм передаются половым путем, однако возможны и другие варианты заражения.
Распространенность носительства инфекции варьируется от 8% до 16%. Исключительно патогенные виды микоплазм передаются половым путем, однако возможны и другие варианты заражения.
Способы заражения и факторы риска.
- Незащищенный оральный или вагинальный половой контакт. Микоплазмоз, передающийся таким путем, часто сочетается с герпесом, кандидозом и хламидиозом.
- Бытовая передача, обусловленная совместным использованием предметов личной гигиены.
- Внутриутробное поражение плода и перенос инфекции во время родов.
- Нарушение работы иммунной системы, приводящее к активному размножению условно патогенной флоры.
- Наличие других инфекций мочеполовых органов в индивидуальном анамнезе.
- Беспорядочные половые связи.
Из-за бессимптомного течения пациенты могут продолжать заражать других людей, поэтому важно проходить скрининг на мочеполовые инфекции даже при отсутствии жалоб. Отмечается, что носительство и скрытое течение микоплазмоза в большей степени характерно для женщин.
Симптомы
Бессимптомное течение заболевания наблюдается примерно у 10% пациентов. У носителей инфекции микоплазмоз также может проявиться при воздействии неблагоприятных факторов, вроде ухудшения работы местного иммунитета. Обычно на ранних стадиях бактерии поражают слизистую оболочку мочеиспускательного канала, однако по мере развития болезни микоплазмы могут ретроградно распространяться в область матки, мочеточников, почек и других органов. Также восходящая инфекция является причиной поражения плода у беременных женщин.
Возможные симптомы:
- боль в нижней части живота;
- выделение прозрачной вязкой жидкости из мочеиспускательного канала и шейки матки;
- повышение температуры тела (лихорадка) при острой форме инфекции;
- вагинальное кровотечение, не связанное с менструацией;
- боли во время мочеиспускания и полового контакта;
- нарушение менструального цикла;
- слабость и усталость;
- снижение либидо.

Из-за частого коинфицирования врачам не всегда удается выявить симптомы микоплазмоза, поэтому основные методы диагностики основаны на лабораторных показателях.
Диагностика
Для прохождения обследования необходимо обратиться к урологу или гинекологу. Врач расспросит пациента о жалобах, соберет анамнестическую информацию и проведет первичный осмотр органов мочеполовой системы. Микоплазмоз не имеет специфических внешних и симптоматических признаков, поэтому для постановки окончательного диагноза специалисту потребуются результаты нескольких лабораторных исследований. Также может быть необходимо визуальное обследование внутренних органов для выявления осложнений болезни.
Достоверные методы диагностики.
- Выделение бактериальной культуры. Такое исследование подходит для обнаружения Mycoplasma hominis и Ureaplasma urealyticum. На основе полученной бактериальной культуры также можно определить восприимчивость микроорганизмов к антибиотикам.
- Мазок с последующим микроскопическим исследованием для исключения других бактериальных инфекций.

- Полимеразная цепная реакция – получение специфических участков ДНК бактерии. Этот метод позволяет с высокой точностью идентифицировать возбудителя болезни.
- Серологические исследования, направленные на обнаружение специфических иммуноглобулинов в крови пациента.
- Ультразвуковое обследование почек и мочевого пузыря.
На основании полученных данных врачу предстоит сделать вывод о том, какой инфекционный агент вызывает клинические проявления заболевания. При хронической форме патологии важно провести тест на чувствительность к антибиотикам перед началом лечения.
Лечение
Методы терапии зависят от конкретного возбудителя болезни, наличия вторичной инфекции и клинических проявлений микоплазмоза. Условно патогенные представители микоплазм, включая Mycoplasma hominis и Ureaplasma urealyticum, могут быть компонентами естественной микрофлоры урогенитального тракта, поэтому вопрос обязательного устранения этих микроорганизмов при отсутствии жалоб со стороны пациента остается спорным. Напротив, обнаружение Mycoplasma genitalium в лабораторных анализах без сомнения указывает на необходимость медикаментозной терапии.
Напротив, обнаружение Mycoplasma genitalium в лабораторных анализах без сомнения указывает на необходимость медикаментозной терапии.
Основные методы лечения:
- доксициклин или азитромицин – рекомендованные антибиотики при микоплазмозе;
- антибиотики тетрациклинового ряда, макролиды, фторхинолоны в качестве альтернативной противомикробной терапии;
- топические антимикробные средства и антисептики;
- противогрибковые препараты для исключения оппортунистической инфекции;
- физиотерапия для устранения осложнений.
Медикаменты могут быть назначены только врачом. Важно соблюдать дозировку и частоту приема антибиотиков для предотвращения перехода болезни в хроническую форму. При беременности важно подобрать безопасные лекарственные средства, не влияющие на состояние плода. В среднем медикаментозная терапия микоплазмоза продолжается в течение 2-3 недель, после чего врач оценивает лабораторные показатели и принимает решение о прекращении лечения.
Прогноз и осложнения
Своевременное применение антибиотиков позволяет устранить симптомы микоплазмоза у большинства пациентов. При скрытой форме патологии многие женщины и мужчины слишком поздно обращаются к врачу, в результате чего возникают различные негативные последствия. Микоплазмоз не вызывает опасные для жизни пациента осложнения, однако необходимо учитывать риск развития вторичной инфекции.
Возможные осложнения.
- Мужское и женское бесплодие. Такие негативные последствия инфекции развиваются при поражении репродуктивных органов.
- Различные осложнения при беременности, включая выкидыш. Микоплазмы переносятся в ткани плода с кровотоком и нарушают развитие нового организма.
- Воспаление органов малого таза.
- Воспаление мозговых оболочек и сердца.
- Микоплазменная пневмония, характеризующаяся тяжелым течением.
Наибольшему риску возникновения осложнений подвергаются люди с ослабленным иммунитетом. В первую очередь это ВИЧ-инфицированные пациенты. Также следует учитывать патологическое влияние других патогенных микроорганизмов, развивающихся на фоне микоплазмоза.
В первую очередь это ВИЧ-инфицированные пациенты. Также следует учитывать патологическое влияние других патогенных микроорганизмов, развивающихся на фоне микоплазмоза.
Профилактика
Инфекционные заболевания, вызываемые микоплазмой, не так хорошо поддаются профилактике, как другие венерические инфекции. В первую очередь это связано с условно патогенными видами бактерий, присутствующими в естественной микрофлоре урогенитального тракта. Эти микроорганизмы могут начать размножаться при воздействии на организм человека любых неблагоприятных факторов. Тем не менее, существуют методы предотвращения передачи Mycoplasma genitalium от одного человека к другому.
Рекомендуемые методы профилактики:
- использование латексного презерватива во время интимных контактов;
- во избежание нарушения естественной урогенитальной микрофлоры рекомендуется избегать частого семяизвержения в область влагалища;
- тщательная гигиена наружных половых органов.
Таким образом, микоплазмоз отлично поддается лечению. Из-за риска бессимптомного течения инфекции сексуально активным мужчинам и женщинам рекомендуется регулярно проходить скрининговые обследования на венерические инфекции. Также скрининг необходим при планировании беременности.
Из-за риска бессимптомного течения инфекции сексуально активным мужчинам и женщинам рекомендуется регулярно проходить скрининговые обследования на венерические инфекции. Также скрининг необходим при планировании беременности.
Микоплазменная пневмония — mon-crb
– атипичная легочная инфекция, возбудителем которой является Мycoplasma pneumoniae. Заболевание сопровождается катаральными и респираторными проявлениями (заложенностью носа, першением в горле, приступами навязчивого малопродуктивного кашля), интоксикационным синдромом (субфебрилитетом, слабостью, головной болью, миалгией), явлениями диспепсии (дискомфортом в ЖКТ). Микоплазменная этиология пневмонии подтверждается данными рентгенографии и КТ легких, серологического и ПЦР исследований. При микоплазменной пневмонии показаны макролиды, фторхинолоны, бронходилататоры, отхаркивающие средства, иммуномодуляторы, физиолечение, массаж.
Причины микоплазменной пневмонии
Микоплазменную пневмонию вызывают высоковирулентные штаммы анаэробных микроорганизмов рода Мycoplasma – M. pneumoniae. Возбудитель представлен мелкими (по размеру сравнимыми с вирусными частицами), не имеющими клеточной стенки (аналогично L-формам бактерий), прокариотическими организмами. Микоплазмы легко адсорбируются на поверхностных рецепторах клеток-мишеней (эпителиоцитов трахеи и бронхов, альвеолоцитов, эритроцитов и др.) и паразитируют на мембране или внутри клетки-хозяина. Интеграция микоплазмы в клеточную мембрану или ее проникновение внутрь клетки превращает последнюю в иммунологически инородную, что провоцирует развитие аутоиммунных реакций. Именно аутоантителообразование служит причиной нереспираторных проявлений микоплазменной инфекции.
pneumoniae. Возбудитель представлен мелкими (по размеру сравнимыми с вирусными частицами), не имеющими клеточной стенки (аналогично L-формам бактерий), прокариотическими организмами. Микоплазмы легко адсорбируются на поверхностных рецепторах клеток-мишеней (эпителиоцитов трахеи и бронхов, альвеолоцитов, эритроцитов и др.) и паразитируют на мембране или внутри клетки-хозяина. Интеграция микоплазмы в клеточную мембрану или ее проникновение внутрь клетки превращает последнюю в иммунологически инородную, что провоцирует развитие аутоиммунных реакций. Именно аутоантителообразование служит причиной нереспираторных проявлений микоплазменной инфекции.
Микоплазмы способны длительно персистировать в эпителиальных клетках и лимфоглоточном кольце; легко передаются воздушно-капельным путем от больных и бессимптомных носителей со слизью из носоглотки и респираторного тракта. Микоплазмы малоустойчивы во внешних условиях: чувствительны к перепаду pH, нагреванию и высушиванию, ультразвуку и УФО, не растут на недостаточно влажных питательных средах.
Кроме микоплазменной пневмонии, микроорганизмы также могут стать причиной острого воспаления верхних дыхательных путей (фарингита), бронхиальной астмы, обострений хронического обструктивного бронхита и развития нераспираторной патологии (перикардита, отита, энцефалита, менингита, гемолитической анемии) у практически здоровых людей.
Отсутствие клеточной оболочки обеспечивает микоплазмам резистентность к β-лактамным антибиотикам – пенициллинам, цефалоспоринам. При микоплазменной инфекции отмечается развитие локального воспаления с выраженной иммуноморфологической реакцией, местным антителогенезом (всех классов иммуноглобулинов — IgM, IgA, IgG), активацией клеточного иммунитета. Симптомы микоплазменной пневмонии обусловлены преимущественно агрессивной ответной воспалительной реакцией макроорганизма (постинфекционной гиперсенситивностью, опосредованной Т-лимфоцитами).
Симптомы микоплазменной пневмонии
Инкубационный период при микоплазменной пневмонии может длиться 1-4 недели (обычно 12-14 дней). Начало заболевания, как правило, постепенное, но может быть подострым или острым. Выделяют респираторные, нереспираторные и генерализованные проявления микоплазменной пневмонии.
Начало заболевания, как правило, постепенное, но может быть подострым или острым. Выделяют респираторные, нереспираторные и генерализованные проявления микоплазменной пневмонии.
В начальном периоде возникает поражение верхних дыхательных путей, которое протекает в виде катарального назофарингита, ларингита, реже острого трахеобронхита. Отмечается заложенность носа, сухость в носоглотке, першение в горле, осиплость голоса. Ухудшается общее состояние, постепенно нарастает температура до субфебрильных значений, появляется слабость, потливость. В острых случаях симптомы интоксикации возникают в первые сутки заболевания, при постепенном развитии — только на 7-12 день.
Характерен продолжительный (не менее 10-15 дней) малопродуктивный пароксизмальный кашель. Во время приступа кашель очень сильный, изнурительный с выделением незначительного количества вязкой слизистой мокроты. Кашель может приобретать хронический характер, сохраняясь на протяжении 4-6 недель из-за обструкции дыхательных путей и гиперреактивности бронхов.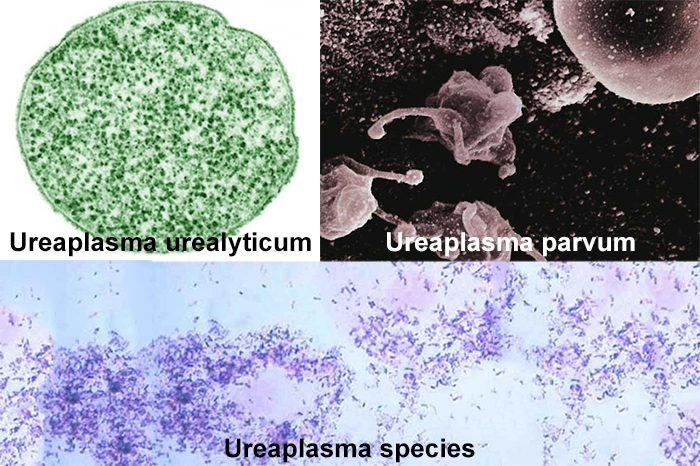 Спектр проявлений микоплазменной пневмонии может включать признаки острой интерстициальной пневмонии.
Спектр проявлений микоплазменной пневмонии может включать признаки острой интерстициальной пневмонии.
Из внелегочной симптоматики для микоплазменной пневмонии наиболее характерны высыпания на коже и барабанных перепонках (по типу острого мирингита), миалгия, дискомфорт в ЖКТ, нарушение сна, умеренная головная боль, парестезии. Присоединение нереспираторных проявлений утяжеляет течение микоплазменной пневмонии.
Может возникать умеренный фибринозный или экссудативный плеврит, иногда — плевритическая боль. При наличии сопутствующей хронической обструкции микоплазменная пневмония способствует обострению обструктивного синдрома. Для детей младше 3-летнего возраста характерно малосимптомное течение.
В неосложненных случаях симптомы микоплазменной пневмонии в течение 7-10 дней постепенно исчезают, заболевание разрешается самостоятельно. Имеется риск перехода в смешанную (микоплазменно-бактериальную) форму пневмонии вследствие присоединения вторичной инфекции (обычно, пневмококка). Осложнениями микоплазменной пневмонии выступают синдром Стивенса-Джонсона, синдром Гийена-Барре, миелит, энцефалит, менингит.
Осложнениями микоплазменной пневмонии выступают синдром Стивенса-Джонсона, синдром Гийена-Барре, миелит, энцефалит, менингит.Респираторные инфекции, вызванные микоплазмой пневмонии
Микоплазма пневмонии является «атипичной» бактерией, которая вызывает респираторные инфекции верхних и нижних дыхательных путей. Наиболее распространённой формой заболевания, особенно у детей, является трахеобронхит, который часто наблюдается вместе с другими симптомами поражения верхних дыхательных путей. Реже встречаются фарингиты, ринофарингиты, ларингофарингиты, бронхиты. Данный возбудитель также может приводить к развитию более серьезного заболевания – воспалению легких (пневмонии).
Распространение инфекции происходит воздушно – капельным путем: при кашле и чихании бактерии попадают в окружающую среду в виде инфекционного аэрозоля. Для передачи инфекции нужен длительный тесный контакт. Непродолжительное нахождение с больным человеком, как правило, не приводит к заражению. Чаще данное заболевание распространяется между членами одной семьи, которые живут вместе. Микоплазменной инфекцией можно заболеть в любое время года.
Чаще данное заболевание распространяется между членами одной семьи, которые живут вместе. Микоплазменной инфекцией можно заболеть в любое время года.
По сравнению с другими респираторными инфекциями для инфекций, вызванных микоплазмой пневмонии, характерен более длительный инкубационный период, первые симптомы заболевания появляются через 2 – 3 недели после инфицирования.
Среди наиболее частых симптомов пневмонии наблюдаются: боли в горле, усталость, лихорадка, головные боли, приступообразный кашель, который может длиться неделями или месяцами. При развитии пневмонии к данным симптомам присоединяются затрудненное дыхание и, в некоторых случаях, боли в области грудной клетки при дыхании или кашле.
В любом возрасте существует риск заражения микоплазменной инфекцией, но чаще болеют школьники и лица молодого возраста (до 25 лет). Люди с ослабленным иммунитетом, недавно перенесшие другие респираторные инфекции, имеющие хронические бронхиты и астму также имеют более высокий риск развития данного заболевания.
В ответ на микоплазменную инфекцию в нашем организме вырабатываются антитела двух классов IgM и IgG.
Первыми в крови обнаруживаются IgM, их уровень повышается в течение короткого периода времени и определяется, как правило, в течение нескольких месяцев. Вслед за образованием IgM начинают вырабатываться IgG, со временем их уровень повышается и достигает определенного предела. После перенесенного заболевания в течение длительного времени в крови обнаруживаются IgG. Определение иммуноглобулинов М и G помогает врачу – инфекционисту в диагностике респираторной инфекции, вызванной микоплазмой пневмонии. В дополнение к данным исследованиям может быть проведено ПЦР- исследование, позволяющее выявить ДНК возбудителя в отделяемом из носоглотки.
В большинстве случаев микоплазменная инфекция имеет умеренное течение, необходимость назначения антибактериальных препаратов определяется только лечащим врачом. При правильном лечении заболевания наступает полное выздоровление.
В медицинском центре «Биомедика» Вы можете записаться на прием к врачу-инфекционисту и выполнить необходимые лабораторные исследования.
Лечение микоплазмоза у женщин, мужчин, детей
Вы плохо себя чувствуете, но вы не знаете, в чём причина? Пытаетесь помочь себе лекарствами, но даже длительное лечение не даёт никаких результатов? Возможно – причина в микоплазмах — патогенных микроорганизмах, которые вызывают урогенитальные инфекции у мужчин и женщин. Эта группа микроорганизмов открыта относительно недавно и поэтому очень многое об их воздействии на организм не известно. Патогенность этих организмов находится под вопросом, так как они обнаруживаются у многих здоровых людей.
ЛЕЧЕНИЕ МИКОПЛАЗМОЗА ДОСТУПНО В ФИЛИАЛАХ:
Лечение микопламоза в Приморском районе
Адрес: г. Санкт-Петербург, Приморский район, ул. Репищева, 13
Лечение микопламоза в Петроградском районе
Адрес: г. Санкт-Петербург, Петроградский район, ул. Ленина, 5
Лечение микопламоза во Всеволожске
Адрес: г. Всеволожск, Октябрьский пр-т, 96 А
Всеволожск, Октябрьский пр-т, 96 А
Микоплазмы принадлежат к группе безъядерных микроорганизмов, их размер не превышает 0,25 мкм, они содержат обе нуклеиновые кислоты РНК и ДНК (имеют самое маленькое количество генов — только 470 генов). Общепринято считать их бактериями, но в отличие от этой группы, у микоплазм нет клеточной стенки. Но зато у них формируется толстая, гибкая, богатая стеринами мембрана, поэтому они обладают способностью принимать различные формы и обладают устойчивостью к воздействию некоторых антибиотиков. Заражение микоплазмами происходит за счёт адгезии (сцепления) с клетками эпителия, в результате чего подавляется активность клеток. Прикрепление настолько сильно, что микроорганизмы не вымываются из полости мочой или слизью, а собственные иммунные клетки человека перестают воспринимать микоплазмы, как чужеродные элементы. Некоторые виды так и остаются прикреплёнными к мембране клеток, а другие проникают внутрь клетки и начинают вести внутриклеточный паразитический образ жизни, проявляя цитотоксическую активность (выделяют вредные для клеток вещества).
Микоплазмы представлены более 100 видами. Шесть из них, возбудители микоплазмоза, вызывают тяжелые инфекции мочеполового тракта у человека – урогенитальный микоплазмоз (Mycoplasma hominis, М. primatum, M. genitalium, spermatophilum и M. penetrant). Другие представители являются возбудителями инфекций у животных и растений. Передача инфекции может происходить либо воздушно-капельным путём (Mycoplasma pneumoniae — вызывает пневмонию, респираторный микоплазмоз), либо половым путём (M. hominis, M. genitalium при сексе без использования презерватива).
Mycoplasma genitalium относится к группе половых микоплазм, которая встречается как у мужчин, так и у женщин. Заражение происходит путём сексуального контакта. Генитальный микоплазмоз часто сопровождается воспалением мочеиспускательного канала. Клинические исследования показали, что среди женщин, инфицированных микоплазмами, 14% являлись носителями хламидиоза и 15% страдали уретритом. Это обусловлено тем, что присутствие бактерий уменьшает защитные силы организма, в результате чего организм поражается и другими патогенами.
Исследование, проведенное в Англии и Франции среди мужчин, страдающих рецидивирующим воспалением мочеиспускательного канала, в 20% показало наличие Mycoplasma genitalium. У женщин, эта инфекция может поражать влагалище, шейку матки, эндометрий, маточные трубы, вызывать развитие воспалительных заболеваний органов малого таза, что, в свою очередь, приводит к бесплодию у женщин.
У мужчин микоплазмы влияют на подвижность сперматозоидов, что снижает их способность к оплодотворению.
Mycoplasma hominis может быть причиной уретрита, цервицита воспаления яичников, фаллопиевой трубы, пиелонефрита. Наличие этой микоплазмы у беременных увеличивает риск преждевременных родов, результате хориоамнионита (воспаление оболочек плода) при заражении М. hominis.
Симптомы микоплазмоза
Большинство венерических заболеваний, в том числе и микоплазмоз, часто не дает видимых проявлений симптомов и человек может неосознанно являться носителем заболевания. Малые размеры микоплазмы порой позволяют им преодолевать барьерные препятствия и проникать в полового партнёра даже через латексные поры презерватива. Из чего следует, что ведение беспорядочной половой жизни увеличивает риск заболевания микоплазмозом. Почему очень важно, при наличии активной половой жизни, регулярно проводить обследования на выявление возбудителей венерических инфекций.
Малые размеры микоплазмы порой позволяют им преодолевать барьерные препятствия и проникать в полового партнёра даже через латексные поры презерватива. Из чего следует, что ведение беспорядочной половой жизни увеличивает риск заболевания микоплазмозом. Почему очень важно, при наличии активной половой жизни, регулярно проводить обследования на выявление возбудителей венерических инфекций.
При нарушении микрофлоры, стрессах, сбоях иммунной системы, микоплазма начинает активно размножаться и атаковать клетки эпителия. Симптомы микоплазмоза могут возникать в начале заражения или только спустя 3 недели после полового акта.
Чаще всего в острой фазе симптомы микоплазмоза у женщин проявляются как:
- болезненное мочеиспускание — это связано с тем, что микоплазма поражает мочеиспускательный канал пациента, вызывая воспаление и чувствительность окружающих очаг тканей
- боль во время секса — ткани мочеиспускательного канала находятся в непосредственной близости со стенкой влагалища, и, таким образом, являются чувствительными к раздражениям во время полового акта и другим стимуляциям
- выделения с неприятным запахом и необычной консистенции
- из-за выделений может появляться зуд и ощущение жжения во влагалище
Микоплазмоз при беременности сопровождается описанными выше симптомами для женщин. При отсутствии лечения происходит заражение плода во время его прохождения через родовые пути. 30-50% девочек становятся носителями микоплазмы. Что интересно, мальчики практически не подвержены инфицированию. При рождении микоплазмоз у детей (как правило, Mycoplasma hominis) вызывает конъюнктивит, пневмонию, воспаление мозговых оболочек – менингит, хронические заболевания лёгких.
При отсутствии лечения происходит заражение плода во время его прохождения через родовые пути. 30-50% девочек становятся носителями микоплазмы. Что интересно, мальчики практически не подвержены инфицированию. При рождении микоплазмоз у детей (как правило, Mycoplasma hominis) вызывает конъюнктивит, пневмонию, воспаление мозговых оболочек – менингит, хронические заболевания лёгких.
У мужчин симптомами микоплазмоза могут быть:
- бесцветные выделения из уретры
- жжение при мочеиспускании
- тянущие боли в паху
- увеличение яичек
- увеличение лимфатических узлов
- болезненности мошонки
Часто у мужчин микоплазмы существуют на половых органах и не вызывают никакого дискомфорта.
Диагностика микоплазмоза
Диагностика микоплазмоза, из-за отсутствия симптомов или схожести проявлений с другими заболеваниями, может быть весьма затруднительна.
Классический цитологический анализ не всегда даёт правильный результат из-за небольшого размера бактерии, бактериологический посев сопровождается трудностями при подборе специальных питательных сред.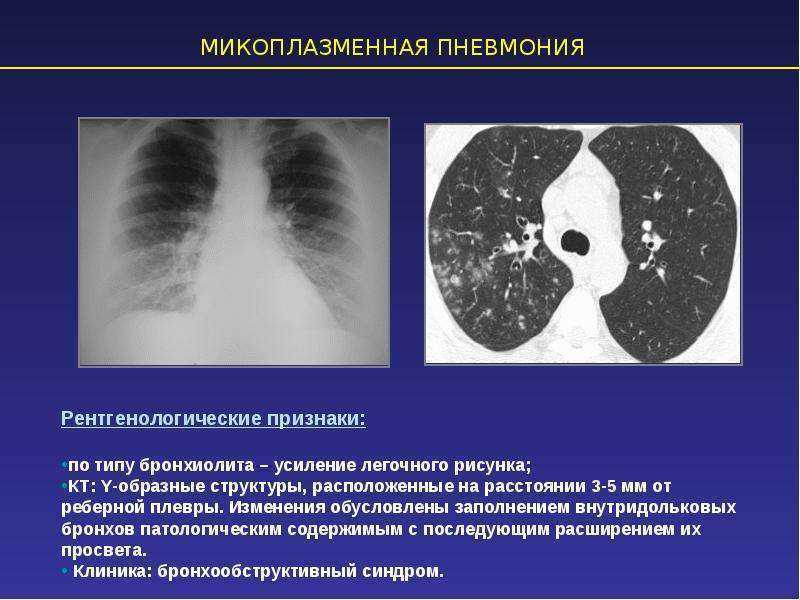
С появлением методики ПЦР, полимеразной цепной реакции, диагностика микоплазмоза стала более точной. Вероятность выявить микоплазму с помощью ПЦР составляет около 96%. Потому для правильной диагностики необходимо провести комплексное обследование, включающее:
При беременности необходимо учитывать количество патогенных возбудителей при лабораторных исследованиях.
Регулярное посещение врачей позволит своевременно обнаружить проблему, избежать осложнений и передачи инфекции. При наличии перечисленных симптомов можно обратиться к таким врачам, как венеролог, иммунолог, гинеколог.
Лечение микоплазмоза
Несмотря на то, что бактерия микоплазма устойчива ко многим токсическим эффектам антибиотиков, при правильной диагностике успешно поддаётся лечению. Лечение урогенитального микоплазмоза сводится к приёму антибиотиков тетрациклиновой (Тетрациклин) или эритромициновой группы (Азитромицин). Такие антибиотики ингибируют (тормозят) рост бактерий, блокируя синтез белка и помогая организму человека нейтрализовать ослабленных бактерий.
Лечение антибиотиками может быть комплексным (1-2 недели), при котором применяются терапия витаминами, иммуномодуляторами, ферментами, а так же проводят местные процедуры (физиотерапия). Либо однократным – использование одной дозы высокоэффективного антибиотика. Это метод проверен и довольно часто назначается по индивидуальным показаниям.
Схема лечения определяется исключительно врачом по результатам анализов и с учётом индивидуальных особенностей пациента!
Следует помнить, что пролечиваться необходимо обоим партнёрам, так как возможны вторичные заражения.
В нашей клинике Вы можете пройти консультацию у квалифицированных специалистов, которые проведут диагностику Вашего состояния и при необходимости подберут современное подходящее лечение.
Прием ведут врачи:
Выберите филиал“Династия” на Новочеркасском пр-те, Красногвардейский район“Династия” на Ленина, Петроградский район“Династия” на Репищева, Приморский район“Династия” во ВсеволожскеВыездная служба
Стоимость лечения микоплазмоза:
| Наименование услуг | Цена в рублях | |
| Санкт-Петербург | Всеволожск | |
| Первичный прием акушера-гинеколога 1 ступени | 1850 | 1500 |
| Повторный прием акушера-гинеколога 1 ступени | 1650 | 1300 |
| Первичный прием акушера-гинеколога 2 ступени | 2100 | — |
| Повторный прием акушера-гинеколога 2 ступени | 1900 | — |
| МАНИПУЛЯЦИИ | ||
| Введение акушерского пессария | 1500 | 1500 |
| Введение внутриматочной спирали (ВМС) | 2500 | 2500 |
| Введение внутриматочной спирали «Мирена» | 4000 | 4000 |
| Введение имплантируемого контрацепива «ИМПЛАНОН» (без стоимости контрацептива) | 2500 | 2100 |
| Видеокольпоскопия | 1700 | 1700 |
| Забор мазков (гинекологический) | 400 | 400 |
| Инструментальное удаление внутриматочной спирали (ВМС) | 2500 | 2100 |
| Интравагинальное введение свечей (без стоимости медикаментов), 1 процедура | 500 | 500 |
| Лечебная обработка влагалища | 700 | 700 |
| Медикаментозное прерывание беременности | 8000 | — |
| Местная обработка наружных половых органов | 700 | 700 |
| Удаление акушерского пессария | 1000 | 1000 |
| Удаление внутриматочной спирали (ВМС) | 1500 | 1500 |
| Удаление внутриматочной спирали «Мирена» | 3000 | 3000 |
| Удаление имплантируемого контрацепива «ИМПЛАНОН» | 2500 | 2300 |
| Удаление инородного тела из влагалища | 1800 | 1800 |
| Штрих-биопсия эндометрия (пайпель-диагностика) | 1500 | 1200 |
| PRP-терапия | — | 3500 |
| УЛЬТРАЗВУКОВАЯ И ФУНКЦИОНАЛЬНАЯ ДИАГНОСТИКА | ||
| УЗИ органов малого таза (одним датчиком) | 1600 | 1300 |
| УЗИ органов малого таза (двумя датчиками) | 1900 | 1500 |
| КТГ (кардиотокография плода) | 1800 | — |
| КТГ (многоплодная беременность) | 2300 | — |
| Фолликулометрия (1 исследование) | 1400 | 1400 |
| Фолликулометрия (4 исследования) | 3900 | 3900 |
| ЛАЗЕРНАЯ ХИРУРГИЯ | ||
| Биопсия шейки матки + гистология | 5000 | 4000 |
| Единичная киста шейки матки | 1500 | 1500 |
| Единичные папилломы и кондиломы стенок влагалища | 3000 | 3000 |
| Распространенный кондиломатоз, папилломатоз | от 6000 | от 6000 |
Удаление единичных кондилом, папиллом вульвы, шейки матки (за 1 ед. ) ) | 600 | 600 |
| Эктопия (эрозия) шейки матки (менее 2 см) | 6000 | 4000 |
| Эктопия (эрозия) шейки матки (более 2 см) | 9000 | 9000 |
| Эндометриоз шейки матки (единичный очаг) | 1000 | 1000 |
| РАДИОХИРУРГИЯ | ||
| Биопсия шейки матки радионожом | 2500 | 2000 |
| Лечение лейкоплакии и крауроза вульвы с помощью радиохирургического ножа | 5300 | 5100 |
| Лечение патологии шейки матки с помощью радиохирургического ножа до 1 см | 5000 | 3700 |
| Лечение патологии шейки матки с помощью радиохирургического ножа до 2 см | 6500 | 6000 |
| Удаление полипов шейки матки с помощью радиохирургического ножа | 4000 | 2500 |
| Фульгурация кист, эндометриоидных очагов с помощью радиохирургического ножа | 3500 | 2200 |
Электрокоагуляция кондилом на коже в области промежности радионожом (за 1 ед. ) ) | 800 | 800 |
| Электрокоагуляция кондилом, папиллом вульвы радионожом | 1400 | 1400 |
| Электрокоагуляция кондилом, папиллом влагалища радионожом | от 3200 | от 3200 |
| ОПЕРАЦИИ | ||
| Интимная контурная пластика | — | 26000 |
| Хирургическая дефлорация | 8000 | 8000 |
ЗАПИСЬ НА ЛЕЧЕНИЕ МИКОПЛАЗМОЗА
Ваша заявка отправлена
Менеджер свяжется с вами для уточнения деталей
Мы ценим ваше обращение в наш медицинский центр «Династия»
Лечение микоплазменной инфекции у женщин в клиниках МЕДСИ в Москве: симптомы и причины
Лечение микоплазмоза имеет комплексный характер. При возникновении инфекции, вызванной микоплазмой гениталиум, необходимо лечиться антибиотиками по назначению врача, направленными на уничтожение возбудителя заболевания, лекарствами, укрепляющими иммунитет, и симптоматическими препаратами для уменьшения зуда, болей и других местных симптомов инфекции.
При возникновении инфекции, вызванной микоплазмой гениталиум, необходимо лечиться антибиотиками по назначению врача, направленными на уничтожение возбудителя заболевания, лекарствами, укрепляющими иммунитет, и симптоматическими препаратами для уменьшения зуда, болей и других местных симптомов инфекции.
Часто из антибактериальных средств выбирают препараты из группы макролидов. Также лечение может проводиться препаратами тетрациклинового ряда. В зависимости от выраженности, давности и степени распространенности инфекционного процесса врач подберет пациентке индивидуальную дозировку препарата и определенную длительность курса его приема. Для восстановления нарушенной микрофлоры влагалища после приема антибиотиков врач назначает пробиотики, содержащие лакто- и бифидобактерии, в виде вагинальных свечей или капсул для приема внутрь с целью восстановления микрофлоры влагалища. Также рекомендуется прием общеукрепляющих препаратов, поливитаминов для поддержания иммунитета.
Лечение микоплазмы гениталиум у беременных женщин проводится на любом сроке беременности, с учетом токсического влияния препарата на плод.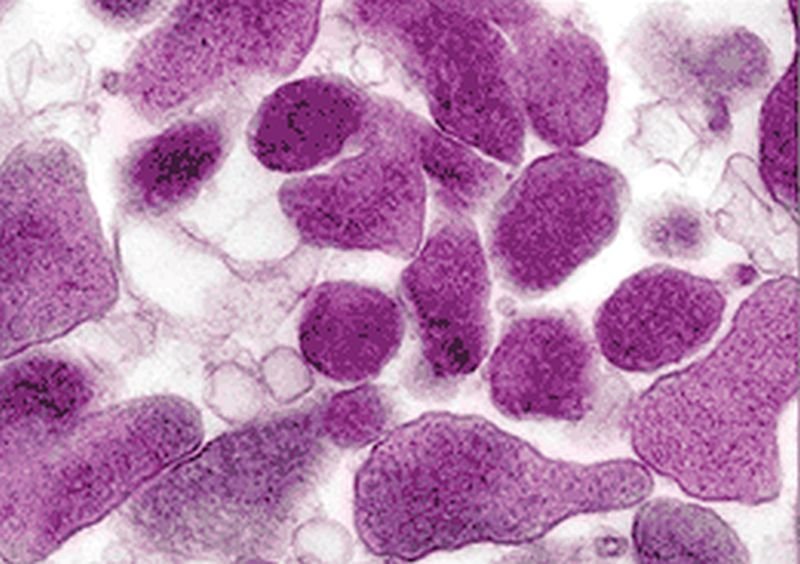 При распространении патологического процесса на органы малого таза нельзя медлить с лечением заболевания, так как возможны внутриутробное заражение плода и самопроизвольный выкидыш. В этом случае ожидаемая польза превышает возможный риск токсического воздействия препарата на плод.
При распространении патологического процесса на органы малого таза нельзя медлить с лечением заболевания, так как возможны внутриутробное заражение плода и самопроизвольный выкидыш. В этом случае ожидаемая польза превышает возможный риск токсического воздействия препарата на плод.
Мужчинам также назначают эффективное лечение, которое представляет собой индивидуально подобранный врачом курс антибиотиков.
Лечение микоплазмы хоминис
Микоплазмоз, вызванный микоплазмой хоминис, следует лечить только при наличии клинических и лабораторных признаков воспаления, у женщин с диагностированным бесплодием, а также у тех, у кого ранее были случаи невынашивания беременности.
У беременных женщин микоплазмоз, вызванный микоплазмой хоминис, лечат при наличии клинических и лабораторных признаков воспаления, перед предстоящим оперативным вмешательством при патологии органов мочеполовой системы. Обычно используют те же самые препараты, что и при лечении инфекции, вызванной микоплазмой гениталиум. Дозировку и длительность лечения врач определяет индивидуально.
Дозировку и длительность лечения врач определяет индивидуально.
Контроль эффективности лечения проводится не ранее чем через месяц после окончания лечения. При обнаружении возбудителя в исследуемом материале и наличии признаков воспаления меняют антибактериальный препарат на другой и обследуют пациента на наличие сочетанной инфекции.
Ожидаемые результаты лечения
Признаками излечения от заболевания, вызванного Mycoplasma genitalium, являются:
- Полное отсутствие возбудителя в исследуемом материале
- Отсутствие признаков воспаления
- Отсутствие осложнений
Критериями излечения от инфекционного процесса, вызванного Mycoplasma hominis, считаются:
- Отсутствие симптомов воспаления и признаков воспаления в мазке
Обнаружение микроорганизмов в исследуемом материале не является признаком неэффективности лечения, так как микоплазма хоминис часто присутствует в составе нормальной микрофлоры половых путей.
Преимущества МЕДСИ
- Высококвалифицированные гинекологи и урологи
- Современная диагностическая лаборатория
- Подбор индивидуальной схемы лечения, ведение пациента в течение всего процесса лечения, контроль эффективности назначенной терапии, разработка методов профилактики возобновления заболевания
Микоплазмоз
Микоплазмоз — инфекционное заболевание, относящееся к классу инфекций, передаваемых половым путем (ИППП), которое вызывается специфическим возбудителем – микоплазмами. Микоплазмы открыты в 30-е годы ХХ века, занимают промежуточное положение между бактериями и вирусами, и долгое время считались сапрофитной микрофлорой, не влияющей на здоровье человека. С 1960-х годов они впервые привлекли внимание как источник патологических, чаще всего, воспалительных процессов в человеческом организме. В настоящее время известно множество видов микоплазм, из которых опасность для человека представляют несколько видов – Mycoplasma genitalium, Mycoplasma hominis, Mycoplasma pneumonia и Ureaplasma urealiticum. Помимо поражений мочеполовой системы, микоплазмы могут вызывать поражения органов дыхания, воспалительные заболевания гортани, носоглотки, легких, бронхов. Во внешней среде микоплазмы неустойчивы и быстро погибают при нагревании, под действием прямых солнечных лучей, под действием слабых дезинфицирующих средств. Источником заболевания уреаплазмозом и микоплазмозом является больной человек. Чаще всего, заражение происходит половым путем, но существует и бытовой путь передачи инфекции через предметы домашнего обихода, белье, полотенца, мочалки. При воспалительных заболеваниях мочеполовой системы микоплазмы (уреаплазмы) обнаруживаются в 45 – 50% случаев. Выявляются они в 5 -8% случаев и у здоровых людей, что свидетельствует о существовании бессимптомных форм заболевания или микоплазмоносительства. Инфекция активизируется под действием внешних и внутренних факторов – стрессов, переохлаждения, снижения иммунитета в связи с перенесенными ранее заболеваниями, при беременности и родах.
Помимо поражений мочеполовой системы, микоплазмы могут вызывать поражения органов дыхания, воспалительные заболевания гортани, носоглотки, легких, бронхов. Во внешней среде микоплазмы неустойчивы и быстро погибают при нагревании, под действием прямых солнечных лучей, под действием слабых дезинфицирующих средств. Источником заболевания уреаплазмозом и микоплазмозом является больной человек. Чаще всего, заражение происходит половым путем, но существует и бытовой путь передачи инфекции через предметы домашнего обихода, белье, полотенца, мочалки. При воспалительных заболеваниях мочеполовой системы микоплазмы (уреаплазмы) обнаруживаются в 45 – 50% случаев. Выявляются они в 5 -8% случаев и у здоровых людей, что свидетельствует о существовании бессимптомных форм заболевания или микоплазмоносительства. Инфекция активизируется под действием внешних и внутренних факторов – стрессов, переохлаждения, снижения иммунитета в связи с перенесенными ранее заболеваниями, при беременности и родах.Симптомы.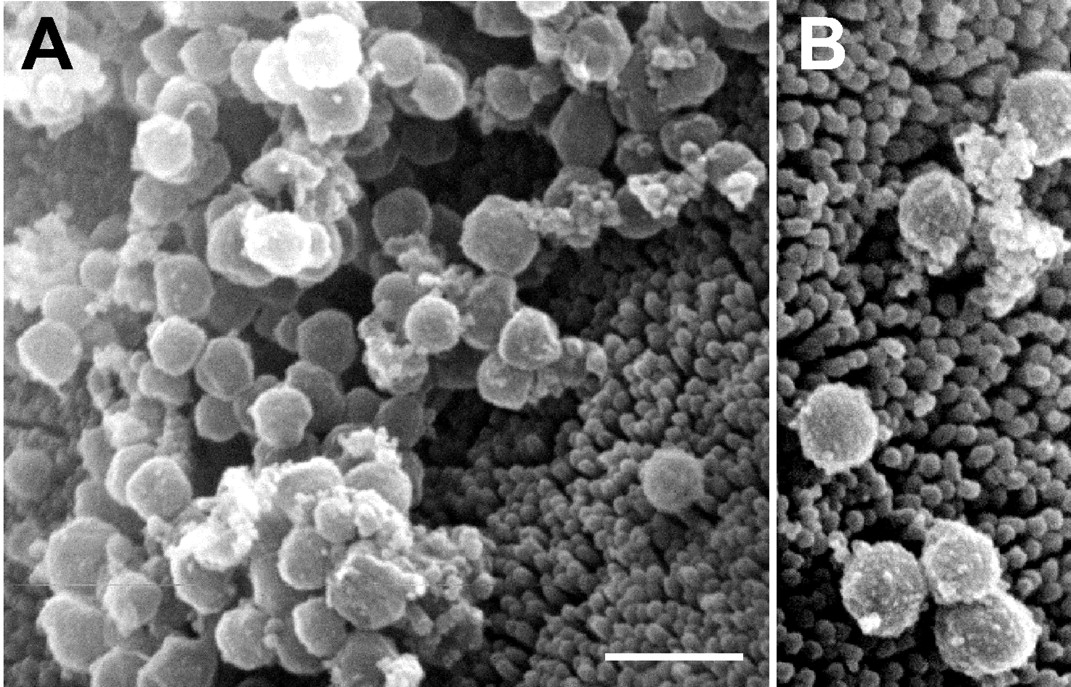
Микоплазмоз (уреаплазмоз), как правило, имеет хроническое течение, с маловыраженными симптомами разнообразного порядка, а также бессимптомное течение заболевания. Продолжительность скрытого периода болезни может составлять от нескольких дней до нескольких месяцев и даже лет. У мужчин поражаются мочеиспускательный канал, парауретральные ходы, мочевой пузырь, предстательная железа, семенные пузырьки, яички и придатки яичек. У женщин поражаются мочеиспускательный канал, парауретральные ходы, влагалище, малые и большие вестибулярные железы, шейка и тело матки, маточные трубы, яичники, брюшина малого таза. При хроническом течении заболевания симптомы не всегда привлекают внимание больного. У мужчин могут иметь место скудные слизистые выделения по утрам, после принятия острой пищи или переохлаждений. Хронический микоплазменный или уреаплазменный уретрит может сопровождаться ощущением тяжести, дискомфорта, иногда легкого жжения в мочеиспускательном канале. Как правило, больной обращается к врачу при наличии симптомов уже имеющихся осложнений – простатита, везикулита, орхита или эпидидимита. У женщин микоплазмоз также большей частью протекает почти бессимптомно, лишь у части больных сопровождаясь чувством тяжести в нижних отделах живота и болями в поясничной области, особенно во время менструации. Микоплазмоз у женщин может приводить к развитию преждевременных родов, раннему отхождению околоплодных вод, может служить причиной лихорадочной реакции во время родов и в послеродовом периоде, провоцируя воспаление легких и развитие менингита у новорожденных. Как для мужчин, так и для женщин микоплазменная инфекция часто служит причиной бесплодия.
У женщин микоплазмоз также большей частью протекает почти бессимптомно, лишь у части больных сопровождаясь чувством тяжести в нижних отделах живота и болями в поясничной области, особенно во время менструации. Микоплазмоз у женщин может приводить к развитию преждевременных родов, раннему отхождению околоплодных вод, может служить причиной лихорадочной реакции во время родов и в послеродовом периоде, провоцируя воспаление легких и развитие менингита у новорожденных. Как для мужчин, так и для женщин микоплазменная инфекция часто служит причиной бесплодия.
Диагностика.
Также как и для других, скрыто протекающих инфекций, передаваемых половым путем (ИППП), важным принципом диагностики микоплазменной инфекции является периодичность и регулярность. Для мужчин и женщин, ведущих активную половую жизнь вне брака, исследования на наличие микоплазм необходимо проходить один раз в полгода. Для людей, живущих в браке, периодичность должна составлять срок от одного года до полутора лет. Обязательному исследованию на наличие микоплазм должны подвергаться больные с заболеваниями носоглотки, миндалин, бронхов, хроническими пневмониями, бронхиальной астмой. В диагностике микоплазмоза основное значение имеют молекулярно-биологические методы, прежде всего ПЦР (ДНК-диагностика) и методы серологической иммуноферментной диагностики (ИФА). Важным этапом диагностики микоплазменной и уреаплазменной инфекции является диагностика осложнений – воспалительных процессов в органах мочеполовой системы. У мужчин проводится диагностика предстательной железы, семенных пузырьков, мочевого пузыря, органов мошонки, исследуется секрет простаты, моча в трех порциях, спермограмма, функция мочеиспускания (УФМ), проводятся ультразвуковые исследования. У женщин проводятся исследования выделений и мочи, осмотр преддверия влагалища, кольпоскопия, ультразвуковые исследования органов малого таза. С учетом частой сочетаемости микоплазмоза и уреаплазмоза с другими инфекциями урогенитальной системы, показано проведение ДНК-диагностики или культуральных посевов на иные специфические ИППП.
В диагностике микоплазмоза основное значение имеют молекулярно-биологические методы, прежде всего ПЦР (ДНК-диагностика) и методы серологической иммуноферментной диагностики (ИФА). Важным этапом диагностики микоплазменной и уреаплазменной инфекции является диагностика осложнений – воспалительных процессов в органах мочеполовой системы. У мужчин проводится диагностика предстательной железы, семенных пузырьков, мочевого пузыря, органов мошонки, исследуется секрет простаты, моча в трех порциях, спермограмма, функция мочеиспускания (УФМ), проводятся ультразвуковые исследования. У женщин проводятся исследования выделений и мочи, осмотр преддверия влагалища, кольпоскопия, ультразвуковые исследования органов малого таза. С учетом частой сочетаемости микоплазмоза и уреаплазмоза с другими инфекциями урогенитальной системы, показано проведение ДНК-диагностики или культуральных посевов на иные специфические ИППП.
Лечение.
Лечение проводится под непосредственным контролем и по назначению врача. Срок лечения неосложненного микоплазмоза или уреаплазмоза составляет около 3-х недель, но может быть увеличен при наличии развившихся осложнений. Общим обязательным условием успешного лечения является одновременность лечения половых партнеров – включая ситуации, когда микоплазмы или уреаплазмы достоверно выявлены только у одного из них. В период прохождения лечебного процесса и последующего контроля половая жизнь запрещена для обоих партнеров. Лечебный процесс имеет комплексный характер и включает как специфические антибактериальные препараты, так и неспецифические средства и физиопроцедуры. Помимо специфических антибактериальных средств (доксициклин, вибрамицин, офлоксацины, ципрофлоксацины и пр.), больным также назначаются иммуномодулирующие препараты, чаще всего, индукторы эндогенного интерферона. Лечение проводится строго индивидуально, с учетом особенностей течения заболевания, стадии воспалительного процесса, его локализации, наличия или отсутствия других осложнений. Больной микоплазмозом считается излеченным, если спустя 1 месяц после проведенного лечения, в контрольных лабораторных исследованиях микоплазмы или уреаплазмы не обнаруживаются.
Срок лечения неосложненного микоплазмоза или уреаплазмоза составляет около 3-х недель, но может быть увеличен при наличии развившихся осложнений. Общим обязательным условием успешного лечения является одновременность лечения половых партнеров – включая ситуации, когда микоплазмы или уреаплазмы достоверно выявлены только у одного из них. В период прохождения лечебного процесса и последующего контроля половая жизнь запрещена для обоих партнеров. Лечебный процесс имеет комплексный характер и включает как специфические антибактериальные препараты, так и неспецифические средства и физиопроцедуры. Помимо специфических антибактериальных средств (доксициклин, вибрамицин, офлоксацины, ципрофлоксацины и пр.), больным также назначаются иммуномодулирующие препараты, чаще всего, индукторы эндогенного интерферона. Лечение проводится строго индивидуально, с учетом особенностей течения заболевания, стадии воспалительного процесса, его локализации, наличия или отсутствия других осложнений. Больной микоплазмозом считается излеченным, если спустя 1 месяц после проведенного лечения, в контрольных лабораторных исследованиях микоплазмы или уреаплазмы не обнаруживаются.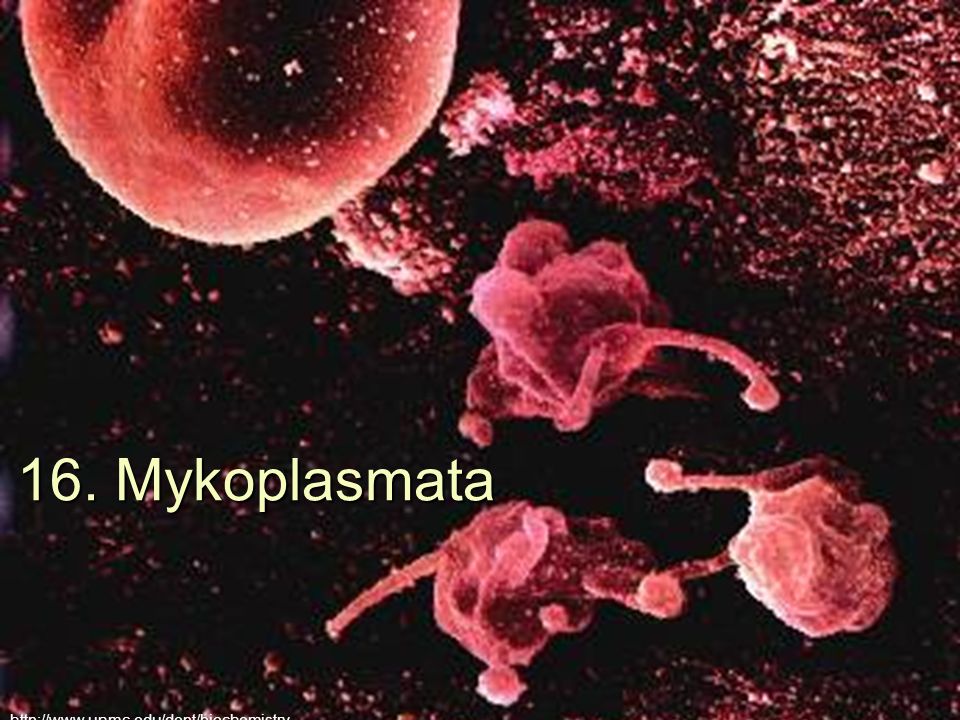
Инфекции Mycoplasma pneumoniae — HealthyChildren.org
Некоторые инфекции легких, в том числе многие случаи легкой пневмонии (также называемой ходячей пневмонией ), вызываются микроорганизмом под названием Mycoplasma pneumoniae. Он передается от человека к человеку с выделениями, такими как мокрота из дыхательных путей, и имеет инкубационный период от 2 до 3 недель. Передача этого микроорганизма обычно происходит при тесном контакте. Вспышки случались и обычны в летних лагерях и колледжах, а также в домохозяйствах среди членов семьи.
Хотя инфекции M pneumoniae редко встречаются у детей младше 5 лет, они являются основной причиной пневмонии у детей школьного возраста и молодых людей. Эпидемии этого заболевания в масштабах всего сообщества происходят каждые 4–7 лет.
Признаки и симптомы
Инфекции, вызываемые M pneumoniae , обычно вызывают легкие симптомы. У некоторых детей со временем они могут ухудшиться. Наиболее распространенные симптомы
У некоторых детей со временем они могут ухудшиться. Наиболее распространенные симптомы
- Бронхит
Инфекции верхних дыхательных путей, включая ангину и иногда ушные инфекции
У детей с этой инфекцией также может наблюдаться высокая температура, длительная слабость, а в некоторых случаях головные боли и сыпь.Их кашель может меняться от сухого до флегматического. В редких случаях у детей может развиться круп и синусит.
Когда звонить педиатру
Если эти симптомы, включая лихорадку, длятся более нескольких дней, обратитесь к педиатру.
Как ставится диагноз?
Ваш педиатр проведет медицинский осмотр вашего ребенка. Врач может назначить анализы крови на антитела к M pneumoniae или холодовых агглютининов, , которые являются особым типом антител.Разрабатываются специальные тесты для идентификации организма в образцах из горла и дыхательных путей, но они пока не доступны.
Лечение
В большинстве случаев бронхит и заболевания верхних дыхательных путей, связанные с инфекцией M pneumoniae , протекают в легкой форме и проходят сами по себе без лечения антибиотиками. Однако антибиотики, такие как эритромицин, азитромицин или доксициклин, могут назначаться при более серьезных симптомах, связанных с пневмонией и ушными инфекциями.
Каков прогноз?
Эта инфекция часто вызывает свистящее дыхание у детей с астмой или реактивными дыхательными путями. Большинство людей полностью выздоравливают от этой инфекции, даже если антибиотики не используются. Смертность достаточно низкая.
Информация, содержащаяся на этом веб-сайте, не должна использоваться в качестве замены медицинской помощи и рекомендаций вашего педиатра. Могут быть варианты лечения, которые ваш педиатр может порекомендовать в зависимости от индивидуальных фактов и обстоятельств.
Детские микоплазменные инфекции: основы практики, патофизиология, эпидемиология
Санчес-Варгас FM, Гомес-Дуарте О.Г. Mycoplasma pneumoniae — новый внелегочный возбудитель. Clin Microbiol Infect . 2008 г., 14 февраля (2): 105–17. [Медлайн].
Аткинсон Т.П., Балиш М.Ф., Уэйтс К.Б. Эпидемиология, клиника, патогенез и лабораторная диагностика микоплазменной пневмонии. FEMS Microbiol Rev . 2008 г. 32 ноября (6): 956-73. [Медлайн].
Grosher M, Alexandre M, Poszepczynska-Guigne E, Revuz J, Roujeau J. Рецидивирующая мультиформная эритема в связи с рецидивирующими инфекциями Mycoplasma pneumoniae. J Am Acad Дерматол . 2007. 56:S118-9.
2007. 56:S118-9.
Гулерия Р., Нисар Н., Чавла ТЦ, Бисвас НР. Mycoplasma pneumoniae и осложнения со стороны центральной нервной системы: обзор. J Lab Clin Med . 2005 авг. 146(2):55-63. [Медлайн].
Манвани Н.С., Баласубраманиан С., Дханалакшми К., Сумант А. Синдром Стивенса-Джонсона в сочетании с микоплазменной пневмонией. Индийский J Педиатр . 2012 авг. 79(8):1097-9.
Тэм С.С., О’Брайен С.Дж., Родригес Л.С.Инфекции гриппа, кампилобактера и микоплазмы и госпитализация по поводу синдрома Гийена-Барре, Англия. Внезапное заражение Dis . 12 (12) декабря 2006 г.: 1880-7. [Медлайн].
Нарита М. Патогенез внелегочных проявлений инфекции Mycoplasma pneumoniae с особым упором на пневмонию. J Заражение Chemother . 2010 июнь 16 (3): 162-9.
2010 июнь 16 (3): 162-9.
Банерджи Б., Петерсен К. Психоз после микоплазменной пневмонии. Мил Мед . 2009 Сентябрь 174 (9): 1001-4.
Шах СС. Микоплазменная пневмония. Лонг С.С., Пикеринг Л.К., Пробер К.Г. Принципы и практика детских инфекционных болезней . 4-е изд. Филадельфия, Пенсильвания: Эльзевир Черчилль Ливингстон; 2012. 993-998.
Гольденберг Р.Л., Эндрюс В.В., Гепферт А.Р. и др. Исследование преждевременных родов в Алабаме: культура пуповинной крови Ureaplasma urealyticum и Mycoplasma hominis у очень недоношенных новорожденных. Am J Obstet Gynecol . 2008 янв. 198(1):43.e1-5. [Медлайн].
Санчес П.Дж., Сейгель Д.Д. Генитальные микоплазмы. Макмиллан Дж. А., Фейгин Р. Д., ДеАнджелис К. Д., Джонс М. Д., ред. Педиатрия Оски: принципы и практика . 4-е изд. Филадельфия, Пенсильвания: Липпинкотт, Уильямс и Уилкинс; 2006. 539-41.
4-е изд. Филадельфия, Пенсильвания: Липпинкотт, Уильямс и Уилкинс; 2006. 539-41.
Андерсен Б., Соколовский И., Остергаард Л. и др. Mycoplasma genitalium: распространенность и поведенческие факторы риска среди населения в целом. Заражение сексом . июнь 2007 г. 83(3):237-41.
Вискарди РМ. Виды уреаплазмы: роль в неонатальной заболеваемости и исходах. Arch Dis Child Fetal Neonatal Ed . Январь 2014 г. 99(1):F87-92.
Дон М., Канчиани М., Корппи М. Внебольничная пневмония у детей: что устарело? Какие новости?. Акта Педиатр . ноябрь 2010 г. 99(11):1602-8.
Уэйтс К.Б., Аткинсон Т.П. Роль микоплазм при инфекциях верхних дыхательных путей. Curr Infect Dis Rep . 2009 май. 11(3):198-206.
Лю С.Л., Цао Дж.Г., Чжоу П. и др. Вспышка микоплазменной пневмонии в детском саду. Чжунхуа Юй Фан И Сюэ За Чжи . март 2009 г. 43(3):206-9.
Ньюкомб, округ Колумбия, Пиблз Р.С. мл.Насекомые и астма: разные болезни? Proc Am Thorac Soc . 1 мая 2009 г. 6(3):266-71.
Хассан Дж., Ирвин Ф., Дули С., Коннелл Дж. Инфекция Mycoplasma pneumoniae у детей: анализ растворимых иммунных маркеров как факторов риска астмы. Хум Иммунол . декабрь 2008 г. 69(12):851-5.
Пападопулос Н.Г., Христодулу И., Роде Г. и др. Вирусы и бактерии при обострениях астмы — систематический обзор GA² LEN-DARE. Аллергия . апрель 2011 г. 66(4):458-68.
Аллергия . апрель 2011 г. 66(4):458-68.
Корппи М. Бактериальные инфекции и детская астма. Immunol Allergy Clin North Am . ноябрь 2010 г. 30(4):565-74.
Гилберт Т.В., Денлингер Л.С. Роль инфекции в развитии и обострении бронхиальной астмы. Expert Respir Med . февраль 2010 г. 4(1):71-83.
Миллер СТ. Как я лечу острый грудной синдром у детей с серповидноклеточной анемией. Кровь . Май 2011 г. 117(20):5297-305.
Manhart LE, Holmes KK, Hughes JP, Houston LS, Totten PA. Mycoplasma genitalium среди молодых людей в США: новая инфекция, передающаяся половым путем. Am J Общественное здравоохранение . июнь 2007 г. 97(6):1118-25.
Юн Ю.С., Ли К. И. Микоплазменная пневмония у детей. Корейский J Pediatr . февраль 2012 г. 55(2):42-7.
И. Микоплазменная пневмония у детей. Корейский J Pediatr . февраль 2012 г. 55(2):42-7.
Судзуки Ю., Итагаки Т., Сето Дж., Канеко А., Абико С., Мизута К. и др.Вспышка инфекции, вызванной резистентной к макролидам Mycoplasma pneumoniae, в Ямагате, Япония, в 2009 г. Pediatr Infect Dis J . март 2013 г. 32(3):237-40.
Инчли К.С., Берг А.С., Вахдани Бенам А., Квиссел А.К., Лигаард Т.М., Накстад Б. Mycoplasma Pneumoniae: перекрестное популяционное сравнение тяжести заболевания у детей дошкольного и школьного возраста. Pediatr Infect Dis J . 2017 36 октября (10): 930-936. [Медлайн].
Корппи М.Лечение бактериальных инфекций у детей с бронхиальной астмой. Expert Rev Anti Infect Ther . сентябрь 2009 г. 7(7):869-77.
Cairns C, Adler K, Moss T, Crews A, Chu H, Kraft M. Mycoplasma pneumoniae увеличивает выработку муцина в дыхательных путях у астматиков. Академия скорой медицинской помощи . 2007. 14:С193.
Дидерен Б.М., Ван дер Валк П.Д., Клютманс Дж.А., Петерс М.Ф., Хендрикс Р. Роль атипичных респираторных патогенов в обострениях хронической обструктивной болезни легких. Евр Респир J . август 2007 г. 30(2):240-4.
Кенни GE. Генитальные микоплазмы: виды Mycoplasma genitalium, Mycoplasma hominis и Ureaplasma. Манделл Г.Л., Беннетт Дж.Е., Долин Р., ред. Принципы и практика инфекционных заболеваний Манделла, Дугласа и Беннета . 7-е изд. Филадельфия, Пенсильвания: Эльзевир Черчилль Ливингстон; 2010. Том 2: 2491-5.
7-е изд. Филадельфия, Пенсильвания: Эльзевир Черчилль Ливингстон; 2010. Том 2: 2491-5.
Росс Дж.Д., Дженсен Дж.С. Mycoplasma genitalium как инфекция, передающаяся половым путем: значение для скрининга, тестирования и лечения. Заражение сексом . август 2006 г. 82(4):269-71.
Кос Л., Гэлбрейт С.С., Лион В.Б. Язвы влагалища при острой микоплазменной инфекции. J Am Acad Дерматол . 2007. 56:S117-8.
Тейлор-Робинсон Д.Роль микоплазм в исходе беременности. Best Pract Res Clin Obstet Gynaecol . 2007 21 июня (3): 425-38.
Тош А.К., Ван Дер Пол Б., Фортенберри Д.Д. и др. Mycoplasma genitalium среди женщин-подростков и их партнеров. J Adolesc Health . 2007 май. 40(5):412-7.
Гжеско Дж., Элиас М., Мановец М., Габрис М.С. Генитальные микоплазмы — заболеваемость и потенциальное влияние на фертильность человека. Мед Веку Розвой . 2006. 10:985-92.
Daxboeck F. Инфекции центральной нервной системы Mycoplasma pneumoniae. Карр Опин Нейрол . 2006. 19:374-8.
Хата А., Хонда Ю., Асада К., Сасаки Ю., Кенри Т., Хата Д. Mycoplasma hominis менингит у новорожденного: история болезни и обзор. J Заразить . октябрь 2008 г. 57(4):338-43.
Hsieh SC, Kuo YT, Chern MS, Chen CY, Chan WP, Yu C. Микоплазменная пневмония: клинические и рентгенологические признаки у 39 детей. Педиатр Инт . июнь 2007 г. 49(3):363-7.
Микоплазменная пневмония: клинические и рентгенологические признаки у 39 детей. Педиатр Инт . июнь 2007 г. 49(3):363-7.
Нисар Н., Гулерия Р., Кумар С. и др. Mycoplasma pneumoniae и ее роль в развитии бронхиальной астмы. Постград Мед J . 2007 фев. 83 (976): 100-4.
Отман Н., Исаакс Д., Дейли А.Дж., Кессон А.М.Инфекция Mycoplasma pneumoniae в клинических условиях. Педиатр Инт . 2008 г. 50 октября (5): 662-6.
Гарсия К., Угальде Э., Монтеагудо И., Саес А., Агуэро Х., Мартинес-Мартинес Л. и др. Выделение Mycoplasma hominis у больных в критическом состоянии с легочными инфекциями: клинико-микробиологический анализ в отделении реанимации. Медицинская интенсивная терапия . 2007. 33:143-7.
Шалок П.С., Динулос Дж. Г., Пейс Н., Шварценбергер К., Венгер Дж.К.Многоформная эритема, вызванная инфекцией Mycoplasma pneumoniae, у двух детей. Педиатр Дерматол . ноябрь-декабрь 2006 г. 23(6):546-55.
Г., Пейс Н., Шварценбергер К., Венгер Дж.К.Многоформная эритема, вызванная инфекцией Mycoplasma pneumoniae, у двух детей. Педиатр Дерматол . ноябрь-декабрь 2006 г. 23(6):546-55.
Latsch K, Girschick HJ, Abele-Horn M. Синдром Стивенса-Джонсона без кожных поражений. J Med Microbiol . Декабрь 2007 г. 56 (Pt 12): 1696-9.
Веттер Д.А., Камиллери М.Дж. Клинические, этиологические и гистопатологические особенности синдрома Стивенса-Джонсона в течение 8 лет в клинике Майо. февраль 2010 г.; Mayo Clin Proc . февраль 2010 г. 85(2):131-8.
ЦКЗ. Вспышка узловатой эритемы неизвестной этиологии — Нью-Мексико, ноябрь 2007 г. — январь 2008 г. MMWR Morb Mortal Wkly Rep . 2009 11 декабря. 58(48):1347-51.
Kano Y, Mitsuyama Y, Hirahara K, Shiohara T. Узловатая эритема, анафилактоидная пурпура и острая крапивница, вызванная инфекцией Mycoplasma pneumoniae, у 3 человек в одной семье. J Am Acad Дерматол . 2007 авг.57 (2 Дополнение): S33-5.
Узловатая эритема, анафилактоидная пурпура и острая крапивница, вызванная инфекцией Mycoplasma pneumoniae, у 3 человек в одной семье. J Am Acad Дерматол . 2007 авг.57 (2 Дополнение): S33-5.
Fearon D, Hesketh EL, Mitchell AE, Grimwood K. Инфекция Mycoplasma pneumoniae, осложненная пневмомедиастином и тяжелым мукозитом. J Педиатр Детское здоровье . 2007 май. 43(5):403-5.
Ву К.С., Куо Х.К., Ю. Х.Р., Ван Л., Ян К.Д. Ассоциация острой крапивницы с инфекцией Mycoplasma pneumoniae у госпитализированных детей. Энн Аллергия Астма Иммунол . 2009 авг. 103(2):134-9.
Смит Л.Г.Микоплазменная пневмония и ее осложнения. Заразить Dis Clin North Am . 2010 март 24 (1): 57-60.
Нарита М. Патогенез неврологических проявлений инфекции Mycoplasma pneumoniae. Педиатр Нейрол . 2009 сен. 41 (3): 159-66.
Педиатр Нейрол . 2009 сен. 41 (3): 159-66.
Аслан М., Касапкопур О., Ясар Х. и др. Вызывают ли инфекции ювенильный идиопатический артрит? Ревматол Инт . 2011 31 февраля (2): 215-20.
Адзумагава К., Камбара Ю., Мурата Т., Тамаи Х.Четыре случая артрита, связанного с инфекцией Mycoplasma pneumoniae. Педиатр Инт . август 2008 г. 50 (4): 511-3.
Harjacek M, Ostojic J, Djakovic Rode O. Ювенильные спондилоартропатии, связанные с инфекцией Mycoplasma pneumoniae. Клин Ревматол . 2006 г. 25 июля (4): 470-5.
Хан Ф.Ю., А. Яссин М. Mycoplasma pneumoniae, ассоциированная с тяжелой аутоиммунной гемолитической анемией: клинический случай и обзор литературы. Braz J Infect Dis .февраль 2009 г. 13(1):77-9.
Гурсель О., Алтун Д., Атай А.А., Бедир О., Курекчи А.Е. Инфекция Mycoplasma pneumoniae, связанная с панцитопенией: клинический случай. J Pediatr Hematol Oncol . 2009 31 октября (10): 760-2.
Witmer CM, Steenhoff AP, Shah SS, Raffini LJ. Mycoplasma pneumoniae, инфаркт селезенки и транзиторные антифосфолипидные антитела: новая ассоциация? Педиатрия . Январь 2007 г. 119 (1): e292-5.
Турман К.А., Уолтер Н.Д., Шварц С.Б., Митчелл С.Л., Диллон М.Т., Боман А.Л.Сравнение лабораторных диагностических процедур для обнаружения Mycoplasma pneumoniae при вспышках среди населения. Клин Заражение Дис . 1 мая 2009 г. 48(9):1244-9.
Nir-Paz R, Michael-Gayego A, Ron M, Block C. Оценка восьми коммерческих тестов на антитела к Mycoplasma pneumoniae при отсутствии острой инфекции. Clin Microbiol Infect . июль 2006 г. 12(7):685-8.
Clin Microbiol Infect . июль 2006 г. 12(7):685-8.
Лю Ф.К., Чен П.Ю., Хуан Ф., Цай Ч.Р., Ли С.И., Ван Л.С.Экспресс-диагностика микоплазменной пневмонии у детей методом полимеразной цепной реакции. J Microbiol Immunol Infect . декабрь 2007 г. 40(6):507-12.
Ким Н.Х., Ли Дж.А., Ын Б.В., Шин С.Х., Чунг Э.Х., Пак К.В. Сравнение полимеразной цепной реакции и теста антител с непрямой агглютинацией частиц для диагностики микоплазменной пневмонии у детей во время двух вспышек. Pediatr Infect Dis J . 2007 26 октября (10): 897-903.
Нильссон А.С., Бьоркман П., Перссон К.Полимеразная цепная реакция превосходит серологию в диагностике острой инфекции Mycoplasma pneumoniae и выявляет высокую частоту персистирующей инфекции. ВМС Микробиол . 2008. 8:93.
Принципи Н., Эспозито С.Устойчивая к макролидам Mycoplasma pneumoniae: ее роль в респираторной инфекции. J Антимикробный химиопрепарат . 2013 март 68 (3): 506-11.
Ли Х, Аткинсон Т.П., Хагуд Дж., Макрис С., Даффи Л.Б., Уэйтс К.Б. Возникающая устойчивость к макролидам у Mycoplasma pneumoniae у детей: обнаружение и характеристика устойчивых изолятов. Pediatr Infect Dis J . август 2009 г. 28(8):693-6.
Чжэн С., Ли С., Селваранган Р., Цинь С., Тан Ю.В., Стайлз Дж. и др.Устойчивая к макролидам Mycoplasma pneumoniae, США 1 . Внезапное заражение Dis . 2015 авг. 21 (8): 1470-1472. [Медлайн]. [Полный текст].
2015 авг. 21 (8): 1470-1472. [Медлайн]. [Полный текст].
Chambert-Loir C, Ouachee M, Collins K, Evrard P, Servais L. Немедленное облегчение симптомов энцефалита Mycoplasma pneumoniae после внутривенного введения иммуноглобулина. Педиатр Нейрол . ноябрь 2009 г. 41(5):375-7.
Ямадзаки Т., Сасаки Т., Такахата М. Активность гареноксацина в отношении чувствительных к макролидам и устойчивых к макролидам Mycoplasma pneumoniae. Противомикробные агенты Chemother . июнь 2007 г. 51(6):2278-9.
Mycoplasma pneumoniae pneumoniae у детей
Korean J Pediatr. 2012 февраль; 55(2): 42–47.
, MD и , MDYou-Sook Youn
Кафедра педиатрии, Медицинский колледж, Католический университет Кореи, Сеул, Корея.
Kyung-Yil Lee
Кафедра педиатрии, Медицинский колледж, Корейский католический университет, Сеул, Корея.
Кафедра педиатрии, Медицинский колледж, Корейский католический университет, Сеул, Корея.
Автор, ответственный за переписку. Автор переписки: Kyung-Yil Lee, MD. Кафедра педиатрии, Корейский католический университет, Больница Святой Марии в Тэджоне, 64 Тэхын-ро, Чун-гу, Тэджон 301-723, Корея. Тел.: +82-42-220-9541, факс: +82-42-221-2925, rk.ca.cilohtac@liygnuykeelПоступила в редакцию 15 декабря 2011 г.; Принято 11 января 2012 г.
Copyright © 2012 Корейского педиатрического общества.org/licenses/by-nc/3.0/), который разрешает неограниченное некоммерческое использование, распространение и воспроизведение на любом носителе при условии правильного цитирования оригинальной работы. Эта статья цитировалась в других статьях PMC.Abstract
Mycoplasma pneumoniae (MP), мельчайшая самовоспроизводящаяся биологическая система, является частой причиной инфекций верхних и нижних дыхательных путей, приводящих к широкому спектру легочных и внелегочных проявлений. MP-пневмония регистрируется в 10-40% случаев внебольничной пневмонии и еще выше во время эпидемий.Инфекция МП эндемична в крупных сообществах мира с циклическими эпидемиями каждые 3–7 лет. В Корее с середины 1980-х годов по настоящее время наблюдаются 3–4-летние циклы. Хотя для диагностики МП-инфекции доступны различные серологические анализы и методы полимеразной цепной реакции (ПЦР), ранняя диагностика МП-пневмонии ограничена отсутствием антител к иммуноглобулину (Ig) М и изменчивыми результатами ПЦР на ранних стадиях инфекции. инфекционное заболевание. Таким образом, краткосрочные парные серологические тесты IgM могут быть обязательными для раннего и окончательного диагноза.Инфекция МП обычно представляет собой легкое и самоограничивающееся заболевание без специфического лечения, и при необходимости макролиды обычно используются в качестве препаратов первого выбора для детей. Недавно во всем мире были зарегистрированы устойчивые к макролидам штаммы MP. Однако имеется несколько сообщений о явной неэффективности лечения, например о прогрессировании пневмонии до острого респираторного дистресс-синдрома, несмотря на лечение макролидами.
MP-пневмония регистрируется в 10-40% случаев внебольничной пневмонии и еще выше во время эпидемий.Инфекция МП эндемична в крупных сообществах мира с циклическими эпидемиями каждые 3–7 лет. В Корее с середины 1980-х годов по настоящее время наблюдаются 3–4-летние циклы. Хотя для диагностики МП-инфекции доступны различные серологические анализы и методы полимеразной цепной реакции (ПЦР), ранняя диагностика МП-пневмонии ограничена отсутствием антител к иммуноглобулину (Ig) М и изменчивыми результатами ПЦР на ранних стадиях инфекции. инфекционное заболевание. Таким образом, краткосрочные парные серологические тесты IgM могут быть обязательными для раннего и окончательного диагноза.Инфекция МП обычно представляет собой легкое и самоограничивающееся заболевание без специфического лечения, и при необходимости макролиды обычно используются в качестве препаратов первого выбора для детей. Недавно во всем мире были зарегистрированы устойчивые к макролидам штаммы MP. Однако имеется несколько сообщений о явной неэффективности лечения, например о прогрессировании пневмонии до острого респираторного дистресс-синдрома, несмотря на лечение макролидами. Иммунопатогенез MP-пневмонии, как полагают, представляет собой гипериммунную реакцию хозяина на повреждения, вызванные MP-инфекцией, включая гиперпродукцию цитокинов и активацию иммунных клеток (Т-клеток).В этом контексте иммуномодулирующее лечение (кортикостероиды и/или внутривенные Ig) в дополнение к лечению антибиотиками может быть рассмотрено для пациентов с тяжелой инфекцией.
Иммунопатогенез MP-пневмонии, как полагают, представляет собой гипериммунную реакцию хозяина на повреждения, вызванные MP-инфекцией, включая гиперпродукцию цитокинов и активацию иммунных клеток (Т-клеток).В этом контексте иммуномодулирующее лечение (кортикостероиды и/или внутривенные Ig) в дополнение к лечению антибиотиками может быть рассмотрено для пациентов с тяжелой инфекцией.
Ключевые слова:
Ключевые слова: Mycoplasma pneumoniae , пневмония, макролиды, лекарственная устойчивость, дети, кортикостероиды
Введение . Хотя на сегодняшний день у животных и человека обнаружено более 200 видов микоплазм, МП является наиболее признанным патогеном человека среди них.Инфекция МП характеризуется разнообразием клинических проявлений, начиная от бессимптомной инфекции и заканчивая фатальной пневмонией или внелегочными заболеваниями. МП-пневмония регистрируется в 10–40% случаев внебольничной пневмонии, и дети являются наиболее восприимчивой группой к МП-инфекции1,2).
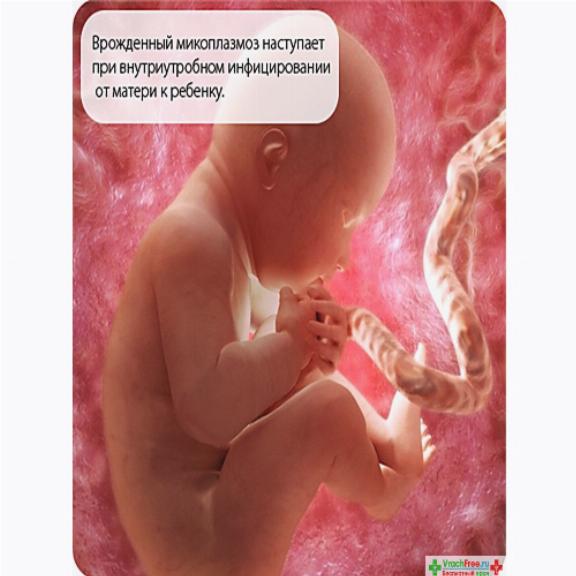 С лета 2011 г. по всей Корее распространяется новая эпидемия МП. Эта эпидемия имеет некоторые клинические и лабораторные характеристики, которые, по-видимому, отличаются от характеристик предыдущих эпидемий, хотя подтипы штаммов в этой эпидемии еще не идентифицированы.В этом обзоре мы кратко даем обзор патогенеза, эпидемиологии, клинических проявлений, диагностики и лечения инфекции МП, в том числе резистентной к макролидам МП (MRMP).
С лета 2011 г. по всей Корее распространяется новая эпидемия МП. Эта эпидемия имеет некоторые клинические и лабораторные характеристики, которые, по-видимому, отличаются от характеристик предыдущих эпидемий, хотя подтипы штаммов в этой эпидемии еще не идентифицированы.В этом обзоре мы кратко даем обзор патогенеза, эпидемиологии, клинических проявлений, диагностики и лечения инфекции МП, в том числе резистентной к макролидам МП (MRMP).Биологическая характеристика и иммунопатогенез
МП является исключительно мелким прокариотом, который, как и вирусы, может проходить через фильтровальную бумагу. Из-за отсутствия клеточной стенки этот микроорганизм нечувствителен к бета-лактамным антибиотикам и не окрашивается по Граму. Кроме того, MP имеет чрезвычайно маленький геном, что делает ее прихотливо растущей бактерией, требующей присутствия множества веществ, включая нуклеотиды и стеролы, для ее репликации как внутри хозяина, так и в культуральных системах in vitro 3). MP является внеклеточным патогеном слизистых оболочек, а не внутриклеточным патогеном, как вирусы, и не оказывает цитопатического действия на другие системы культивирования клеток, за исключением респираторного реснитчатого эпителия4). Считалось, что размножающиеся агенты МП распространяются на клетки нижних дыхательных путей и вызывают пневмонию. В этом контексте выживание МП изначально зависит от цитоадгезии к респираторному эпителию хозяина. МП имеет кончик прикрепления, в котором локализован комплекс адгезивных и взаимодействующих адгезивно-акцессорных белков.После прикрепления MP может потребоваться размножение, чтобы установить инфекцию, включая колонизацию и дальнейшее воспаление других тканей5). Исследования in vitro показали, что виды микоплазм предпочтительно прикрепляются к реснитчатым респираторным эпителиальным клеткам и вызывают цитопатический эффект, вызванный перекисью водорода или другими токсинами (например, АДФ-рибозилирующим и вакуолизирующим цитотоксином), а также скользящей подвижностью6,7).
MP является внеклеточным патогеном слизистых оболочек, а не внутриклеточным патогеном, как вирусы, и не оказывает цитопатического действия на другие системы культивирования клеток, за исключением респираторного реснитчатого эпителия4). Считалось, что размножающиеся агенты МП распространяются на клетки нижних дыхательных путей и вызывают пневмонию. В этом контексте выживание МП изначально зависит от цитоадгезии к респираторному эпителию хозяина. МП имеет кончик прикрепления, в котором локализован комплекс адгезивных и взаимодействующих адгезивно-акцессорных белков.После прикрепления MP может потребоваться размножение, чтобы установить инфекцию, включая колонизацию и дальнейшее воспаление других тканей5). Исследования in vitro показали, что виды микоплазм предпочтительно прикрепляются к реснитчатым респираторным эпителиальным клеткам и вызывают цитопатический эффект, вызванный перекисью водорода или другими токсинами (например, АДФ-рибозилирующим и вакуолизирующим цитотоксином), а также скользящей подвижностью6,7).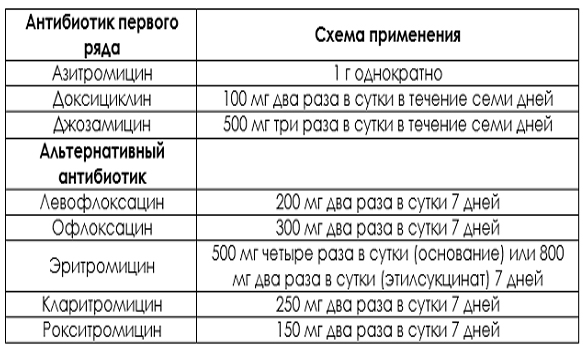 С другой стороны, при быстро растущем характере МП показания возбудителей МП в патологических тканях ограничены.МП не обнаруживаются ни под, ни внутри клеток респираторного эпителия на животных моделях, а также не эффективны электронно-микроскопическое исследование образцов от пациентов с тяжелой МП пневмонией и анализ методом полимеразной цепной реакции (ПЦР) аспирата легких детей с внебольничной пневмонией. для поиска агентов MP8,9).
С другой стороны, при быстро растущем характере МП показания возбудителей МП в патологических тканях ограничены.МП не обнаруживаются ни под, ни внутри клеток респираторного эпителия на животных моделях, а также не эффективны электронно-микроскопическое исследование образцов от пациентов с тяжелой МП пневмонией и анализ методом полимеразной цепной реакции (ПЦР) аспирата легких детей с внебольничной пневмонией. для поиска агентов MP8,9).
Поскольку инфекция МП, как и другие инфекции, контролируется иммунной системой хозяина, а большинство пациентов, инфицированных МП, выздоравливают от болезни без пневмонии, возможно, что острое повреждение легких у пораженных пациентов связано с иммунодефицитом пациента. отклик.При инфекции МП врожденная и адаптивная иммунная система хозяина работают вместе против повреждений, вызванных инфекцией. Медиаторы (белки) врожденной иммунной реакции могут влиять на адаптивную иммунную реакцию. Толл-подобные рецепторы (TLR) и, возможно, внутриклеточные сенсоры в инфицированных клетках и макрофагах, которые распознают компоненты MP, индуцируют антипатогенные белки и другие белки, включая провоспалительные цитокины10,11). Эти белки могут воздействовать на клетки адаптивной иммунной системы.Сообщалось, что липопротеины, полученные из микоплазм, такие как липопептид 2, активирующий макрофаги, индуцируют цитокины и хемокины из макрофагов через TLRs12,13). Эти цитокины привлекают иммунные клетки, включая Т-клетки, что приводит к дальнейшей продукции цитокинов и может быть вовлечено в воспалительные реакции на инфекцию МП.
Эти белки могут воздействовать на клетки адаптивной иммунной системы.Сообщалось, что липопротеины, полученные из микоплазм, такие как липопептид 2, активирующий макрофаги, индуцируют цитокины и хемокины из макрофагов через TLRs12,13). Эти цитокины привлекают иммунные клетки, включая Т-клетки, что приводит к дальнейшей продукции цитокинов и может быть вовлечено в воспалительные реакции на инфекцию МП.
Многие иммунологические исследования показали, что различные цитокины, включая интерлейкин (IL)-2, IL-8 и IL-18; другие реактивные вещества; и иммунные клетки, включая антигенпрезентирующие клетки и Т-клетки, участвуют в иммунной реакции на MP14-16).Поскольку считается, что основные провоспалительные цитокины, индуцируемые МП-инфекцией, являются важными медиаторами защиты легких и повреждения легких, дисбаланс цитокинов может быть ответственным за повреждение легких при этой инфекции.
Т-клетки могут играть решающую роль в остром повреждении легких, вызванном инфекцией MP, а также другими вирусными инфекциями, такими как вирус гриппа. Предыдущие отчеты об этих инфекциях показали, что у мышей с дефицитом Т-клеток или у мышей с депрессией Т-клеток и иммунодепрессантами была менее тяжелая пневмония с увеличенным временем выживания и незначительными патологическими изменениями по сравнению с контрольными мышами17-19).Кроме того, некоторые клинические характеристики МП-пневмонии также помогают предположить патогенез повреждения легких, вызванного МП. Ранее мы обнаружили, что тяжесть пневмонии коррелировала с количеством лимфоцитов при поступлении, а раннее введение иммуномодуляторов (кортикостероидов) вызывало быстрое восстановление тяжелых легочных консолидаций в течение нескольких дней20,21).
Предыдущие отчеты об этих инфекциях показали, что у мышей с дефицитом Т-клеток или у мышей с депрессией Т-клеток и иммунодепрессантами была менее тяжелая пневмония с увеличенным временем выживания и незначительными патологическими изменениями по сравнению с контрольными мышами17-19).Кроме того, некоторые клинические характеристики МП-пневмонии также помогают предположить патогенез повреждения легких, вызванного МП. Ранее мы обнаружили, что тяжесть пневмонии коррелировала с количеством лимфоцитов при поступлении, а раннее введение иммуномодуляторов (кортикостероидов) вызывало быстрое восстановление тяжелых легочных консолидаций в течение нескольких дней20,21).
Наконец, неизвестно, вызывает ли иммунологическое воспаление при поражениях легких весь агент МП или другие вещества (компоненты МП или медиаторы хозяина).В этом выпуске мы вводим новую концепцию иммунопатогенеза острого повреждения легких при МП или инфекциях, вызванных вирусом гриппа, используя гипотезу, включающую «систему белкового гомеостаза» хозяина2,19). Вкратце, мы постулировали, что адаптивная иммунная система является одной из систем белкового гомеостаза in vivo . В-клетки контролируют белки, за исключением малых белков, через антитела, а Т-клетки контролируют малые белки (пептиды) посредством продукции цитокинов или посредством их воздействия на связанные с клеткой патогенные белки или через рецепторы Т-клеток.В инкубационный период МП-инфекции вещества, в том числе патогенные белки, продуцируются в очаге (возможно, вторичном иммунном органе вблизи очагов первичной инфекции). Вещества распространяются и достигают клеток легких как основных клеток-мишеней, а при внелегочных проявлениях — различных тканей через системный кровоток. Иммунные клетки начинают контролировать эти вещества, и начинают проявляться клинические симптомы и признаки. Патогенные белки связываются с клетками нижних дыхательных путей, рецепторы которых имеют к ним сродство, и этот процесс вызывает повреждение клеток и/или продукцию других белков через сигнальные пути к ядру пораженных клеток.
Вкратце, мы постулировали, что адаптивная иммунная система является одной из систем белкового гомеостаза in vivo . В-клетки контролируют белки, за исключением малых белков, через антитела, а Т-клетки контролируют малые белки (пептиды) посредством продукции цитокинов или посредством их воздействия на связанные с клеткой патогенные белки или через рецепторы Т-клеток.В инкубационный период МП-инфекции вещества, в том числе патогенные белки, продуцируются в очаге (возможно, вторичном иммунном органе вблизи очагов первичной инфекции). Вещества распространяются и достигают клеток легких как основных клеток-мишеней, а при внелегочных проявлениях — различных тканей через системный кровоток. Иммунные клетки начинают контролировать эти вещества, и начинают проявляться клинические симптомы и признаки. Патогенные белки связываются с клетками нижних дыхательных путей, рецепторы которых имеют к ним сродство, и этот процесс вызывает повреждение клеток и/или продукцию других белков через сигнальные пути к ядру пораженных клеток. Иммунные клетки привлекаются к очагам поражения, чтобы контролировать действие патогенных белков и белков из поврежденных клеток. Первоначально в эту реакцию вовлекаются неспецифические Т-клетки и неспецифические антитела. Во время этого процесса гиперактивированные иммунные клетки (в основном Т-клетки) продуцируют воспалительные цитокины и противовоспалительные цитокины, что приводит к дисбалансу цитокинов, связанному с дальнейшим повреждением клеток легких. После появления специфических клонов Т-клеток и специфических антител, которые эффективно контролируют патогенные белки, повреждение тканей прекращается и начинается реакция восстановления с участием иммунных клеток.
Иммунные клетки привлекаются к очагам поражения, чтобы контролировать действие патогенных белков и белков из поврежденных клеток. Первоначально в эту реакцию вовлекаются неспецифические Т-клетки и неспецифические антитела. Во время этого процесса гиперактивированные иммунные клетки (в основном Т-клетки) продуцируют воспалительные цитокины и противовоспалительные цитокины, что приводит к дисбалансу цитокинов, связанному с дальнейшим повреждением клеток легких. После появления специфических клонов Т-клеток и специфических антител, которые эффективно контролируют патогенные белки, повреждение тканей прекращается и начинается реакция восстановления с участием иммунных клеток.
Эпидемиология
Инфекция МП эндемична в больших сообществах мира, но эпидемии продолжительностью от нескольких месяцев до лет периодически возникают каждые 3-7 лет. В Корее с середины 1980-х годов по настоящее время наблюдаются 3–4-летние циклы MP-пневмонии. Пик заболеваемости пневмонией в основном приходится на осенний или зимний периоды, а эпидемии длятся примерно от 12 до 18 месяцев22,23). Иногда сообщалось о локальных вспышках в местах тесного контакта, например, в школах, военных казармах и стационарных учреждениях.
Иногда сообщалось о локальных вспышках в местах тесного контакта, например, в школах, военных казармах и стационарных учреждениях.
Эпидемиологические и клинические характеристики инфекции МП, такие как появление циклической эпидемии и лимфопении, аналогичны другим системным вирусным инфекциям, включая корь и грипп2). Восприимчивое население к МП, особенно молодая возрастная группа, будет увеличиваться в течение 3-4 лет межэпидемического периода, и эта возрастная группа может служить резервуаром эпидемий. Восприимчивая группа перейдет к более молодому поколению, и большая часть взрослого поколения со временем приобретет иммунитет к МП.Сероэпидемиологические исследования инфекции МП подтвердили этот вывод: серопозитивность антител иммуноглобулина (Ig) G против МП прогрессивно возрастает с возрастом24), а у лиц старше 40 лет уровень серопозитивности может достигать почти 100%. Хотя известно, что МП-пневмония преобладает у детей школьного возраста, в Корее возрастная группа от 4 до 6 лет была наиболее распространенной группой, а возраст детей, среди которых преобладала МП-инфекция, стал моложе, с низкой частотой инфекции во взрослой группе во время недавних эпидемий МП22,23).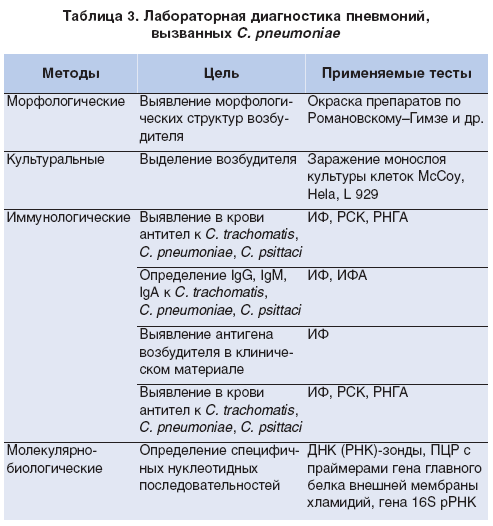
Точный уровень заражения населения во время эпидемии МП неизвестен. Однако серологические исследования позволяют предположить, что во время эпидемии значительная часть восприимчивого населения (>50%) может быть инфицирована, проявляя бессимптомные или легкие фенотипы, хотя доля больных МП пневмонией может быть очень низкой.
Считается, что подтипы МП различны в каждой эпидемии, как и при сезонном (межпандемическом) гриппе, хотя существует мало исследований для генов, отличных от гена P1.В предыдущем отчете было обнаружено, что в эпидемии преобладает один подтип МП P1; однако в других эпидемиях может преобладать другой подтип P125). Недавно штаммы MRMP были идентифицированы при эпидемиях в странах Дальнего Востока Азии, включая Японию, Китай, Корею и другие страны26-29). Штаммы мутировали в основном в нуклеиновых последовательностях 23S рРНК или рибосомных белках. В Корее исследовательская группа обнаружила, что во время эпидемии 2011 г. более 50% выделенных штаммов MP были штаммами MRMP30). Хотя сообщалось, что у пациентов, инфицированных MRMP, была более длительная лихорадка по сравнению с пациентами, инфицированными штаммами, чувствительными к макролидам, в нескольких случаях наблюдалась неэффективность лечения макролидами31,32). Учитывая, что MP-пневмония является иммуноопосредованным и самокупирующимся заболеванием, клинические последствия альтернативного лечения антибиотиками у пациентов со штаммами MRMP требуют дальнейшей оценки. Кроме того, Нарита недавно предложил интересный постулат о том, что штаммы MRMP могут демонстрировать менее эффективный синтез белка из-за рибосомных мутаций и что лекарственная устойчивость MP сама по себе не приводит непосредственно к клинической тяжести33).Мы обнаружили, что во время эпидемии 2011 года частота положительных результатов ПЦР была намного ниже, а исходная частота отрицательных результатов IgM-антител при поступлении была выше, чем во время эпидемии 2006–2007 годов (неопубликованные наблюдения).
Хотя сообщалось, что у пациентов, инфицированных MRMP, была более длительная лихорадка по сравнению с пациентами, инфицированными штаммами, чувствительными к макролидам, в нескольких случаях наблюдалась неэффективность лечения макролидами31,32). Учитывая, что MP-пневмония является иммуноопосредованным и самокупирующимся заболеванием, клинические последствия альтернативного лечения антибиотиками у пациентов со штаммами MRMP требуют дальнейшей оценки. Кроме того, Нарита недавно предложил интересный постулат о том, что штаммы MRMP могут демонстрировать менее эффективный синтез белка из-за рибосомных мутаций и что лекарственная устойчивость MP сама по себе не приводит непосредственно к клинической тяжести33).Мы обнаружили, что во время эпидемии 2011 года частота положительных результатов ПЦР была намного ниже, а исходная частота отрицательных результатов IgM-антител при поступлении была выше, чем во время эпидемии 2006–2007 годов (неопубликованные наблюдения).
Клинические проявления
Наиболее частым клиническим проявлением инфекции МП является пневмония. Также наблюдаются другие респираторные симптомы, такие как фарингит, средний отит, бронхит, синусит, круп и бронхиолит. Инкубационный период МП пневмонии составляет от 1 до 3 недель.Больные МП пневмонией проявляют острое начало лихорадки, боли в горле, недомогания и головной боли; однако насморк не является обычным, как при гриппе. Через 3–7 дней появляются конституциональные симптомы, кашель и рентгенологические признаки пневмонии. Обычно наблюдается лихорадка от 38℃ до 39,5℃. Клинические симптомы и физические признаки подозрения на пневмонию часто плохо коррелируют с рентгенологическими признаками пневмонии (ходячая пневмония). Клиническое течение у нелеченных пациентов вариабельно, но большинство симптомов разрешается в течение 2–4 недель, даже при прогрессирующей пневмонии, не отвечающей на антибиотики20).
Также наблюдаются другие респираторные симптомы, такие как фарингит, средний отит, бронхит, синусит, круп и бронхиолит. Инкубационный период МП пневмонии составляет от 1 до 3 недель.Больные МП пневмонией проявляют острое начало лихорадки, боли в горле, недомогания и головной боли; однако насморк не является обычным, как при гриппе. Через 3–7 дней появляются конституциональные симптомы, кашель и рентгенологические признаки пневмонии. Обычно наблюдается лихорадка от 38℃ до 39,5℃. Клинические симптомы и физические признаки подозрения на пневмонию часто плохо коррелируют с рентгенологическими признаками пневмонии (ходячая пневмония). Клиническое течение у нелеченных пациентов вариабельно, но большинство симптомов разрешается в течение 2–4 недель, даже при прогрессирующей пневмонии, не отвечающей на антибиотики20).
Рентгенологические признаки МП пневмонии плеоморфны. Обычны интерстициальные и бронхопневмонические модели, а сегментарная и/или долевая пневмония с плевральными выпотами не является редкостью. Ранее мы обнаружили, что дети старшего возраста (> 6 лет), которые имеют более зрелую иммунную систему, имели более длительную продолжительность лихорадки, более высокий уровень С-реактивного белка и более тяжелые поражения легких и более низкое количество лейкоцитов с дифференциацией лимфоцитов, чем младшая группа (< 5 лет)21).
Ранее мы обнаружили, что дети старшего возраста (> 6 лет), которые имеют более зрелую иммунную систему, имели более длительную продолжительность лихорадки, более высокий уровень С-реактивного белка и более тяжелые поражения легких и более низкое количество лейкоцитов с дифференциацией лимфоцитов, чем младшая группа (< 5 лет)21).
Инфекция MP показала связь с астмой.Инфекция может предшествовать возникновению астмы, усугублять течение астмы или играть роль в хронизации астмы у некоторых детей и взрослых1,34). Внелегочное вовлечение при инфекции МП было выявлено при неврологических, дерматологических, гематологических и других иммунологических заболеваниях. Кожная сыпь является наиболее частым проявлением, а осложнения со стороны центральной нервной системы, такие как менингоэнцефалит и синдром Гийена-Барре, наблюдаются редко. МП является основной причиной детского энцефалита. Известно, что во внелегочные проявления МП35 вовлечены иммунопатогенетические механизмы.
Диагностика
Несмотря на то, что для диагностики МП-инфекции использовались различные серологические анализы и методы ПЦР, методы ранней диагностики МП-пневмонии ограничены из-за отсутствия IgM-антител и различной степени обнаружения продуктов ПЦР в ранние стадии инфекции1,2).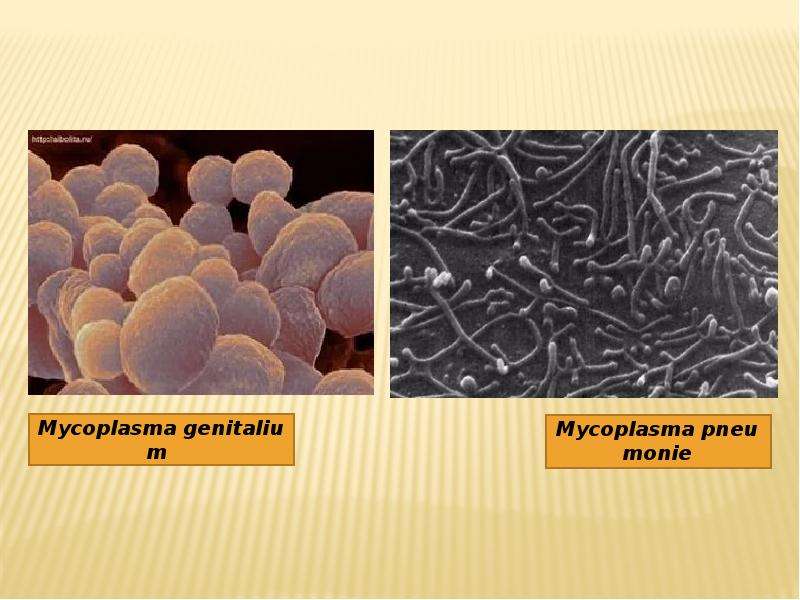
Серологические анализы, включая анализ связывания комплемента, анализ агглютинации микрочастиц, иммуноферментный анализ и иммуноферментный анализ, требуют парных образцов сыворотки для окончательного диагноза, демонстрирующего сероконверсию или 4-кратное увеличение титра.Известно, что чувствительность серологических анализов для обнаружения антител к MP варьирует36,37). Ранее мы сообщали, что более 45% пациентов с МП-пневмонией были сероконвертерами, чьи IgM-антитела были отрицательными на ранней стадии МП-инфекции20,21). Таким образом, краткосрочные парные серологические тесты IgM могут быть обязательными для ранней и окончательной диагностики у пациентов с тяжелой пневмонией2,21).
В последнее время для раннего выявления инфекции MP применяется ПЦР. ПЦР является привлекательным альтернативным тестом для культуры МП.Было использовано несколько генов-мишеней, включая ген P1 и ген 16S рРНК37). Результаты исследований ПЦР показали различную чувствительность и специфичность между группами детей и взрослых по сравнению с серологическими результатами38,39). На результаты ПЦР могут влиять материалы, полученные из разных отделов дыхательных путей, стадия заболевания и различные технические ошибки. В наших исследованиях уровень обнаружения ПЦР-тестов во время эпидемии с 2006 по 2007 год составлял от 12 до 30%21,40), но во время эпидемии 2011 года он был менее 5%.Неизвестно, плохо ли штаммы MRMP колонизируются в верхних дыхательных путях по сравнению с другими штаммами. Кроме того, МП может длительное время оставаться в дыхательных путях бессимптомно, особенно у детей младшего возраста после первичного инфицирования41). Таким образом, одного ПЦР-исследования недостаточно для окончательного диагноза инфекции МП. Использование комбинации серологических анализов и ПЦР может быть идеальным методом диагностики инфекции МП.
На результаты ПЦР могут влиять материалы, полученные из разных отделов дыхательных путей, стадия заболевания и различные технические ошибки. В наших исследованиях уровень обнаружения ПЦР-тестов во время эпидемии с 2006 по 2007 год составлял от 12 до 30%21,40), но во время эпидемии 2011 года он был менее 5%.Неизвестно, плохо ли штаммы MRMP колонизируются в верхних дыхательных путях по сравнению с другими штаммами. Кроме того, МП может длительное время оставаться в дыхательных путях бессимптомно, особенно у детей младшего возраста после первичного инфицирования41). Таким образом, одного ПЦР-исследования недостаточно для окончательного диагноза инфекции МП. Использование комбинации серологических анализов и ПЦР может быть идеальным методом диагностики инфекции МП.
Лечение
МП инфекция обычно протекает в легкой форме и проходит самостоятельно, не требуя специального лечения.Поскольку МП не имеет клеточной стенки, для лечения МП пневмонии используются антибиотики, такие как макролиды, тетрациклины и хинолоны./ST18/Untitled-1.gif) Для детей используются только макролиды (эритромицин, кларитромицин, рокситромицин и азитромицин) из-за потенциальных побочных эффектов альтернативных препаратов (тетрациклин и фторхинолоны). Хотя в более ранних исследованиях сообщалось, что антибиотикотерапия у молодых взрослых пациентов вызывала более быстрое разрешение лихорадки и кашля52, 43), эта терапия не могла предотвратить прогрессирование тяжелой пневмонии у некоторых пациентов, а также связанные с ней внелегочные заболевания.Пациенты, инфицированные штаммами MRMP, имеют длительную лихорадку; однако в целом прогрессирования заболевания при лечении макролидами не наблюдалось31,32). Эти данные свидетельствуют о том, что при инфекции МП вещества, вызывающие лихорадку, и вещества, вызывающие пневмонию, могут различаться in vivo . Более того, эффекты лечения антибиотиками МП пневмонии у детей до сих пор остаются спорными44).
Для детей используются только макролиды (эритромицин, кларитромицин, рокситромицин и азитромицин) из-за потенциальных побочных эффектов альтернативных препаратов (тетрациклин и фторхинолоны). Хотя в более ранних исследованиях сообщалось, что антибиотикотерапия у молодых взрослых пациентов вызывала более быстрое разрешение лихорадки и кашля52, 43), эта терапия не могла предотвратить прогрессирование тяжелой пневмонии у некоторых пациентов, а также связанные с ней внелегочные заболевания.Пациенты, инфицированные штаммами MRMP, имеют длительную лихорадку; однако в целом прогрессирования заболевания при лечении макролидами не наблюдалось31,32). Эти данные свидетельствуют о том, что при инфекции МП вещества, вызывающие лихорадку, и вещества, вызывающие пневмонию, могут различаться in vivo . Более того, эффекты лечения антибиотиками МП пневмонии у детей до сих пор остаются спорными44).
Некоторые исследователи сообщают, что смена антибиотиков показала хорошие результаты у пациентов, инфицированных MRMP45,46). Однако другие сообщают, что у пациентов, получавших правильное лечение антибиотиками, наблюдалась прогрессирующая пневмония47,48). Многие исследователи сообщают об эффективности дополнительных кортикостероидов у детей и взрослых, которые не реагировали на антибиотики и у которых наблюдалось прогрессирование заболевания, в том числе с MRMP, особенно у пациентов с тяжелой MP пневмонией20,47-51). Кроме того, в экспериментальных исследованиях также сообщалось о благотворном влиянии кортикостероидов на инфекции MP52,53). Ранее мы сообщали, что использование иммуномодуляторов (преднизолона) у пациентов с невосприимчивой к антибиотикам МП пневмонией было эффективным для улучшения клинических и рентгенологических результатов20,21).Во время этой эпидемии 2011 г. мы использовали преднизолон (1 мг/кг) на ранней стадии вместе с макролидом (хларитромицином) или/и немакролидным антибиотиком (амоксициллин/клавуланат или цефуроксим) у пациентов с МП пневмонией, у которых сохранялась лихорадка в течение >48 часов после допуск.
Однако другие сообщают, что у пациентов, получавших правильное лечение антибиотиками, наблюдалась прогрессирующая пневмония47,48). Многие исследователи сообщают об эффективности дополнительных кортикостероидов у детей и взрослых, которые не реагировали на антибиотики и у которых наблюдалось прогрессирование заболевания, в том числе с MRMP, особенно у пациентов с тяжелой MP пневмонией20,47-51). Кроме того, в экспериментальных исследованиях также сообщалось о благотворном влиянии кортикостероидов на инфекции MP52,53). Ранее мы сообщали, что использование иммуномодуляторов (преднизолона) у пациентов с невосприимчивой к антибиотикам МП пневмонией было эффективным для улучшения клинических и рентгенологических результатов20,21).Во время этой эпидемии 2011 г. мы использовали преднизолон (1 мг/кг) на ранней стадии вместе с макролидом (хларитромицином) или/и немакролидным антибиотиком (амоксициллин/клавуланат или цефуроксим) у пациентов с МП пневмонией, у которых сохранялась лихорадка в течение >48 часов после допуск. У большинства пациентов лихорадка снижалась без прогрессирования заболевания в течение 24–48 часов, даже у тех, кто получал только немакролидный антибиотик. Небольшая группа пациентов, не ответивших на эту терапию, получала метилпреднизон внутривенно (10 мг/кг в течение 2–3 дней, постепенное снижение дозы в течение недели) или внутривенно Ig (1 г/кг/день, 1–2 дозы), и все состояние пациентов улучшилось клинически и рентгенологически в течение нескольких дней без побочных эффектов (неопубликованное наблюдение).Эти данные могут еще раз подтвердить представление об иммуноопосредованном патогенезе пневмонии при МП-инфекции2). Тем не менее необходимы дальнейшие контролируемые клинические исследования кортикостероидов и антибиотиков-кандидатов (хинолонов и тетрациклинов) у детей с MRMP-инфекцией.
У большинства пациентов лихорадка снижалась без прогрессирования заболевания в течение 24–48 часов, даже у тех, кто получал только немакролидный антибиотик. Небольшая группа пациентов, не ответивших на эту терапию, получала метилпреднизон внутривенно (10 мг/кг в течение 2–3 дней, постепенное снижение дозы в течение недели) или внутривенно Ig (1 г/кг/день, 1–2 дозы), и все состояние пациентов улучшилось клинически и рентгенологически в течение нескольких дней без побочных эффектов (неопубликованное наблюдение).Эти данные могут еще раз подтвердить представление об иммуноопосредованном патогенезе пневмонии при МП-инфекции2). Тем не менее необходимы дальнейшие контролируемые клинические исследования кортикостероидов и антибиотиков-кандидатов (хинолонов и тетрациклинов) у детей с MRMP-инфекцией.
Ссылки
1. Аткинсон Т.П., Балиш М.Ф., Уэйтс К.Б. Эпидемиология, клиника, патогенез и лабораторная диагностика микоплазменной пневмонии. FEMS Microbiol Rev. 2008; 32:956–973.[PubMed] [Google Scholar]2. Ли КЙ. Детские респираторные инфекции Mycoplasma pneumoniae. Expert Rev Anti Infect Ther. 2008; 6: 509–521. [PubMed] [Google Scholar]4. Денни Ф.В., Клайд В.А., младший, Глезен В.П. Заболевание Mycoplasma pneumoniae: клинический спектр, патофизиология, эпидемиология и контроль. J заразить дис. 1971; 123: 74–92. [PubMed] [Google Scholar]5. Shimizu T, Kida Y, Kuwano K. Цитоадгезивно-зависимая индукция воспалительных реакций Mycoplasma pneumoniae. Иммунология. 2011; 133:51–61. [Бесплатная статья PMC] [PubMed] [Google Scholar]6.Techasaensiri C, Tagliabue C, Cagle M, Iranpour P, Katz K, Kannan TR, et al. Различия в колонизации, АДФ-рибозилировании и вакуолизации цитотоксина, а также тяжести заболевания легких среди штаммов микоплазмы пневмонии. Am J Respir Crit Care Med. 2010; 182:797–804. [Бесплатная статья PMC] [PubMed] [Google Scholar]7. Чанг Х.И., Джордан Дж.Л., Краузе Д.К. Анализ домена белка Р30 в цитоадгезивной и скользящей подвижности Mycoplasma pneumoniae. J Бактериол. 2011;193:1726–1733.
Ли КЙ. Детские респираторные инфекции Mycoplasma pneumoniae. Expert Rev Anti Infect Ther. 2008; 6: 509–521. [PubMed] [Google Scholar]4. Денни Ф.В., Клайд В.А., младший, Глезен В.П. Заболевание Mycoplasma pneumoniae: клинический спектр, патофизиология, эпидемиология и контроль. J заразить дис. 1971; 123: 74–92. [PubMed] [Google Scholar]5. Shimizu T, Kida Y, Kuwano K. Цитоадгезивно-зависимая индукция воспалительных реакций Mycoplasma pneumoniae. Иммунология. 2011; 133:51–61. [Бесплатная статья PMC] [PubMed] [Google Scholar]6.Techasaensiri C, Tagliabue C, Cagle M, Iranpour P, Katz K, Kannan TR, et al. Различия в колонизации, АДФ-рибозилировании и вакуолизации цитотоксина, а также тяжести заболевания легких среди штаммов микоплазмы пневмонии. Am J Respir Crit Care Med. 2010; 182:797–804. [Бесплатная статья PMC] [PubMed] [Google Scholar]7. Чанг Х.И., Джордан Дж.Л., Краузе Д.К. Анализ домена белка Р30 в цитоадгезивной и скользящей подвижности Mycoplasma pneumoniae. J Бактериол. 2011;193:1726–1733. [Бесплатная статья PMC] [PubMed] [Google Scholar]8.Роллинз С., Колби Т., Клейтон Ф. Открытая биопсия легкого при пневмонии, вызванной Mycoplasma pneumoniae. Arch Pathol Lab Med. 1986; 110:34–41. [PubMed] [Google Scholar]9. Вуори-Холопайнен Э., Сало Э., Саксен Х., Хедман К., Хююпия Т., Лахденпера Р. и др. Этиологическая диагностика детской пневмонии с использованием трансторакальной игольной аспирации и современных микробиологических методов. Клин Инфекция Дис. 2002; 34: 583–590. [PubMed] [Google Scholar] 11. Кумар Х., Каваи Т., Акира С. Распознавание патогенов врожденной иммунной системой. Int Rev Immunol.2011;30:16–34. [PubMed] [Google Scholar] 12. Mühlradt PF, Kiess M, Meyer H, Süssmuth R, Jung G. Выделение, выяснение структуры и синтез липопептида, стимулирующего макрофаги, из Mycoplasma fermentans, действующего при пикомолярной концентрации. J Эксперт Мед. 1997; 185:1951–1958. [Бесплатная статья PMC] [PubMed] [Google Scholar]14. Нарита М., Танака Х., Ямада С., Абэ С., Арига Т., Сакияма Ю.
[Бесплатная статья PMC] [PubMed] [Google Scholar]8.Роллинз С., Колби Т., Клейтон Ф. Открытая биопсия легкого при пневмонии, вызванной Mycoplasma pneumoniae. Arch Pathol Lab Med. 1986; 110:34–41. [PubMed] [Google Scholar]9. Вуори-Холопайнен Э., Сало Э., Саксен Х., Хедман К., Хююпия Т., Лахденпера Р. и др. Этиологическая диагностика детской пневмонии с использованием трансторакальной игольной аспирации и современных микробиологических методов. Клин Инфекция Дис. 2002; 34: 583–590. [PubMed] [Google Scholar] 11. Кумар Х., Каваи Т., Акира С. Распознавание патогенов врожденной иммунной системой. Int Rev Immunol.2011;30:16–34. [PubMed] [Google Scholar] 12. Mühlradt PF, Kiess M, Meyer H, Süssmuth R, Jung G. Выделение, выяснение структуры и синтез липопептида, стимулирующего макрофаги, из Mycoplasma fermentans, действующего при пикомолярной концентрации. J Эксперт Мед. 1997; 185:1951–1958. [Бесплатная статья PMC] [PubMed] [Google Scholar]14. Нарита М., Танака Х., Ямада С., Абэ С., Арига Т., Сакияма Ю.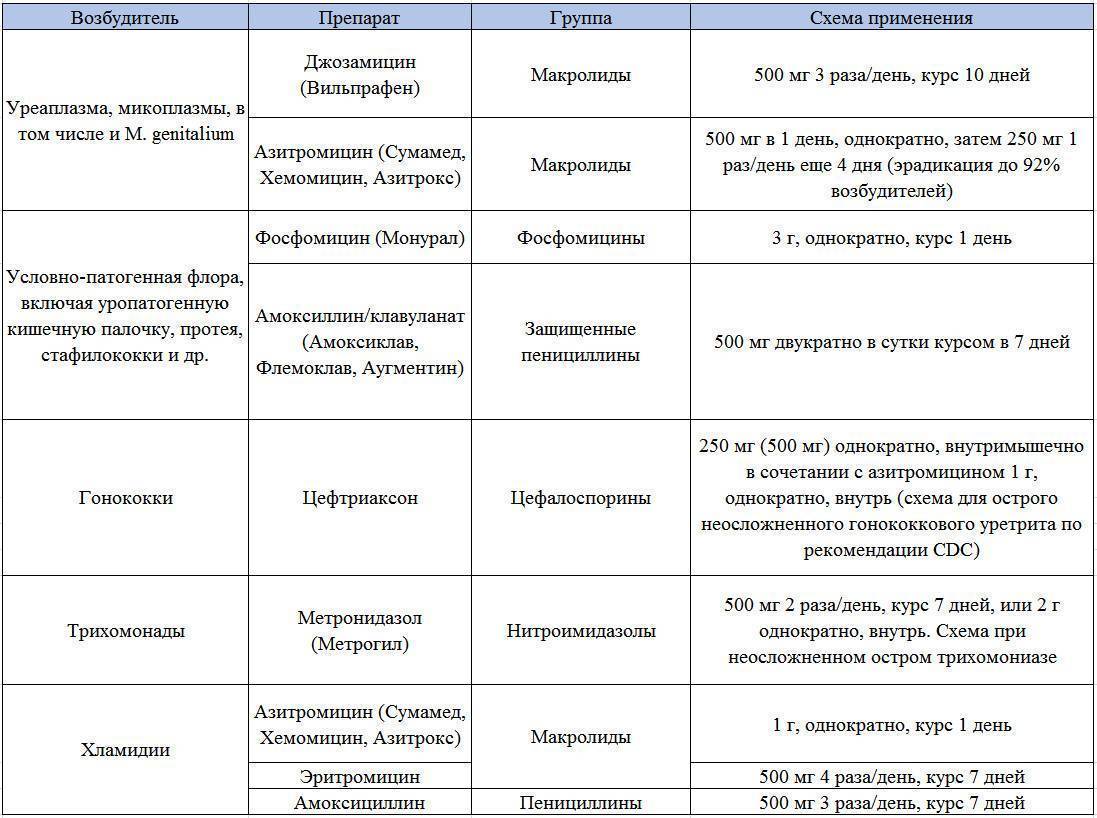 Значительная роль интерлейкина-8 в патогенезе легочных заболеваний, вызванных инфекцией Mycoplasma pneumoniae. Клин Диагн Лаб Иммунол.2001; 8: 1028–1030. [Бесплатная статья PMC] [PubMed] [Google Scholar]15. Харди Р.Д., Джафри Х.С., Олсен К., Вордеманн М., Хэтфилд Дж., Роджерс Б.Б. и др. Повышенные уровни цитокинов и хемокинов и длительное сопротивление легочному воздушному потоку в мышиной модели пневмонии Mycoplasma pneumoniae: микробиологический, гистологический, иммунологический и респираторный плетизмографический профиль. Заразить иммун. 2001; 69: 3869–3876. [Бесплатная статья PMC] [PubMed] [Google Scholar]16. Yang J, Hooper WC, Phillips DJ, Talkington DF. Цитокины при инфекциях Mycoplasma pneumoniae.Цитокиновый фактор роста, ред. 2004; 15:157–168. [PubMed] [Google Scholar] 17. Денни Ф.В., Тейлор-Робинсон Д., Эллисон А.С. Роль тимусзависимого иммунитета при инфицировании мышей Mycoplasma pulmonis. J Med Microbiol. 1972; 5: 327–336. [PubMed] [Google Scholar] 18. Танака Х., Хонма С., Абэ С.
Значительная роль интерлейкина-8 в патогенезе легочных заболеваний, вызванных инфекцией Mycoplasma pneumoniae. Клин Диагн Лаб Иммунол.2001; 8: 1028–1030. [Бесплатная статья PMC] [PubMed] [Google Scholar]15. Харди Р.Д., Джафри Х.С., Олсен К., Вордеманн М., Хэтфилд Дж., Роджерс Б.Б. и др. Повышенные уровни цитокинов и хемокинов и длительное сопротивление легочному воздушному потоку в мышиной модели пневмонии Mycoplasma pneumoniae: микробиологический, гистологический, иммунологический и респираторный плетизмографический профиль. Заразить иммун. 2001; 69: 3869–3876. [Бесплатная статья PMC] [PubMed] [Google Scholar]16. Yang J, Hooper WC, Phillips DJ, Talkington DF. Цитокины при инфекциях Mycoplasma pneumoniae.Цитокиновый фактор роста, ред. 2004; 15:157–168. [PubMed] [Google Scholar] 17. Денни Ф.В., Тейлор-Робинсон Д., Эллисон А.С. Роль тимусзависимого иммунитета при инфицировании мышей Mycoplasma pulmonis. J Med Microbiol. 1972; 5: 327–336. [PubMed] [Google Scholar] 18. Танака Х., Хонма С., Абэ С. , Тамура Х. Влияние интерлейкина-2 и циклоспорина А на патологические особенности микоплазменной пневмонии. Am J Respir Crit Care Med. 1996; 154 (6 ч. 1): 1908–1912. [PubMed] [Google Scholar] 19. Ли К.И., Рим Д.В., Канг Д.Х. Гиперактивные иммунные клетки (Т-клетки) могут быть ответственны за острое повреждение легких при инфекциях, вызванных вирусом гриппа: в тяжелых случаях требуется раннее введение иммуномодуляторов.Мед Гипотезы. 2011;76:64–69. [Бесплатная статья PMC] [PubMed] [Google Scholar]20. Ли К.И., Ли Х.С., Хонг Дж.Х., Ли М.Х., Ли Дж.С., Бургнер Д. и др. Роль лечения преднизолоном при тяжелой микоплазменной пневмонии у детей. Педиатр Пульмонол. 2006; 41: 263–268. [PubMed] [Google Scholar] 21. Юн Й.С., Ли К.И., Хван Дж.И., Рим Дж.В., Кан Дж.Х., Ли Дж.С. и др. Различие клинических признаков микоплазменной пневмонии у детей. БМС Педиатр. 2010;10:48. [Бесплатная статья PMC] [PubMed] [Google Scholar]22.Kim JW, Seo HK, Yoo EG, Park SJ, Yoon SH, Jung HY и др. Mycoplasma pneumoniae pneumoniae у корейских детей с 1979 по 2006 год — метаанализ.
, Тамура Х. Влияние интерлейкина-2 и циклоспорина А на патологические особенности микоплазменной пневмонии. Am J Respir Crit Care Med. 1996; 154 (6 ч. 1): 1908–1912. [PubMed] [Google Scholar] 19. Ли К.И., Рим Д.В., Канг Д.Х. Гиперактивные иммунные клетки (Т-клетки) могут быть ответственны за острое повреждение легких при инфекциях, вызванных вирусом гриппа: в тяжелых случаях требуется раннее введение иммуномодуляторов.Мед Гипотезы. 2011;76:64–69. [Бесплатная статья PMC] [PubMed] [Google Scholar]20. Ли К.И., Ли Х.С., Хонг Дж.Х., Ли М.Х., Ли Дж.С., Бургнер Д. и др. Роль лечения преднизолоном при тяжелой микоплазменной пневмонии у детей. Педиатр Пульмонол. 2006; 41: 263–268. [PubMed] [Google Scholar] 21. Юн Й.С., Ли К.И., Хван Дж.И., Рим Дж.В., Кан Дж.Х., Ли Дж.С. и др. Различие клинических признаков микоплазменной пневмонии у детей. БМС Педиатр. 2010;10:48. [Бесплатная статья PMC] [PubMed] [Google Scholar]22.Kim JW, Seo HK, Yoo EG, Park SJ, Yoon SH, Jung HY и др. Mycoplasma pneumoniae pneumoniae у корейских детей с 1979 по 2006 год — метаанализ. Корейский J Педиатр. 2009;52:315–323. [Google Академия] 23. Ли С.Х., Но С.М., Ли К.И., Ли Х.С., Хонг Д.Х., Ли М.Х. и др. Клинико-эпидемиологическое исследование пневмонии, вызванной Mycoplasma pneumoniae (1993–2003 гг.) Korean J Pediatr. 2005; 48: 154–157. [Google Академия] 24. Бруннер Х., Прескотт Б., Гринберг Х., Джеймс В.Д., Хорсвуд Р.Л., Чанок Р.М. Неожиданно высокая частота антител к Mycoplasma pneumoniae в сыворотке крови человека, измеренная с помощью чувствительных методов.J заразить дис. 1977; 135: 524–530. [PubMed] [Google Scholar] 25. Сасаки Т., Кенри Т., Окадзаки Н., Исеки М., Ямасита Р., Шинтани М. и др. Эпидемиологическое исследование инфекций Mycoplasma pneumoniae в Японии на основе полиморфизма длины ПЦР-рестрикционных фрагментов гена цитадгезина P1. Дж. Клин Микробиол. 1996; 34: 447–449. [Бесплатная статья PMC] [PubMed] [Google Scholar]26. Morozumi M, Takahashi T, Ubukata K. Устойчивая к макролидам Mycoplasma pneumoniae: характеристики изолятов и клинические аспекты внебольничной пневмонии.
Корейский J Педиатр. 2009;52:315–323. [Google Академия] 23. Ли С.Х., Но С.М., Ли К.И., Ли Х.С., Хонг Д.Х., Ли М.Х. и др. Клинико-эпидемиологическое исследование пневмонии, вызванной Mycoplasma pneumoniae (1993–2003 гг.) Korean J Pediatr. 2005; 48: 154–157. [Google Академия] 24. Бруннер Х., Прескотт Б., Гринберг Х., Джеймс В.Д., Хорсвуд Р.Л., Чанок Р.М. Неожиданно высокая частота антител к Mycoplasma pneumoniae в сыворотке крови человека, измеренная с помощью чувствительных методов.J заразить дис. 1977; 135: 524–530. [PubMed] [Google Scholar] 25. Сасаки Т., Кенри Т., Окадзаки Н., Исеки М., Ямасита Р., Шинтани М. и др. Эпидемиологическое исследование инфекций Mycoplasma pneumoniae в Японии на основе полиморфизма длины ПЦР-рестрикционных фрагментов гена цитадгезина P1. Дж. Клин Микробиол. 1996; 34: 447–449. [Бесплатная статья PMC] [PubMed] [Google Scholar]26. Morozumi M, Takahashi T, Ubukata K. Устойчивая к макролидам Mycoplasma pneumoniae: характеристики изолятов и клинические аспекты внебольничной пневмонии. J заразить Chemother. 2010; 16:78–86. [PubMed] [Google Scholar] 27. Liu Y, Ye X, Zhang H, Xu X, Li W, Zhu D и др. Характеристика устойчивости к макролидам Mycoplasma pneumoniae, выделенной от детей в Шанхае, Китай. Диагностика Microbiol Infect Dis. 2010;67:355–358. [PubMed] [Google Scholar] 28. Думке Р., фон Баум Х., Люк П.С., Якобс Э. Возникновение устойчивых к макролидам штаммов Mycoplasma pneumoniae в Германии. Клин Микробиол Инфект. 2010;16:613–616. [PubMed] [Google Scholar] 29. О CE, Choi EH, Lee HJ.Выявление генетических мутаций, связанных с устойчивостью Mycoplasma pneumoniae к макролидам. Корейский J Педиатр. 2010;53:178–183. [Google Академия] 30. Хонг К.Б., Ли С.И., Чой Э.Х., Ли Дж., Ан Ю.М., Ли Х.Дж. Распространенность генетических мутаций, связанных с устойчивостью Mycoplasma pneumoniae к макролидам в Корее; Программа и тезисы осеннего собрания Корейского общества детских инфекционных заболеваний 2011 г.; 2011 12 ноября; Сеул: Корейское общество детских инфекционных заболеваний; 2011.
J заразить Chemother. 2010; 16:78–86. [PubMed] [Google Scholar] 27. Liu Y, Ye X, Zhang H, Xu X, Li W, Zhu D и др. Характеристика устойчивости к макролидам Mycoplasma pneumoniae, выделенной от детей в Шанхае, Китай. Диагностика Microbiol Infect Dis. 2010;67:355–358. [PubMed] [Google Scholar] 28. Думке Р., фон Баум Х., Люк П.С., Якобс Э. Возникновение устойчивых к макролидам штаммов Mycoplasma pneumoniae в Германии. Клин Микробиол Инфект. 2010;16:613–616. [PubMed] [Google Scholar] 29. О CE, Choi EH, Lee HJ.Выявление генетических мутаций, связанных с устойчивостью Mycoplasma pneumoniae к макролидам. Корейский J Педиатр. 2010;53:178–183. [Google Академия] 30. Хонг К.Б., Ли С.И., Чой Э.Х., Ли Дж., Ан Ю.М., Ли Х.Дж. Распространенность генетических мутаций, связанных с устойчивостью Mycoplasma pneumoniae к макролидам в Корее; Программа и тезисы осеннего собрания Корейского общества детских инфекционных заболеваний 2011 г.; 2011 12 ноября; Сеул: Корейское общество детских инфекционных заболеваний; 2011. 7 стр. [Google Scholar]31.Судзуки С., Ямадзаки Т., Нарита М., Окадзаки Н., Судзуки И., Андох Т. и др. Клиническая оценка устойчивости к макролидам Mycoplasma pneumoniae. Противомикробные агенты Chemother. 2006; 50: 709–712. [Бесплатная статья PMC] [PubMed] [Google Scholar]32. Мацубара К., Морозуми М., Окада Т., Мацусима Т., Комияма О., Сёдзи М. и др. Сравнительное клиническое исследование чувствительных к макролидам и резистентных к макролидам инфекций Mycoplasma pneumoniae у педиатрических пациентов. J заразить Chemother. 2009; 15: 380–383. [PubMed] [Google Scholar] 33.Нарита М. Два неожиданных явления в инфекции Mycoplasma pneumoniae, устойчивой к макролидам, в Японии и уникальные биологические характеристики Mycoplasma pneumoniae. J заразить Chemother. 2011; 17: 735–736. [Бесплатная статья PMC] [PubMed] [Google Scholar]34. Сазерленд Э.Р., Мартин Р.Дж. Бронхиальная астма и атипичная бактериальная инфекция. Грудь. 2007; 132:1962–1966. [PubMed] [Google Scholar] 35. Нарита М. Патогенез внелегочных проявлений инфекции Mycoplasma pneumoniae с особым упором на пневмонию.
7 стр. [Google Scholar]31.Судзуки С., Ямадзаки Т., Нарита М., Окадзаки Н., Судзуки И., Андох Т. и др. Клиническая оценка устойчивости к макролидам Mycoplasma pneumoniae. Противомикробные агенты Chemother. 2006; 50: 709–712. [Бесплатная статья PMC] [PubMed] [Google Scholar]32. Мацубара К., Морозуми М., Окада Т., Мацусима Т., Комияма О., Сёдзи М. и др. Сравнительное клиническое исследование чувствительных к макролидам и резистентных к макролидам инфекций Mycoplasma pneumoniae у педиатрических пациентов. J заразить Chemother. 2009; 15: 380–383. [PubMed] [Google Scholar] 33.Нарита М. Два неожиданных явления в инфекции Mycoplasma pneumoniae, устойчивой к макролидам, в Японии и уникальные биологические характеристики Mycoplasma pneumoniae. J заразить Chemother. 2011; 17: 735–736. [Бесплатная статья PMC] [PubMed] [Google Scholar]34. Сазерленд Э.Р., Мартин Р.Дж. Бронхиальная астма и атипичная бактериальная инфекция. Грудь. 2007; 132:1962–1966. [PubMed] [Google Scholar] 35. Нарита М. Патогенез внелегочных проявлений инфекции Mycoplasma pneumoniae с особым упором на пневмонию. J заразить Chemother. 2010;16:162–169. [PubMed] [Google Scholar] 36. Beersma MF, Dirven K, van Dam AP, Templeton KE, Claas EC, Goossens H. Оценка 12 коммерческих тестов и теста фиксации комплемента на антитела иммуноглобулина G (IgG) и IgM, специфичные для Mycoplasma pneumoniae, с использованием ПЦР в качестве «золотого» стандарт». Дж. Клин Микробиол. 2005;43:2277–2285. [Бесплатная статья PMC] [PubMed] [Google Scholar]37. Loens K, Goossens H, Ieven M. Острая респираторная инфекция, вызванная Mycoplasma pneumoniae: текущее состояние методов диагностики.Eur J Clin Microbiol Infect Dis. 2010;29:1055–1069. [Бесплатная статья PMC] [PubMed] [Google Scholar]38. Мартинес М.А., Руис М., Зунино Э., Лучсингер В., Авенданьо Л.Ф. Выявление Mycoplasma pneumoniae при внебольничной пневмонии у взрослых с помощью ПЦР и серологии. J Med Microbiol. 2008; 57 (часть 12): 1491–1495. [PubMed] [Google Scholar] 39. Zhang L, Zong ZY, Liu YB, Ye H, Lv XJ. ПЦР в сравнении с серологией для диагностики инфекции Mycoplasma pneumoniae: систематический обзор и метаанализ.
J заразить Chemother. 2010;16:162–169. [PubMed] [Google Scholar] 36. Beersma MF, Dirven K, van Dam AP, Templeton KE, Claas EC, Goossens H. Оценка 12 коммерческих тестов и теста фиксации комплемента на антитела иммуноглобулина G (IgG) и IgM, специфичные для Mycoplasma pneumoniae, с использованием ПЦР в качестве «золотого» стандарт». Дж. Клин Микробиол. 2005;43:2277–2285. [Бесплатная статья PMC] [PubMed] [Google Scholar]37. Loens K, Goossens H, Ieven M. Острая респираторная инфекция, вызванная Mycoplasma pneumoniae: текущее состояние методов диагностики.Eur J Clin Microbiol Infect Dis. 2010;29:1055–1069. [Бесплатная статья PMC] [PubMed] [Google Scholar]38. Мартинес М.А., Руис М., Зунино Э., Лучсингер В., Авенданьо Л.Ф. Выявление Mycoplasma pneumoniae при внебольничной пневмонии у взрослых с помощью ПЦР и серологии. J Med Microbiol. 2008; 57 (часть 12): 1491–1495. [PubMed] [Google Scholar] 39. Zhang L, Zong ZY, Liu YB, Ye H, Lv XJ. ПЦР в сравнении с серологией для диагностики инфекции Mycoplasma pneumoniae: систематический обзор и метаанализ. Индийская J Med Res. 2011; 134: 270–280.[Бесплатная статья PMC] [PubMed] [Google Scholar]40. Юн Й.С., Ли К.И., Хван Дж.И., Йим Дж.В., Кан Дж.Х., Ли Дж.С. Сравнение методов диагностики и изменений подклассов IgG у детей с микоплазменной пневмонией. Pediatr Allergy Respir Dis. 2009; 19: 137–145. [Google Академия] 41. Dorigo-Zetsma JW, Wilbrink B, van der Nat H, Bartelds AI, Heijnen ML, Dankert J. Результаты молекулярного выявления Mycoplasma pneumoniae среди больных острой респираторной инфекцией и в их бытовых контактах выявляют детей как резервуары человека.J заразить дис. 2001; 183: 675–678. [PubMed] [Google Scholar]42. Shames JM, George RB, Holliday WB, Rasch JR, Mogabgab WJ. Сравнение антибиотиков при лечении микоплазменной пневмонии. Arch Intern Med. 1970; 125: 680–684. [PubMed] [Google Scholar]43. McCracken GH., Jr Текущее состояние лечения антибиотиками инфекций Mycoplasma pneumoniae. Педиатр Infect Dis. 1986; 5: 167–171. [PubMed] [Google Scholar]44. Малхолланд С., Гавранич Д.Б., Чанг А.
Индийская J Med Res. 2011; 134: 270–280.[Бесплатная статья PMC] [PubMed] [Google Scholar]40. Юн Й.С., Ли К.И., Хван Дж.И., Йим Дж.В., Кан Дж.Х., Ли Дж.С. Сравнение методов диагностики и изменений подклассов IgG у детей с микоплазменной пневмонией. Pediatr Allergy Respir Dis. 2009; 19: 137–145. [Google Академия] 41. Dorigo-Zetsma JW, Wilbrink B, van der Nat H, Bartelds AI, Heijnen ML, Dankert J. Результаты молекулярного выявления Mycoplasma pneumoniae среди больных острой респираторной инфекцией и в их бытовых контактах выявляют детей как резервуары человека.J заразить дис. 2001; 183: 675–678. [PubMed] [Google Scholar]42. Shames JM, George RB, Holliday WB, Rasch JR, Mogabgab WJ. Сравнение антибиотиков при лечении микоплазменной пневмонии. Arch Intern Med. 1970; 125: 680–684. [PubMed] [Google Scholar]43. McCracken GH., Jr Текущее состояние лечения антибиотиками инфекций Mycoplasma pneumoniae. Педиатр Infect Dis. 1986; 5: 167–171. [PubMed] [Google Scholar]44. Малхолланд С., Гавранич Д.Б., Чанг А. Б. Антибиотики при внебольничных инфекциях нижних дыхательных путей, вторичных по отношению к Mycoplasma pneumoniae, у детей.Cochrane Database Syst Rev. 2010;(7):CD004875. [PubMed] [Google Scholar]45. Мияшита Н., Маруяма Т., Кобаяши Т., Кобаяши Х., Тагучи О., Каваи Ю. и др. Внебольничная резистентная к макролидам пневмония Mycoplasma pneumoniae у пациентов старше 18 лет. J заразить Chemother. 2011;17:114–118. [PubMed] [Google Scholar]46. Averbuch D, Hidalgo-Grass C, Moses AE, Engelhard D, Nir-Paz R. Устойчивость к макролидам у Mycoplasma pneumoniae, Израиль, 2010. Emerg Infect Dis. 2011;17:1079–1082. [Бесплатная статья PMC] [PubMed] [Google Scholar]47.Косуги Ю., Кацура Х. Случай молниеносной пневмонии, вызванной Mycoplasma pneumoniae, несмотря на адекватное лечение антибиотиками. Нихон Кокюки Гаккай Дзаси. 2009; 47: 471–475. [PubMed] [Google Scholar]48. Kim DH, Lee KY, Kim MS, Youn YS, Hwang JY, Rhim JW и др. Лечение кортикостероидами братьев и сестер с тяжелой пневмонией, вызванной Mycoplasma pneumoniae.
Б. Антибиотики при внебольничных инфекциях нижних дыхательных путей, вторичных по отношению к Mycoplasma pneumoniae, у детей.Cochrane Database Syst Rev. 2010;(7):CD004875. [PubMed] [Google Scholar]45. Мияшита Н., Маруяма Т., Кобаяши Т., Кобаяши Х., Тагучи О., Каваи Ю. и др. Внебольничная резистентная к макролидам пневмония Mycoplasma pneumoniae у пациентов старше 18 лет. J заразить Chemother. 2011;17:114–118. [PubMed] [Google Scholar]46. Averbuch D, Hidalgo-Grass C, Moses AE, Engelhard D, Nir-Paz R. Устойчивость к макролидам у Mycoplasma pneumoniae, Израиль, 2010. Emerg Infect Dis. 2011;17:1079–1082. [Бесплатная статья PMC] [PubMed] [Google Scholar]47.Косуги Ю., Кацура Х. Случай молниеносной пневмонии, вызванной Mycoplasma pneumoniae, несмотря на адекватное лечение антибиотиками. Нихон Кокюки Гаккай Дзаси. 2009; 47: 471–475. [PubMed] [Google Scholar]48. Kim DH, Lee KY, Kim MS, Youn YS, Hwang JY, Rhim JW и др. Лечение кортикостероидами братьев и сестер с тяжелой пневмонией, вызванной Mycoplasma pneumoniae.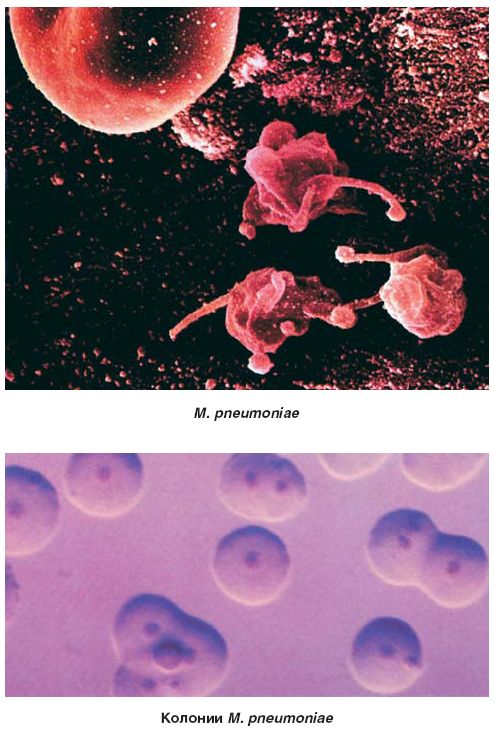 Заразить Чематер. 2009;41:190–195. [Google Академия] 49. Тамура А., Мацубара К., Танака Т., Нигами Х., Юра К., Фукая Т. Импульсная терапия метилпреднизолоном при рефрактерной пневмонии, вызванной Mycoplasma pneumoniae, у детей.J заразить. 2008; 57: 223–228. [Бесплатная статья PMC] [PubMed] [Google Scholar]50. Мияшита Н., Обасе Ю., Оучи К., Кавасаки К., Каваи Ю., Кобаши Ю. и др. Клинические особенности тяжелой микоплазменной пневмонии у взрослых, госпитализированных в отделение интенсивной терапии. J Med Microbiol. 2007; 56 (часть 12): 1625–1629. [PubMed] [Google Scholar]51. Лу А., Ван Л., Чжан С., Чжан М. Комбинированное лечение рефрактерной к Mycoplasma pneumoniae пневмонии у детей ципрофлоксацином и глюкокортикоидом. Педиатр Пульмонол. 2011;46:1093–1097.[PubMed] [Google Scholar]52. Tagliabue C, Salvatore CM, Techasaensiri C, Mejias A, Torres JP, Katz K, et al. Влияние стероидов на фоне терапии макролидами на экспериментальную респираторную инфекцию Mycoplasma pneumoniae. J заразить дис.
Заразить Чематер. 2009;41:190–195. [Google Академия] 49. Тамура А., Мацубара К., Танака Т., Нигами Х., Юра К., Фукая Т. Импульсная терапия метилпреднизолоном при рефрактерной пневмонии, вызванной Mycoplasma pneumoniae, у детей.J заразить. 2008; 57: 223–228. [Бесплатная статья PMC] [PubMed] [Google Scholar]50. Мияшита Н., Обасе Ю., Оучи К., Кавасаки К., Каваи Ю., Кобаши Ю. и др. Клинические особенности тяжелой микоплазменной пневмонии у взрослых, госпитализированных в отделение интенсивной терапии. J Med Microbiol. 2007; 56 (часть 12): 1625–1629. [PubMed] [Google Scholar]51. Лу А., Ван Л., Чжан С., Чжан М. Комбинированное лечение рефрактерной к Mycoplasma pneumoniae пневмонии у детей ципрофлоксацином и глюкокортикоидом. Педиатр Пульмонол. 2011;46:1093–1097.[PubMed] [Google Scholar]52. Tagliabue C, Salvatore CM, Techasaensiri C, Mejias A, Torres JP, Katz K, et al. Влияние стероидов на фоне терапии макролидами на экспериментальную респираторную инфекцию Mycoplasma pneumoniae. J заразить дис. 2008; 198:1180–1188. [Бесплатная статья PMC] [PubMed] [Google Scholar]53. Хирао С., Вада Х., Накагаки К., Сарая Т., Кураи Д., Микура С. и др. Воспаление, вызванное экстрактом Mycoplasma pneumoniae: последствия комбинированного лечения кларитромицином и дексаметазоном.FEMS Immunol Med Microbiol. 2011;62:182–189. [PubMed] [Google Scholar]
2008; 198:1180–1188. [Бесплатная статья PMC] [PubMed] [Google Scholar]53. Хирао С., Вада Х., Накагаки К., Сарая Т., Кураи Д., Микура С. и др. Воспаление, вызванное экстрактом Mycoplasma pneumoniae: последствия комбинированного лечения кларитромицином и дексаметазоном.FEMS Immunol Med Microbiol. 2011;62:182–189. [PubMed] [Google Scholar]Микоплазменная инфекция (ходячая пневмония, атипичная пневмония)
Последняя проверка: октябрь 2011 г.
Что такое микоплазменная инфекция?
Микоплазменная инфекция — респираторное заболевание, вызываемое Mycoplasma pneumoniae, микроскопическим организмом, родственным бактериям.
Кто заражается микоплазмой?
Заболеть может любой, но чаще всего от него страдают дети старшего возраста и молодые люди.
Когда возникают микоплазменные инфекции?
Микоплазменные инфекции возникают спорадически в течение года. Также могут возникать широко распространенные вспышки в сообществе. Микоплазменная инфекция наиболее распространена в конце лета и осенью.
Как распространяется микоплазма?
Микоплазма распространяется при контакте с каплями из носа и горла инфицированных людей, особенно при кашле и чихании. Считается, что передача требует длительного тесного контакта с инфицированным человеком.Распространение в семьях, школах и учреждениях происходит медленно. Заразный период, вероятно, составляет менее 10 дней, а иногда и дольше.
Каковы симптомы микоплазменной инфекции?
Типичные симптомы включают лихорадку, кашель, бронхит, боль в горле, головную боль и усталость. Распространенным результатом микоплазменной инфекции является пневмония (иногда называемая «ходячей пневмонией», поскольку она обычно протекает в легкой форме и редко требует госпитализации). Также могут возникнуть инфекции среднего уха (средний отит).Симптомы могут сохраняться от нескольких дней до более месяца.
Как скоро после воздействия появляются симптомы?
Симптомы обычно проявляются через две-три недели после заражения, но могут длиться от одной до четырех недель.
Как диагностируется микоплазменная инфекция?
Микоплазменная инфекция обычно диагностируется на основании типичных симптомов и рентгенографии органов грудной клетки. Могут быть сделаны анализы крови.
Дает ли перенесенная инфекция микоплазмы иммунитет?
Иммунитет после микоплазменной инфекции возникает, но не пожизненно.Известно, что случаются вторичные инфекции, хотя они могут быть более легкими. Продолжительность иммунитета неизвестна.
Что такое лечение микоплазменной инфекции?
Антибиотики, такие как эритромицин, кларитромицин или азитромицин, являются эффективным средством лечения. Однако, поскольку микоплазменная инфекция обычно проходит сама по себе, лечение антибиотиками легких симптомов не всегда необходимо.
Что можно сделать для предотвращения распространения микоплазмы?
В настоящее время отсутствуют вакцины для профилактики микоплазменной инфекции и отсутствуют надежно эффективные меры борьбы.Как и при любом респираторном заболевании, все люди должны соблюдать гигиену рук и прикрывать нос и рот при кашле или чихании.
Mycoplasma pneumoniae как возбудитель внебольничной пневмонии у детей: особенности клиники и лабораторной диагностики | Italian Journal of Pediatrics
Waites K, Talkington D: Mycoplasma pneumoniae и ее роль в качестве патогена человека. Clin Microbiol Rev. 2004, 17: 697-728. 10.1128/CMR.17.4.697-728.2004.
Центральный пабмед Статья КАС пабмед Google Scholar
Harris M, Clark J, Coote N, Fletcher P, Harden A, McKean M, Thomson A, Комитет по стандартам медицинской помощи Британского торакального общества: рекомендации Британского торакального общества по лечению внебольничной пневмонии у детей: обновление 2011 г. Thorax. 2011, 66: 1-23. 10.1136/thoraxjnl-2011-200598.
Артикул Google Scholar
Loens K, Ursi D, Goossens H, Leven M: Молекулярная диагностика Mycoplasma pneumoniae инфекций дыхательных путей.Дж. Клин Микробиол. 2003, 41: 4915-4923. 10.1128/JCM.41.11.4915-4923.2003.
Центральный пабмед Статья КАС пабмед Google Scholar
Макинтош К. Внебольничная пневмония у детей. N Engl J Med. 2002, 346: 429-437. 10.1056/NEJMra011994.
Артикул пабмед Google Scholar
Davies H, Wang E, Manson D, Babyn P, Shuckett B: Надежность рентгенограммы грудной клетки при диагностике инфекций нижних дыхательных путей у детей раннего возраста.Pediatr Infect Dis J. 1996, 15: 600-604. 10.1097/00006454-199607000-00008.
Артикул КАС пабмед Google Scholar
Варис М.Е., Тойкка П., Сааринен Т., Никкари С., Меурман О., Вайнионпаа Р., Мерцола Дж., Руусканен О.: Диагностика Mycoplasma pneumoniae пневмонии у детей. Дж. Клин Микробиол. 1998, 36: 3155-3159.
Центральный пабмед КАС пабмед Google Scholar
Nadal D, Bossart W, Zucol F, Steiner F, Berger C, Lips U, Altwegg M: Внебольничная пневмония у детей, вызванная Mycoplasma pneumoniae : диагностическая эффективность полувложенной 16S рДНК-ПЦР. Диагностика Microbiol Infect Dis. 2001, 39: 15-19. 10.1016/S0732-8893(00)00216-9.
Артикул КАС пабмед Google Scholar
Puljiz I, Kuzman I, Dakovic-Rode O, Schönwald N, Mise B: Chlamydia pneumoniae и Mycoplasma pneumoniae pneumoniae: сравнение клинических, эпидемиологических характеристик и лабораторных профилей.Эпидемиол инфекции. 2006, 134: 548-555. 10.1017/S0950268805005522.
Центральный пабмед Статья КАС пабмед Google Scholar
Дефилиппи А., Сильвестри М., Такчелла А., Джаккино Р., Мелиоли Г., Ди Марко Э., Чирилло С., Ди Пьетро П., Росси Г.А.: Эпидемиология и клинические особенности инфекции Mycoplasma pneumoniae у детей. Респир Мед. 2008, 2: 1762-1768. 10.1016/j.rmed.2008.06.022.
Артикул Google Scholar
Almasri M, Diza E, Papa A, Eboriadou M, Souliou E: Mycoplasma pneumoniae инфекции дыхательных путей среди греческих детей. Гиппократия. 2011, 15: 147-152.
Центральный пабмед КАС пабмед Google Scholar
Kicinski P, Wisniewska-Ligier M, Wozniakowska-Gesicka T: Пневмония, вызванная Mycoplasma pneumoniae и Chlamydophila pneumoniae у детей — сравнительный анализ клинической картины.Adv Med Sci. 2011, 56: 56-63. 10.2478/в10039-011-0017-з.
Артикул КАС пабмед Google Scholar
Кашьяп Б., Кумар С., Сети Г.Р., Дас Б.К., Сайгал С.Р.: Сравнение ПЦР, культуральных и серологических тестов для диагностики Mycoplasma pneumoniae при внебольничных инфекциях нижних дыхательных путей у детей. Индийская J Med Res. 2008, 128: 134-139.
КАС пабмед Google Scholar
Liu FC, Chen PY, Huang FL, Tsai CR, Lee CY, Wang LC: Быстрая диагностика инфекции Mycoplasma pneumoniae у детей с помощью полимеразной цепной реакции. J Microbiol Immunol Infect. 2007, 40: 507-512.
ПабМед Google Scholar
Samransamruajkit R, Jitchaiwat S, Wachirapaes W, Deerojanawong J, Sritippayawan S, Prapphal N: Распространенность Mycoplasma и Chlamydia pneumonia при тяжелой внебольничной пневмонии среди госпитализированных детей в Таиланде.Jpn J Infect Dis. 2008, 61: 36-39.
ПабМед Google Scholar
Liu CL, Wang GQ, Zhang B, Xu H, Hu LP, He XF, Wang JH, Zhang JH, Liu XY, Wei M, Liu ZY: Mycoplasma pneumoniae пневмония у госпитализированных детей с диагнозом острого стадии парными сыворотками. Чин Мед Дж. 2010, 123: 3444-3450.
ПабМед Google Scholar
Сидал М., Килич А., Унувар Э., Огуз Ф., Онел М., Агацифидан А., Айдын Д., Коксалан К., Бека Х. Частота инфекций Chlamydia pneumoniae и Mycoplasma pneumoniae у детей.Джей Троп Педиат. 2007, 53: 225-231. 10.1093/тропей/fmm003.
Артикул Google Scholar
Esposito S, Blasi F, Bellini F, Allergra L, Principi N и исследовательская группа Mogwil: Mycoplasma pneumoniae и Chlamydia pneumoniae инфекции у детей с пневмонией. Евр Респир Дж. 2001, 17: 241-245. 10.1183/0
36.01.17202410.
Артикул КАС пабмед Google Scholar
Туати А., Перейр С., Бузири А., Ачур В., Халди А., Бен Джабалла Н., Бебеар С., Бен Хассен А. Распространенность инфекций дыхательных путей, ассоциированных с Mycoplasma pneumoniae , у госпитализированных детей: результаты 4-летнего проспективного исследования в Тунисе. Диагностика Microbiol Infect Dis. 2010, 68: 103-109. 10.1016/j.diagmicrobio.2010.05.010.
Артикул пабмед Google Scholar
Hsieh SC, Kuo YT, Chern MS, Chen CY, Chan WP, Yu C: Mycoplasma pneumonia : клинические и рентгенологические признаки у 39 детей.Педиатр Междунар. 2007, 49: 363-367. 10.1111/j.1442-200X.2007.02363.x.
Артикул пабмед Google Scholar
Vervloet LA, Camargos PA, Soares DR, Oliveira GA, Oliveira JN: Клинические, рентгенографические и гематологические характеристики пневмонии Mycoplasma pneumoniae . J Педиатр. 2010, 86: 480-487. 10.1590/S0021-75572010000600006.
Артикул Google Scholar
Эспозито С., Блази Ф., Арозио С., Фиораванти Л., Фагетти Л., Дрогетти Р., Тарсия П., Аллегра Л., Принципи Н.: Важность острых инфекций Mycoplasma pneumoniae и Chlamydia pneumoniae у детей с хрипами. Eur Respir J. 2000, 16: 1142-1146. 10.1034/j.1399-3003.2000.16f21.x.
Артикул КАС пабмед Google Scholar
Othman N, Isaacs D, Kesson A: Mycoplasma pneumoniae инфекций у австралийских детей.J Педиатр Здоровье ребенка. 2005, 41: 671-676. 10.1111/j.1440-1754.2005.00757.х.
Артикул КАС пабмед Google Scholar
Уэйтс К.Б., Такер В.Л., Токингтон Д.Ф.: Значение посева и серологии для выявления инфекций Mycoplasma pneumoniae в клинической лаборатории в эпоху молекулярной диагностики. Информационный бюллетень Clin Microbiol. 2001, 23: 123-129. 10.1016/S0196-4399(01)89042-5.
Артикул Google Scholar
Chang HY, Chang LY, Shao PL, Lee PI, Chen JM, Lee CY, Lu CY, Huang LM: Сравнение полимеразной цепной реакции в реальном времени и серологических тестов для подтверждения инфекции Mycoplasma pneumoniae у детей с клиническим диагнозом атипичной пневмонии. J Microbiol Immunol Infect. 2014, 47: 137-144. 10.1016/j.jmii.2013.03.015.
Артикул КАС пабмед Google Scholar
Аткинсон Т.П., Балиш М.Ф., Уэйтс К.Б.: Эпидемиология, клинические проявления, патогенез и лабораторное выявление инфекций Mycoplasma pneumoniae .FEMS Microbiol Rev. 2008, 32: 956-973. 10.1111/j.1574-6976.2008.00129.х.
Артикул КАС пабмед Google Scholar
Морозуми М., Накаяма Э., Ивата С., Аоки Й., Хасэгава К., Кобаяси Р., Тиба Н., Тадзима Т., Убуката К.: Одновременное выявление возбудителей в клинических образцах пациентов с внебольничной пневмонией методом реального временная ПЦР с патоген-специфическими молекулярными зондами-маяками. Дж. Клин Микробиол. 2006, 44: 1440-1446.10.1128/JCM.44.4.1440-1446.2006.
Центральный пабмед Статья КАС пабмед Google Scholar
Chaudhry R, Sharma S, Javed S, Passi K, Dey AB, Malhotra P: Молекулярное обнаружение Mycoplasma pneumoniae с помощью количественной ПЦР в реальном времени у пациентов с внебольничной пневмонией. Индийская J Med Res. 2013, 138: 244-251.
Центральный пабмед пабмед Google Scholar
Qu J, Gu L, Wu J, Dong J, Pu Z, Gao Y, Hu M, Zhang Y, Gao F, Cao B, Wang C, Пекинская сеть по внебольничной пневмонии у взрослых (BNACAP): Точность антител IgM тестирование, FQ-ПЦР и посев в лабораторной диагностике острой инфекции Mycoplasma pneumoniae у взрослых и подростков с внебольничной пневмонией. BMC Infect Dis. 2013, 13: 172-10.1186/1471-2334-13-172.
Центральный пабмед Статья пабмед Google Scholar
Martínez MA, Ruiz M, Zunino E, Luchsinger V, Avendaño LF: Обнаружение Mycoplasma pneumoniae при внебольничной пневмонии у взрослых с помощью ПЦР и серологии. J Med Microbiol. 2008, 57: 1491-1495. 10.1099/jmm.0.2008/003814-0.
Артикул пабмед Google Scholar
Zhang L, Zong ZY, Liu YB, Ye H, Lv XJ: ПЦР в сравнении с серологией для диагностики инфекции Mycoplasma pneumoniae : систематический обзор и метаанализ.Индийская J Med Res. 2011, 134: 270-280.
Центральный пабмед пабмед Google Scholar
Daxboeck F, Khanakah G, Bauer C, Stadler M, Hoffmann H, Stanek G: Обнаружение Mycoplasma pneumoniae в образцах сыворотки пациентов с Mycoplasma pneumoniae методом ПЦР. Inter J Med Microbiol. 2005, 295: 279-285. 10.1016/j.ijmm.2005.05.001.
Артикул КАС Google Scholar
Уэйтс К.Б., Балиш М.Ф., Аткинсон Т.П.: Новое понимание патогенеза и обнаружения инфекций Mycoplasma pneumoniae . Будущая микробиология. 2008, 3: 635-648. 10.2217/17460913.3.6.635.
Центральный пабмед Статья пабмед Google Scholar
Рациональный пошаговый подход к Mycoplasma pneumoniae пневмонии у детей пневмония.В прошлом
M. pneumoniae были чувствительны к макролидным антибиотикам, а M. pneumoniae пневмония (MPP) обычно была доброкачественной и самоизлечивающейся болезнью. Однако, несмотря на использование соответствующих антибиотиков, может наблюдаться постоянная лихорадка и клиническое ухудшение, что приводит к тяжелому заболеванию. Двумя основными сложными состояниями, которые могут встречаться клинически, являются резистентный к макролидам MPP и рефрактерный MPP. Что касается эпидемий на Тайване, то до 2017 г. средний уровень устойчивости к макролидам был ниже 30%.Примечательно, что с 2018 года распространенность резистентного к макролидам MPP на Тайване быстро увеличилась. Резистентный к макролидам MPP характеризуется стойкой лихорадкой и/или отсутствием радиологической регрессии на фоне антибиотиков-макролидов и может даже прогрессировать в тяжелую и осложненную пневмонию. Тетрациклины (доксициклин или миноциклин) или фторхинолоны являются альтернативными методами лечения резистентного к макролидам MPP. Рефрактерный МПП характеризуется избыточным иммунным ответом против возбудителя. В этом контексте кортикостероиды были предложены в качестве иммуномодулятора для подавления сверхактивной иммунной реакции хозяина.Чрезмерное использование макролидов может способствовать резистентности к макролидам, а затем и увеличению резистентности к макролидам. Отсроченное эффективное антимикробное лечение связано с длительным и/или более тяжелым течением заболевания. Таким образом, важное значение имеет правильное назначение антибиотиков, а также быстрая и точная диагностика МПП. Точная начальная точка, доза и продолжительность иммуномодулятора еще не установлены. Мы обсудим эти важные вопросы в этом обзоре.Ключевые слова
М.Пневмококк пневмония
макролиды резистентность
огнеупорного микоплазма пневмония пневмония
кортикостероидов Сокращения
MPPM. Пневмококк пневмония
CAPвнебольничная пневмония
RMPPогнеупорных микоплазмы пневмония пневмония
Рекомендованных статьи articlesCiting ( 0)
© Тайваньское общество микробиологии, 2020 г. Опубликовано Elsevier Taiwan LLC.
Рекомендуемые статьи
Ссылки на статьи
Атипичная (ходячая) пневмония: лечение и лечение
Обзор
Что такое «ходячая» пневмония?«Ходячая» пневмония — легкая форма пневмонии (инфекция легких).Этот немедицинский термин стал популярным описанием, потому что вы можете чувствовать себя достаточно хорошо, чтобы ходить, выполнять свои повседневные дела и даже не осознавать, что у вас пневмония.
Большую часть времени ходячая пневмония вызывается атипичными бактериями под названием Mycoplasma pneumoniae , которые могут жить и расти в носу, горле, трахее (трахее) и легких (ваших дыхательных путях). Его можно лечить антибиотиками.
Ходячая пневмония, вызванная микоплазмой, ученые называют «атипичной» из-за уникальных особенностей самих бактерий.Несколько факторов, которые делают его нетипичным, включают:
- Легкие симптомы
- Естественная устойчивость к лекарствам, которые обычно лечат бактериальные инфекции
- Часто ошибочно принимают за вирус, потому что у них отсутствует типичная клеточная структура других бактерий
Да. Другие типы атипичной пневмонии включают:
Чем ходячая пневмония отличается от «обычной» пневмонии?Ходячая пневмония отличается от типичной пневмонии по нескольким параметрам, в том числе:
- Ходячая пневмония — более легкая форма пневмонии.
- Ходячая пневмония обычно не требует постельного режима или госпитализации.
- Ходячая пневмония обычно вызывается Mycoplasma pneumoniae . Типичная пневмония чаще всего вызывается _Streptococcus_pneumonia или вирусом гриппа (гриппа) или риновирусом.
На Mycoplasma pneumoniae приходится от 10 до 40 процентов случаев внебольничной пневмонии (пневмонии, заразившейся вне медицинского учреждения).
Ходячая пневмония может возникнуть в любое время года, хотя чаще всего осенью и зимой.
Является ли ходячая пневмония заразной? Если да, то как он распространяется и кто подвергается наибольшему риску?Да, ходячая пневмония, вызванная Mycoplasma pneumoniae , заразна (передается от человека к человеку). Когда инфицированный человек кашляет или чихает, крошечные капельки, содержащие бактерии, попадают в воздух и могут вдыхаться другими людьми, находящимися поблизости.
Инфекция может легко распространяться в многолюдных или общих жилых помещениях, таких как дома, школы, общежития и дома престарелых. Это, как правило, влияет на молодых людей и детей школьного возраста больше, чем на пожилых людей.
Риск заболеть более тяжелой пневмонией еще выше среди тех, у кого есть респираторные заболевания, такие как:
Как долго я заразен ходячей пневмонией?Если у вас ходячая пневмония, вызванная Mycoplasma pneumoniae , вы можете считаться заразным от двух до четырех недель до появления симптомов (так называемый инкубационный период).В течение этого времени вы не будете осознавать, что вы заразны и распространяете пневмонию. Как только симптомы начинаются, вы остаетесь заразными до тех пор, пока симптомы не исчезнут.
Симптомы и причины
Что вызывает ходячую пневмонию?Ходячая пневмония чаще всего вызывается бактериями Mycoplasma pneumoniae .
Каковы симптомы ходячей пневмонии?Симптомы ходячей пневмонии включают:
- Боль в горле (фарингит)
- Чувство усталости (усталость)
- Боль в груди
- Легкий озноб
- Субфебрильная лихорадка
- Постоянный кашель, который может быть сухим или с выделением слизи
- Чихание
- Головная боль
Симптомы ходячей пневмонии могут проявляться медленно, начиная от одной до четырех недель после заражения.На более поздних стадиях болезни симптомы могут ухудшаться, лихорадка может повышаться, а при кашле может выделяться обесцвеченная мокрота (слизь).
Диагностика и тесты
Как диагностируется ходячая пневмония?Ваш врач спросит вас о ваших симптомах, о том, как долго они у вас есть, и есть ли у других членов семьи или людей, с которыми вы регулярно общаетесь, аналогичные симптомы. Он или она прослушает ваши легкие с помощью стетоскопа, чтобы проверить наличие аномальных звуков дыхания.Ваш врач может назначить рентген грудной клетки, чтобы увидеть, есть ли инфекция в легких. Ваша кровь или слизь могут быть проверены, чтобы определить, вызвана ли ваша пневмония Mycoplasma pneumoniae , другой бактерией, вирусом или грибком.
Управление и лечение
Как лечится ходячая пневмония?Ходячая пневмония обычно протекает в легкой форме, не требует госпитализации и лечится антибиотиками (если ваш врач считает, что ваши симптомы вызваны бактериями).Эффективны несколько видов антибиотиков. Антибиотики, используемые для лечения ходячей пневмонии, вызванной M ycoplasma pneumoniae , включают:
- Антибиотики-макролиды: Препараты-макролиды являются предпочтительным лечением для детей и взрослых. Макролиды включают азитромицин (Zithromax®) и кларитромицин (Biaxin®). За последнее десятилетие некоторые штаммы Mycoplasma pneumoniae стали устойчивыми к макролидным антибиотикам, возможно, из-за широкого использования азитромицина для лечения различных заболеваний.
- Фторхинолоны: Эти препараты включают ципрофлоксацин (Cipro®) и левофлоксацин (Levaquin®). Фторхинолоны не рекомендуются детям младшего возраста.
- Тетрациклины: Эта группа включает доксициклин и тетрациклин. Они подходят для взрослых и детей старшего возраста.
Часто можно также принимать безрецептурные лекарства, которые облегчают симптомы заложенности носа, кашля и разжижают скопление слизи в груди. Если у вас жар:
- Пейте больше жидкости
- Остальное
- Принять лекарство
Профилактика
Как можно предотвратить ходячую пневмонию?К сожалению, вакцин для предотвращения ходячей пневмонии, вызванной Mycoplasma pneumoniae, не существует. Даже если вы переболели ходячей пневмонией, вы не станете невосприимчивы, поэтому в будущем возможно повторное заражение.
Советы по профилактике ходячей пневмонии включают:
- Прикрывайте нос и рот салфеткой, когда чихаете или кашляете. Если салфетки нет, чихайте или кашляйте во внутреннюю часть локтя или рукава. Никогда не чихайте и не кашляйте в руки. Поместите использованные салфетки в корзину для мусора.
- Часто мойте руки теплой водой с мылом не менее 20 секунд.Используйте дезинфицирующее средство для рук на спиртовой основе, если мыло и вода недоступны.
- Носите маску рядом с больными людьми, если у вас есть респираторные заболевания (такие как астма, бронхит, эмфизема) или другие хронические заболевания (заболевания сердца, печени или почек или диабет), которые могут сделать пневмонию еще более рискованной для вас.
- Сделайте ежегодную прививку от гриппа. Бактериальная пневмония может развиться после перенесенного гриппа.
- Спросите своего врача о пневмококковой вакцине.Доступны два типа вакцин: Превнар 13® и Пневмовакс 23®. Каждая вакцина рекомендуется для людей в разном возрасте или с повышенным риском пневмококковой инфекции, включая пневмонию.
Перспективы/прогноз
Когда я почувствую себя лучше, если у меня ходячая пневмония?Большинство людей с ходячей пневмонией чувствуют себя лучше после нескольких дней приема антибиотиков.

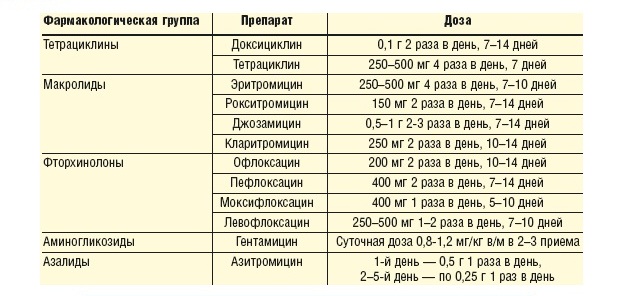

.gif)