Надпочечниковая недостаточность у детей > Клинические протоколы МЗ РК
4. Нагрузочная проба с синактеном
Основные клинические симптомы проявления XHH связаны с недостаточной секрецией кортикостероидов и альдостерона. Клинические симптомы при XHH обычно развиваются медленно, исподволь — пациенты не могут определить, когда началось заболевание. Однако в случае врожденной гипоплазии надпочечников симптомы заболевания могут появляться вскоре после рождения и связаны они с потерей соли. Такие дети вялые, плохо прибавляют в весе (потеря в весе после рождения превышает физиологическую норму на 300–500 г), срыгивают, мочеиспускания вначале обильные, частые, тургор ткани снижен, с удовольствием пьют подсоленную воду. Часто диспептические расстройства, интеркуррентные заболевания провоцируют кризы острой надпочечниковой недостаточности.У детей старшего возраста основными симптомами хронической надпочечниковой недостаточности являются слабость, утомляемость, адинамия, особенно в конце дня. Эти симптомы проходят после ночного отдыха, но могут возникать периодически, в связи с интеркуррентными заболеваниями, оперативными вмешательствами, психическими нагрузками. В патогенезе данного синдрома основное значение придается нарушениям углеводного и минерального обмена.
Наряду с общей слабостью отмечаются потеря аппетита, снижение массы тела, извращение вкуса (едят соль горстями), особенно во второй половине дня. Нередко больные жалуются на тошноту, иногда рвоту, боли в животе, снижается секреция пепсина и соляной кислоты. Изменения стула сопровождаются поносами и запорами. У других детей отмечается жажда, полиурия. Рвота и диарея ведут к еще большей потере натрия и ускоряют развитие острой надпочечниковой недостаточности.
Часто у больных возникает ортостатическая гипотония, с чем связаны головокружения и обморочные состояния. Гипогликемические состояния, появляющиеся натощак или через 2–3 ч после приема пищи, типичны для надпочечниковой недостаточности и связаны с дефицитом глюкокортикоидов, снижением запасов гликогена в печени. Гипогликемические приступы протекают легко и сопровождаются чувством голода, потливостью, бледностью, тремором пальцев рук. Нейрогипогликемический синдром характеризуется апатией, недоверчивостью, подавленностью, чувством страха, возможны судороги.
Изменения функции центральной нервной системы проявляются в снижении памяти, быстрой эмоциональной утомляемости, рассеянности внимания, расстройстве сна. Надпочечниковая недостаточность сопутствует адренолейкодистрофии. Это генетическое, сцепленное с Х-хромосомой рецессивное заболевание, которое протекает с поражением белого вещества нервной системы и коры надпочечников. Быстро прогрессирует демиелинизация, проявляющаяся генерализованной атаксией, судорогами. Неврологической симптоматике предшествуют клинические признаки надпочечниковой недостаточности.
Следует обратить внимание на потемнение кожи, реже — слизистых оболочек. Пигментация кожи и слизистых наблюдается почти у всех больных и может быть выражена задолго до появления других симптомов XHH. Генерализованная пигментация обусловливается избыточной секрецией АКТГ и β-меланоцитостимулирующего гормона. Кожа детей чаще имеет золотисто-коричневую окраску, реже — светло-коричневую или бронзовый оттенок. Наиболее насыщенная пигментация выражена в области сосков грудных желез, мошонки и полового члена у мальчиков, белой линии живота, в местах трения кожи одеждой, рубцов, коленных, локтевых суставов, мелких суставов кистей, слизистой десен. Иногда первым указанием на наличие заболевания служит длительно сохраняющийся загар. Пигментация усиливается в период нарастания надпочечниковой недостаточности. У 15% больных пигментация может
сочетаться с участками депигментации. Редко встречается беспигментная форма заболевания, которая характерна для вторичной XHH.
При рано начавшемся заболевании дети отстают в физическом и половом развитии. Нередко XHH у детей протекает стерто и диагностируется в случае присоединения интеркуррентных заболеваний.
Один из ранних симптомов Аддисоновой болезни — артериальная гипотония: снижается как систолическое, так и диастолическое артериальное давление. Это связано с уменьшением объема циркулирующей крови, а также глюкокортикоидов, которые важны для поддержания тонуса сосудов. Пульс мягкий, малый, замедленный.
Однако следует иметь в виду, что артериальное давление при надпочечниковой недостаточности у больных с гипертонией может быть нормальным.
Лабораторные исследования
При типичном течении XHH в крови выявляются увеличение количества эозинофилов, относительный лимфоцитоз, умеренная анемия. Характерным биохимическим признаком заболевания является повышение в сыворотке крови уровня калия, креатинина, мочевины, при одновременном снижении содержания натрия и хлоридов. Гиперкальциемия сочетается с полиурией, никтурией, гипоизостенурией, гиперкальциурией. Подтверждает диагноз низкий уровень кортизола в крови (менее 170 нмоль/л), взятой в утренние часы. Для определения стертых форм гипокортицизма и дифференциальной диагностики рекомендуется проведение
Прямым подтверждением наличия первичной надпочечниковой недостаточности является резкое
Инструментальные исследования
Изменения на ЭКГ обусловлены внутриклеточной гиперкалиемией, проявляются в виде желудочковой экстрасистолии, уплощенного двухфазного зубца Т, удлинения интервала PQ и комплекса QRS.
Визуализация надпочечников (УЗИ, компьютерная томография) также позволяет уточнить форму надпочечниковой недостаточности.— детского кардиолога
— детского невролога.
diseases.medelement.com
Надпочечниковая недостаточность у детей | #05/05
Надпочечниковая недостаточность у детей (НН), или гипокортицизм, — это клинический синдром, обусловленный дефицитом секреции гормонов коры надпочечников. В зависимости от локализации патологического процесса выделяют первичную, вторичную и третичную НН. При первичной НН поражается сама ткань надпочечников, при вторичной — передняя доля гипофиза с нарушением секреции АКТГ, третичная форма связана с патологией гипоталамуса и дефицитом продукции последним кортикотропин-релизинг гормона. Подразделяют НН на острую и хроническую. Хроническая надпочечниковая недостаточность (ХНН) была описана еще в середине XIX в. Аддисоном на основании результатов вскрытия. Эта форма встречается с периодичностью 1 случай на 10 тыс. чел., в 2 раза чаще у лиц мужского пола зрелого и пожилого возраста. Многие авторы отмечают, что ХНН у детей диагностируется редко, в связи с многообразием и неспецифичностью симптомов гипокортицизма.
Клинические симптомы хронической надпочечниковой недостаточности возникают при поражении 95% ткани коры надпочечников. Почти у 60% больных недостаточность надпочечников возникает в результате идиопатической атрофии надпочечников.
В этой группе основной причиной развития заболевания в настоящее время считается аутоиммунная деструкция коры надпочечников (аутоиммунный адреналит 70–85%).
В ткани пораженных надпочечников при этой форме патологии отмечается обширная лимфоплазмоцитарная инфильтрация, надпочечники уменьшены в размерах, кора атрофирована. В сыворотке крови таких больных обнаруживаются антитела к микросомальным и митохондриальным антигенам коры надпочечников, а также антитела к 21-гидроксилазе — одному из ключевых ферментов стероидогенеза.
Аутоиммунный адреналит нередко сочетается с другими аутоиммунными эндокринопатиями. Аутоиммунный полигландулярный синдром типа 1 (АПС-1) включает в себя недостаточность надпочечников, гипопаратиреоз и кандидамикоз. У части больных этот синдром сочетается с гипогонадизмом, алопецией, витилиго, пернициозной анемией, аутоиммунными заболеваниями щитовидной железы, хроническим гепатитом.
Аутоиммунный полигландулярный синдром типа 2 (АПС-2) характеризуется сочетанием сахарного диабета 1 типа, аутоиммунных заболеваний щитовидной железы и надпочечниковой недостаточности (синдром Шмидта). АПС-1 наследуется по аутосомно-рецессивному типу, а АПС-2 — по аутосомно-доминантному. О генетической предрасположенности к аутоиммунной недостаточности надпочечников свидетельствует обнаружение у большинства больных ассоциации с генами системы НLADR3, DR4 и HLAB8. У этих пациентов имеет место снижение супрессорной активности Т-лимфоцитов. Описывают семейные формы данного поражения. Деструкция коркового вещества надпочечников возможна в результате ее поражения при туберкулезе, диссеминированной грибковой инфекции, токсоплазмозе, цитомегалии. Возникновение XНН отмечается после тяжело перенесенных вирусных инфекций (ОРВИ, корь и др.), реже причинами ее развития становятся адренолейкодистрофия, опухолевые процессы, врожденная жировая гиперплазия надпочечников. Иногда XНН развивается на фоне обызвествления надпочечников, являющегося следствием любого из вышеперечисленных процессов. В других случаях петрификаты в надпочечниках обнаруживаются случайно, при рентгенологическом исследовании — задолго до появления клинических симптомов XНН.
Значительно реже встречаются вторичные и третичные XНН, при которых атрофия коры надпочечников является следствием недостаточной продукции гипофизом АКТГ, или гипоталамусом — кортиколиберина. Снижение секреции этих гормонов может наблюдаться при различных патологических процессах гипоталамо-гипофизарной области: опухолях, сосудистых нарушениях, травме, инфекции, внутриутробном поражении гипофиза. Снижение продукции АКТГ может наблюдаться при различных органических поражениях ЦНС, длительном применении глюкокортикоидов, опухолевом поражении коры надпочечников.
Основные клинические симптомы проявления XHH связаны с недоста-точной секрецией кортикостероидов и альдостерона. Клинические симптомы при XHH обычно развиваются медленно, исподволь — пациенты не могут определить, когда началось заболевание. Однако в случае врожденной гипоплазии надпочечников симптомы заболевания могут появляться вскоре после рождения и связаны они с потерей соли. Такие дети вялые, плохо прибавляют в весе (потеря в весе после рождения превышает физиологическую норму на 300–500 г), срыгивают, мочеиспускания вначале обильные, частые, тургор ткани снижен, с удовольствием пьют подсоленную воду. В таких случаях следует обратить внимание на потемнение кожи, реже — слизистых оболочек. Часто диспептические расстройства, интеркуррентные заболевания провоцируют кризы острой надпочечниковой недостаточности.
У детей старшего возраста основными симптомами хронической надпочечниковой недостаточности являются слабость, утомляемость, адинамия, особенно в конце дня. Эти симптомы проходят после ночного отдыха, но могут возникать периодически, в связи с интеркуррентными заболеваниями, оперативными вмешательствами, психическими нагрузками. В патогенезе данного синдрома основное значение придается нарушениям углеводного и минерального обмена.
Наряду с общей слабостью отмечаются потеря аппетита, снижение массы тела, извращение вкуса (едят соль горстями), особенно во второй половине дня. Нередко больные жалуются на тошноту, иногда рвоту, боли в животе, снижается секреция пепсина и соляной кислоты. Изменения стула сопровождаются поносами и запорами. У других детей отмечается жажда, полиурия. Рвота и диарея ведут к еще большей потере натрия и ускоряют развитие острой надпочечниковой недостаточности. Один из ранних симптомов Аддисоновой болезни — артериальная гипотония: снижается как систолическое, так и диастолическое артериальное давление. Это связано с уменьшением объема циркулирующей крови, а также глюкокортикоидов, которые важны для поддержания тонуса сосудов. Пульс мягкий, малый, замедленный.
Часто у больных возникает ортостатическая гипотония, с чем связаны головокружения и обморочные состояния. Однако следует иметь в виду, что артериальное давление при надпочечниковой недостаточности у больных с гипертонией может быть нормальным. Размеры сердца уменьшаются, могут наблюдаться одышка, сердцебиение, нарушение сердечного ритма. Изменения на ЭКГ обусловлены внутриклеточной гиперкалиемией, проявляются в виде желудочковой экстрасистолии, уплощенного двухфазного зубца Т, удлинения интервала PQ и комплекса QRS.
Гипогликемические состояния, появляющиеся натощак или через 2–3 ч после приема пищи, типичны для надпочечниковой недостаточности и связаны с дефицитом глюкокортикоидов, снижением запасов гликогена в печени. Гипогликемические приступы протекают легко и сопровождаются чувством голода, потливостью, бледностью, тремором пальцев рук. Нейрогипогликемический синдром характеризуется апатией, недоверчивостью, подавленностью, чувством страха, возможны судороги.
Изменения функции центральной нервной системы проявляются в снижении памяти, быстрой эмоциональной утомляемости, рассеянности внимания, расстройстве сна. Надпочечниковая недостаточность сопутствует адренолейкодистрофии. Это генетическое, сцепленное с Х-хромосомой рецессивное заболевание, которое протекает с поражением белого вещества нервной системы и коры надпочечников. Быстро прогрессирует демиелинизация, проявляющаяся генерализованной атаксией, судорогами. Неврологической симптоматике предшествуют клинические признаки надпочечниковой недостаточности.
Пигментация кожи и слизистых наблюдается почти у всех больных и мо-жет быть выражена задолго до появления других симптомов XHH. Генерализованная пигментация обусловливается избыточной секрецией АКТГ и β-меланоцитостимулирующего гормона. Кожа детей чаще имеет золотисто-коричневую окраску, реже — светло-коричневую или бронзовый оттенок. Наиболее насыщенная пигментация выражена в области сосков грудных желез, мошонки и полового члена у мальчиков, белой линии живота, в местах трения кожи одеждой, рубцов, коленных, локтевых суставов, мелких суставов кистей, слизистой десен. Иногда первым указанием на наличие заболевания служит длительно сохраняющийся загар. Пигментация усиливается в период нарастания надпочечниковой недостаточности. У 15% больных пигментация может сочетаться с участками депигментации. Редко встречается беспигментная форма заболевания, которая характерна для вторичной XHH.
При рано начавшемся заболевании дети отстают в физическом и половом развитии. Нередко XHH у детей протекает стерто и диагностируется в случае присоединения интеркуррентных заболеваний.
При типичном течении XHH в крови выявляются увеличение количества эозинофилов, относительный лимфоцитоз, умеренная анемия. Характерным биохимическим признаком заболевания является повышение в сыворотке крови уровня калия, креатинина, мочевины, при одновременном снижении содержания натрия и хлоридов. Гиперкальциемия сочетается с полиурией, никтурией, гипоизостенурией, гиперкальциурией. Подтверждает диагноз низкий уровень кортизола в крови (менее 170 нмоль/л), взятой в утренние часы. Для определения стертых форм гипокортицизма и дифференциальной диагностики рекомендуется проведение нагрузочных проб с синактеном. Синтетический АКТГ стимулирует кору надпочечников и позволяет выявить наличие резервов. После определения уровня кортизола в плазме крови, внутримышечно вводят синактен и через полчаса вновь исследуют концентрацию кортизола. Пробы считаются положительными, если уровень кортизола удваивается. Исследование можно проводить на фоне заместительной терапии преднизолоном. Эта проба позволяет также дифференцировать первичную и вторичную HH.
Прямым подтверждением наличия первичной надпочечниковой недостаточности является резкое повышение уровня АКТГ в плазме крови, при вторичной — его снижение. С целью диагностики гипоальдостеронизма определяют содержание альдостерона и ренина в плазме крови. При первичной надпочечниковой недостаточности содержание альдостерона снижено или находится на нижней границе нормы, а уровень ренина повышается. Визуализация надпочечников (УЗИ, компьютерная томография) также позволяет уточнить форму надпочечниковой недостаточности.
Дифференциальный диагноз Аддисоновой болезни необходимо проводить с рядом заболеваний, протекающих с потерей веса, гипотонией, полиурией, анорексией: кишечными инфекциями, интоксикациями другой этиологии, глистной инвазией, хроническим пиелонефритом, несахарным диабетом, с сольтеряющей формой дисфункции коры надпочечников, с гипоальдостеронизмом. Диагноз XHH облегчается наличием пигментации кожи, хотя при вторичной XHH она может отсутствовать. Необходимо учесть, что при условии своевременной диагностики и правильно подобранной заместительной терапии хроническая надпочечниковая недостаточность имеет благоприятный прогноз.
Часть больных поступают с ошибочным диагнозом: астения, вегетососудистая дистония, гипотрофия неясной этиологии, глистная инвазия, гастрит и т. д.
Диагностические ошибки при кризе XHH связаны с недооценкой основных симптомов заболевания. Среди неправильных диагнозов фигурируют острый аппендицит, гастрит, холецистит, опухоль мозга, энцефалит, ацетонемическая рвота.
Угрожающим жизни больных XHH должен быть признан аддисонический криз — острая надпочечниковая недостаточность (ОНН), развивающаяся вследствие быстрого снижения продукции гормонов коры надпочечников. Это состояние может развиваться после многолетнего субклинического течения XHH, либо появлению ОНН предшествует острая инфекция или другая стрессовая ситуация (травма, операция). Усиливаются слабость и гиперпигментация кожных покровов и слизистых оболочек, аппетит прогрессивно ухудшается вплоть до отвращения к пище. Тошнота переходит в рвоту, с развитием криза она становится неукротимой, появляется жидкий стул. У некоторых больных возникают резкие боли в животе. Ведущими клиническими симптомами ОНН обычно являются: глубокое снижение артериального давления, пульс слабого наполнения, тоны сердца глухие, слизистые бледные, периферический акроцианоз, профузный пот, конечности холодные, гипотермия. Нарастают электролитные нарушения, гипогликемия, гиперазотемия. Гиперкалиемия оказывает токсическое действие на миокард и может привести к остановке сердца.
Основным принципом заместительной терапии XHH и аддисонического криза является сочетанное использование препаратов глюкокортикоидов и минералокортикоидов, которые поддерживают жизненно важные функции: обеспечивают адаптацию организма к стрессовым воздействиям внешней среды и сохранение водно-солевого баланса. Предпочтение отдают гидрокортизону, преднизолону, флудрокортизону. Гидрокортизон обладает как глюкокортикоидным, так и минералокортикоидным действием.
Монотерапия минералокортикоидами или глюкокортикоидами проводится в небольшом проценте случаев. В настоящее время в клинической практике широко используются эффективные и удобные в употреблении таблетированные препараты гидрокортизона и флудрокортизона.
Большинство больных с XHH нуждаются в постоянной заместительной глюкокортикоидной терапии, чаще всего с этой целью используются гидрокортизон и преднизолон. Предпочтение отдается гидрокортизону, который обладает как глюкокортикоидным, так и минералокортикоидным действием. Заместительная терапия глюкокортикостероидами должна имитировать физиологическую секрецию этих гормонов. Согласно циркадному ритму глюкокортикоидов, гидрокортизон или преднизолон при легкой форме следует назначать в утренние часы, при заболевании средней тяжести — утром и после обеда.
При постоянной заместительной терапии XHH доза гидрокортизона у детей раннего возраста ориентировочно должна составлять 1–3 мг, а у больных старшего возраста — до 15 мг и 7,5 мг соответственно.
Следует помнить, что уровень секреции глюкокортикоидов в норме зависит от функционального состояния организма. При травмах, острых инфекциях, физическом или психическом стрессе суточная доза глюкокортикоидов должна быть увеличена в 2–3 раза. Перед малыми вмешательствами (гастродуоденоскопия, применение наркоза, экстракция зубов и др.) больному необходимо однократное парентеральное введение гидрокортизона 12,5–25–50 мг за 30 мин до манипуляции. При плановых операциях повышение дозы глюкокортикоидов рекомендуется начинать накануне вмешательства и вводить их только парентерально. Гидрокортизон вводят внутримышечно по 12,5–25–50 мг 2–4 раза в сут. В день операции дозу препарата увеличивают в 2–3 раза, причем часть лекарства вводят внутривенно капельно, а остальное — внутримышечно каждые 4–6 ч в течение 1–2 с. В последующие дни постепенно переходят на заместительную терапию.
Критерием адекватности глюкокортикоидной терапии являются поддер-жание нормальной массы тела, отсутствие жалоб на постоянное чувство голода и признаков передозировки гормонов, гиперпигментации кожи, нормальное артериальное давление.
Если при использовании глюкокортикоидов не происходит нормализации артериального давления, отсутствует прибавка в весе, сохраняется гипонатриемия, необходимо назначить минералокортикоиды. Комбинированная терапия глюко- и минералокортикоидами, как правило, необходима большинству больных с тяжелой формой XHH.
Суточная доза флудрокортизона подбирается индивидуально. Потребность в этом гормоне может возникать ежедневно или раз в 2–3 дня. У детей грудного возраста в первые месяцы жизни потребность флудрокортизона на килограмм массы тела выше.
Об адекватности дозы минералокортикоидов свидетельствуют нормальные уровни калия и натрия плазмы, активности ренина плазмы.
При передозировке минералокортикоидов могут развиться периферические отеки, отек мозга, нарушение сердечного ритма в связи с задержкой воды. Для устранения этих осложнений надо отменить минералокортикоиды, повысить дозы глюкокортикоидов в 1,5–2 раза, ограничить содержание в пище поваренной соли, назначить соки, 10 % раствор хлорида калия.
Экстренные мероприятия требуются при развитии аддисонического криза. Наибольшая опасность для жизни возникает в первые сутки острого гипокортицизма. Первоочередными задачами являются введение достаточного количества кортикостероидов или его синтетических аналогов, борьба с обезвоживанием, коррекция электролитных нарушений.
При парентеральном введении кортикостероидов предпочтение отдается препаратам гидрокортизона, тогда как преднизолон и дексаметазон должны использоваться только в крайнем случае.
Гидрокортизон вводится внутривенно капельно вместе с глюкозой в течение 4–6 ч. В первые сутки доза гидрокортизона составляет 10–15 мг/кг, преднизолона — 5 мг/кг. В последующие сутки доза внутривенно вводимых препаратов уменьшается в 2–3 раза. Одновременно внутримышечно вводят гидрокортизон через 4–6 ч 25–75 мг/сут.
Наряду с введением глюкокортикоидов проводят лечебные мероприятия по борьбе с обезвоживанием и явлениями шока. Количество изотонического раствора натрия хлорида и 5–10% раствора глюкозы составляет примерно 10% от массы тела, половина суточного объема жидкости вводится в первые 6–8 ч. При многократной рвоте рекомендуется внутривенное введение 5–10 мл 10% раствора хлорида натрия. В капельницу добавляют аскорбиновую кислоту 5–10 мл.
При улучшении состояния больного заканчивают внутривенное введение гидрокортизона, продолжая его внутримышечное введение 4 раза в сут 25–50 мг на прием. Затем постепенно уменьшают дозу гидрокортизона и удлиняют интервал между введениями. После стабилизации болезни можно перевести больного на таблетированный гидрокортизон.
У части больных возникает необходимость сочетать введение гидрокортизона и обязательно, при применении преднизолона, назначение препарата ДОКСА, который вводится по 1–2 мл в день внутримышечно. После прекращения рвоты, вместо инъекции ДОКСА используются таблетки флудрокортизона по 0,1 мг/сут. Своевременная диагностика XHH и правильно подобранная заместительная терапия, которая проводится пожизненно, являются залогом профилактики аддисонического криза: при этих условиях дети, как правило, развиваются нормально.
В. В. Смирнов, доктор медицинских наук, профессор
И. С. Мавричева, кандидат медицинских наук
РГМУ, Москва
www.lvrach.ru
Болезни надпочечников у детей клинические формы. Заболевания надпочечников у детей
Надпочечниками называют железы (их две), которые расположены сверху над почками. Работа надпочечников очень важна для функционирования организма человека. Если эти органы некорректно выполняют свою функцию, происходит сбой в работе всех органов, этот сбой может привести не только к непоправимым последствиям для здоровья, но и к летальному исходу.
Функция надпочечников сводится к следующим аспектам:
- синтез гормонов;
- регулирование метаболических процессов;
- проявление адекватной реакции на стрессы;
- регулирование постоянства внутренней среды.
Надпочечники состоят из двух слоев – коркового и мозгового. В свою очередь корковый слой делится на клубочковый, пучковый и сетчатый, каждый из которых выполняет свою определенную функцию.
В клубочковой зоне вырабатываются следующие гормоны – кортикостеромы, альдостерон, дезоксикортикостерон. В пучковой зоне синтезируется кортикостерон, а в сетчатой продуцируются половые гормоны.
Кроме синтеза гормонов, корковое вещество регулирует водно-электролитный баланс, стимулирует работу сердца, отвечает за расширение бронхиол, нормализует артериальное давление, вырабатывает адреналин и норадреналин, повышает уровень сахара.
Функция надпочечников у мужчин, помимо перечисленного, заключается в следующем:
- функциональность половых органов;
- увеличение силы мышц.
Надпочечники повышают устойчивость организма к разным заболеваниям, повышают положительные эмоции, активно помогают бороться с стрессами и депрессивными ситуациями. Гормоны, которые синтезируют эти парные органы крайне необходимы для работы организма, любое их отклонение от нормы приводят к серьезным недугам.
Как проверить работу надпочечников? Для проверки существуют эффективные диагностические методы, которые будут рассмотрены ниже.
Нарушения в работе надпочечников
Болезни надпочечников сопровождаются нарушением баланса гормонов (избыток или недостаток), но могут протекать без гормонального сбоя. Снижение синтеза гормонов наблюдается при острой и хронической надпочечниковой недостаточности. В этом случае гормонов надпочечников организму не хватает, в результате чего развиваются различные недуги. Причины первичной надпочечной недостаточности может быть в разрушении ткани органа различными инфекционными заболеваниями (например, туберкулезом). Вторичная недостаточность надпочечников возникает при сниженной функциональности гипоталамуса и гипофиза.
Чрезмерный синтез гормонов наблюдается при опухолях, увеличении коры органов, при заболевании Иценко-Кушинга. Но некоторые нарушения в их работе могут протекать и без изменения гормонального фона, к ним относятся кистозные образования и опухоли, которые не проявляют гормональную активность.
Симптоматика заболеваний
Синдром Кушинга – избыточный синтез гормонов. Признаки:
- пациент имеет лишний вес, причем набор веса в основном приходится на переднюю часть туловища и лицо. Конечности же теряют в весе;
- на коже отмечаются растяжки багрового цвета;
- кожа покрывается прыщами;
- у женщин наблюдается повышенное оволосение, сбивается цикл;
- у мужчин развивается половое бессилие;
- слабость;
- кости становятся хрупки
gcchili.ru
Заболевания надпочечников. Справочник педиатра
Заболевания надпочечников
Гипофункция коры надпочечников
Термин «гипофункция коры надпочечников» объединяет все состояния, при которых секреция стероидных гормонов надпочечников оказывается ниже потребностей организма в ней.
Первичная недостаточность коры надпочечников, связанная с первичной неспособностью надпочечников вырабатывать достаточные количества гормонов, встречается редко и может возникать в любом возрасте независимо от пола. Вторичная недостаточность обусловлена малой продукцией АКТГ, может развиваться в результате применения экзогенных стероидов в лечебных целях. Различают острую и хроническую недостаточность коры надпочечников.
Этиология. Острая недостаточность коры надпочечников развивается при врожденной гипоплазии, кровоизлияниях в надпочечники при родовой травме, асфиксии или применении акушерских щипцов. Провоцирующие факторы: инфекционные заболевания, оперативное удаление опухоли надпочечника при атрофии оставшегося надпочечника, двустороннее удаление надпочечников, внезапное прекращение лечения кортизоном и его аналогами, врожденная гиперплазия надпочечников.
Хроническая недостаточность коры надпочечников (болезнь Аддисона) сопровождается недостаточной продукцией кортизола и (или) альдостерона вследствие поражения надпочечников (первичная), гипофиза (вторичная) или гипоталамуса (третичная).
Причинами развития болезни Аддисона могут быть врожденная гипоплазия или аплазия надпочечников; врожденные дисфункции коры надпочечников; кровоизлияния в периоде новорожденности; при острых инфекциях, в частности менингококковой – синдром Уотерхауса-Фридериксена; при туберкулезе; внезапном прекращении кортикостероидной терапии; тотальной адреналэктомии.
Наиболее частой причиной ХНН у школьников и взрослых является аутоиммунное поражение. Клинические проявления ХНН развиваются, когда деструктивным процессом поражено более 90 % коркового вещества.
Вторичная и третичная ХНН возникают при поражении гипофиза или гипоталамуса при травме, инфекции, опухоли ЦНС, как правило, сопровождаются множественной гормональной недостаточностью.
В основе патогенеза гипокортицизма лежит снижение выработки корой надпочечников гормонов минерало– и глюкокортикоидов. Недостаток минералокортикоидов приводит к потерям с мочой натрия и хлора и снижению выделения калия, недостаток глюкокортикоидов – к падению уровня сахара в крови, повышению чувствительности к инсулину, увеличению количества лимфоцитов и эозинофилов в крови.
Клиника. При острой недостаточности надпочечников отмечаются следующие симптомы: повышение температуры тела, частое дыхание, цианоз, кожа холодная и влажная, головная боль, тошнота, боль в животе, снижение артериального давления, явления прострации и сосудистого коллапса. В крови – низкий уровень натрия, хлоридов, сахара и повышение калия. При аутопсии отмечаются деструктивные изменения клеток коры надпочечников. Прогноз при острой недостаточности надпочечников весьма серьезен. Смертность высокая.
Для хронической недостаточности надпочечников характерно постепенно прогрессирующее течение. У детей старшего возраста симптомы нарастают в течение длительного времени (месяцы, годы). Характерны гиподинамия, мышечная слабость, головные боли, сниженный аппетит, жажда, полиурия. Больной худеет, предпочитает соленую пищу. Типичны эпизоды болей в животе, рвота, диареи при стрессах, заболеваниях, после прививок, травм, операций. Ребенок отстает в росте, половом развитии, могут быть обмороки, снижено АД (преимущественно диастолическое), имеются признаки миокардиодистрофии (приглушение тонов сердца, функциональный шум). Дети с ХНН чаще болеют, медленно выздоравливают, годами наблюдаются по поводу вегетососудистой дистонии по гипотоническому типу или дискинезии желчевыводящих путей.
Нередко при первичной хронической недостаточности надпочечников появляется тотальная гиперпигментация кожи, наиболее выраженная в области сосков, белой линии живота, наружных гениталий, в местах трения одежды (шея, локти, колени), в области крупных складок, вокруг рубцов, на слизистой полости рта. Участки гиперпигментации могут чередоваться с очагами депигментации (витилиго), проявлениями кожно-слизистого кандидоза, что особенно характерно для аутоиммунного процесса.
Могут возникать острые кризы недостаточности надпочечников, которые провоцируют острые инфекционные заболевания, психическая или физическая травма, необоснованное применение АКТГ. Такие кризы проявляются симптомами острой недостаточности надпочечников.
Диагноз хронической надпочечниковой недостаточности основывается на триаде характерных симптомов: адинамия, пигментация кожи и гипотензия. Наряду с этим отмечаются резкое обезвоживание, потребность в соли, кризы.
Для первичной хронической надпочечниковой недостаточности характерно снижение уровней кортизола, альдостеронав крови, экскреции 17-КС и 17-ОКС при повышенном уровне АКТГ и ренина плазмы. При неясной клинической картине проводят функциональную пробу с экзогенным АКТГ. Дополнительное значение имеет определение гиперкалиемии, гипонатриемии и гипохлоремии. В крови выявляют гипохромную анемию, лимфоцитоз, эозинофилию, гипогликемию натощак и плоский тип пробы на толерантность к углеводам. У детей старше 2–3 лет обычно задержан «костный возраст».
Лечение острой недостаточности надпочечников проводят в отделениях реанимации. При лечении болезни Аддисона проводят заместительную терапию гормонами, обязательно включающую глюкокортикоиды и минерало-кортикоиды. При стрессовых ситуациях дозу глюкокортикоидов повышают в 3–5 раз. Девочкам проводят оперативную коррекцию наружных гениталий в 3-4-летнем возрасте.
В случаях криза лечение такое же, как при острой недостаточности надпочечников.
Адреногенитальный синдром
Этиология. Наследственное заболевание. Гиперплазия надпочечников развивается во внутриутробном периоде. К факторам, способствующим врожденной гиперплазии коры надпочечников, относятся функциональные нарушения в организме беременной, токсикоз, применение кортикальных препаратов и АКТГ во время беременности.
Наследственный дефект приводит к значительному понижению в организме кортизона и альдостерона, но синтез половых гормонов в коре надпочечников не нарушается. Низкий уровень кортизола в крови по принципу обратной связи стимулирует повышение секреции АКТГ. В свою очередь завышенный уровень АКТГ способствует гиперплазии коры надпочечников именно той зоны, в которой не нарушен синтез гормонов, – преимущественно андрогенов. Одновременно с андрогенами образуются промежуточные продукты синтеза кортизола. Наследуется по аутосомно-рецессивному типу. Встречается у детей обоего пола.
Клиника. Различают вирильную (простую), сольтеряющую и гипертензивную формы адреногенитального синдрома. Проявляется чаще в постнатальном и препубертатном периодах. Явления вирильности могут быть при сольтеряющей и гипертензивной формах.
Вирильная форма заболевания проявляется у девочек уже при рождении и выражается ложным гермафродитизмом. Клитор увеличен. Отверстие мочеиспускательного канала открывается у основания клитора. Большие половые губы имеют вид расщепленной мошонки. Иногда изменения наружных половых органов резко выражены и пол ребенка определить трудно. В 3–6 лет наблюдается избыточное оволосение на лобке, ногах, спине, физическое развитие и мышечная сила повышены. По внешнему виду девочка напоминает мальчика. В дальнейшем половое развитие прекращается, молочные железы слабо развиты, менструации скудные, с неправильным циклом, без овуляции или вовсе отсутствуют.
Развитие адреногенитального синдрома у мальчиков наблюдается с 2-3-летнего возраста: интенсивное физическое развитие сопровождается заметным увеличением полового члена, появлением чрезмерного оволосения, могут появляться эрекции. Яички инфантильны, и в дальнейшем развитие их прекращается.
Несмотря на интенсивный рост вначале, дети остаются низкорослыми, коренастыми (раннее закрытие эпифизарных зон роста).
Для солыперяющего варианта характерны нарушения электролитного равновесия, быстрая потеря натрия. Наиболее характерными симптомами, которые можно обнаружить у детей первого года, являются рвота, эксикоз, быстрая потеря веса, раздражительность, коллапс. Без лечения ребенок погибает. Смерть может наступить и без предшествующего коллапса и быть результатом гиперкалиемии. Распознавание сольтеряющей формы облегчается наличием у девочек псевдогермафродитизма, повышенным содержанием в моче 17-кетостероидов, гиперкалиемии и гипонатриемии.
Гипертензивная форма встречается очень редко. Она обусловлена избыточным выделением в кровь дезоксикортикостерона. Кроме гипертонии, у таких больных отмечаются признаки вирилизма. При всех формах врожденной гиперплазии надпочечников возможна пигментация кожи коричневого цвета или цвета кофе с молоком.
Диагноз. Представляют важность данные анамнеза и клиники (аномалии развития наружных половых органов, гирсутизм, ускоренное физическое развитие). Кроме этого, диагностика основывается на данных рентгенографии кистей рук (ускорение костного возраста), снижения экскреции 17-оксикортикостероидов, высокого уровня в крови АКТГ, 17-оксипрогестерона. Дифференциальный диагноз синдрома проводят с надпочечниковой недостаточностью, опухолью надпочечников, гермафродитизмом другого генеза, различными вариантами преждевременного полового созревания. Сольтеряющую форму необходимо дифференцировать с диспепсиями (простой и токсической), пилоростенозом.
Лечение. Наиболее рациональной терапией адреногенитального синдрома на почве врожденной гиперплазии надпочечников является назначение кортикостероидных препаратов (кортизона и его производных), так как в основе заболевания лежит дефицит продукции кортизола (гидрокортизона) и минералокортикоидов.
По достижении эффекта лечение продолжают поддерживающими дозами кортикостероидов, руководствуясь уровнем экскреции в мочу 17-кетостероидов. Из производных кортизона весьма эффективны преднизон и преднизолон. Их преимущество перед кортизоном состоит в более активном подавлении секреции АКТГ гипофизом, они мало задерживают соль в организме, хорошо переносятся детьми. Лечение поддерживающими дозами кортизона или преднизолона у мальчиков должно проводиться до окончания периода полового созревания, а у девочек – всю жизнь. Девочкам с выраженными дефектами строения наружных половых органов производят пластические операции.
При сольтеряющей форме с резко выраженной дегидратацией организма необходимо парентеральное введение физиологического раствора в смеси с 5 % раствором глюкозы, кортизона и дезоксикортикостерона (ДОКСА). Гипертензивные формы не требуют назначения ДОКСА и других гормонов, так как они задерживают натрий и воду. В таких случаях ограничиваются назначением преднизолона. При адреногенитальном синдроме, в основе которого лежит опухоль надпочечников, проводится хирургическое лечение.
Поделитесь на страничкеСледующая глава >
info.wikireading.ru
Надпочечники у детей: лечение, строение, функции
Такой синдром, как надпочечниковая недостаточность у детей встречается довольно редко, не имеет характерных проявлений и представляет серьезную угрозу для жизни ребенка. Заболевание может быть как врожденным, так и приобретенным. Гипофункция надпочечников проявляется в том, что гормоны, которые выделяются органами, вырабатываются в недостаточном количестве. Это и влечет за собой сбои в обменных процессах вплоть до развития смертельных процессов.

Строение и функции надпочечников у детей
Органы состоят из двух слоев: корковый наружный слой и мозговой внутренний. Функциональная часть коры органа отвечает за переработку стероидов. Взаимодействие стероидов и холестерина обеспечивает производство гормонов, основной функцией которых является регуляция обмена веществ в организме. Таким образом, надпочечники участвуют в производстве сложных биовеществ, аналогов которых не существует в природе.
Вернуться к оглавлениюУ каждого ребенка с момента рождения до десятого дня жизни существует угроза развития патологии как недостаточность надпочечников.
Возможные проявления заболевания
Врожденная агенезия, слияние
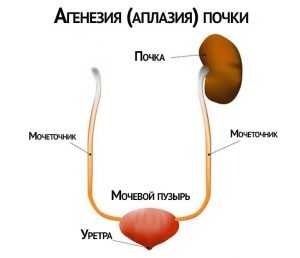 Врожденная аплазия почек у маленьких детей является редким заболеванием.
Врожденная аплазия почек у маленьких детей является редким заболеванием.Отклонение представляет собой отсутствие развития органа. Диагностируется достаточно редко, но в случаях подтверждения диагноза исход болезни летальный. Еще в более редких случаях отмечается слабое развитие одного органа, но если второй орган полностью берет на себя работу первого, то проявление проблемы может отсутствовать вовсе. Зафиксированы такие патологии, как сращивание надпочечников. Слияние может происходить как с аортой (в передней или задней части), так и с близлежащими органами — печень или почки. В случае аномального развития брюшной стенки надпочечники могут сращиваться даже с легкими.
Вернуться к оглавлениюАдренолейкодистрофия
Относится к наследственной патологии, которое проявляется в разрушении нервных клеток головного мозга на уровне мембраны. При адренолейкодистрофии организм не может самостоятельно расщеплять жирные кислоты, что влечет за собой поражение нервной системы и сбои в работе надпочечников. По статистике подобная патология поражает чаще мужчин, но носителем, предрасполагающим к развитию патологии, являются женщины. У детей патология развивается стремительно, и если вовремя не начать лечение, летальный исход наступает через 7—10 лет.
Вернуться к оглавлениюНадпочечниковая недостаточность
Острое и хроническое течение патологии опасно резким снижением выработки необходимых гормональных веществ. В результате этого процесса снижается концентрация хлорида и ионов натрия, вследствие невозможности их всасывания в кишечник. Постепенно происходит снижение жидкости в теле, сгущается кровь, у почки ослабевает функция фильтрации от токсических веществ. Когда подобные нарушения в выработке гормонов имеют постоянную природу, патология приобретает хроническую форму.
Вернуться к оглавлениюПервичный гиперальдостеронизм
Избыток альдостерона провоцирует появление первичного гиперальдостеронизма.Основной проблемой этого процесса является избыточная выработка альдостерона, который отвечает за выведение почками калия и регулирование уровня натрия. Когда гормон вырабатывается в избытке, нарушается действие фермента ренина, который, в свою очередь, ответственен за сужение сосудов и балансировку кровяного давления. Как следствие давление резко повышается, развивается процесс дефицита полезных элементов (магний и калий). Недостаточная концентрация калия в крови приводит к сердечным патологиям, головным болям и ночным судорогам. На фоне этого процесса понижаются показатели кальция, что опасно приступами нехватки воздуха, онемением рук и ног.
Вернуться к оглавлениюПрепараты с повышенным содержанием калия и кальция в этом случае неэффективны, так как концентрация элементов в организме достаточная, но вследствие патологической активности надпочечников, они не усваиваются.
Врожденная гиперплазия коры надпочечников
Эта патология влечет за собой целый спектр различных проблем. Происходят сбои в работе коры надпочечников и как следствие — блокируется белок. В результате этого процесса у больного происходит гиперплазия, которая заключается в увеличении количества клеток, после чего орган увеличивается в размерах. Заболевание приводит к развитию надпочечниковой недостаточности, которая провоцирует нарушение в развитии детей в будущем, вплоть до появления бесплодия.
Вернуться к оглавлениюКровоизлияние
Кровоизлияние – часто встречаемая проблема.В случае инфицирования, сепсиса или различного рода родовых травм у недоношенных детей может появиться кровоизлияние в надпочечники. Подобные проблемы приводят к весьма серьезным последствиям: от омертвения отдельных участков тканей до формирования кист. Бывают случаи двусторонних кровоизлияний, такие моменты обычно становятся причиной смерти пациента.
Вернуться к оглавлениюОпухолевые образования
Если речь идет об опухолевых поражениях надпочечников, то, как правило, это доброкачественные образования. Подобные новообразования имеют тенденцию разрастаться как во внешнем, так и во внутреннем слое. Основной метод лечения патологических формирований — удаление их хирургическим путем. В этом случае больному также не обойтись без поддерживающей медикаментозной терапии. Если запустить процесс, опухоли будут расти, а это может привести к развитию сахарного диабета, почечной недостаточности и прочих патологий, опасных для жизни пациента.
Вернуться к оглавлениюРак (адренокортикальный)
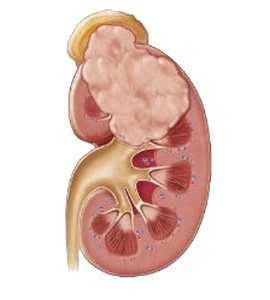 Онкологическая опухоль – встречается у детей подросткового возраста.
Онкологическая опухоль – встречается у детей подросткового возраста.Адренокортикальный рак сложно поддается диагностике и еще сложнее лечению. В группу риска попадают дети до 6-ти лет, в очень редких случаях патология фиксируется у подростков до 15-ти лет. Сказать, что именно провоцирует болезнь, и какие характерные симптомы проявления сложно, поэтому чаще всего диагностируется на позднем сроке, когда лечение теряет свою эффективность.
Вернуться к оглавлениюФеохромоцитома
Патологии, спровоцированные такой опухолью, встречается достаточно редко. Из-за болезни в организме ребенка начинают избыточно синтезироваться вещества катехоламины. Все высшие нервные процессы, а также физическая активность регулируется под действием обменных процессов. Любые сбои, связанные с катехоламинами могут привести к серьезным патологиям нервной, эндокринной и сердечно-сосудистой системы.
Вернуться к оглавлениюНейробластома
Самое часто диагностированное злокачественное заболевание у детей. Из основных причин, влияющих на развитие недуга, кроме наследственной предрасположенности, врачи не обнаружили. Связь между появлением проблемы и влиянием внешних факторов не была зафиксирована. Основная доля детей, болеющих нейробластомой, входит в возрастной рубеж до 5-ти лет, но при этом зафиксированы случаи формирования новообразования у малышей до года, еще маловероятнее появление болезни у старших детей до 10-ти лет.
Вернуться к оглавлениюГанглионейробластома
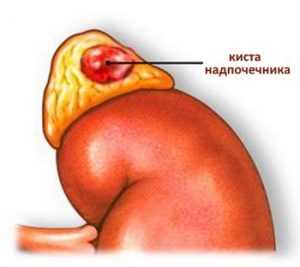 Такая патология сложно диагностируется.
Такая патология сложно диагностируется.Это злокачественная форма доброкачественного заболевания нервных узлов. Как и для прочих злокачественных образований, в случае гангионейробластомы установить четкую причину развития патологии сложно. Чаще всего к подобной болезни предрасположены дети от 6-ти до 10-ти лет. Патология развивается спонтанно, характерные симптомы заключаются в расстройствах пищеварительной системы, малокровии, лихорадочных приступов. Патология опасна проявлением метастазов в других органах, поэтому лечение должно наступить незамедлительно.
Вернуться к оглавлениюКисты надпочечника
Спонтанное и достаточно редко диагностируемое заболевание в виде кист развивается абсолютно бессимптомно, так что длительный промежуток времени больной может даже не догадываться о существовании проблемы. Подобные отклонения врачи выявляют при ультразвуковом обследовании, как правило, случайно. Кистозные образования у детей встречают довольно редко и не оказывают влияния на работу надпочечников.
Вернуться к оглавлениюМетоды диагностики
Самый простой и безвредный метод.Подтверждение должно проходить с учетом заключений лабораторных исследований и инструментального исследования. Если у ребенка есть подозрение на развитие надпочечниковой недостаточности, необходимо провести комплекс лабораторных анализов: диагностика на гормоны, проверка электролитного состава крови пациента и других ферментов. Вдобавок к проведению анализов больному назначают:
- ультразвуковое исследование органов малого таза;
- рентген;
- ЭКГ;
- магнитно-резонансная томография и другие.
Вернуться к оглавлениюДети обязаны проходить плановую проверку у эндокринолога 2 раза в год, чтобы исключить риск перерождения в злокачественные формы болезни, при которых шанс на выживание минимальный.
Лечение и профилактика
Подход к устранению недостаточности надпочечников зависит в первую очередь от формы проявления. Если речь идет об острой недостаточности, то лечение проводится в реанимационном отделении с применением препаратов различного действия для регулировки электролитного дисбаланса, а в отдельных случаях устранения шока и кровоизлияний. Больному назначают гормоны, препараты для снижения уровня сахара, а в случае наличия инфекции — глюкокортикоиды. Хроническая форма лечится с пожизненным применением медикаментов, функция которых заключается в постоянном поддерживании организма необходимыми элементами. При своевременном лечении проявления заболевания ребенок имеет все шансы на полноценную жизнь.
Судя по тому, что вы сейчас читаете эти строки — победа в борьбе с почечными заболеваниями пока не на вашей стороне…
И вы уже думали о хирургическом вмешательстве? Оно и понятно, ведь почки — очень важный орган, а их правильное функционирование- залог здоровья и хорошего самочувствия. Слабость, отечность, потеря аппетита, боли в спине и пояснице… Все эти симптомы знакомы вам не понаслышке.
Но возможно правильнее лечить не следствие, а причину? Рекомендуем прочитать историю Галины Савиной, как она вылечила почки… Читать статью >>
ВАЖНО ЗНАТЬ! Даже ‘запущенные’ почки лечатся дома, без операций и уколов. Просто прочитайте что сделала Галина Савина читать далее…
prourinu.ru
НАДПОЧЕЧНИКОВАЯ НЕДОСТАТОЧНОСТЬ — Синдромная диагностика в педиатрии (Баранов А.А. (ред.))
Клинические и лабораторные признаки надпочечниковой недостаточности возникают при уменьшении или прекращении секреции гормонов корой надпочечников.
Функция коры надпочечников имеет жизненно важное значение, поскольку синтезируемые ею гормоны обладают очень широким спектром действия. Минералокортикоиды (альдостерон и др.) регулируют электролитный гомеостаз организма и объем эк-страцеллюлярной жидкости, стимулируют реабсорбцию ионов натрия и экскрецию ионов калия, водорода, аммония и магния в канальцах почек. Глюкокортикоиды (гидрокортизон и кортикос-терон) принимают участие в регуляции углеводного, белкового, жирового и водно-электролитного обмена, АД, оказывают противовоспалительное, противоаллергическое и иммуносупрессивное действие, подавляют размножение и активность фибробластов, вызывают усиленную секрецию хлористоводородной кислоты и пепсина. Андрогены влияют на развитие наружных половых органов и вторичных половых признаков, обладают выраженным анаболическим свойством. В коре надпочечников также синтезируются следовые количества женских половых гормонов — эстрогенов. Гормоны коры надпочечников способствуют адаптации
Организма к меняющимся условиям внешней среды, в том числе в экстремальных условиях. Яркие клинические симптомы первичной надпочечниковой недостаточности, обусловленные дефицитом в первую очередь альдостерона и кортизола, появляются после деструкции не менее 90 % коркового вещества обоих надпочечников. Вторичная недостаточность коры надпочечников возникает в результате неспособности гипофиза секретировать АКТГ (секреция альдостерона при этом не нарушается).
Различают острую и хроническую недостаточность надпочечников.
Острая недостаточность надпочечников
Это тяжелое общее состояние, угрожающее жизни больного, которое развивается при внезапном резком снижении функции надпочечников на фоне стресса. Надпочечниковые, или аддисонические, кризы развиваются чаще на фоне первичной или вторичной хронической недостаточности надпочечников или их латентной гипофункции.
Острая недостаточность надпочечников может возникнуть при повреждении коры надпочечников вследствие травмы или кровоизлияния. Кровоизлияние в кору надпочечников Часто развивается у новорожденных, особенно у недоношенных, вследствие внутриутробной гипоксии плода, асфиксии и родовой травмы, вирусных и бактериальных инфекций. У детей старшего возраста подобные кровоизлияния наблюдаются реже. Они возможны при стрессах, объемных операциях, сепсисе, ожогах, лечении препаратами АКТГ и антикоагулянтами, а также при заболеваниях крови, злокачественных опухолях, СПИДе.
Причиной острой надпочечниковой недостаточности может быть геморрагический инфаркт надпочечников вследствие тромбоза или эмболии вен последних — Синдром Уотерхауса—Фридерик-сена. Этот синдром развивается чаще всего на фоне менингокок-ковой, реже пневмо- или стрептококковой бактериемии и полиомиелита. Инфаркты надпочечников также могут развиться при вас-кулитах. Надпочечниковая недостаточность возможна у детей с лимфатико-гипопластическим диатезом, гипотрофией.
При быстрой отмене глюкокортикостероидов у больных, длительно их получавших, возникает «синдром отмены», Протекающий как острая надпочечниковая недостаточность. Удаление надпочечника, Пораженного гормонально-активной опухолью, может обусловить острую надпочечниковую недостаточность в связи с атрофией парного органа.
Клиническая картина. Для развития острой надпочечниковой недостаточности на фоне хронической характерен период предвестников — усиление всех основных симптомов заболевания. При аддисоническом кризе развернутая картина острой недостаточности формируется в течение 2—3 дней. Заболевание характеРизуется нарастающей слабостью, вялостью, бледностью, отсутствием аппетита, тошнотой, нередко рвотой, болями в области живота, повышением температуры тела, развитием одышки. Кожа становится цианотичной, холодной на ощупь. У 73 больных на коже нижних конечностей, живота, грудной клетки появляются темно-синие пятна, имеющие сходство с экхимозами. Они в последующем увеличиваются и сливаются между собой. Отмечаются прогрессивное падение систолического АД ниже его порогового значения (60 мм рт. ст.), нитевидный пульс, поверхностное дыхание (или типа Чейна—Стокса), глухие тоны сердца. Развивается сопор, переходящий в кому, с тоническими судорогами. Температура тела снижается до субнормальной. Появляются признаки ДВС-синдро-ма: вначале рвота «кофейной гущей», затем макрогематурия и кровотечение из мест инъекций. Иногда развивается картина острого живота и динамической непроходимости кишечника. При прогрес-сировании процесса возможен летальный исход.
Симптомы острой надпочечниковой недостаточности при кровоизлиянии в надпочечники или их некрозе развиваются в течение 3—5 ч. Смерть нередко наступает уже в первые сутки.
Среди клинических форм острой надпочечниковой недостаточности выделяют кризы, протекающие с преобладанием сердечнососудистой декомпенсации, желудочно-кишечных или нервно-психических расстройств.
При сердечно-сосудистой форме преобладают симптомы сосудистой недостаточности: снижение АД и температуры тела, слабый пульс, глухие сердечные тоны, цианоз. В дальнейшем развивается коллапс. Желудочно-кишечные расстройства характеризуются анорексией, отвращением к пище, тошнотой, рвотой (в некоторых случаях неукротимой), жидким стулом. Многократная рвота и жидкий стул могут привести к обезвоживанию организма. Характерным симптомом являются боли разлитого характера в области живота. Иногда развивается картина острого живота с симптомами, характерными для острого аппендицита, панкреатита, холецистита, прободной язвы, кишечной непроходимости, в связи с чем ошибочно предпринимается оперативное вмешательство.
Церебральные нарушения проявляются повышенной возбудимостью, эпилептиформными судорогами, менингеальными симптомами, бредом со зрительными галлюцинациями или депрессией, адинамией, астенией, заторможенностью, затемнением сознания, ступором. Нарушения деятельности ЦНС обусловлены отеком мозга, изменениями электролитного баланса, гипогликемией. Ги-перкалиемия приводит к нарушению нервно-мышечной возбудимости, появлению парестезии, проводниковых расстройств поверхностной и глубокой чувствительности. Мышечные судороги развиваются в результате уменьшения внеклеточной жидкости. В крови у больных определяются лейкоцитоз, эозинофилия, лимфоци-тоз, гипогликемия, гипохолестеринемия, гиперкалиемия, гипонат-риемия, метаболический ацидоз.
Преходящая недостаточность коры надпочечников может наблюдаться у детей грудного возраста при различных токсикозах и ток-сико-септических состояниях. Заболевание в таких случаях сопровождается вялостью, токсикозом, эксикозом и принимает затяжное течение.
Лечение. При острой надпочечниковой недостаточности показаны:
▲ немедленная госпитализация ребенка в отделение реанимации или интенсивной терапии;
▲ срочное внутривенное введение гидрокортизона в дозе 3—5 мг/кг;
▲ одновременно такую же дозу гидрокортизона вводят внутримышечно;
▲ при отсутствии эффекта через 20—30 мин внутривенную инъекцию гидрокортизона повторяют в той же дозе с добавлением 0,1 мг/кг дезоксикортикостерона ацетата (ДОКСА) и гипертонического раствора натрия хлорида (3—5 мл/кг) для повышения чувствительности сосудистой стенки к гормональным препаратам;
▲ при отсутствии эффекта внутривенно капельно вводят допамин с начальной скоростью 8—10 мкг/кг/мин, или 0,2 % раствор нор-адреналина, или 1 % раствор мезатона;
▲ каждые 5 мин необходимо измерять АД. В связи с развитием воЛемии и дегидратации показана инфузионная терапия;
▲ после стабилизации гемодинамики проводят поддерживающую гормональную терапию. В 1-е сутки дозу гидрокортизона рассчитывают следующим образом: дозу, введением которой удалось стабилизировать гемодинамику, делят на время, потребовавшееся для этого, в часах. Полученную почасовую дозу умножают на 24. Со 2-х суток дозу уменьшают, переходя только на внутримышечное введение препарата. Параллельно корригируют нарушения обмена — гипогликемию, метаболический ацидоз, электролитный баланс.
Хроническая недостаточность надпочечников
Болезнь Аддисона (бронзовая болезнь) у детей наблюдается относительно редко. Ранее считали, что наиболее часто причиной хронической надпочечниковой недостаточности является туберкулез надпочечников. В последующем было показано, что в развитии деструктивной атрезии коры надпочечников существенную роль играют аутоиммунные, а также токсические и генетические факторы.
Хроническая надпочечниковая недостаточность развивается у детей в самом раннем возрасте при врожденной гипоплазии или аплазии коры надпочечников, врожденной дисфункции коры надпочечников (адреногенитальном синдроме), семейной сниженной чувствительности к АКТГ, болезни Вольмана. Однако у новорожденных возможно временное нарушение биосинтеза гормонов под влиянием разных причин, что требует многократного исследования секреции гормонов в динамике. У детей более старшего возРаста причинами хронической надпочечниковой недостаточности являются аутоиммунное поражение надпочечников, хронические инфекции (в том числе туберкулез), интоксикации (например, инсектицидами), амилоидоз, гемохроматоз, опухоли, некоторые острые инфекционные заболевания, а также длительное лечение хло-дитаном, кетоконазолом.
Вторичный гипокортицизм Возникает при поражении гипофиза или гипоталамуса, а также при подавлении секреции АКТГ (при лечении глюкокортикостероидами), гиперкортицизме у матери во время беремен-ности, после удаления активно функционирующей опухоли надпочечника.
Клиническая картина. Больные с хронической надпочечниковой недостаточностью жалуются на общую слабость, быструю утомляемость, снижение аппетита, похудание. Для них характерна высокая потребность в соли, поэтому дети любят соленое. Характерным признаком первичной надпочечниковой недостаточности, не встречающимся при ее вторичной форме, является пигментация кожи, которая приобретает оттенок от светло-коричневого до темно-бронзового. Пигментация чаще бывает генерализованной, но она обычно более выражена на открытых участках тела. Характерны симптом «грязных локтей и коленей», потемнение слизистых оболочек, наличие каймы на деснах и языке в виде отдельных пятен. Пигментация усилена в области половых органов, сосков молочных желез, а также на участках кожи, подвергающихся давлению и трению, в области рубцов и царапин. Потемнение кожи почти всегда служит одним из первых признаков заболевания. У 5—20 % детей при первичной надпочечниковой недостаточности наблюдаются депигментированные участки (вити-лиго). Важным симптомом заболевания является также стойкое снижение АД. Дети жалуются на головокружения, у них бывают обморочные состояния. Нарушение анаболических процессов вызывает уменьшение массы тела, снижение мышечной силы. Эти дети плохо переносят физическую нагрузку. Часто отмечаются боли в животе, рвота и понос, что может привести к обезвоживанию. При обследовании выявляются гипацидный гастрит, спастический колит, эрозивно-язвенное поражение желудка и двенадцатиперстной кишки. Желудочно-кишечные симптомы также обусловлены электролитными нарушениями.
У этих детей обычно ослаблена память, заторможены мыслительные процессы, нарушен сон, они безразличны к окружающему, негативны. В период кризов отмечаются нарушения электролитного баланса (гиперкалиемия, гипонатриемия и гипохлоремия). Ги-перкалиемия может вызвать функциональные расстройства сердечной деятельности вплоть до остановки сердца.
При снижении секреции глюкокортикостероидов у больного нарушается глюконеогенез, отмечаются более низкие показатели глюкозы в крови, плоская сахарная кривая. При голодании или вследствие инфекционных заболеваний у этих больных легко разВиваются гипогликемические кризы. Характерны задержка роста и созревания скелета, отставание в половом развитии, снижение иммунитета, присоединение инфекционных заболеваний. В крови уменьшается количество эритроцитов, содержание гемоглобина, отмечается лимфоцитоз. Снижена относительная плотность мочи, в ней обнаруживают белок и цилиндры.
Диагностика основывается на анамнестических, клинических и лабораторных данных. Об уменьшении секреции глюкокор-тикостероидов свидетельствует появление гипогликемии, адинамии, общей слабости. Кроме того, у этих больных отмечаются гиперплазия лимфоидной ткани, гиперпигментация кожи, уменьшение размеров сердца. Снижение продукции минералокортикоидов обусловливает низкое АД, головокружение, похудание, нарушение деятельности желудочно-кишечного тракта, гиперкалиемию и гипонатри-емию, усиленное выделение натрия с мочой. При вторичной над-почечниковой недостаточности эти симптомы обычно отсутствуют. В связи с низкой секрецией андрогенов происходят атрофия кожи, выпадение волос, снижение мышечной силы, задержка роста и полового развития, похудание.
С помощью КТ — и МРТ-исследования, эхографии можно определить размеры и структуру надпочечников, выявить кальцинаты и другие очаговые изменения. Диагноз аутоиммунного адреналита ставят на основании обнаружения антител к ткани надпочечников. Для оценки функционального состояния коры надпочечников исследуют содержание в крови и моче АКТГ, кортизола и альдосте-рона, экскрецию 17-ОКС и И-КС с мочой.
Для подтверждения диагноза проводят специальные тесты:
▲ проба со стимуляцией АКТГ короткого действия позволяет выявить имеющиеся, а с пролонгированным АКТГ — потенциальные резервы коры надпочечников;
▲ проба с метапироном позволяет определить резервы эндогенного АКТГ и реакцию коры надпочечников на введение АКТГ;
▲ проба с введением инсулина способствует выявлению у больных хронической надпочечниковой недостаточностью повышенной чувствительности даже к малым дозам инсулина;
▲ проба на чувствительность к стероидам основана на эозинопе-ническом эффекте.
Лечение. Детям с хронической надпочечниковой недостаточностью показана постоянная пожизненная заместительная терапия глюко — и минералокортикоидами. Экзогенное введение стероидов подавляет секрецию АКТГ гипофизом, приводя Ко вторичной надпочечниковой недостаточности. После отмены длительно проводимого лечения кортикостероидами наблюдается угнетение ги-поталамо-гипофизарно-надпочечниковой системы в течение 1 года и более, поэтому больные нуждаются во введении гормонов при стрессовых ситуациях, например, при хирургическом вмешательстве. В этих случаях вводят гидрокортизон в дозе 12—15 мг/м2.
wume.ru
Заболевания надпочечников у детей, Эндокринология, Детская эндокринология
(Средняя оценка: 5)
Надпочечники вырабатывают определенные гормоны, которые регулируют многие процессы в организме. Нарушение нормальной работы надпочечников может привести к развитию тяжелого состояния. Патология надпочечников связана со снижением или повышением уровня гормонов в крови.
Каждая гормональная железа вырабатывает гормональный секрет (химическое соединение), попадающий в кровоток. Гормоны надпочечников участвуют в обмене веществ (комплексе всех химических, физических и энергетических процессов, происходящих в живых тканях и клетках), поддержании водного обмена путем регулирования содержания солей, регулировании роста волос на лобке, в подмышечных впадинах и на лице (так называемая половая растительность) и функциональной активности вегетативной нервной системы.
Источник
U-mama.ru
Мне нравится
Нравится
Твитнуть
+1
Одноклассники
Задать вопрос врачу
Приобрести эффективные лекарства для лечения этого заболевания
www.medkrug.ru
