Перинатальное поражение центральной нервной системы (ППЦНС) – это группа патологий, при которых нарушается нормальная работа спинного головного мозга у новорожденных. Процесс может развиваться по разным причинам, одной из них является гипоксия, то есть кислородное голодание. Перинатальный период включает последний триместр беременности, роды и первую неделю жизни ребенка. За это время организм испытывает стресс при переходе на легочное дыхание, а также при адаптации к различным факторам окружающей среды, поэтому гипоксически-ишемическое поражение ЦНС – частый диагноз. 10% новорожденных испытывают дефицит кислорода в разной степени, особенно недоношенные. Состояние требует срочной медицинской помощи, но в 80% случаев имеет благоприятный исход и никак не отражается на дальнейшем развитии ребенка.
Механизм развития гипоксии
Центральная нервная система – это головной и спинной мозг. Эти структуры способны нормально функционировать только при достаточном поступлении кислорода, который переносится с кровью. У новорожденных и детей младшего возраста потребность в кислороде значительно выше, чем у взрослых, а его дефицит может становиться причиной серьезной задержки физического и умственного развития. Поражение ЦНС ишемического генеза связано с недостаточным кровоснабжением тканей головного мозга, в связи с чем наблюдается постепенное отмирание нервных клеток.
Гипоксией называется нехватка кислорода в тканях. При перинатальном поражении это происходит во время беременности, при родах и в первые дни жизни ребенка. Состояние обратимо, поскольку в младшем возрасте процессы регенерации протекают быстрее. Со временем можно нейтрализовать пагубное влияние кислородного голодания и восстановить нервную проводимость. Ишемия – более опасное состояние. Этот термин подразумевает полное прекращение поступления кислорода в клетки, что приводит к их быстрому некрозу.
Причины поражения ЦНС
Основная причина заболевания – это ишемическая гипоксия, то есть повреждение клеток нервной системы из-за их недостаточного кровоснабжения. Тип нарушений зависит от ряда факторов, в том числе от длительности кислородного голодания. Так, при острой гипоксии повреждаются стволовые части и подкорковые структуры, при длительном дефиците кислорода – кора головного мозга. Процесс развивается в период внутриутробного развития и сразу после рождения, а его причинами могут становиться следующие факторы:
- со стороны матери: различные нарушения кровообращения в матке, обильные кровотечения, различные патологии развития плаценты;
- во время беременности: вредные привычки, системный прием некоторых групп препаратов;
- во время родов: обвитие пуповины, массивные кровопотери у матери, пониженное артериальное давление и низкий пульс у ребенка;
- в первые дни жизни: пороки сердца и врожденные заболевания системы дыхания, ДВС-синдром и другие патологии.
Различные патологии сердечно-сосудистой системы являются пусковым механизмом к развитию гипоксически-ишемического поражения ЦНС. Дефицит кислорода в артериальной крови вызывает его нехватку в нервной ткани. Так возникает некроз (отмирание) некоторых нервных клеток либо их групп. В таком состоянии снижение артериального давления провоцирует ухудшение ситуации, может приводить к хронизации процесса и необратимым изменениям. Из-за замедления обмена веществ происходит ацидоз (окисление) клеток, что становится причиной отечности. Ишемические изменения часто включают повышение внутричерепного давления, а также патологии внутренних органов (легких, почек, печени).
СПРАВКА! Под ишемически-гипоксическим поражением ЦНС подразумевают необратимые изменения в тканях головного мозга, вызванные их недостаточным кровоснабжением. Менее опасные нарушения чаще классифицируют как гипоксически-ишемическую энцефалопатию, но эти термины могут быть взаимозаменяемы.
Признаки
Клиническая картина ишемического синдрома индивидуальна для каждого пациента. Она проявляется в зависимости степени и длительности гипоксии. Стоит отметить, что прогноз в детском возрасте в большинстве случаев благоприятный. Центральная нервная система обладает свойствами регенерации, поэтому осложнения развиваются только на последних стадиях.
Диагноз можно поставить уже на первых минутах жизни, особенно если болезнь проявляется в тяжелой форме
Тяжесть состояния больного оценивают по шкале Апгар. Она включает ряд показателей, в том числе пульс и дыхание, состояние кожи, выраженность рефлексов. Так, поражение головного мозга гипоксического генеза можно диагностировать непосредственно после рождения. Выделяют 3 основные степени болезни, третья из которых наиболее опасна.
1 степень
При гипоксическом повреждении ЦНС первой степени симптомы выражены незначительно. Общее состояние ребенка оценивается на 6–7 баллов (оптимальным результатом считается оценка 7–10 баллов). Клиническая картина включает следующие признаки:
- бледность, синюшность кожи;
- ухудшение мышечного тонуса, тремор;
- беспокойный сон;
- активизация либо ухудшение рефлексов.
Повреждения первой степени не представляют опасности для пациента. Уже в течение первой недели жизни все показатели возвращаются в норму, а далее ребенок развивается наравне со сверстниками.
2 степень
Вторая степень поражения головного мозга чаще возникает при гипоксии как во время беременности, так и при родах. По шкале Апгар состояние ребенка можно оценить на 5 баллов. Патологический процесс проявляется следующими симптомами:
- недостаточность рефлексов;
- повышение либо снижение мышечного тонуса;
- выраженный цианоз кожи и слизистых оболочек;
- повышение внутричерепного давления – этот показатель продолжает увеличиваться, проявляется выпиранием родничков, расстройствами сна, непроизвольными движениями мышц;
- вегетативные нарушения, в том числе аритмии, замедление сердечного ритма, апноэ (остановки дыхания), проблемы с работой органов пищеварительного тракта.
ВАЖНО! В первые дни жизни ребенка важно следить за показателями внутричерепного давления. При своевременном лечении состояние может улучшиться к концу первой недели жизни, при его отсутствии – болезнь прогрессирует.
3 степень
Поражение ЦНС третьей степени – это последствие гестозов во второй половине беременности. Состояние ребенка осложняется при аномальных родах. Новорожденный нуждается в проведении реанимационных мероприятий, поскольку у него может отсутствовать дыхательная активность, резко выражены патологии сердечно-сосудистой системы. Рефлексы отсутствуют, в том числе глотательный, поэтому кормление естественным способом невозможно. Часто у таких пациентов диагностируют почечную и печеночную недостаточность, ДВС-синдром (патологию свертывания крови).
Этапы развития болезни и прогноз
В развитии заболевания выделяют несколько стадий. Установлено, что наиболее эффективно лечение в первую неделю жизни ребенка – именно за это время происходит наиболее интенсивное восстановление функций. Каждый этап характеризуется определенной клинической картиной, а их выраженность указывает на тяжесть патологии.
Острый период
Острым считается период с рождения ребенка и до первого месяца жизни. Вне зависимости от сложности его состояния, лечебные мероприятия лучше проводить именно в это время, чтоб избежать отдаленных последствий. Клиническая картина отличается, но может включать следующие синдромы:
- гипертензионно-гидроцефальный – повышение внутричерепного давления за счет нарушения оттока жидкости из желудочков головного мозга;
- судорожный – непроизвольные мышечные сокращения;
- вегетативно-висцеральный – у ребенка появляется мраморный оттенок кожи, а также различные нарушения работы пищеварительного тракта, сердца и сосудов;
- апатии – рефлексы замедлены, мышечный тонус снижен;
- повышение нервной возбудимости, что проявляется повышением либо снижением тонуса мышц;
- коматозный – наиболее опасный признак гипоксии головного мозга.
Первые улучшения должны появиться в течение первой недели. Лечение проводится в стационаре, а в тяжелых случаях – в реанимационном отделении. Основная цель – нормализовать кровоснабжение головного мозга и препятствовать отечности тканей.
Восстановительный период
Восстановительный этап длится до года, у недоношенных детей – до двух лет. Вначале появляются заметные улучшения: нормализуются рефлексы и тонус мышц, исчезает цианоз тканей. Однако, болезнь может протекать с обострениями, особенно при второй и третьей стадиях. Стоит помнить, что при нарушении питания головного мозга у ребенка может наблюдаться отставание в росте и психическом развитии, но с возрастом эти изменения исчезнут. На этом этапе необходимо делать акцент на постоянном наблюдении за пациентом, а также на проведении реабилитационных мероприятий (массаж, гимнастика).

Лечение в домашних условиях невозможно, поскольку ребенку необходимо быстро восстанавливать мозговое кровообращение и находиться под постоянным наблюдением
Исход заболевания
Дальнейшее состояние пациента можно прогнозировать в годовалом возрасте. К этому времени уже не должны быть заметны отличия в росте и развитии, особенно при легкой степени. Исход зависит от своевременности терапии и типа нарушений, вызванных гипоксией, и может быть следующим:
- полное выздоровление;
- неблагоприятным, с прогрессированием неврологической картины;
- инвалидность;
- латентное течение – симптомы проявляются с возрастом.
СПРАВКА! Даже при благоприятном исходе могут сохраняться такие отдаленные последствия, как задержка речи, гиперактивность, нарушения сна и перепады настроения. В тяжелых случаях возможно развитие гидроцефалии, эпилепсии и ДЦП.
Методы диагностики и лечения
Гипоксически-ишемическое поражение ЦНС выявляют непосредственно после рождения. На первом этапе проводят полный осмотр и диагностику рефлексов. При подозрении на поражение головного мозга дальнейшее обследование включает следующие методы:
- нейросонография – УЗ-исследование тканей головного мозга через родничок, возможно только у новорожденных;
- МРТ, КТ – наиболее информативные способы определения состояния ЦНС;
- электроэнцефалография – диагностика активности головного мозга;
- допплерография – исследование активности кровотока.
Лечение подбирается индивидуально и зависит от стадии патологии. Оно чаще проводится консервативными способами и заключается в использовании определенных групп препаратов:
- противосудорожные средства;
- ноотропы – лекарства для улучшения кровоснабжения головного мозга;
- мочегонные препараты для снижения внутричерепного давления;
- успокоительные средства на растительной основе (экстракт валерианы) при расстройствах сна;
- дополнительные методы по показаниям.
В восстановительный период полезно посещать сеансы лечебного массажа, делать пассивную гимнастику. Возможно, потребуется длительный систематический прием препаратов для улучшения мозгового кровообращения.
Заключение
Гипоксически-ишемическое поражение центральной нервной системы – это распространенный диагноз, но он чаще проявляется в легкой форме. Патология возникает из-за недостаточного кровоснабжения головного мозга в период внутриутробного развития плода и во время родов. Большинство детей (до 80%), которые при рождении имели подобные нарушения, ничем не отличаются от сверстников. Однако, недооценивать болезнь опасно, поскольку она может становиться причиной опасных последствий и нервных расстройств.
© Автор: А. Олеся Валерьевна, к.м.н., практикующий врач, преподаватель медицинского ВУЗа, специально для СосудИнфо.ру (об авторах)
Гипоксически-ишемическое поражение ЦНС у новорожденных представляет значимую проблему современной неонатологии, ведь по статистике едва ли не каждый десятый новорожденный малыш имеет те или иные признаки нарушения деятельности мозга в связи с гипоксией. Среди всех патологических состояний периода новорожденности гипоксические повреждения мозга занимают первое место. Особенно часто заболевание диагностируется у недоношенных детей.
Несмотря на довольно большую частоту патологии, до сих пор не разработаны эффективные меры борьбы с ней, а против необратимых структурных повреждений мозга современная медицина бессильна. Ни одно из известных лекарств не может восстановить погибшие нервные клетки головного мозга, однако исследования в этой области продолжаются, а препараты новейших поколений проходят клинические испытания.
ЦНС (центральная нервная система) очень чувствительна к недостатку кислорода в крови. У растущего плода и новорожденного ребенка незрелые структуры мозга нуждаются в питании еще больше, нежели у взрослого, поэтому любые неблагоприятные воздействия на будущую маму или сам плод во время беременности и родов могут оказаться пагубными для нервной ткани, что впоследствии проявится неврологическими нарушениями.
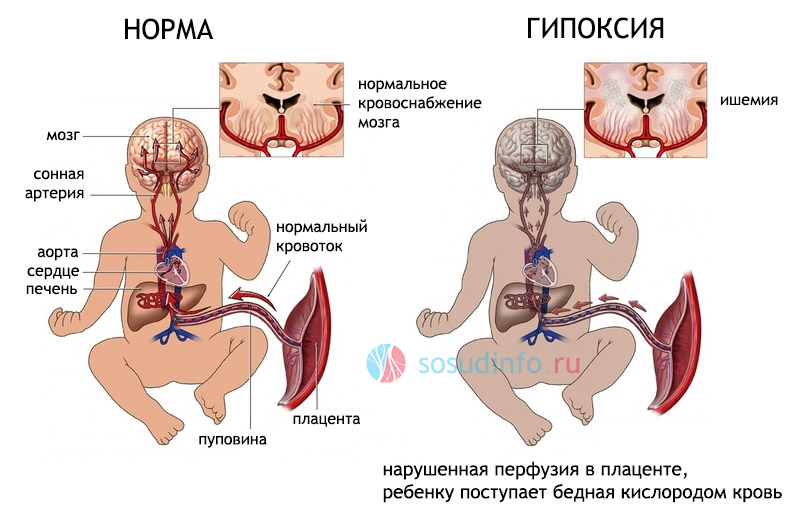

пример гипоксии из-за недостаточности маточно-плацентарного кровотока
Гипоксия может быть выраженной или легкой, она длится продолжительное время или несколько минут во время родов, но всегда провоцирует расстройства функции мозга.
В случае легких повреждений процесс вполне обратим, и через какое-то время после рождения мозг восстановит свою работу.
При глубокой гипоксии и асфиксии (полное прекращение поступления кислорода к мозгу) развиваются органические повреждения, зачастую служащие причиной инвалидизации маленьких пациентов.
Чаще всего гипоксия мозга возникает во внутриутробном периоде или в процессе родов при патологическом их течении. Однако и после рождения гипоксически-ишемические изменения могут возникнуть в случае нарушения дыхательной функции у малыша, падения артериального давления, нарушений свертывания крови и т. д.
В литературе можно встретить два названия описываемой патологии — гипоксически-ишемическое поражение ЦНС и гипоксически-ишемическая энцефалопатия (ГИЭ). Первый вариант чаще употребляют при диагностике тяжелых нарушений, второй — при легких формах повреждения мозга.
Дискуссии относительно прогнозов при гипоксическом поражении мозга не утихают, однако накопленный опыт специалистов-неонатологов показывает, что нервная система ребенка обладает рядом механизмов самозащиты и даже способна к регенерации. Об этом говорит и тот факт, что далеко не все дети, перенесшие тяжелую гипоксию, имеют грубые неврологические отклонения.
При тяжелой гипоксии страдают в первую очередь незрелые структуры стволовой части и подкорковые узлы, при длительной, но не интенсивной гипоксии развиваются диффузные поражения коры мозга. Один из факторов защиты мозга у плода или новорожденного — перераспределение кровотока в пользу стволовых структур, поэтому при длительной гипоксии и страдает в большей степени серое вещество мозга.
Задача неврологов при осмотре новорожденных, перенесших гипоксию разной степени тяжести, – объективно оценить неврологический статус, исключить адаптационные проявления (тремор, например), которые могут быть физиологичными, и выявить действительно патологические изменения в деятельности мозга. При диагностике гипоксического поражения ЦНС зарубежные специалисты основываются на стадийности патологии, российские врачи используют синдромный подход, указывая на конкретные синдромы со стороны той или иной части мозга.
Причины и стадии гипоксически-ишемического поражения
Перинатальное поражение ЦНС у новорожденных формируется при действии неблагоприятных факторов внутриутробно, в родах либо во время новорожденности. Причинами этих изменений способны стать:
- Расстройства кровотока в матке и плаценте, кровотечения у беременных, патология плаценты (тромбозы), отставание развития плода;
- Курение, употребление алкоголя, прием некоторых лекарственных препаратов во время беременности;
- Массивные кровотечения во время родов, обвитие пуповины вокруг шеи плода, выраженная брадикардия и гипотония у младенца, родовые травмы;
- После родов — гипотония у новорожденного, врожденные пороки сердца, ДВС-синдром, эпизоды остановки дыхания, нарушения функции легких.
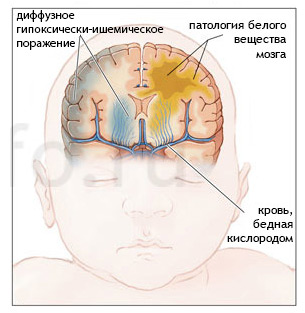

пример гипоксически-ишемического поражения мозга
Начальным моментом развития ГИЭ служит дефицит кислорода в артериальной крови, который провоцирует патологию метаболизма в нервной ткани, гибель отдельных нейронов или целых их групп. Головной мозг становится чрезвычайно чувствительным к колебаниям артериального давления, а гипотония только усугубляет имеющиеся поражения.
На фоне метаболических нарушений происходит «закисление» ткани (ацидоз), нарастает отек и набухание мозга, увеличивается внутричерепное давление. Эти процессы провоцируют распространенный некроз нейронов.
Тяжелая асфиксия отражается и на работе других внутренних органов. Так, системная гипоксия вызывает острую почечную недостаточность из-за некроза эпителия канальцев, некротические изменения слизистой кишечника, поражения печени.
У доношенных детей отмечают постгипоксическое поражение преимущественно в области коры, подкорковых структур, ствола мозга, у недоношенных ввиду особенностей созревания нервной ткани и сосудистого компонента диагностируется перивентрикулярная лейкомаляция, когда некрозы сконцентрированы преимущественно вокруг боковых желудочков мозга.
В зависимости от глубины ишемии мозга выделяют несколько степеней тяжести гипоксической энцефалопатии:
- Первая степень — легкая — преходящие нарушения неврологического статуса, продолжающиеся не более недели.
- ГИЭ второй степени — длится дольше 7 суток и проявляется угнетением либо возбуждением центральной нервной системы, судорожным синдромом, временным увеличением внутричерепного давления, вегетативной дисфункцией.
- Тяжелая форма гипоксически-ишемического поражения — расстройство сознания (сопор, кома), судороги, проявления отека мозга со стволовой симптоматикой и нарушением деятельности жизненно важных органов.
Симптоматика гипоксически-ишемического повреждения ЦНС
Поражение ЦНС у новорожденных диагностируется на первых минутах жизни младенца, при этом симптоматика зависит от выраженности и глубины патологии.

I степень
При легком течении ГИЭ состояние остается стабильным, по шкале Апгар ребенок оценивается не менее чем в 6-7 баллов, заметен цианоз, снижение тонуса мышц. Неврологические проявления первой степени гипоксического поражения ЦНС:
- Высокая нервно-рефлекторная возбудимость;
- Расстройства сна, беспокойство;
- Дрожание конечностей, подбородка;
- Возможны срыгивания;
- Рефлексы могут быть как усилены, так и снижены.
Описанные симптомы обычно проходят на протяжении первой недели жизни, ребенок становится более спокойным, начинает набирать вес, грубые неврологические расстройства не развиваются.
II степень
При гипоксии мозга средней тяжести признаки угнетения мозга более очевидны, что выражается в более глубоких расстройствах работы мозга. Обычно вторая степень ГИЭ сопровождает сочетанные формы гипоксии, которая диагностируется и в течение внутриутробного этапа роста, и в момент родов. При этом фиксируются глухие тоны сердца плода, учащение ритма либо аритмии, по шкале Апгар новорожденный набирает не более 5 баллов. Неврологическая симптоматика состоит в:
- Угнетении рефлекторной активности, в том числе сосательного;
- Снижении либо увеличении тонуса мышц, самопроизвольная двигательная активность может не проявляться в первые дни жизни;
- Выраженной синюшности кожных покровов;
- Нарастании внутричерепного давления;
- Вегетативной дисфункции — остановка дыхания, ускорение пульса или брадикардия, нарушения перистальтики кишечника и терморегуляции, склонность к запорам или диарее, срыгивания, медленный набор веса.
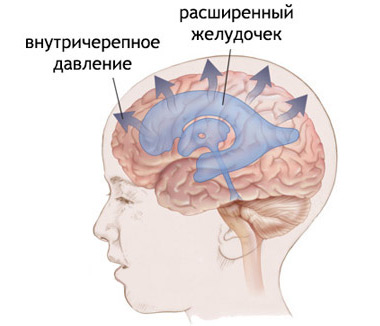

внутричерепная гипертензия, сопровождающая выраженные формы ГИЭ
По мере увеличения внутричерепного давления нарастает беспокойство малыша, появляется избыточная чувствительность кожи, нарушается сон, усиливается тремор подбородка, ручек и ножек, становится заметным выбухание родничков, характерен горизонтальный нистагм и глазодвигательные расстройства. Признаками внутричерепной гипертонии могут быть судороги.
К концу первой недели жизни состояние новорожденного со второй степенью ГИЭ постепенно стабилизируется на фоне интенсивного лечения, но неврологические изменения не исчезают полностью. При неблагоприятном стечении обстоятельств возможно ухудшение состояния с угнетением мозга, снижением мышечного тонуса и двигательной активности, истощением рефлексов, комой.
III степень
Перинатальное поражение ЦНС гипоксически-ишемического генеза тяжелой степени обычно развивается при тяжелых гестозах второй половины беременности, сопровождающихся высокой гипертензией у беременной, нарушением работы почек, отеками. На этом фоне новорожденный уже рождается с признаками гипотрофии, внутриутробной гипоксии, задержкой в развитии. Аномальное течение родов только усугубляет имеющиеся гипоксические повреждения ЦНС.
При третьей степени ГИЭ новорожденный имеет признаки выраженного нарушения кровообращения, дыхание отсутствует, тонус и рефлексы резко снижены. Без срочной сердечно-легочной реанимации и восстановления жизненно важных функций такой младенец не выживет.
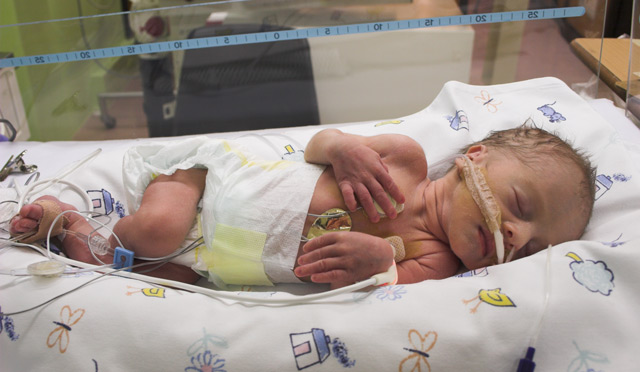

На протяжении первых часов после родов происходит резкое угнетение мозга, наступает кома, сопровождающаяся атонией, почти полным отсутствием рефлексов, расширением зрачков со сниженной реакцией на световой раздражитель или ее отсутствием.
Неизбежно развивающийся отек мозга проявляется судорогами генерализованного типа, остановкой дыхания и сердца. Полиорганная недостаточность проявляется повышением давления в системе легочной артерии, снижением фильтрации мочи, гипотонией, некрозом слизистой кишечника, печеночной недостаточностью, электролитными нарушениями, расстройствами свертывания крови (ДВС-синдром).
Проявлением тяжелого ишемического поражения ЦНС становится так называемый постасфиксический синдром — малыши малоподвижны, не кричат, не реагируют на боль и прикосновения, кожа у них бледно-синюшная, характерно общее снижение температуры тела. Важными признаками тяжелой гипоксии мозга считают расстройства глотания и сосания, что делает невозможным естественное кормление. Для спасения жизни таким пациентам необходима интенсивная терапия в условиях реанимации, но нестабильное состояние все же сохраняется до 10 дня жизни, а прогноз нередко остается плохим.
Особенностью течения всех форм ГИЭ считается нарастание неврологического дефицита с течением времени даже при условии интенсивной терапии. Это явление отражает прогрессирующую гибель нейронов, которые уже были повреждены во время нехватки кислорода, а также определяет дальнейшее развитие малыша.
В целом, ишемически-гипоксическое поражение ЦНС может протекать по-разному:
- Благоприятно с быстрой положительной динамикой;
- Благоприятное течение с быстрым регрессом неврологического дефицита, когда к моменту выписки изменения либо проходят остаются минимальными;
- Неблагоприятное течение с прогрессированием неврологических симптомов;
- Инвалидизация в течение первого месяца жизни;
- Скрытое течение, когда по прошествии полугода нарастают двигательные и когнитивные расстройства.
В клинике принято различать несколько периодов ишемической энцефалопатии новорожденных:
- Острый — первый месяц.
- Восстановительный — в пределах одного года.
- Период отдаленных последствий.
Острый период проявляется всей гаммой неврологических расстройств от едва заметных до коматозного состояния, атонии, арефлексии и др. В период восстановления на первый план выходит синдром избыточной нервно-рефлекторной возбудимости, судорожный синдром, возможна гидроцефалия, задержка интеллектуального и физического развития. По мере роста ребенка симптоматика меняется, некоторые симптомы исчезают, другие становятся более заметны (нарушения речи, например).
Лечение и прогноз при ГИЭ
Диагноз ГИЭ устанавливается на основании симптоматики, данных о течении беременности и родов, а также специальных методов исследования, среди которых чаще всего применяют нейросонографию, эхокардиографию, КТ, МРТ мозга, коагулограмму, УЗИ с допплерографией мозгового кровотока.
Лечение ишемических поражений ЦНС у новорожденных — большая проблема неонатологов, поскольку добиться регресса необратимых изменений нервной ткани не позволяет ни одно лекарственное средство. Тем не менее, хотя бы частично восстановить деятельность мозга при выраженных формах патологии все же удается.
Медикаментозное лечение ГИЭ проводится в зависимости от выраженности конкретного синдрома или симптома.
При легкой и средней степени заболевания назначается противосудорожная терапия, диуретики, ноотропы, тяжелая форма перинатальной энцефалопатии требует незамедлительных реанимационных мероприятий и интенсивной терапии.
 При повышенной возбудимости нервной системы без судорожного синдрома неонатологи и педиатры обычно ограничиваются наблюдением за ребенком, не прибегая к специфической терапии. В редких случаях возможно применение диазепама, но не длительно, так как употребление подобных препаратов в педиатрии чревато задержкой дальнейшего развития.
При повышенной возбудимости нервной системы без судорожного синдрома неонатологи и педиатры обычно ограничиваются наблюдением за ребенком, не прибегая к специфической терапии. В редких случаях возможно применение диазепама, но не длительно, так как употребление подобных препаратов в педиатрии чревато задержкой дальнейшего развития.
Возможно назначение фармакологических средств, оказывающих сочетанный ноотропный и тормозящий эффект на ЦНС (пантогам, фенибут). При нарушениях сна допускается применение нитразепама и растительных успокоительных средств — экстракт валерианы, мята, мелисса, пустырник. Хороший успокоительный эффект оказывают массаж, водолечение.
При тяжелых гипоксических поражениях помимо противосудорожных средств необходимы мероприятия по ликвидации отека мозга:
- Диуретики — фуросемид, маннитол, диакарб;
- Магния сульфат.
Нарушения дыхания и сердцебиения требуют незамедлительных реанимационных мероприятий, налаживания искусственной вентиляции легких, введения кардиотонических средств и инфузионной терапии.
При гипертензионно-гидроцефальном синдроме основное место в лечении занимают диуретики, а препаратом выбора для детей всех возрастов считается диакарб. Если медикаментозная терапия не приводит к желаемому результату, то показано оперативное лечение гидроцефалии — шунтирующие операции, направленные на сброс ликвора в брюшную или перикардиальную полости.
При судорожном синдроме и повышенной возбудимости ЦНС могут назначаться антиконвульсанты — фенобарбитал, диазепам, клоназепам, фенитоин. Новорожденным детям обычно дают барбитураты (фенобарбитал), грудным малышам — карбамазепин.
Синдром двигательных нарушений лечится при помощи препаратов, снижающих гипертонус (мидокалм, баклофен), при гипотонусе показан дибазол, галантамин в низких дозах. Для улучшения моторной активности пациента применяют массаж, лечебные упражнения, физиотерапевтические процедуры, водную и рефлексотерапию.
Запаздывание психического развития и становления речи соответственно возрасту ребенка становится заметным к концу первого года жизни. В таких случаях применяются ноотропные препараты (ноотропил, энцефабол), витамины группы В. Очень важную роль играют специальные занятия с педагогами и дефектологами, специализирующимися на работе с отстающими в развитии детьми.
Очень часто родители детей, перенесших перинатальную энцефалопатию, сталкиваются с назначением большого количества разнообразных препаратов, что далеко не всегда оправданно. Гипердиагностика, «перестраховка» педиатров и неврологов приводят к широкому назначению диакарба, ноотропов, витаминов, актовегина и других средств, которые не только не эффективны при легкой форме ГИЭ, но и часто противопоказаны по возрасту.
Прогноз при гипоксически-ишемических поражениях ЦНС вариабелен: возможны и регрессия мозговых нарушений с выздоровлением, и прогрессирование с инвалидизацией, и малосимптомная форма неврологических расстройств — минимальная мозговая дисфункция.
Отдаленными последствиями ГИЭ считаются эпилепсия, детский церебральный паралич, гидроцефалия, задержка умственного развития (олигофрения). Олигофрения всегда имеет стойкий характер, не регрессирует, а несколько запоздалое развитие психомоторной сферы на протяжении первого года жизни может со временем пройти, и ребенок не будет ничем отличаться от большинства своих сверстников.
Видео: о гипоксически-ишемическом поражении ЦНС и важности своевременного лечения
Вывести все публикации с меткой:Рекомендации читателям СосудИнфо дают профессиональные медики с высшим образованием и опытом профильной работы.
На ваш вопрос в форму ниже ответит один из ведущих авторов сайта.
В данный момент на вопросы отвечает: А. Олеся Валерьевна, к.м.н., преподаватель медицинского вуза
Поблагодарить специалиста за помощь или поддержать проект СосудИнфо можно произвольным платежом по ссылке.
что это такое, лечение, последствия
Гипоксические поражения головного мозга с развитием ишемии наблюдаются у 15-30% доношенных новорожденных. У недоношенных младенцев патология встречается чаще – в 40-60% случаев. Часто подобные нарушения являются предвестниками детского церебрального паралича (ДЦП), симптоматической эпилепсии, слабоумия, возникающего на фоне органического повреждения мозговых структур.


Перечисленные заболевания, возникающие в центральной нервной системе, приводят к детской инвалидности, являются основной причиной социальной дезадаптации. Особое значение приобретает комплексная диагностика ишемических изменений, произошедших в головном мозге у новорожденных. Диагностические исследования нервной системы плода во время беременности целесообразно проводить, начиная с антенатального периода.
Проявления ишемии у грудничков
Ишемия структур головного мозга – это такое заболевание, которое сопровождается у новорожденных гипоксией (пониженное содержание кислорода в тканях) или аноксией (отсутствие кислорода в тканях), что приводит к острому кислородному голоданию. В 40% случаев поражения ЦНС в детском возрасте связаны с перинатальной патологией.
Недоношенность – ведущий фактор, с которым ассоциируется морфофункциональная незрелость мозговых структур, из-за чего повышается риск возникновения ишемии головного мозга у недоношенных детей при преждевременных родах. Вследствие кислородного голодания развивается некроз (отмирание тканей), что приводит к очаговым и диффузным структурным изменениям мозгового вещества. В зависимости от локализации и характера повреждений выделяют:
- Мультикистозную лейкомаляцию (диффузное поражение белого вещества гипоксической, ишемической этиологии).
- Субкортикальную (подкорковую) лейкомаляцию.
- Ишемический некроз (очаговый или диффузный).
Атрофические изменения мозговых структур выявляются в ходе инструментальной диагностики. При проведении Эхо-ЭГ (эхоэнцефалография) исследования в 80% случаев наблюдаются уплотнения в перивентрикулярной (около желудочков) области, в 20% случае картина дополняется расширением желудочков и пространств, в которых находится цереброспинальная жидкость (протоки, субарахноидальное пространство).
Нередко (около 18% случаев) ишемия, поразившая головной мозг у ребенка, протекает без явных отклонений в структуре мозгового вещества. Исследование ЭЭГ (электроэнцефалография) у недоношенных младенцев в 73% случаев показывает непостоянный характер биоэлектрической активности мозга с преобладанием медленных, низкоамплитудных волн, периодически чередующихся с кратковременно продолжающимися регулярными волнами.
У 23% детей выявляются разноплановые патологические паттерны (схемы-образцы) ЭЭГ и волны эпилептической природы в общем колебательном ритме. Редко (3% случаев) ЭЭГ не показывает существенных отклонений от нормы у детей с ишемией, протекающей в головном мозге.
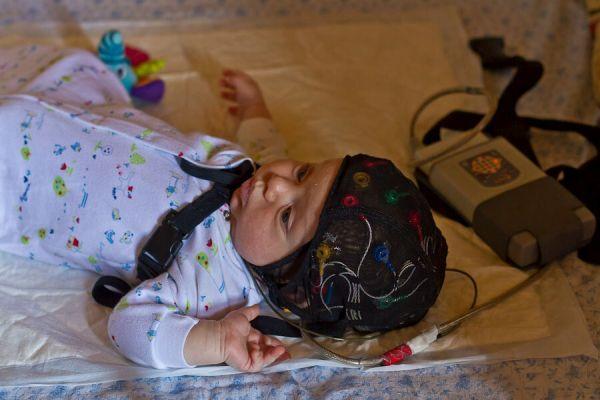

Основные признаки заболевания
Ишемическая болезнь, поразившая головной мозг, у новорожденных сопровождается преимущественно неврологической симптоматикой. Оценка состояния новорожденного по шкале Апгар 2-5 баллов указывает на наличие интранатальной (во время родов) асфиксии. В особо тяжелых случаях возможно развитие коматозного состояния и тяжелое угнетение деятельности ЦНС, что требует незамедлительного проведения реанимационных мероприятий с подключением к аппарату искусственной вентиляции легких. Другие признаки:
- Судорожный синдром.
- Бульбарные расстройства. Нарушение функций глотания и сосания.
- Чередование мышечной гипотонии и мышечного гипертонуса пирамидного, пирамидно-экстрапирамидного типа.
- Спастическая тетраплегия. Частичный или полный паралич конечностей.
- Спастические тетрапарезы. Обессиливание моторной активности всех конечностей в результате нарушения функций нервной системы.
- Дистонические эпизоды (спазматическое сокращение мышц постоянного характера) с характерным застыванием в позе ассиметричного тонического шейного рефлекса.
- Гиперкинезы (непроизвольные движения одной или группы мышц) с атетозом (непроизвольные подергивания) кистей рук.
- Мышечная ригидность. Неподатливость, твердость мышц.
- Нарушение сна, частый плач.
Стоит обратить внимание на аномальный тонус мышц и тремор некоторых частей тела – подбородка, кистей рук. Оценка по шкале Infanib 12-20 баллов. Оценка спастичности по шкале Эшворта (Ashworth scale) 3-4 балла. Поражение структур нервной системы проявляется характерными синдромами:
- Усиленная нервно-рефлекторная возбудимость.
- Вегето-висцеральная дисфункция (расстройство нейроэндокринной регуляции).
- Мышечная дистония (спазматические сокращения мышц).
Статистика показывает, признаки церебральной ишемии, развивающейся в головном мозге у новорожденных, чаще носят неврологический характер. Интенсивность и выраженность проявлений неврологических симптомов зависит от характера и степени поражения мозговых структур.
Перинатальные повреждения мозговых структур более выражены у недоношенных малышей (угнетение деятельности ЦНС – 18%, судорожная готовность – 19%, гипертензионно-гидроцефальный синдром – 9%). У младенцев более позднего срока гестации (33 недели) сильнее проявляются вегето-висцеральные расстройства (в 44% случаев). У доношенных детей чаще наблюдается усиленная нервно-рефлекторная возбудимость, развивающаяся на фоне гипертонуса мышц (в 31% случаев).


Степени патологии у новорожденных
Различают 3 степени ишемического поражения мозговых структур. Ишемия 1 степени в тканях головного мозга у новорожденных проявляется гиперактивностью, расстройством сна, ухудшением аппетита, беспричинным, частым плачем, повышенным тонусом мышц.
Симптомы ишемии 2 степени в тканях головного мозга у новорожденного включают судорожный синдром, повышение значений внутричерепного давления с сопутствующей симптоматикой. Наблюдается выпячивание родничка, непроизвольное запрокидывание головы, частый плач, неконтролируемые движения глазными яблоками, гидроцефалия (аномальное увеличение диаметра головы). Рефлексы вялые, периодически происходит замедление дыхания и сердечного ритма.
Для ишемии 3 степени характерно тяжелое угнетение функций ЦНС, вплоть до острой легочной недостаточности, отсутствия рефлексов, комы.
Причины развития
Ишемия в тканях головного мозга развивается вследствие кислородного голодания, все случаи патологии связаны с нарушением кровотока, вызванного закупоркой или сильным сужением сосудистого просвета. Основные причины:
- Соматические заболевания инфекционной этиологии у матери.
- Вредные привычки матери (курение, злоупотребление алкоголем).
- Родовые травмы, полученные плодом.
- Сбои в работе эндокринной системы у матери.
- Неблагоприятное течение беременности (токсикозы, угрозы выкидыша, преждевременные, осложненные роды).
Развитию ишемического поражения подвержены младенцы, которые в перинатальный период перенесли заболевания: легочная и сердечная недостаточность, паразитарные инвазии, опухоли мозга, нарушение свертываемости крови, другие патологии системы гемостаза.
Диагностика
На первом этапе сразу после родов выполняется визуальный осмотр новорожденного, оценка дыхательной и сердечной деятельности, проверка рефлексов, определение неврологического статуса. Для подтверждения диагноза ишемия головного мозга у младенца используются методы:
- Сбор анамнеза. Состояние плода в период беременности и во время родов. Учитываются данные соматического и акушерско-гинекологического анамнеза матери, особенности течения беременности и родов.
- Неврологический статус ребенка в динамике. Оценка мышечно-постурального тонуса и рефлексов (шкала Infanib).
- Нейросонография.
- Допплерография сосудов.
- Эхоэнцефалография.
- КТ, МРТ.
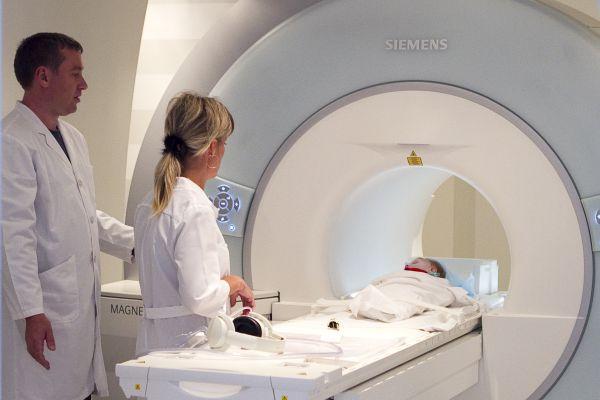

Инструментальные исследования отражают характер и локализацию органических поражений мозговых структур, а также динамику развития нарушений (прогресс или регресс). При подозрении на гипоксические, ишемические повреждения участков мозга электроэнцефалографическое исследование проводится многократно, примерно в возрасте 40, 44 недели с момента зачатия, в 6 и 12 месяцев. Электроэнцефалография с топографическим картированием и визуализацией позволяет судить о биоэлектрической активности мозга грудничков. Исследование ЭЭГ показывает:
- Ирритацию (раздражение) корковых структур, которая приводит к нарушению функций коры. Часто возникает на фоне ухудшения кровоснабжения участков мозга.
- Полиморфную полиритмию (множественность). Несколько параллельных основных ритмов мозга, близких по амплитуде.
- Диффузные колебания, которые превышают нормальные амплитудные значения.
Патологические изменения чаще указывают на понижение порога судорожной готовности и предвещают эпилептические приступы. Количественное содержание в крови оксида азота косвенно указывает на сократительную способность гладкой мускулатуры сосудистой стенки. Он является медиатором вазодилатации, регулирует расширение сосудистого просвета.
Оксид азота участвует в передаче нервных импульсов, улучшая взаимодействие между нейронами. С увеличением его концентрации повышается способность мышц расслабляться, благодаря чему уменьшается вероятность существенного сужения сосудистого просвета и закупорки сосуда тромбом. В организме ускоряется процесс продуцирования оксида азота в случае гипоксии или поражения эндотелия сосудистых стенок.
У детей с ишемическим повреждением мозга уровень метаболитов оксида азота в крови повышен. Анализ крови также показывает ферментный статус лимфоцитов, концентрацию ксантинов и гипоксантинов, параметры коагуляционного гемостаза. Обычно наблюдается сокращение промежутка протромбинового времени, повышенный уровень фибриногена и растворимых фибринмономерных комплексов.
Методы лечения
Избежать серьезных последствий ишемии головного мозга у новорожденных поможет своевременная диагностика нарушений и лечение. Комплексная нейрореабилитация включает:
- Медикаментозную терапию с использованием препаратов с нейропротекторным действием.
- Лечебный массаж.
- Пассивную лечебную гимнастику.
- Аппликации озокеритом в области конечностей.
- Сухую иммерсию. Без использования водной среды создают условия частичной невесомости наподобие тех, в которых плод пребывает в период внутриутробного развития. Эффективное реабилитационное мероприятие, которое позволяет уменьшать неврологическую симптоматику и стабилизировать некоторые гемодинамические показатели.
- Физиотерапию (лазеротерапия, магнитотерапия).
- Музыкотерапию.


Терапия фармацевтическими средствами направлена на устранение судорожного синдрома, устранение последствий гипоксии и отека мозга. Коррекция психомоторных функций выполнятся при помощи препаратов:
- Витамины группы B1, B6.
- Лекарства на основе L-карнитина (Элькар, Левокарнитин). Нормализуют обменные процессы на клеточном уровне, обладают антигипоксическим действием.
- Нейропротекторы на основе аминокислот и нейропептидов (Актовегин). Улучшают взаимосвязь между нейронами, стимулируют репаративные (восстановительные) процессы в ЦНС.
- Ангиопротекторы. Улучшают состояние сосудистых стенок, повышают тонус гладкой мускулатуры, препятствуют проникновению ионов кальция сквозь клеточные мембраны.
- Ноотропные (Глицин, Фенотропил, Глиатилин). Повышают устойчивость мозговых структур к гипоксии. Ускоряют утилизацию глюкозы, стимулируют обмен нуклеиновых кислот, ускоряют синтез белков, АТФ, РНК.
- Противосудорожные.
- Миорелаксанты. Восстанавливают нормальный тонус мышц.
При легкой форме патологии рекомендуется делать профессиональный массаж, лечебную гимнастику, физиотерапевтические и водные процедуры, причем восстановительное лечение может проводиться без использования каких-либо фармацевтических препаратов.
Возможные последствия заболевания
Распространенные (78% случаев) последствия ишемии головного мозга у новорожденных – расстройство слуховой и зрительной афферентации (непрерывный поток нервных импульсов от органов чувств к нервной системе). Частые осложнения ишемического поражения головного мозга у новорожденных: ДЦП, эпилепсия, ишемический инсульт, которые приводят к инвалидности и летальному исходу (7-28% случаев). На фоне кислородного голодания может развиться слабоумие, нейросенсорная глухота и корковая слепота.
Профилактика
Для профилактики заболевания будущей матери необходимо вести здоровый, активный образ жизни, отказаться от вредных привычек, организовать полноценное, правильное питание с достаточным количеством белков, жиров, углеводов, витаминов и микроэлементов. В период беременности нужно регулярно посещать врача акушера-гинеколога, по его назначению проходить диагностическое УЗИ-обследование с целью выявления нарушений в развитии плода на ранней стадии.
Ишемия в тканях головного мозга у новорожденных – опасная патология, которая может стать причиной инвалидности и смерти ребенка. Прогноз при незначительных поражениях мозгового вещества благоприятный. Диагностика в ранний перинатальный период и корректная терапия способствуют улучшению состояния малыша и выздоровлению.
ПОЖАЛУЙСТА, ОЦЕНИТЕ СТАТЬЮ!
Просмотров: 1 416
Рейтинг автора
Автор статьи
Терапевт, образование: Северный медицинский университет. Стаж работы 10 лет.
Написано статей
Нехватка кислорода в организме человека в считаные секунды наносит иногда непоправимый вред. Гипоксически-ишемическая энцефалопатия (ГИЭ) иногда звучит страшным приговором как для ребенка, так и для взрослого. Давайте разберемся, что это за болезнь, ее симптомы и насколько опасно гипоксически-ишемическое поражение головного мозга в любом возрасте.

Особенности патологии
Дефицит кислорода неизбежно отражается на функционировании организма. Гипоксически-ишемическая энцефалопатия у новорожденных случается часто: как у доношенных деток, так и недоношенных. У 10% младенцев, перенесших ее, в дальнейшем ставят диагноз «ДЦП». Именно поэтому будущая мать должна чаще бывать на свежем воздухе и точно соблюдать рекомендации врача, чтобы снизить риск гипоксии до минимума.
У взрослых частой причиной патологии становятся травмы или имеющиеся серьезные заболевания. Если при приступе удушья помощь не будет оказана вовремя, то есть серьезный риск летального исхода или инвалидности. Немаловажную роль играет и степень тяжести патологии, чем она выше, тем меньше шансов у человека на возврат к полноценной жизни.
Когда наступает кислородное голодание в важнейшей части центральной нервной системы, это приводит к дефициту этого вещества в клетках мозга, что замедляет кровоток и все метаболические процессы. При таком недостатке питания нейроны мозга в некоторых участках органа начинают отмирать, приводя к неврологическим нарушениям.
Ускоряет процесс отек мозга, возникающий также из-за сбоя в кровообращении. Давление растет, и клетки начинают быстрее гибнуть. Чем быстрее проходит процесс, тем больше шансов на то, что повреждения будут необратимыми.
Причины возникновения
Гипоксическая энцефалопатия у взрослых и у детей возникает по разным причинам. Их важно знать, чтобы принять все меры для ее предупреждения.
У взрослых
Гипоксическая ишемическая энцефалопатия возникает на фоне нехватки кислорода, к чему приводят следующие причины:
- состояние удушья;
- удушение;
- сбой дыхательной системы любого рода происхождения;
- наркотическая зависимость, передозировка;
- патологии кровеносной системы, приводящие к ее непроходимости или разрыву;
- цианид, окись углерода — отравление;
- длительное пребывание в задымленном месте;
- травма трахеи;
- остановка сердца;
- болезни, приводящие к параличу мышечной ткани дыхательной системы.
Острая гипоксическая энцефалопатия наступает, если кислород не поступал в организм несколько минут. Это тяжелое течение патологии, которое чаще всего заканчивается летальным исходом. Зафиксированы единичные случаи, когда люди выживали, но для них это заканчивалось тяжелой формой серьезных психических болезней.
У новорожденных
Причиной такого состояния у только родившегося ребенка может быть:
- удушье во время родов из-за слабой родовой деятельности;
- преждевременный родовой процесс или с патологическими факторами, такими как выпадение пуповины;
- болезни инфекционного генеза у матери;
- ряд физических факторов от грязного воздуха до радиационного излучения.

Именно асфиксия у грудничков является самым частым фактором, приводящим к ГИЭ. Врачи выделяют следующие факторы риска для ее возникновения:
- гипотония острой формы у роженицы;
- недоразвитость легких, что приводит к недостатку кислорода в крови;
- сложности в работе сердца;
- травмирование плода узким тазом матери или из-за проблем с пуповиной;
- сложности в родовой деятельности, травма, стресс;
- гипоксия;
- родовое кровотечение;
- халатность медицинского персонала;
- отслойка плаценты;
- изменение формы черепа плода из-за давления;
- родовая травма, разрыв матки;
- низкое предлежание плаценты.
Степени тяжести и характерные симптомы
Гипоксически-ишемическая энцефалопатия имеет 3 степени тяжести, для которых характерны свои проявления. По ним врачи часто дают предварительную характеристику повреждений мозговой деятельности и приблизительный прогноз.
Легкая степень
При такой степени у больного будет:
- расширен зрачок и широко открыты веки;
- отсутствовать концентрация внимания;
- нарушена координация движений, блуждающее поведение;
- выявлена либо сонливость, либо гипервозбудимость;
- высокая степень раздражительности;
- отсутствовать аппетит;
- нарушено мозговое кровообращение.
Средняя степень
Неврология при ней будет более выражена, т. к. нарушение насыщения мозга кислородом более длительное:
- у малыша спонтанные крики без причины;
- защитный и опорный рефлекс либо ослаблен, либо отсутствует вовсе;
- признаки мышечной слабости;
- опущение верхнего века;
- увеличение давления цереброспинальной жидкости;
- метаболический ацидоз крови;
- невралгические приступы;
- сбой в глотательном процессе.
Тяжелая степень
Поражение в таких случаях более тяжелое, что проявляется в:
- судорожности;
- синюшности кожи;
- потере сознания;
- гипертензии;
- отсутствии двигательных возможностей;
- косоглазии;
- коме или прекоме;
- отсутствии реакции зрачков на свет;
- сбое дыхательного процесса с сильной аритмией;

ПЭП — это разновидность гипоксически-ишемической энцефалопатии у детей раннего возраста. Ее диагностируют как сразу после рождения, так и на первом году жизни. Развивается ПЭП как внутриутробно, в процессе родовой деятельности, так и в первые 10 дней с момента рождения.
Она может быть трех степеней тяжести с характерной симптоматикой и протекать в острой форме — до месяца, в раннем восстановлении функций — до 4 месяцев, при позднем восстановлении — до 2 лет.
Диагностика
Перинатальный синдром ишемии на фоне гипоксии мозга начинают диагностировать, делая визуальный осмотр ребенка. Так же и со взрослыми. Несмотря на все достижения медицины, уникальный тест, позволяющий точно выявить ГИЭ, до сих пор не придуман. Все лабораторные методики направлены на выявление того, насколько сильно поврежден мозг и текущее состояние всего организма.
Какими будут исследования, зависит от симптомов, и как они развивались. Для расшифровки анализов есть специальные биомаркеры, которые дают полную картину о степени ГИЭ. Для исследования нужна кровь больного.
Нейровизуализацию проводят с помощью:
- нейросонографа и/или МРТ, томографа, показывающего внутренние повреждения мозга и изменения в нем;
- доплерографа, фиксирующего работу мозгового кровотока;
- электронейромиографа для определения чувствительности волокон периферии нервной системы.
Дополнительного могут использовать:
- электроэнцефалограф для выявления задержки развития на ранней стадии и есть ли эпилепсия;
- видеомониторинг для изучения двигательной активности малышей.

При необходимости пострадавшего осматривает окулист, чтобы определить состояние зрительных нервов и глазного дна, а также на наличие болезней генетического типа в этой области.
Лечение и уход
За пострадавшими должен быть особый уход, а за детьми, перенёсшими ГИЭ, он строится на контроле за:
- температурой в помещении — не более 25 градусов;
- его комфортной позой, поэтому тугое пеленание под запретом;
- тем, чтобы свет был мягким и приглушенным;
- тишиной;
- кормлением, которое должно быть с контактом «кожа к коже» и согласно потребностям малыша;
- дыханием, при сбое в котором подключают специальный аппарат.
Терапию проводят:
- Хирургически, для восстановления и улучшения кровообращения в мозгу. Чаще всего для этих целей используют эндоваскулярную методику, которая не нарушает целостность тканей.
- Медикаментозно, выбирая препараты в зависимости от того, насколько тяжелая степень поражения и ее клинической картины.
- На антиконвульсантах, которые купируют судороги. Обычно это Фенобарбитал, дозировку которого подбирают индивидуально. Внутривенный способ самый быстрый. Но сам препарат противопоказан при сверхчувствительности, тяжелой форме гипоксической и гиперкаптической дыхательной недостаточности, проблемах с почкам и печенью, при беременности. Может быть использован Лоразепам, у него аналогичное воздействие и список противопоказаний.
- На сердечно-сосудистых средствах, чтобы увеличить системное сопротивление сосудов и сократительную функцию миокарда, что приводит к повышенному сердечному выбросу. Все средства этой группы влияют на почки, а при передозировке побочные эффекты предсказать сложно. Чаще всего используют Допамин, Добутамин.
Дальнейшее наблюдение
Из стационара выписывают только после прохождения полного курса физической терапии и комплексной оценки нервно-психического развития. Чаще всего после выписки пациенты не требуют специфического ухода, но регулярные осмотры в клинике обязательны, особенно для детей.
Если болезнь была тяжелой, то ребенок будет наблюдаться в специальном центре, где ему будет помогать врач по нервно-психическому развитию.
Лечение судорожности зависит от симптоматики центральной нервной системы и результатов исследований. Выписывают только с легким отклонением от нормы или вовсе в ее пределах. Фенобарбитал убирают постепенно, но обычно его пьют после выписки не менее 3 месяцев.
Прогноз и последствия
У взрослых прогноз зависит от степени поражения мозга патологией. Самыми частыми последствиями перинатальной ГИЭ являются:
- задержка в развитии ребенка;
- дисфункции мозга в плане внимания, сосредоточенности на обучении;
- нестабильная работа внутренних систем организма;
- эпилептические припадки;
- гидроцефалия;
- вегетососудистая дистония.

Не нужно думать, что это приговор, даже разлад в центральной нервной системе корректируют, обеспечивая нормальную жизнь пациентам. Треть людей с этим расстройством излечивается полностью.
Профилактика
Если речь идет о взрослых, то все профилактические мероприятия должны быть направлены на полный отказ от вредных привычек. При этом нужно регулярно заниматься спортом, избегая чрезмерных нагрузок, правильно питаться, проходить регулярные медицинские осмотры, чтобы выявить опасные патологии на ранней стадии для их успешного купирования.
От травм никто не застрахован, но если более осторожно себя вести, то и их можно минимизировать.
Снизить риск ГИЭ у новорожденного может только его мама еще в период беременности. Для этого нужно:
- строго следить за режимом дня и личной гигиеной;
- отказаться от никотина и алкоголя даже в минимальной дозировке;
- проходить вовремя обследования у врачей и диагностику, особенно у невролога;
- доверить роды только квалифицированному персоналу.
Гипоксически-ишемическая энцефалопатия опасная болезнь, но ее можно предотвратить, и даже вылечить, но только если помощь была оказана вовремя и в дальнейшем врачебные рекомендации не нарушаются.
Гипоксия головного мозга у новорожденных
Гипоксия у детей может возникнуть в период внутриутробного развития или при рождении. Нехватка кислорода может привести к проблемам со здоровьем у ребёнка. Если диагностирована гипоксия головного мозга у новорожденных, последствия интересуют всех родителей.
Многое будет зависеть от того, как долго малышу не хватало кислорода, а также от своевременности и правильности решения. Патология достаточно распространена, и она обнаруживается у 6% новорожденных. Родители должны понимать, с чем им приходится иметь дело, чтобы можно было принять правильные меры.
Характеристика
Гипоксия головного мозга у новорожденных — это патология, при которой ребёнок испытывает недостаток кислорода, поступающего от матери к плоду. Часто данная проблема возникает в период беременности, поэтому женщине нужно внимательно следить за своим здоровьем и за состоянием малыша.

Гипоксия встречается острая и хроническая. Первый вид часто возникает из-за тяжёлых родов, которые значительно сказались на здоровье ребёнка. При хронической форме ребёнок длительное время испытывает кислородное голодание.
Важно знать особенности данного состояния, чтобы не усугубить ситуацию и не допустить значительного ухудшения здоровья малыша.
Нехватку кислорода нельзя назвать безопасной патологией, потому как она имеет немало осложнений. Нарушение сказывается на внутренних органах, особенно на лёгких, сердце и печени. В некоторых случаях малыш может даже получить статус инвалида. Только своевременное лечение позволит не допустить появления опасных осложнений.
Разновидности
Гипоксия головного мозга у детей может развиваться как из-за внешних, так и из-за внутренних факторов. Существует несколько разновидностей патологии, которые важно определить для дальнейшего лечения.

Типы гипоксии:
- Дыхательная гипоксия. Она появляется из-за того, что у человека нарушена работа дыхательной системы. Нередко болезнь выступает в виде побочного эффекта астмы, повреждения мозга и паралича мускулатуры.
- Болезнь гипоксического характера. Она определяется, когда голова не получает достаточное количество кислорода из внешнего мира. Подобная ситуация возникает, например, при подъёме на высоту.
- Циркуляторная патология. Её выделяют, если у человека имеются болезни сердечно-сосудистой системы. На их фоне может быть нарушение кровотока, из-за чего кислород не попадет в достаточном количестве в центральную нервную систему. Как итог, человек пребывает в состоянии шока. Из-за данного состояния нередко возникает ишемический инсульт.
- Патология тканей. Она появляется тогда, когда наблюдаются проблемы с поглощением кислорода клетками. Голодание возникает из-за ферментной блокады. Нередко патология может появиться, если человек постоянно контактирует с ядами или опасными для здоровья лекарствами.
- Гемическая гипоксия. Данная болезнь возникает, когда есть проблемы с транспортировкой кислорода. Сосудам не достаёт данного элемента, а также гемоглобина. Проблема появляется при отравлении ядовитыми элементами, а также газами.
Независимо от вида заболевания, важно своевременно начать лечение, чтобы не допустить серьёзных осложнений. Для начала придётся пройти диагностику, чтобы можно было убедиться в наличии конкретного заболевания.
Причины
Существует немало причин, по которым появляются гипоксические изменения головного мозга у новорожденных. Причём многие негативные факторы можно предотвратить, что особенно актуально для беременных женщин. Условно причины можно поделить на 3 группы в зависимости от того, при каких обстоятельствах возникло нарушение.

Отклонения при беременности:
- Вероятность выкидыша.
- Плацентарные нарушения.
- Обвитие шеи пуповиной.
- Преждевременные роды, либо вынашивание ребёнка дольше положенного срока.
- Многоплодная беременность.
- Гистоз.
Если у женщины беременность не проходит гладко, важно постоянно наблюдаться у врача и удостовериться в том, что плод находится в нормальном состоянии. Чтобы новорожденный ребёнок был здоровым, крайне важно не допускать гипоксические нарушения.
Отклонения у матери:
- Наличие анемии, либо малокровие.
- Проблемы с сердечно-сосудистой системой.
- Болезни бронхолёгочного типа.
- Возникновение беременности у женщины, которой меньше 18 лет или больше 35 лет.
- Патологии мочеиспускательных органов.
- Вредные привычки, такие как употребление наркотиков, алкоголя или никотина.
- Постоянные стрессы, плохое питание, отсутствие сна.

По этой причине важно следить беременной женщине за своим здоровьем. Также следует обязательно отказаться от вредных привычек и пересмотреть свой образ жизни. От этого будет зависеть то, насколько правильно будет развиваться плод.
Проблемные роды:
- Обвитие плода пуповиной. Это одна из наиболее частых причин, по которым возникает нехватка воздуха у ребёнка.
- Родовые травмы.
- Тяжёлые роды, как для матери, так и для ребёнка.
- Использование лекарственных средств, которые могут сказаться на состоянии малыша.
- Большой размер плода.
Если возможно, негативные факторы следует устранить, чтобы не пришлось потом сталкиваться с негативными последствиями. Каждая молодая должна позаботиться о том, чтобы снизить вероятность развития гипоксических изменений у малыша. Если же предотвратить данное состояние не удалось, тогда стоит своевременно заметить характерные симптомы.
Признаки
При гипоксии головного мозга у новорожденного возникают различные проявления, которые могут заметить как родители, так и врачи. Самостоятельно диагностировать патологию невозможно, поэтому важно сразу обратиться к доктору. После проведения обследований можно будет однозначно сказать, с какой проблемой пришлось столкнуться.

Главные симптомы:
- Сбои в работе сердца. Могут присутствовать шумы, повышенный пульс, аритмия, брадикардия.
- У ребёнка наблюдается небольшой кровяной объём.
- Родившийся ребёнок не плачет в момент появления на свет.
- Имеются сосудистые тромбы.
Данные отклонения в большинстве случаев выявляются ещё в родильном доме. Их обнаружение – задача врачей, а не родителей. При этом мама самостоятельно может заметить нарушения у ребёнка, которые могут говорить о гипоксии. На них обязательно стоит обратить внимание для того, чтобы своевременно диагностировать гипоксию.
Признаки:
- Наличие судорог.
- Неспокойный сон у новорожденного.
- Постоянный плач без какой-либо причины.
- Ребёнок вздрагивает, когда к нему касаются.
- Дрожание рук, ног и подбородка во время плача.
- Нарушение тонуса мышц.
- Малыш постоянно замерзает.

В этом случае следует обязательно проконсультироваться с врачами, чтобы своевременно принять меры. При этом важно определить степень гипоксии, чтобы понимать, насколько нарушения серьёзные. Если кислородное голодание в тяжёлой форме, тогда возможны наиболее неблагоприятные последствия.
Степени по шкале Апгар
Ребёнку при рождении даётся оценка в зависимости от того, насколько хорошо функционируют все системы в организме. Для этого используется шкала Апгар, по которой ориентируются врачи. Сначала оценивается состояние на первой минуте жизни, а затем спустя 5 минут.
Какие могут быть баллы:
- От 0 до 3 – тяжёлая форма гипоксии.
- От 4 до 5 – средняя тяжесть кислородного голодания.
- От 6 до 7 — лёгкое нарушение.
- От 8 до 10 – с ребёнком всё хорошо.
Оцениваться будет частота дыхания, наличие рефлекторной активности, окрас кожи, мышечный тонус. Также внимание уделяется частоте сокращений сердца. В зависимости от того, имеются ли у ребёнка нарушения, будет ставиться конкретный балл. Лёгкая гипоксия самостоятельно проходит в течение 5 минут, а вот остальные степени требуют лечения.
Диагностика и лечение
Для того чтобы поставить точный диагноз, важно пройти обследование. Ещё в период беременности женщине необходимо будет выполнить УЗИ плода, тест на шевеления, а также прослушать сердцебиение. По результатом исследований можно будет понять, есть ли угроза для малыша.

После рождения малышу делают УЗИ головного мозга и неврологическое обследование. Если будут замечены отклонения, тогда можно заподозрить наличие гипоксии.
При лечении сначала восстанавливают дыхание при помощи аспирации, затем могут применить искусственную вентиляцию лёгких. В пуповину вводят раствор глюкозы и кокорбоксилазу. При бардикардии делают массаж сердца, а также в вену вводят адреналин и другие лекарства. После этого ребёнку потребуется давать витамины, выполнять инфузионное лечение, а также проводить оксигенотерапию.
Последствия — видео
Наиболее опасной является острая форма гипоксии головного мозга. Именно данная разновидность может привести к различным отклонениям, которые сказываются на качестве жизни человека. Обязательно нужно своевременно пройти курс лечения, если хочется сохранить здоровье ребёнка.
Различные последствия возникают в том случае, когда малышу не была оказана правильная помощь. В такой ситуации патология способна негативно влиять на качество жизни. Осложнения могут быть как лёгкими, так и серьёзными.
Возможные последствия:
- Ускоренное сокращение сердца. При этом наблюдается повышенное артериальное давление. При гипоксии перераспределяется кровоток, из-за чего возможны трофические нарушения. Опасность заключается в том, что внутренние органы могут перестать нормально функционировать.
- Становится другой частота дыхания. У человека появляется одышка.
- Мозг вырабатывает большое количество эритроцитов. Из-за этого возникает риск появления тромбов.
- Часто появляются судороги в детском возрасте.
- Ухудшается зрительная функция.
Церебральная гипоксия либо патология иного вида не должна пускаться на самотёк. Должна быть пройдена терапия, при этом ребёнок должен наблюдаться у врача для контроля над изменениями. Если не начать своевременно лечение, нередко может наблюдаться отставание в развитии. Дети хуже набирают вес, долго не говорят, а также имеют расстройства неврологического характера. Чтобы этого не допустить, достаточно вовремя посетить врача и пройти курс лечения.
Гипоксия у новорожденных сопровождается кислородным голоданием тканей головного мозга ребенка. Это патологическое состояние не является самостоятельной болезнью, а развивается вследствие влияния на младенца ряда патологических факторов.
Гипоксия опасна для новорожденного. В редких случаях она способна сделать ребенка инвалидом, либо вовсе лишить его жизни. Встречается патология у 4-6% грудничков.
Причины
Гипоксия головного мозга у новорожденных может возникать из-за влияния различных факторов. Основные причины развития патологии:
- Полученная травма младенца во время его прохождения по родовым путям.
- Родоразрешение с применением щипцов.
- Резкое снижение кровяного давления у беременной женщины во время родов.
- Занесение инфекции в организм плода во время прохождения по родовым путям или во время его нахождения в матке. Приводить к гипоксии головного мозга способны такие заболевания, как сифилис, краснуха, цитомегаловирус, герпес.
- Резус-конфликт матери и ребенка.
- Антифосфолипидный синдром.
- Порок сердца.
- Закупорка дыхательных путей младенца околоплодными водами, слизью или каловыми массами.
- Опасные неинфекционные болезни матери. К ним относятся: анемия, патологии органов дыхания, сахарный диабет, нарушения в функционировании щитовидной железы, порок сердца. В таких условиях организм не в состоянии обеспечить достаточным уровнем кислорода даже саму женщину, поэтому большинство младенцев появляются на свет с признаками гипоксии.
- Вынашивание и рождение сразу нескольких детей.
- Отягощенный гестационный период. Спровоцировать патологию способна ранняя отслойка плаценты, позднее родоразрешение и токсикоз на последних неделях беременности.
- Рождение недоношенного ребенка.
- Многоводие и маловодие.
- Вредные привычки у женщины, которые она не оставила на время вынашивания плода. Гипоксия может возникать из-за курения беременной, алкоголизма или наркомании.
- Прием беременной женщиной лекарственных препаратов.
- Серьезные погрешности в питании будущей матери.
- Хронический стресс у беременной женщины.
- Проживание будущей матери в экологически неблагоприятных условиях, работа на вредном производстве.
- Неполное расправление легких у младенца. Эта причина приводит к гипоксии на фоне пневмопатий (неинфекционное поражение легочной ткани младенца).
- Нарушение мозгового кровообращения у ребенка.
Причины гипоксии, которые действуют на ребенка во время его нахождения в утробе матери, называют антеральными. Те факторы, которые провоцируют дефицит кислорода после рождения малыша, относятся к интранатальным.
Иногда причиной гипоксии становится пуповина. Кислородное голодание развивается у младенцев с обвитием, наличием истинных узлов, сжатием пуповины или разрывом ее сосудов.

Симптомы
Гипоксия у новорожденного ребенка приводит к тому, что симптомы будут давать о себе знать в течение долгого времени. Главным критерием является наличие дыхательных расстройств, которые провоцируют сбой в работе сердца и в системе кровообращения.
Тяжесть гипоксии определяется по шкале Апгар. Она имеет три степени:
- От 6 до 7 баллов – у новорожденного легкая гипоксия. При этом ребенок делает вдох в течение первых 60 секунд после появления на свет. Дыхание ослабленное, окраска кожи синюшная. Тонус мышц снижен. Такое состояние не требует специальных мероприятий.
- От 4 до 5 баллов – гипоксия средней степени тяжести. Вдох ребенок выполняет в течение первых 60 секунд, дыхание слабое, сбивчивое. Малыш тихо кричит, его пуповина пульсирует. Лицо и конечности синего цвета, мышечный тонус снижен. При грамотно организованной терапии справиться с патологией удастся за несколько дней.
- От 1 до 3 баллов – тяжелое удушье. Дыхание редкое, либо появляется в виде хрипов, ребенок не кричит, пуповина не пульсирует. Кожа младенца бледная. У детей с тяжелым удушьем диагностируется недостаточность функционирования надпочечников. Для спасения жизни ребенка требуются экстренные реанимационные мероприятия.
Если врач выставляет 0 баллов, то говорят о клинической смерти новорожденного.
Баллы по шкале Апгар выставляются на основании ряда критериев. К ним относятся: частота сердцебиения и дыхания, цвет кожных покровов, мышечный тонус и пяточный рефлекс.
Практически у всех детей, появившихся на свет, имеется легкая гипоксия. В норме она самостоятельно проходит через 5 минут.
Симптомы, указывающие на кислородное голодание:
- Слабость дыхания, либо его отсутствие.
- Тахикардия, которая сменяется брадикардией.
- Сбой сердечного ритма.
- Наличие шумов в сердце.
- Синюшность кожи.
- Низкая двигательная активность, либо ее отсутствие.
- Наличие зелени в околоплодных водах.
- Появление подкожных кровоизлияний.
По этим признакам врач сразу же выставляет диагноз.
Поздние признаки гипоксии
Кислородное голодание у новорожденных может быть пропущено в силу определенных обстоятельств. Если верный диагноз не был выставлен на первых минутах жизни младенца, натолкнуть на мысль о том, что с ним не все в порядке, должны следующие симптомы:
- Сонливость ребенка. Грудные дети должны просыпаться для обеспечения своих естественных нужд. В норме, они спят не более 21 часа в сутки. Оставшиеся 3 часа малыш должен бодрствовать.
- Беспокойный сон. Ребенок часто плачет, все время вздрагивает.
- Кожа рук и ног имеет мраморный окрас.
- Во время переодевания и выполнения гигиенических мероприятий ребенок мерзнет. Его конечности в течение длительного времени остаются холодными на ощупь.
- В состоянии покоя и во время плача у ребенка подрагивают лицевые мышцы.
Если мать замечает у младенца такие симптомы, она должна сообщить об этом педиатру.

Последствия и осложнения
Гипоксия у новорожденных способна вызвать тяжелые последствия. В первую очередь страдает головной мозг ребенка. Эта патология носит название гипоксической энцефалопатии. Если кислородное голодание тканей было легким, то все симптомы нарушения самостоятельно пройдут через неделю.
Тяжелая энцефалопатия проявляется заторможенностью младенца, вплоть до развития судорог и комы. Ребенку требуется стационарное лечение. Полноценное восстановление может занять месяцы и даже годы. В течение этого времени он должен находиться под регулярным врачебным присмотром. Иногда последствия ишемии сохраняются в течение всей жизни.
К ранним осложнениям гипоксии относятся: водянка головного мозга, менингит, сепсис, воспаление легочной ткани, неврологические патологии. Поэтому так важно следовать всем врачебным рекомендациям, которые направлены на устранение явлений гипоксии.
Другие осложнения гипоксии, развивающиеся в отдаленном периоде:
- Повышенная тревожность.
- Беспричинное беспокойство ребенка.
- Нестабильность психики.
- Задержка физического и умственного развития, что приводит к низкой успеваемости в школе.
- Регулярные головные боли.
- Стойкое повышение внутричерепного давления.
- Вегетососудистая дистония.
- Развитие эпилептических припадков.
- Поражение нервных тканей.
Современная медицина позволяет избежать тяжелых последствий гипоксии головного мозга. Поэтому инвалидизация ребенка и летальный исход наблюдаются редко.
Своевременная диагностика и лечение гипоксии – это залог здоровья ребенка в будущем.
Диагностика
Врач определяет кислородное голодание у ребенка, отталкивается от шкалы Апгар. Важно учитывать частоту дыхания и сердечных сокращений, наличие рефлексов у младенца, его мышечный тонус. Обязательно выполняется забор крови для проведения лабораторного анализа КОС (кислотно-основное состояние).

Младенцу показано раннее проведение УЗИ головного мозга. Это исследование носит название ультрасонографии. Состояние мозга оценивается через незаросший родничок. Врач получает информацию о состоянии церебральных сосудов, о наличии и расположении кровоизлияний, если таковые имелись.
В отличие от взрослых людей, гипоксия головного мозга у новорожденных вызывает тяжелые последствия в виде повышенной нервной возбудимости, а очаговая симптоматика у них отсутствует. Это означает, что у младенца может не быть судорог, но он не переносит ношения на руках, быстро мерзнет, сильно плачет без имеющейся на то причины. В тяжелых случаях наблюдается угнетение деятельности центральной нервной системы.
Лечение
Гипоксия у грудничка – это опасное состояние, которое требует незамедлительного начала лечения. Головной мозг особенно восприимчив к дефициту кислорода, поэтому последствия могут быть самыми серьезными. Отсутствие терапии приводит к необратимым изменениям в его структуре.
Тяжелая гипоксия требует реанимационных действий со стороны медицинского персонала. Они должны быть направлены на устранение дыхательной недостаточности, на нормализацию сердечной деятельности. Важно восстановить обменные процессы в организме малыша, стабилизировать баланс электролитов.

Алгоритм лечебных мероприятий:
- Освобождение органов дыхания от попавшей в них слизи, каловых масс, околоплодных вод. Их удаляют с помощью специального аспиратора.
- Подача младенцу кислорода с помощью маски и через носовой катетер. Тяжелое поражение мозга требует подключения к аппарату искусственной вентиляции легких. Иногда выполняется интубация.
- Подача раствора глюкозы концентрацией 20% и кокарбоксилазы. Дозу рассчитывают согласно весу ребенка. Капельницу подключают к пуповинной вене.
- Выполнение непрямого массажа сердца. Его проводят при развивающейся брадикардии или отсутствии сердечной деятельности.
- Переливание крови. Процедуру выполняют при развитии гемолитической болезни новорожденных.
- Устранение патологической симптоматики. Может потребоваться купирование судорог, снижение внутричерепного давления, устранение явлений гипотонии.
После устранения острой стадии гипоксии ребенка могут поместить в инкубатор для дальнейшего мониторинга его состояния. Когда угроза для жизни и здоровья будет устранена, младенца переводят в палату к матери.
После выписки из родильного дома за ребенком устанавливается особый режим наблюдения. Он позволит вовремя обнаружить и предупредить развитие поздних осложнений гипоксии.
Отсроченная реабилитация младенца
Ребенку, пережившему кислородное голодание, требуется посещать физиотерапевтический кабинет. В обязательном порядке ему назначают лечебный массаж и гимнастику. Врач подбирает оптимальный режим кормления, объясняет родителям правила ухода за младенцем.
Иногда после выписки из роддома необходим прием препаратов, направленных на снижение внутричерепного давления. Чаще всего назначают Диакарб и Аспаркам. По показаниям используются противосудорожные лекарственные средства.
Для профилактики нервных расстройств и для улучшения питания головного мозга может быть использован Пирацетам или Винпоцетин. Народные методы лечения в раннем возрасте не применимы. Если мать замечает, что у младенца начинают проявляться отдаленные последствия гипоксии, откладывать визит к врачу не следует.
Кроме наблюдения у педиатра, ребенок должен несколько раз в месяц осматриваться неврологом.
Профилактика
Профилактика гипоксии у ребенка – это одна из первоочередных задач, которая встает перед беременной женщиной. Чтобы не пришлось долго лечиться от последствий кислородного голодания, будущая мама должна соблюдать следующие рекомендации:
- Проводить время на свежем воздухе. Важно не просто сидеть, а совершать пешие прогулки. Так организм будет получать достаточное количество кислорода.
- Отказаться от вредных привычек. Алкоголь и табачный дым отрицательным образом влияют на состояние плода.
- Заниматься специальной гимнастикой для беременных женщин.
- Регулярно наблюдаться у гинеколога, соблюдать его рекомендации.
- Вовремя сдавать анализы.
- Правильно питаться. В меню обязательно должны присутствовать свежие фрукты и овощи, яйца, зелень, морепродукты, печень. Доказано, что анемия способствует развитию гипоксии плода.
- Придерживаться распорядка дня.
- Все экстрагенитальные инфекции должны быть пролечены до появления ребенка на свет.
Сразу после начала схваток необходимо вызывать скорую помощь и отправляться в медицинское учреждение. Только в условиях роддома новорожденному может быть оказана качественная помощь. Роды на дому являются опасными. Очень часто такие мероприятия заканчиваются тяжелыми последствиями для женщины и ребенка.

С целью профилактики гипоксии, акушеры должны незамедлительно снимать пуповину с шеи ребенка. Важно быстро очищать его дыхательные пути от слизи и других примесей, мешающих нормальному дыханию. Соблюдение акушерского пособия при ведении родов является основной профилактики гипоксии в условиях роддома.
Прогноз
Прогноз зависит от того, как сильно пострадал головной мозг ребенка. Немаловажное значение имеет скорость и полнота оказания медицинской помощи. У большинства младенцев в месячном возрасте и старше наблюдаются различные расстройства. Они проявляются в виде судорог, гипервозбудимости, перинатальной энцефалопатии. При качественной реабилитации к младшему дошкольному возрасту от этих явлений удается избавиться. Хотя лабильность психики, головные боли и некоторое отставание в развитии может сохраняться в течение жизни.
Тяжелая гипоксия способна приводить к формированию кист в головном мозге, развитию эпилепсии, гидроцефалии. Прогноз зависит от конкретного осложнения, возникшего у ребенка.
Каждая будущая мать должна понимать опасность гипоксии для младенца и прикладывать усилия, направленные на ее профилактику.
В модели повреждения головного мозга у приматов в терминах «новорожденный» распределение повреждений было связано с продолжительностью и тяжестью ишемии. В то время как острая глубокая асфиксия приводила к повреждению базальных ганглиев и таламуса, частичная асфиксия вызывала повреждение белого вещества [Myers, 1972, 1975]. Подобные паттерны повреждения обнаруживаются у доношенных новорожденных после гипоксии-ишемии (см. Рис. 17-1). Паттерн с преобладанием базальных ганглиев включает как базальные ганглии и таламус, так и перироландическую кору [Miller et al.2005; Sie et al., 2000; Чау и др., 2009]. Схема водораздела преимущественно включает сосудистый водораздел от белого вещества и до коры головного мозга [Miller et al., 2005; Sie et al., 2000]. Максимальное повреждение как в области водораздела, так и в базальных ядрах приводит к общей структуре повреждения головного мозга [Miller et al., 2005; Sie et al., 2000]. Выявление преобладающего паттерна черепно-мозговой травмы полезно для клинициста, ухаживающего за новорожденным с энцефалопатией, поскольку преобладающий паттерн более тесно связан с исходом развития нервной системы, чем тяжесть травмы в любом конкретном регионе [Miller et al., 2005].
Последним паттерном травмы, все чаще распознаваемым МРТ, является «очаговый или мультифокальный» паттерн: инсульт или повреждение белого вещества (WMI). Последние данные свидетельствуют о том, что инсульты (артериальные или венозные) также связаны с неонатальной энцефалопатией у новорожденного [Cowan et al., 2003]. Многие новорожденные, перенесшие инсульт, имеют множественных факторов риска черепно-мозговой травмы, включая осложнения внутри рода.
В то время как WMI является характерным паттерном черепно-мозговой травмы у недоношенных новорожденных, он все чаще распознается у доношенных новорожденных с энцефалопатией, выявленных у 23 процентов в одной серии (см. Рис. 17-1) [Li et al., 2009]. В этой серии WMI продемонстрировал ограниченную диффузию на картах АЦП практически у всех новорожденных, что позволяет предположить, что эти поражения были приобретены при рождении. Поскольку у новорожденных с WMI была более умеренная энцефалопатия по сравнению с другими новорожденными в когорте, эти повреждения, возможно, были недоопределены в прошлом. Более низкий гестационный возраст при рождении, в пределах диапазона срока рождения, был связан с увеличением степени тяжести WMI, что указывает на роль созревания мозга в этиологии этого паттерна повреждения [Li et al., 2009]. В последовательных исследованиях доношенных новорожденных с энцефалопатией также наблюдается замедленная дегенерация белого вещества, распространяющаяся на первую неделю жизни [Barkovich et al., 2006; Нил и Индер, 2006]. Этот отсроченный WMI может следовать за повреждением базальных ядер, точно так же как валериановая дегенерация кортикально-спинального тракта обнаруживается после некоторых инсультов средней мозговой артерии у термина новорожденный [De Vries et al., 2005; Киртон и др., 2007]. Следует отметить, что доношенные дети с врожденными пороками сердца также имеют поразительно высокую частоту возникновения WMI при МРТ и при вскрытии [McQuillen et al.2007; Mahle et al., 2002; Галли и др., 2004; Жиль и др., 1973; Кинни и др., 2005]. Подобно недоношенным новорожденным и доношенным новорожденным с энцефалопатией, те, у кого врожденные пороки сердца, подвержены риску нарушения доставки энергетических субстратов из-за ишемии, воспаления и окислительного стресса, особенно при сердечно-легочном шунтировании. Последние данные исследований вскрытия и визуализации мозга показывают, что внутриутробное развитие мозга задерживается у новорожденных с некоторыми формами серьезных врожденных пороков сердца [Miller et al.2007; Розенталь, 1996; Лихт и др., 2009]. Эти отклонения в раннем развитии мозга могут объяснить преобладание WMI у доношенных новорожденных с врожденным пороком сердца, в отличие от более ожидаемого «терминального» преобладания повреждения базальных ядер или областей водораздела преимущественно.
,- О
- О нас
- Редакционная команда
- Эксклюзивное интервью
- В новостях
- Партнеры и филиалы
- Реклама у нас
- Карта сайта
- Мое здоровье
- Карьера
- Стажировка
- Medblogs
- Свяжитесь с нами
- английский (США)
- हिन्दी
- франции
- Español
- 中文

- английский (США)
Икс
- हिन्दी
- франции
- Español
- 中文
- Войти / Зарегистрироваться
- Войти / Зарегистрироваться
- Подробнее
- Медицинские центры
- Тревога и депрессия
- Здоровье детей
Ингибирование фермента в мозге новорожденных, страдающих от недостатка кислорода и кровотока, останавливает тип повреждения головного мозга, который является основной причиной церебрального паралича, психического Задержка и смерть, по словам исследователей в Медицинском центре детской больницы Цинциннати.
Сообщая о своих результатах в Journal of Neuroscience , ученые показывают, что блокирование фермента мозга, активатора плазминогена тканевого типа (tPA), предотвращает прогрессирующее повреждение головного мозга, вызванное недостатком кислорода и кровоснабжения.Экспериментальное доклиническое лечение включало введение в мозг новорожденных крыс вещества природного происхождения, называемого ингибитором активатора плазминогена-1 (PAI-1), говорит Чиа-Йи Куан, доктор медицинских наук, старший исследователь исследования и исследователь в отделениях биологии развития и неврологии в Цинциннати Детский.
Помимо демонстрации мозговой системы активатора плазминогена играет ключевую роль в неонатальной церебральной гипоксически-ишемической травме головного мозга, доктор Куан сказал, что исследование также показывает, что эта система может быть многообещающей терапевтической мишенью у младенцев, страдающих гипоксически-ишемической энцефалопатией (HIE).Определение цели лечения является жизненно важным шагом к поиску лучших способов лечения новорожденных с ГИЭ.
«Мало того, что гипоксически-ишемическая энцефалопатия является важной причиной перинатальной смертности и постоянных неврологических заболеваний, но в современной медицинской практике нет специальных препаратов против ГИЭ», — объяснил Тон Дж. ДеГро, доктор медицинских наук, директор по неврологии. в Цинциннати Детский. «Вот почему результаты этого исследования могут иметь важные клинические последствия, потому что в модели HIE на грызунах они показывают, что ингибирование активаторов плазминогена в функциональных областях мозга является мощной стратегией защиты мозга».»
Ранее проведенные исследования указывали на роль определенных протеаз или энзимов головного мозга в повреждении мозга у взрослых после инсульта, но очень мало было известно о том, что эти ферменты делают при неонатальной церебральной гипоксической ишемии, по мнению исследователей. Фермент в этом случае, tPA, обычно расщепляет белки и другие молекулы, чтобы устранить сгустки крови.
В настоящее исследование были включены недельные крысы, у которых индуцировалась гипоксия-ишемия мозга. Исследователи обнаружили, что гипоксия-ишемия приводит к повышению активности tPA.Фермент затем повреждает сосуды головного мозга и гематоэнцефалический барьер. Гематоэнцефалический барьер представляет собой защитную систему, предназначенную для предотвращения проникновения переносимых кровью веществ, в частности воспалительных клеток или потенциальных загрязнителей, в центральную нервную систему.
Доктор Куан и его коллеги сообщают, что повышенная активность tPA запускается раньше при гипоксии головного мозга, чем другие протеазы, особенно матриксные металлопротеиназы, в прогрессирующем молекулярном процессе, который приводит к повреждению головного мозга.Это делает целью терапевтического вмешательства более раннюю остановку процесса травмы.
Чтобы проверить важность активатора плазминогена в HIE, исследовательская группа исследовала терапевтический эффект инъекции PAI-1 новорожденным крысам, страдающим от снижения мозгового кровотока и системной гипоксии. Ингибитор фермента вводили в интрацеребровентрикулярную область мозга, которая включает систему каналов, которые распределяют спинномозговую жидкость по всему органу.
Исследователи обнаружили, что инъекция PAI-1 значительно снижает активность как tPA, так и другого фермента мозга, активатора плазминогена типа урокиназы. Он также блокировал вызванную гипоксической ишемией активацию матричных металлопротеиназ и повреждение гематоэнцефалического барьера. Исследователи также применили тесты магнитно-резонансной томографии и микроскопический анализ тканей головного мозга, которые показали, что лечение PAI-1 значительно снижает отек мозга, дегенерацию аксонов и потерю ткани головного мозга.
Доктор Куан сказал, что необходимы дополнительные исследования для проверки эффективности и безопасности терапии PAI-1 на других моделях экспериментальных животных. Исследовательская группа также рекомендует провести исследования, чтобы определить, имеют ли повышенные уровни tPA и плазмина в мозге или спинномозговой жидкости у младенцев с диагнозом ГИЭ или с высоким риском церебрального паралича.
У новорожденных людей гипоксическое повреждение головного мозга обычно происходит непосредственно перед, во время или вскоре после рождения, затрагивая от двух до четырех из каждых 1000 рождений.Причины в основном неизвестны, хотя некоторые исследования указывают на возможность проблем с плацентой, артериального давления у матери или осложнений, связанных с пуповиной. Почти 20 процентов новорожденных детей с гипоксической ишемией умирают, а 25 процентов выживших страдают от неврологических проблем на протяжении всей жизни.
Финансирование для исследования поступило от Национального института здравоохранения и Ассоциации Альцгеймера. Первым автором исследования является Дианер Ян, доктор философии, научный сотрудник доктораЛаборатория Куана. В исследовании также участвовали Центр исследования изображений / Отделение радиологии в Цинциннати Детский и Отделение внутренней медицины / Отделение сердечно-сосудистой медицины в Медицинской школе Мичиганского университета.
,CINCINNATI — Ингибирование энзима в мозге новорожденных, страдающих от недостатка кислорода и кровотока, останавливает тип повреждения головного мозга, который является основной причиной церебрального паралича, умственной отсталости и смерти, согласно исследователям из Медицинского центра детской больницы Цинциннати.
Сообщая о своих результатах в Journal of Neuroscience , ученые показывают, что блокирование фермента мозга, активатора плазминогена тканевого типа (tPA), предотвращает прогрессирующее повреждение головного мозга, вызванное недостатком кислорода и кровоснабжения.Экспериментальное доклиническое лечение включало введение в мозг новорожденных крыс вещества природного происхождения, называемого ингибитором активатора плазминогена-1 (PAI-1), говорит Чиа-Йи Куан, доктор медицинских наук, старший исследователь исследования и исследователь в отделениях биологии развития и неврологии в Цинциннати Детский.
Помимо демонстрации мозговой системы активатора плазминогена играет ключевую роль в неонатальной церебральной гипоксически-ишемической травме головного мозга, доктор Куан сказал, что исследование также показывает, что эта система может быть многообещающей терапевтической мишенью у младенцев, страдающих гипоксически-ишемической энцефалопатией (HIE).Определение цели лечения является жизненно важным шагом к поиску лучших способов лечения новорожденных с ГИЭ.
«Мало того, что гипоксически-ишемическая энцефалопатия является важной причиной перинатальной смертности и постоянных неврологических заболеваний, но в современной медицинской практике нет специальных препаратов против ГИЭ», — объяснил Тон Дж. ДеГро, доктор медицинских наук, директор по неврологии. в Цинциннати Детский. «Вот почему результаты этого исследования могут иметь важные клинические последствия, потому что в модели HIE на грызунах они показывают, что ингибирование активаторов плазминогена в функциональных областях мозга является мощной стратегией защиты мозга».»
Ранее проведенные исследования указывали на роль определенных протеаз или энзимов головного мозга в повреждении мозга у взрослых после инсульта, но очень мало было известно о том, что эти ферменты делают при неонатальной церебральной гипоксической ишемии, по мнению исследователей. Фермент в этом случае, tPA, обычно расщепляет белки и другие молекулы, чтобы устранить сгустки крови.
Текущее исследование, опубликованное на сайте журнала в этом месяце, включало недельных крыс, у которых индуцировалась гипоксия-ишемия головного мозга.Исследователи обнаружили, что гипоксия-ишемия приводит к повышению активности tPA. Фермент затем повреждает сосуды головного мозга и гематоэнцефалический барьер. Гематоэнцефалический барьер представляет собой защитную систему, предназначенную для предотвращения проникновения переносимых кровью веществ, в частности воспалительных клеток или потенциальных загрязнителей, в центральную нервную систему.
Доктор Куан и его коллеги сообщают, что повышенная активность tPA запускается раньше при гипоксии головного мозга, чем другие протеазы, особенно матриксные металлопротеиназы, в прогрессирующем молекулярном процессе, который приводит к повреждению головного мозга.Это делает целью терапевтического вмешательства более раннюю остановку процесса травмы.
Чтобы проверить важность активатора плазминогена в HIE, исследовательская группа исследовала терапевтический эффект инъекции PAI-1 новорожденным крысам, страдающим от снижения мозгового кровотока и системной гипоксии. Ингибитор фермента вводили в интрацеребровентрикулярную область мозга, которая включает систему каналов, которые распределяют спинномозговую жидкость по всему органу.
Исследователи обнаружили, что инъекция PAI-1 значительно снижает активность как tPA, так и другого фермента мозга, активатора плазминогена типа урокиназы. Он также блокировал вызванную гипоксической ишемией активацию матричных металлопротеиназ и повреждение гематоэнцефалического барьера. Исследователи также применили тесты магнитно-резонансной томографии и микроскопический анализ тканей головного мозга, которые показали, что лечение PAI-1 значительно снижает отек мозга, дегенерацию аксонов и потерю ткани головного мозга.
Доктор Куан сказал, что необходимы дополнительные исследования для проверки эффективности и безопасности терапии PAI-1 на других моделях экспериментальных животных. Исследовательская группа также рекомендует провести исследования, чтобы определить, имеют ли повышенные уровни tPA и плазмина в мозге или спинномозговой жидкости у младенцев с диагнозом ГИЭ или с высоким риском церебрального паралича.
У новорожденных людей гипоксическое повреждение головного мозга обычно происходит непосредственно перед, во время или вскоре после рождения, затрагивая от двух до четырех из каждых 1000 рождений.Причины в основном неизвестны, хотя некоторые исследования указывают на возможность проблем с плацентой, артериального давления у матери или осложнений, связанных с пуповиной. Почти 20 процентов новорожденных детей с гипоксической ишемией умирают, а 25 процентов выживших страдают от неврологических проблем на протяжении всей жизни.
###
Финансирование для исследования поступило от Национального института здравоохранения и Ассоциации Альцгеймера. Первым автором исследования является Dianer Yang, Ph.Д., научный сотрудник лаборатории доктора Куана. В исследовании также участвовали Центр исследования изображений / Отделение радиологии в Цинциннати Детский и Отделение внутренней медицины / Отделение сердечно-сосудистой медицины в Медицинской школе Мичиганского университета.
О Цинциннати Детский
Медицинский центр детской больницы Цинциннати является одной из 10 детских больниц в Соединенных Штатах Америки, которая внесла Почетный знак в США.S. News and World Reports 2009-10 Выпуск лучших детских больниц Америки. Он занял первое место в рейтинге расстройств пищеварения, а также получил высокую оценку за свои знания в области респираторных заболеваний, рака, ухода за новорожденными, ухода за сердцем, нейрохирургии, диабета, ортопедии, заболеваний почек и урологии. Cincinnati Children’s, одна из трех крупнейших детских больниц в США, входит в состав Медицинского колледжа Университета Цинциннати и является одним из двух лучших получателей педиатрических исследовательских грантов от Национального института здравоохранения.
Президент Барак Обама в июне 2009 года назвал Цинциннати Детский «островом совершенства» в области здравоохранения. За свои достижения в преобразовании здравоохранения, Cincinnati Children’s является одной из шести больниц США с 2002 года, которая была удостоена награды Американской ассоциации больниц McKesson Quest за качество за лидерство и инновации в области качества, безопасности и приверженности уходу за пациентами. Больница является национальным и международным справочным центром для сложных случаев. Дополнительную информацию можно найти на сайте www.cincinnatichildrens.org.
Отказ от ответственности: AAAS и EurekAlert! не несем ответственности за точность выпусков новостей, публикуемых EurekAlert! предоставляя учреждения или для использования любой информации через систему EurekAlert.
,