Когда начинается токсикоз после зачатия
Беременность: PixabayКогда начинается токсикоз — этот вопрос заставляет нервничать многих женщин, которые только планируют завести ребенка. Вероятность возникновения проблем со здоровьем пугает и беспокоит будущим мам. Однако не все женщины во время вынашивания малыша страдают от тошноты и слабости. Давайте разберемся, что такое токсикоз, почему он появляется во время беременности, какими признаками сопровождается и что делать, чтобы почувствовать себя лучше.
Токсикоз беременных: признаки
Почему же так происходит, что одни девушки всю беременность испытывают дискомфорт и тошноту, а другие даже не знают, что такое токсикоз? Исследователи затрудняются дать ответ на этот вопрос. Но некоторые специалисты утверждают, что проблема заключается в психологии. Когда будущая мать дала себе команду, что ей будет плохо по утрам, то, вероятнее всего, так и будет случаться.
Моя коллега Е. Е. Вишневская из ФГБУ НИИАГ им. Д. О. Отта СЗО РАМН в научной статье более детально разобралась в вопросе влияния психологического состояния беременной на развитие токсикоза раннего характера.
Е. Вишневская из ФГБУ НИИАГ им. Д. О. Отта СЗО РАМН в научной статье более детально разобралась в вопросе влияния психологического состояния беременной на развитие токсикоза раннего характера.
Что такое токсикоз? Болезнь? На самом деле, нет. Подобное утверждение многих людей является неверным. Считается, что токсикоз — приспособление женского организма к новому положению.
Мейриева П. М., Аушева Р. Б.: Ранний токсикоз беременных / Молодой ученый. — 2019. — №5. — С. 67-68.Врач-гинеколог Г. М. Савельева в собственной книге рассказывает, что это состояние женского организма проявляется такими признаками:
- усталостью;
- депрессивным и агрессивным настроением;
- тошнотой;
- паническими атаками;
- выделением большого количества слюны;
- рвотными рефлексами.
Дополнительно может появиться общая слабость во всем теле, постоянное желание пойти поспать и высокий уровень раздражительности. У некоторых беременных также присутствует высокая температура при токсикозе.
Если заметили такие симптомы, не стоит впадать в панику. Обратитесь к лечащему доктору, который расскажет, чем обусловлен токсикоз и как с ним справиться.
Считается, что тошнота по утрам во время беременности встречается у 60% будущих мам. Позывы происходят около 2–3-х раз в день и не оказывают никакого влияния на аппетит.
Порой случаются ситуации, когда женщины, вынашивающие малыша, не могут съесть даже минимум еды. В результате они теряют массу, организм начинает обезвоживаться, увеличивается количество ударов сердца, а тошнотные позывы только учащаются. Представленные симптомы называют тяжелой степенью недомогания. Подобные признаки говорят о необходимости лечения.
Независимо от того, какая причина токсикоза у женщины при вынашивании ребенка, если степень недомогания легкая, переживать не стоит. Стресс плохо скажется на будущем малыше.
Токсикоз при беременности: причины
Давайте разберемся, почему возникает такой признак токсикоза, как тошнота с утра. К основным факторам риска мои коллеги относят влияние различных внешних раздражителей на организм беременной женщины, а также стрессовые ситуации, наследственную предрасположенность и хронические недуги.
К основным факторам риска мои коллеги относят влияние различных внешних раздражителей на организм беременной женщины, а также стрессовые ситуации, наследственную предрасположенность и хронические недуги.
Существует предположение, что причиной прогрессирования раннего токсикоза является противостояние иммунологического характера организма матери и плода.
Дискомфорт на ранних сроках может появиться вследствие гормональных деформаций, когда уровень гормонов резко подскакивает или снижается. Именно эти элементы оказывают влияние на функционирование органов и систем ЖКТ.
Вне зависимости от причины появления токсикоза у беременной, если недомогание проходит в легкой форме, то волноваться незачем, ведь все знают, что будущим мамочкам нельзя переживать.
Я и мои коллеги часто встречаемся с подобными ситуациями у беременных. На практике причин может оказаться сразу несколько. Их всегда нужно проверять и подтверждать, чтобы принять правильные меры. На своем опыте скажу, что, если вас сильно мучит токсикоз, необходимо обязательно записаться на консультацию к медику, а не искать в интернете какую-либо информацию.
На практике причин может оказаться сразу несколько. Их всегда нужно проверять и подтверждать, чтобы принять правильные меры. На своем опыте скажу, что, если вас сильно мучит токсикоз, необходимо обязательно записаться на консультацию к медику, а не искать в интернете какую-либо информацию.
Когда начинается токсикоз при беременности
Многие женщины задаются актуальным вопросом: «На какой неделе начинается токсикоз?». Как правило, первые симптомы недомогания появляются на 21 день после зачатия. Но иногда у девушек появляется тошнота после приема пищи даже спустя несколько дней. В этот ранний период беременность может не подтвердиться.
Обычно плохое самочувствие у беременных ярко выражено в первые 90 дней. Но это напрямую зависит от самого организма. Моя коллега Скоркина С. М. в диссертации «Влияние раннего токсикоза (рвота беременных) на систему агрегатного состояния крови» выделила основные особенности раннего токсикоза.
Токсикоз начинает исчезать, когда заканчивается образование плаценты и нормализуется уровень гормонов. Зачастую это происходит на 12 неделе вынашивания малыша. К 16 неделе у большей части пациенток пропадают любые признаки недомогания. Если этого не произошло, то, скорее всего, у беременной симптоматика позднего токсикоза. Подобное состояние намного серьезнее простого недомогания.
Зачастую это происходит на 12 неделе вынашивания малыша. К 16 неделе у большей части пациенток пропадают любые признаки недомогания. Если этого не произошло, то, скорее всего, у беременной симптоматика позднего токсикоза. Подобное состояние намного серьезнее простого недомогания.
При позднем токсикозе проявляются следующие симптомы:
- отеки рук и ног;
- повышение артериального давления;
- головные боли;
- судорожные приступы;
- белок в анализе мочи;
- нарушения зрительной функции.
Подобное нарушение в организме беременной появляется в результате регулярного недосыпа, травмирования сосудов и проблем с иммунной системой.
Я была свидетелем подобной ситуации, когда несколько женщин столкнулись с признаками позднего токсикоза. Могу сказать наверняка, что сдача анализов и своевременная консультация у специалиста дают возможность улучшить состояние пациентки в кратчайшие сроки.
Когда появляется токсикоз, облегчить общее состояние можно простыми способами, которые приведены в авторитетном интернет-издании WebMD:
- проснувшись, съедайте ломтик сыра или какой-нибудь фрукт;
- собираясь на прогулку, берите с собой горсть печенья, орехов или фрукт;
- старайтесь не находиться в тесных и душных комнатах, где скапливаются неприятные ароматы;
- регулярно проветривайте квартиру или дом;
- употребляйте чай с мятой и ягодами малины, а также отвары из шиповника;
- старайтесь днем немного отдыхать от повседневных дел.
Моя практика подтверждает: такие простые советы действительно помогают избавиться от плохого самочувствия. Лично я встречала многих женщин, которых мучил токсикоз во время вынашивания ребенка. Как только они начинали придерживаться рекомендаций медиков, их состояние быстро приходило в норму. Подобные способы избавления от токсикоза я, как врач, одобряю и рекомендую.
Теперь вы знаете, на каком сроке начинается токсикоз, его признаки и причины появления.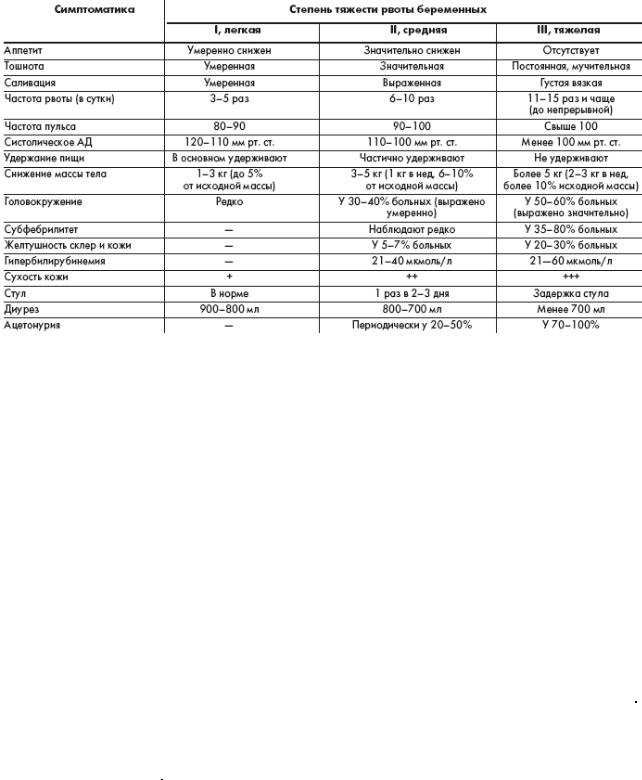 Правильно составленный рацион питания, регулярные прогулки на свежем воздухе, полноценный сон, систематические консультации с лечащим доктором и позитивный настрой помогут справиться с плохим самочувствием. Наслаждайтесь беременностью и ожидайте желанного ребенка, отбросив все волнения в долгий ящик.
Правильно составленный рацион питания, регулярные прогулки на свежем воздухе, полноценный сон, систематические консультации с лечащим доктором и позитивный настрой помогут справиться с плохим самочувствием. Наслаждайтесь беременностью и ожидайте желанного ребенка, отбросив все волнения в долгий ящик.
Внимание! Материал носит лишь ознакомительный характер. Не следует прибегать к описанным в нем методам лечения без предварительной консультации с врачом.
Источники:
- Вишневская Е.Е. Влияние психического состояния беременной на развитие раннего токсикоза // Журнал акушерства и женских болезней. — 2014. — №2. — С. 78–83.
- Савельева Г.М. Акушерство // Московский государственный медико-стоматологический университет им. А.И. Евдокимова.
- Скоркина С.М. Влияние раннего токсикоза (рвота беременных) на систему агрегатного состояния крови // ГУЗ «Московский областной научно-исследовательский институт акушерства и гинекологии».
- Nivin Todd.
 Vomiting During Pregnancy Treatment // WebMD. — 2020. — 14 January.
Vomiting During Pregnancy Treatment // WebMD. — 2020. — 14 January.
Автор: кандидат медицинских наук Анна Ивановна Тихомирова
Рецензент: кандидат медицинских наук, профессор Иван Георгиевич Максаков
Оригинал статьи: https://www.nur.kz/health/motherhood/1766244-kogda-nacinaetsa-toksikoz-posle-zacatia/
С какой недели начинается токсикоз при беременности? Сколько длится токсикоз у беременных
Принято считать, что токсикоз обязательно сопровождает каждую беременность. Утреннюю тошноту многие воспринимают неотъемлемым атрибутом, а также первым симптомом того, что женщина в положении. На самом деле все очень индивидуально. Одной даме назначается коррекционное лечение, чтобы купировать сильную тошноту. Другие напротив, выносив нескольких детей не знают, что это такое. Сегодня поговорим о том, с какой недели начинается токсикоз при беременности.
Другие напротив, выносив нескольких детей не знают, что это такое. Сегодня поговорим о том, с какой недели начинается токсикоз при беременности.
Коротко о главном
На самом деле вынашивание ребенка может проходить легко и просто. Женщина радуется, что у нее будет маленький и расцветает день ото дня. Но если нарушены процессы адаптации к новому состоянию, то начинается при беременности токсикоз. С какой недели чаще всего женщины жалуются на плохое самочувствие? Об этом чуть ниже. Отметим только что явление очень распространенное. Когда начинает развиваться плод, в организм матери поступают токсины и вещества, провоцирующие отравление. Через определенное время запускаются адаптационные процессы, в работу включается плацента и состояние выравнивается. Теперь до окончания развития крохи, будущая мама чувствует себя удовлетворительно.
Основные признаки
На самом деле они могут быть явными и скрытыми. Есть те, которые сложно скрыть от окружающих, к ним можно отнести сильную тошноту, частую рвоту, слюноотделение. Но это еще не все. Токсикоз также проявляется плохим настроением, сильной слабостью и сонливостью. Кто-то отмечает сильнейшую раздражительность, резкую потерю веса. Зная, с какой недели начинается токсикоз при беременности, можно подготовить себя к этому. Кроме того, своевременные профилактические мероприятия позволяют снизить его проявление.
Но это еще не все. Токсикоз также проявляется плохим настроением, сильной слабостью и сонливостью. Кто-то отмечает сильнейшую раздражительность, резкую потерю веса. Зная, с какой недели начинается токсикоз при беременности, можно подготовить себя к этому. Кроме того, своевременные профилактические мероприятия позволяют снизить его проявление.
В некоторых случаях токсикоз вызывает довольно сильные осложнения. Повышенная нагрузка на организм мамы провоцирует развитие дерматозов и дерматитов, проявляется в виде судорожных сокращений мышц, размягчения костей, желтухи и бронхиальной астмы.
Истоки проблемы
Есть статистика, что у одной из двух мамочек развивается умеренная тошнота по утрам. Одна из пяти испытывает сильный дискомфорт в течение всего дня. У одной из десяти такие симптомы продолжаются длительное время. На протяжении всего первого триместра и даже поздней. А что говорят врачи? С какой недели начинается токсикоз при беременности в норме?
Акушеры и гинекологи уверены, что в этом случае его не должно быть вовсе. То есть тошнота и утренняя рвота являются допустимыми, но говорят о конфликте материнского организма и плода. И сегодня истинные причины токсикоза остаются неизвестными. Есть только предположения, которые имеют долю истины.
То есть тошнота и утренняя рвота являются допустимыми, но говорят о конфликте материнского организма и плода. И сегодня истинные причины токсикоза остаются неизвестными. Есть только предположения, которые имеют долю истины.
Возможные причины
Каждая из них может быть основной или дополнительной для отдельной женщины. Но в любом случае разбираться и назначать коррекционные методы должен врач. Перечислим возможные причины для ознакомления:
- Сбой в работе гормональной системы. Как только эмбрион имплантируется в стенку матки, их выработка меняется. Теперь весь организм перестраивается на обеспечение жизнедеятельности плода. Вот и ответ на вопрос, на каком сроке начинается токсикоз у беременных. Первые признаки женщина может испытывать, еще не зная о своем положении. Но особые вещества уже поступают в кровь, что сказывается на самочувствии и настроении. Появляется раздражительность, обидчивость и плаксивость. Кроме того, организм матери воспринимает малыша как инородное тело.
 Чтобы он не избавился от плода, за счет особого механизма угнетается работа иммунной системы. Это тоже тесно связано с работой гормонов. А следовательно, любую простуду вы будете переносить намного тяжелей.
Чтобы он не избавился от плода, за счет особого механизма угнетается работа иммунной системы. Это тоже тесно связано с работой гормонов. А следовательно, любую простуду вы будете переносить намного тяжелей. - Формирование плаценты. Еще одна точка опоры, которая помогает понять, на каком сроке начинается токсикоз у беременных. Когда яйцеклетка имплантируется в полость матки, она бурно растет. Всего через пару недель это уже крохотный организм, естественные выделения которого поступают непосредственно в кровь матери. Примерно к 12 неделе включается в работу плацента. Теперь она берет на себя роль фильтра вредных веществ. То есть токсикоз в первом триместре беременности длиться как раз до этого срока, постепенно ослабевая.
- Защитная реакция. Будущая мама чувствует тошноту от запаха сигарет и алкоголя, кофе.
Дополнительные факторы
Помимо основных, есть еще целый ряд параметров, который определяет развитие токсикоза.
- Хронические заболевания.
 Не все, но большинство из них способствует утренней слабости и тошноте.
Не все, но большинство из них способствует утренней слабости и тошноте. - Нервно-психическое перенапряжение. То есть стрессы могут сильно ухудшить состояние будущей мамы.
- Возраст. Как правило, если это первая и поздняя беременность, то токсикоз проявляется более интенсивно.
- Двойня или тройня. Следовательно, и токсикоз будет в два-три раза сильней.
На каком сроке ждать
Если беременность запланированная, то будущая мама часто с первого дня задержки готова уверять всех, что ее тошнит по утрам. Самовнушение это или особенности организма, сложно сказать однозначно. Да и врачи довольно аккуратны в своих прогнозах. Говоря о том, через сколько после зачатия начинается токсикоз нужно отметить, что врачи выделяют два вида по срокам его появления. То есть ранний и поздний.
- Обычно первый начинается с первых дней задержки месячных и заканчивается к началу второго триместра. То есть вздохнуть с облегчением можно будет к 12 или 13 неделе. Но все женщины разные, не существует конкретных ограничений и рамок в этом вопросе.

- Поздний токсикоз — он же гестоз, начинается в начале последнего триместра или конце второго. Он очень опасен как для матери, так и для ребенка. Поздний токсикоз при беременности является серьезным заболеванием, для которого характерны патологические изменения в работе важнейших систем и органов. Поздний токсикоз проявляется сосудистыми нарушениями и расстройствами кровообращения. Это вызывает гипоксию, изменяются функции мозга, работа печени и почек.
Разновидности токсикоза
Как видите, нельзя однозначно ответить даже на простой вопрос, в каком триместре начинается токсикоз. Помимо перечисленного выше, есть еще довольно много подвидов, каждый из которых характеризуется своими особенностями.
- Стафилококковый токсикоз может быть активизирован специфическими штаммами. Развивается через несколько часов после того, как зараженная пища поступила в организм. Симптомы — тошнота и рвота. Обычно в течение 12 часов они проходят сами собой.
- Вечерний токсикоз.
 Возникает в результате сильного переутомления и недостаточного приема пищи. Побороть его можно, если разнообразить питание и совершать прогулки перед сном.
Возникает в результате сильного переутомления и недостаточного приема пищи. Побороть его можно, если разнообразить питание и совершать прогулки перед сном. - Ранний токсикоз. Он считается нормальным явлением. Точно сказать, с какого месяца начинается токсикоз у беременных невозможно. Но обычно имплантация яйцеклетки происходит за 14 дней после оплодотворения. В течение недели — двух после этого женщина может почувствовать симптомы токсикоза. То есть обычно впервые тошнота появляется к концу первого месяца. Как раз тогда, когда многие начинают догадываться о своем положении.
- Поздний токсикоз. В этом случае анализы показывают белок в моче, высокое давление и прибавка в весе более 400 г за неделю.
- Токсикоз до первой задержки месячных. В редких случаях тошнота появляется сразу после зачатия. То есть, когда еще рано говорить о развитии плода как таковом.
Как бороться с тошнотой
Нельзя однозначно сказать, сколько длится токсикоз у беременных. Кто-то говорит, что всего пару раз ощутил тошноту в утренние часы, другие вспоминают про нескончаемый кошмар. Это приносит малоприятных ощущений, но ничего не поделаешь. Как курс молодого бойца в армии. Но есть несложные рекомендации, которые помогут облегчить состояние.
Это приносит малоприятных ощущений, но ничего не поделаешь. Как курс молодого бойца в армии. Но есть несложные рекомендации, которые помогут облегчить состояние.
- Кушать нужно регулярно, небольшими порциями. Допускать переедания или пропускать обед категорически не рекомендуется. Именно на голодный желудок мамочке и становится плохо.
- Лучше всего завтракать, не вставая с постели, и еще немного полежать после приема пищи. Для этого нужно лишь с вечера положить рядом с кроватью банан или несладкий йогурт.
- Переедать нельзя, как бы ни хотелось еще чего-нибудь вкусненького.
- Исключить жареное, копченое, соленое, острое.
- Резкие движения, высокая физическая нагрузка — этого нужно сейчас избегать.
- Чаще бывать на свежем воздухе. Прогулки способствуют хорошему аппетиту.
- Не зря будущих мам тянет на кислое. Это прекрасное средство от тошноты.
Если ничего не помогает и будущая мама все также страдает необходимо обратиться к лечащему врачу. Он назначит курс препаратов, которые подкорректируют ее состояние. Это может быть «Церукал», который влияет на работу всей пищеварительной системы, блокируя сокращения тканей, которые и приводят к рвоте. Дополнительно вводятся сорбенты, которые будут впитывать токсины.
Он назначит курс препаратов, которые подкорректируют ее состояние. Это может быть «Церукал», который влияет на работу всей пищеварительной системы, блокируя сокращения тканей, которые и приводят к рвоте. Дополнительно вводятся сорбенты, которые будут впитывать токсины.
Когда ждать облегчения
Сроки в любом случае индивидуальны. Чаще всего первый раз тошнота посетит на сроке примерно 1 месяц. Но бывает и так, что лишь к 9 неделе начался токсикоз. Его тоже можно считать ранним. Чаще всего к 12-14 неделе про него забывают, второй триместр не зря называют «золотым периодом». Поздний токсикоз обычно не проходит сам собой, а требует специализированного лечения. В любом случае, если будущая мама чувствует себя неважно, ей необходима помощь специалиста. Только врач может оценить ее состояние и принять меры.
Когда начинается токсикоз при беременности
Вовсе не обязательно, что с наступлением беременности женщину непременно начнет тошнить. И даже совершенно не факт, что тошнота появится на более поздних сроках (очень вам этого не желаем). Тем не менее, приблизительно половину женщин начинает тошнить уже на самых ранних сроках беременности.
Тем не менее, приблизительно половину женщин начинает тошнить уже на самых ранних сроках беременности.
Ранний токсикоз может набрать оборотов на любой из недель в первом триместре. Очень часто именно по появлению тошноты и состояния общего недомогания вместе с задержкой очередных месячных женщина начинает подозревать, что, возможно, забеременела.
Первые признаки токсикоза у некоторых женщин могут появляться уже на 3-4 неделе, когда беременность может быть даже еще не подтверждена. Но отзывы тех, кто пережил это неприятное явление в период вынашивания ребеночка, свидетельствуют о том, что в большинстве случаев токсикоз начинается в среднем с 7-8 недели. В целом же ранние токсикозы возникают в первые 12 недель беременности и обычно проявляются:
- плохим самочувствием;
- угнетенным состоянием;
- слюнотечением;
- тошнотой;
- рвотой.
У вас возможно появление слабости, сонливости, раздражительности. Ко всему прочему, у вас может отмечаться даже снижение веса.
Вероятно, вы отметите, что тошнит вас в определенное время, обычно поутру, — утренняя тошнота беременных даже вошла в поговорку. Но может быть и вечерняя и круглосуточная тошнота. Как долго она продлится?
К 13-14 неделям токсикоз обычно утихает, поскольку уровень гормонов к этому времени снижается. Но некоторые бедняжки мучаются до самых родов.
Почему одни женщины страдают от токсикоза, а другим удается прожить всю беременность без него, ученые точный ответ дать не могут. Между тем существует несколько версий о причинах развития токсикоза. Самыми вероятными среди них специалисты считают гормональную перестройку (уровень и соотношение гормонов в организме женщины с наступлением беременности неизбежно изменяются), а также психоэмоциональное состояние будущей матери. Некоторые женщины изначально настраивают себя на то, что их будет тошнить и рвать с первых дней после зачатия, а многие очень сильно переживают насчет течения беременности и развития крохи.
Токсикоз у разных беременных проявляется в неодинаковой степени. Несильные приступы тошноты и рвоты не представляют угрозы маме и малышу. Более того, существует даже мнение, будто бы они в некотором роде полезны, поскольку защищают мать и дитя от потенциального вреда различных веществ. Однако если токсикоз выражен настолько, что женщина не может употреблять пищу, многократно рвет и ощутимо теряет вес, то, скорее всего, придется лечь в больницу и проходить лечение. По крайней мере, под наблюдением врача нужно находиться обязательно! А потому обратитесь к своему гинекологу, если беременность сопровождается сильно выраженным токсикозом.
Хочется успокоить тех будущих мам, которые столкнулись с данным явлением: врачи заверяют, что как только процесс формирования плаценты будет завершен, ранний токсикоз исчезнет. Обычно, приблизительно с 12 недели признаки токсикоза начинают ослабевать, полностью сходя на нет к 16 неделе беременности.
Обычно, приблизительно с 12 недели признаки токсикоза начинают ослабевать, полностью сходя на нет к 16 неделе беременности.
Между тем, у любой женщины, вынашивающей ребенка, может развиться поздний токсикоз, даже если первая половина беременности протекала совершенно благополучно.
Поздние токсикозы возникают во второй половине беременности (после 20 недель беременности), вызывая такие проблемы в организме, как:
Это все последовательные стадии одного патологического процесса.
Поздний токсикоз еще называют гестозом. Чем раньше появляются его симптомы (например, в 24-26 недель), тем тяжелее его течение и хуже прогноз.
Гестоз — это серьезная болезнь, которую нужно лечить, потому что она может нанести вред как вам, так и вашему малышу. Несмотря на высокий уровень развития современной медицины, причины позднего токсикоза остаются загадкой. Существуют только теории его возникновения. Так, многие ученые предполагают, что виной позднего токсикоза являются серьезное повреждение сосудов, иммунный дисбаланс, стрессы, нарушение режима сна, короткий интервал между родами и многое другое.
Специально для beremennost.net – Ксения Дахно
Сроки токсикоза — на каких сроках начинается токсикоз, сколько длится токсикоз при беременности
Когда начинается и заканчивается токсикоз при беременности
Сроки токсикоза очень индивидуальны и зависят от состояния здоровья каждой женщины. Первый триместр беременности может быть осложнен ранним токсикозом и связанными с ним тошнотой и рвотой. Последний триместр опасен развитием позднего токсикоза.
Токсикоз – это комплекс реакций организма на нарушения нормального процесса беременности. Справедливости ради стоит отметить, что с его симптомами в той или иной степени сталкивается большинство беременных. А такие проявления, как тошнота и рвота, приобрели статус классических признаков беременности.
Природа токсикоза многопланова. Реакция организма на развитие в нем новой жизни поступает со стороны нервной системы, со стороны иммунитета. Меняется гормональный фон, и кардинальным образом перестраивается работа внутренних органов.
Меняется гормональный фон, и кардинальным образом перестраивается работа внутренних органов.
Ранний токсикоз
Большинство будущих мам и тех женщин, которые только планируют беременность, задаются вопросом, на каком сроке начинается токсикоз и когда заканчивается. Обычно первые признаки патологии появляются к моменту задержки менструации. В этот период активно проходит гормональная перестройка организма. Повышается уровень прогестерона, который отвечает за сохранность беременности на протяжении всех 9 месяцев. Прогестерон оказывает расслабляющее действие на матку, снижая ее мышечный тонус. Побочным явлением этого процесса становится снижение тонуса и замедление работы органов желудочно-кишечного такта.
В этот момент женщина может впервые ощутить утреннюю тошноту и даже рвоту. Кроме того, повышенное слюноотделение – достаточно частое явление. Токсикоз сроки начала и окончания имеет зависящие от организма каждой конкретной женщины. Длительность и тяжесть патологии напрямую связаны с образом жизни и состоянием здоровья женщины.
Нет единого ответа на вопрос, сколько длится токсикоз при беременности. Можно лишь сказать, что в большинстве случаев все начинается на 4-5 неделе. То есть примерно в тот момент, когда становится известно, что беременность наступила. Заканчивается ранний токсикоз к тому моменту, как стабилизируется гормональный фон. Обычно это происходит на 12-14 неделе беременности.
Если токсикоз длится более 10 недель, то есть продолжает беспокоить женщин после 15 недели беременности, это является однозначным поводом для обращения к врачу.
Как бороться с симптомами токсикоза и как себя вести
Многие считают, что природа ничего не делает просто так. Любое проявление токсикоза может служить сигналом о том, что нужно что-то изменить. Если беременная испытывает умеренный токсикоз, сгладить его проявления удастся с помощью коррекции образа жизни и рациона питания.
Несомненную пользу будущему ребенку и ощутимое снижение дискомфорта обеспечит восстановление нормального кровотока. Для этого необходимо ежедневно выделять время для физической активности на свежем воздухе. Здесь важны оба фактора – и свежий воздух, и движение. Кровь будет активнее циркулировать, насыщаться кислородом и должным образом обеспечивать питание не только будущего ребенка, но и всех органов будущей мамы.
Для этого необходимо ежедневно выделять время для физической активности на свежем воздухе. Здесь важны оба фактора – и свежий воздух, и движение. Кровь будет активнее циркулировать, насыщаться кислородом и должным образом обеспечивать питание не только будущего ребенка, но и всех органов будущей мамы.
Естественным образом будет усиливаться перистальтика кишечника, и появится аппетит. Токсикоз на ранних сроках сигнализирует о том, какие продукты сейчас необходимы организму, а какие принесут вред. Обычно приступы тошноты вызывают продукты быстрого приготовления из магазинов, жаренное, острое. Токсикоз у беременных также естественным образом поможет определиться с режимом питания. Вероятно, предпочтительнее окажется питание небольшими порциями. Кого-то утренняя тошнота заставит съесть яблоко, не вставая с постели, а для кого-то оптимальным решением станет гимнастика (если нет угрозы прерывания беременности) или прогулка на свежем воздухе перед завтраком.
Женщине важно всегда помнить о том, что от ее самочувствия полностью зависит благополучие ее будущего ребенка. Особенно это важно на первых неделях беременности, когда формируются все органы и системы будущего малыша. На этом этапе любые сбои слишком дороги. Вот почему надо обращать внимание не столько на симптомы токсикоза, сколько следить за общим состоянием организма. Если на фоне раннего токсикоза происходит полная потеря аппетита, снижение веса, женщина ощущает постоянную усталость и тягу ко сну – это повод не только изменить привычки, но и незамедлительно обратиться к врачу.
Особенно это важно на первых неделях беременности, когда формируются все органы и системы будущего малыша. На этом этапе любые сбои слишком дороги. Вот почему надо обращать внимание не столько на симптомы токсикоза, сколько следить за общим состоянием организма. Если на фоне раннего токсикоза происходит полная потеря аппетита, снижение веса, женщина ощущает постоянную усталость и тягу ко сну – это повод не только изменить привычки, но и незамедлительно обратиться к врачу.
Токсикоз при беременности: что делать, виды токсикоза, симптомы
Количество просмотров: 9 270
Токсикоз при беременности испытывают многие женщины. Практически каждая будущая мама хоть раз сталкивалась с утренней тошнотой. Степень токсикоза бывает разной. Есть счастливицы, которые практически не ощущают неудобств, а некоторые вспоминают эти моменты жизни с содроганием.
Вопросов, связанных с утренними недомоганиями, много. Тошнота при беременности — это нормально? Как долго она будет продолжаться? Нужно терпеть или обращаться к доктору? Указывает ли токсикоз на проблемы со здоровьем? Давайте разбираться.
Тошнота при беременности — это нормально? Как долго она будет продолжаться? Нужно терпеть или обращаться к доктору? Указывает ли токсикоз на проблемы со здоровьем? Давайте разбираться.
Статья написана на основе рекомендаций Всемирной организации здравоохранения (ВОЗ).
Причины возникновения токсикоза на ранних сроках
До сих пор нет единого мнения, почему будущие мамы страдают токсикозом. Существует несколько теорий, но большинство медиков склоняется к тому, что причиной данного недомогания является изменение гормонального баланса на начальных сроках беременности. В среднем на 13-14 неделе тело женщины адаптируется к своему новому состоянию и утренняя тошнота проходит.
В случаях мучительного многократного токсикоза, который сопровождается слюнотечением, и не ослабевает после 12 недели, стоит обратиться к врачу.
Помимо гормональной перестройки организма, токсикоз при беременности может быть вызван такими факторами как:
- наличие заболеваний: язва, гастрит, панкреатит, беременность провоцирует их обострение и тошнота является проявлением патологии
- работа иммунной системы — плод состоит из материнских и отцовских генов, тело матери отторгает чужеродные клетки, что приводит к ухудшению самочувствия, после адаптации иммунной системы токсикоз исчезает
- тошнота, связанная с укачиванием, обнаруживает проблемы с вестибулярным аппаратом.

Токсикоз при беременности на поздних сроках
У большинства женщин токсикоз появится на 5-6 неделе, после 10 пойдет на убыль и к 14 неделе пропадет. То есть, во втором триместре данная проблема будет уже не актуальна. Однако, токсикоз может появиться и на поздних сроках. Тошнота, беспокоящая после 20-24 недель, – повод незамедлительно посетить врача. Причиной появления данного симптома являются проблемы со здоровьем, в частности повышения давления, что опасно для здоровья мамы и малыша.
Помощь при токсикозе
Прием медикаментов при токсикозе допустим только по рекомендации врача и под его наблюдением. Самолечение крайне нежелательно.
Облегчить свое состояние женщина может при помощи трав, народных методов, употребления определенных продуктов.
Чувство тошноты могут облегчить продукты, богатые углеводами, такие как хлеб,макароны, картофель. Питаться лучше часто и понемногу, порции должны быть небольшими. Между приемами пищи нужно пить воду, а есть, не торопясь. Беременные женщины часто отмечают у себя избирательность аппетита и изменение вкусовых привычек. Новые предпочтения стоит учитывать при составлении меню наравне с полезностью пищи.
Питаться лучше часто и понемногу, порции должны быть небольшими. Между приемами пищи нужно пить воду, а есть, не торопясь. Беременные женщины часто отмечают у себя избирательность аппетита и изменение вкусовых привычек. Новые предпочтения стоит учитывать при составлении меню наравне с полезностью пищи.
Продукты, которые обычно хорошо переносятся при токсикозе во время беременности: каши, отварные овощи, нежирное мясо, кисломолочные продукты, сыр, лимон.
Завтрак в постели помогает справиться с утренней тошнотой. Вставать нужно не сразу по пробуждении, а несколько позже. Прием пищи организуйте за полчаса до подъема. Можно скушать сухие кукурузные хлопья или сухой крекер, выпить щелочную минеральную воду.
Принцип: вставать когда в желудке уже будет еда.
Для уменьшения тошноты на ранних сроках беременности можно использовать имбирь, ромашку, препараты витамина B6, пройти сеансы акупунктуры. Доказано, что немедикаментозные методы не оказывают неблагоприятного воздействия на женщину и плод.
Доказано, что немедикаментозные методы не оказывают неблагоприятного воздействия на женщину и плод.
Из имбиря можно заваривать чай или нюхать молотый имбирь при приступах тошноты. Ромашковый чай также помогает облегчить токсикоз. Пить травяные чаи можно, если нет противопоказаний и аллергических реакций.
Витамин В6 является водорастворимым витамином, он необходим для нормального течения метаболических процессов в организме человека и помогает в развитии нервной системы. Также он может облегчать тошноту при беременности. Витамин В6 присутствует во многих продуктах питания, включая рыбу, мясо, в том числе и птицы, крахмалосодержащие овощи и не цитрусовые фрукты.
Акупунктура и акупрессура у нас не слишком распространены, но в странах Азии широко используются. Вреда процедуры не принесут, если выполняются специалистами. Однако, если для женщины они являются культурно чуждыми и плохо понимаемыми, не стоит рассматривать эти варианты.
Благоприятное воздействие оказывают также регулярные пешие прогулки, желательно на природе или в парке. При ходьбе кровь насыщается кислородом, нормализуются обменные процессы организма, уменьшаются проявления токсикоза и улучшаются аппетит. Хороший эффект оказывают регулярные проветривания помещений.
При ходьбе кровь насыщается кислородом, нормализуются обменные процессы организма, уменьшаются проявления токсикоза и улучшаются аппетит. Хороший эффект оказывают регулярные проветривания помещений.
Стала ли тема токсикоза для вас более понятной?
Источник информации: Рекомендации ВОЗ по оказанию дородовой помощи как средству формирования позитивного опыта беременности.
Статья написана в рамках информационной стратегии по безопасному течению беременности и положительному опыту рождения для мамы и малыша #Я_меняюсь.
Автор Дарья Совина.
comments powered by HyperComments10 важных фактов и советов врача
Акушер-гинеколог Татьяна Румянцева (@rumyantseva_md) рассказала, какого режима питания придерживаться в первом триместре беременности, и объяснила, что делать, если токсикоз случился в конце срока.
Татьяна Румянцева
к.м.н., акушер-гинеколог в ЦНИИ Эпидемиологии
1. Определить точную причину токсикоза нельзя
Многие удивятся, но точного ответа на вопрос: почему происходит токсикоз, – у врачей и ученых нет. Есть наиболее распространенная точка зрения: токсикоз – это реакция на гормональную перестройку и повышение уровня ХГЧ (хорионического гонадотропина человека). Бывает, что тошнота и рвота вызваны другими причинами, которые не относятся к беременности. Это заболевания щитовидной железы или печени. В идеале их нужно исключить до беременности.
2. Если вы часто испытываете тошноту в обычной жизни, большая вероятность, что во время беременности у вас будет выраженный токсикоз.
Если для вас тошнота – это реакция на переутомление, излишние физические нагрузки, мигрени, определенные запахи и вкусы, контрацептивы, то велики шансы токсикоза во время беременности.
Если женщина беременна двойней, тройней, вероятность токсикоза тоже выше.
3. Токсикоз может быть и на поздних сроках беременности
Классически токсикоз начинается до 9 недели беременности и завершается к 14 неделе. У некоторых он длится дольше и очень редко может сопровождать женщину всю беременность. Тошнота на поздних сроках – это затянувшийся токсикоз или какое-то другое заболевание: язва, отравление, заболевания щитовидной железы, желчевыводящих путей.
Обращайте внимание на симптомы: если на 27 неделе у вас началась резкая тошнота и (или) лихорадка, боли в животе, голове, нарушения стула, срочно идите к врачу.
4. Токсикоз может быть при замершей беременности.
Такое состояние может сопровождать женщину до самопроизвольного прерывания беременности либо до того, как в ситуацию вмешались врачи. В этом случае токсикоз протекает плавно: ни усиливается, ни уменьшается.
Если беременность развивается нормально, токсикоз может постепенно сходить на «нет», а может «выключаться» на пару дней, и женщина резко почувствовует себя лучше.
5. Очень тяжелый токсикоз опасен главным образом для женщины
В редких случаях он действительно может быть опасен. Тяжелая степень проявления токсикоза – неукротимая рвота, когда женщина теряет до 5% от своего добеременного веса, обезвоживание, нарушение баланса основных микроэлементов. В таком состоянии практически невозможно усваивать пищу. Компенсаторные механизмы женского организма развиты так сильно, что на ребенке это не отражается. Но женщине нужно обязательно сообщить врачу. Такие ситуации требуют стационарного лечения с восполнением потерянной жидкости.
6. Сон снижает проявление токсикоза
Следите за своим образом жизни в первом триместре. Максимальное количество сна в сутки улучшит состояние. Пусть на второй план уйдут домашние дела, спите столько, сколько хочет ваш организм, а еще много гуляйте на свежем воздухе.
7. Ешьте часто и по чуть-чуть.
Многих беременных девушек тянет на соленое или сладкое. Не ограничивайте себя в первом триместре, лучше потом наладите правильную схему питания. Если плохо себя чувствуете утром, попробуйте есть что-то соленое до того, как встали с кровати. Сам факт перемещения на голодный желудок и попытка приготовить завтрак ухудшают состояние. Не бойтесь перекусывать во время первого триместра. Кому-то помогают семечки, лимон, имбирь. Пейте максимальное количество жидкости. Если воды не хочется, экспериментируйте с соками и компотами.
Если плохо себя чувствуете утром, попробуйте есть что-то соленое до того, как встали с кровати. Сам факт перемещения на голодный желудок и попытка приготовить завтрак ухудшают состояние. Не бойтесь перекусывать во время первого триместра. Кому-то помогают семечки, лимон, имбирь. Пейте максимальное количество жидкости. Если воды не хочется, экспериментируйте с соками и компотами.
8. Избегайте неприятных для вас запахов.
Туалетная вода мужа, которая вам всегда очень нравилась, во время беременности может вызывать обратный эффект. То же самое и с косметикой.
9. Предупредить классическую форму токсикоза нельзя.
Но выше я уже говорила о случаях, когда тошнота и рвота во время беременности вызваны болезнями. Вот этот момент вы можете контролировать, заранее пройдя обследование до беременности. Во время планирования беременности обсудите с врачом все волнующие вопросы, особенно если у вас есть нарушения стула, аппетита, боли в животе, потливость, раздражительность и пр.
Болезни щитовидной железы, печени, желчевыводящих путей могут усугублять течение токсикоза.
10. Иммуноцитотерапия – недоказанный метод уменьшения признаков токсикоза
Эффективность этого метода абсолютно не доказана. Он не имеет никакого отношения как к токсикозу, так и к другим состояниям, для лечения которых применяется. Иммуноцитотерапия – это иммунизация женщины лимфоцитами мужа. Каким образом его лимфоциты могут влиять на проявление токсикоза, сложно представить! В международных гайдлайнах и протоколах этого метода нет (в отличие от многочисленных обсуждений в интернете), поэтому полагаться на него не стоит: негативных последствий может быть достаточно.
Токсикоз при беременности — Статьи — Родддом г. Видное
Что такое «токсикоз»? Токсикозы беременных (в медицинской практике – ранние гестозы) – это одно из осложнений беременности, которое проявляется различными расстройствами пищеварительной системы и нарушением всех видов обмена. Часто к этому добавляется «ранний» — потому что такие проявления, доставляющие нам массу неудобств, встречаются только в первой половине беременности. Обычно дебют их приходится на 6-7 неделю беременности, когда эмбрион начинает активно вырабатывать вещества, меняющие работу всего материнского организма, и заканчиваются к 12 неделе, совпадая с завершением плацентации.
Часто к этому добавляется «ранний» — потому что такие проявления, доставляющие нам массу неудобств, встречаются только в первой половине беременности. Обычно дебют их приходится на 6-7 неделю беременности, когда эмбрион начинает активно вырабатывать вещества, меняющие работу всего материнского организма, и заканчиваются к 12 неделе, совпадая с завершением плацентации.
Причины развития токсикоза.
Психогенная – считается, что ранний токсикоз бывает у женщин, для которых беременность стала несколько неожиданной новостью. Приятной или не очень – главное неожиданной. Может быть, вы рады, что скоро на свет появится ваш малыш, но планировала сделать это несколько позже. Постоянно разрывающие вас сомнения и волнения приводят к возбуждению определенных участков головного мозга, по соседству с которыми расположены рвотный центр, сосудистый и дыхательный. Ну, а к чему ведет такая постоянная их активация – объяснять не нужно.
Иммунологическая – сторонники этой теории объясняют проявления токсикоза реакцией сопротивления материнского организма на чужеродные папины частички. Ведь наш малыш, безусловно, родной, но на половину (конечно, папину половину) генетически чужеродный.
Ведь наш малыш, безусловно, родной, но на половину (конечно, папину половину) генетически чужеродный.
Гормональная – в начале беременности значительно возрастает уровень хорионического гонадотропина (ХГЧ) – это один из главных гормонов беременности. С его действием и можно связать основные проявления токсикоза. В доказательство этого можно сказать, что при многоплодной беременности, когда выделяется значительно большее количество ХГЧ, рвота беременных возникает особенно часто. Также ответственным за возникновение токсикоза называют плацентарный лактоген (он вырабатывается в тканях предшественника плаценты – хорионе, а затем в самой плаценте). Этот гормон контролирует синтез белков, которые идут на формирование и рост малыша. При этом у мамы этот же процесс затормаживается, приводя к накоплению используемых аминокислот. Их избыток и может служить причиной слабости, тошноты, рвоты, головных болей.
Предрасполагают к токсикозу различные воспалительные заболевания половых органов и хронические интоксикации. А если до наступления беременности у вас были заболевания желудочно-кишечного тракта, печени – то шанс испытать на себе все «радости» токсикоза у вас очень велик.
А если до наступления беременности у вас были заболевания желудочно-кишечного тракта, печени – то шанс испытать на себе все «радости» токсикоза у вас очень велик.
Совершенно объективен тот факт, что такими не лучшими воспоминаниями о своей беременности мы обязаны бешеному ритму современной жизни с хроническим стрессом, неправильному питанию и нездоровому образу жизни. А значит — изменив образ жизни, нормализовав работу пищеварительной системы, избавившись от вредных привычек при планировании беременности, мы можем предотвратить или значительно уменьшить проявления токсикоза первой половины беременности.
Как может проявляться токсикоз.
Существует несколько вариантов течения токсикозов беременных. Чаще всего под токсикозом подразумевается только рвота беременных. Безусловно, на ее долю приходится более 90%, но иногда реакция организма мамы на беременность приобретает и другие редкие формы. К ним относятся: тетания беременных (проявляется судорогами), дерматозы (различные поражения кожи), остеомаляция (размягчение костей), бронхиальная астма беременных, гепатоз (поражение печени с желтухой). Часто токсикоз проявляется слюнотечением – отдельно или вместе с рвотой.
Часто токсикоз проявляется слюнотечением – отдельно или вместе с рвотой.
Рвота беременных.
С наступлением беременности ваш организм начинает приспосабливаться к новым условиям совместного существования с малышом. Достаточно часто этот «кризис перемен» сопровождается тошнотой, рвотой, слабостью. Многие женщины отмечают изменения настроения, плаксивость или повышенную раздражительность. Начинают раздражать некогда любимые вещи, продукты, запахи. А может наоборот вдруг захотеться чего-то для себя необычного.
Причем до 60% случаев рвота беременной расценивается как физиологический признак беременности. И только чуть больше 10% беременных с токсикозом нуждаются в специальном лечении. Важно понимать, что при физиологической беременности рвота может быть не более 2 3 раз в день, чаще по утрам, натощак. Уменьшить проявления таких «неприятностей» беременности помогает соблюдение определенных правил поведения и питания, о которых речь пойдет ниже. Это, однако, не нарушает общего состояния женщины. В противном случае – можно говорить о развитии раннего токсикоза. Это уже требует врачебного вмешательства, а в ряде случаев и госпитализации в стационар для проведения дезинтоксикационной терапии.
Это, однако, не нарушает общего состояния женщины. В противном случае – можно говорить о развитии раннего токсикоза. Это уже требует врачебного вмешательства, а в ряде случаев и госпитализации в стационар для проведения дезинтоксикационной терапии.
Основные средства борьбы с токсикозом.
Конечно, ваше представление о долгожданной беременности было более радужным. А тут откуда-то навалилась слабость, усталость, раздражительность, а от постоянной тошноты и рвоты нет никакой жизни. Главное – не отчаиваться, расслабиться и выполнять все рекомендации врача. Какими бы очевидными они вам не покажутся – при токсикозах беременных это «действительно работает».
И, прежде всего, начнем с устранения психологического аспекта. Позвольте себе быть беременной, со всеми своими слабостями. Не бойтесь перемен, происходящих в своем теле и внутреннем мире. Для борьбы с токсикозом не нужно прикладывать все усилия — с ним нужно просто научиться жить – ведь в большинстве случаев это совершенно естественное явление в начале беременности.
Дальше нормализуем режим дня и питание. Беременной женщине обязательно необходимо гулять на свежем воздухе не менее 1-2 часов в день – кислород усиливает обменные процессы, препятствуя накоплению токсинов. Как «свежий воздух» вам сейчас необходим полноценный сон, желательно, чтобы и днем была возможность отдохнуть – это важно для нормализации работы центральной нервной системы.
Избегайте всех раздражающих и неприятных моментов, у каждой беременной они свои. Тошнит от запахов – на вооружение придет надушенный любимыми сейчас духами платочек – ваш «карманный» спутник. Если от одного вида зубной щетки по утрам начинается рвота – отложите эту гигиеническую процедуру до обеда – большого вреда за столь короткий срок вы своим зубам не принесете.
Сейчас старайтесь есть все, что захочется – главное, чтобы еда была легкоусвояемая с большим количеством витаминов. Конечно, хорошо если это будут продукты, богатые белком (рыба, мясо, молочные продукты, зерновые). Но если даже мысль о мясе сейчас для вас неприятна — не нужно есть через силу, скорее всего, исход такой трапезы будет один. Ваш малыш еще так мал, что не нуждается в большом резерве строительных белков – так что соблюдение полноценной по питательному и количественному составу диеты можно отложить на более позднее время. Это же правило распространяется и на трудно проглатываемые таблетки поливитаминов.
Но если даже мысль о мясе сейчас для вас неприятна — не нужно есть через силу, скорее всего, исход такой трапезы будет один. Ваш малыш еще так мал, что не нуждается в большом резерве строительных белков – так что соблюдение полноценной по питательному и количественному составу диеты можно отложить на более позднее время. Это же правило распространяется и на трудно проглатываемые таблетки поливитаминов.
Проснувшись утром, позвольте себе какое-то время понежиться в постели – вам сейчас это можно, а на прикроватную тумбочку с вечера можно положить орехи или печенье. Кому-то в борьбе с утренней рвотой помогает съесть, не вставая с кровати, ложку нежирного творога или половинку вареного яйца, после чего, конечно, нужно полежать.
Пища должна быть жидкой или полужидкой, но обязательно не горячей. Есть нужно часто до 6-8 раз в день маленькими порциями, а после приема пищи нужно полежать – так она лучше усвоиться. Поздний ужин, например, стакан кефира, тоже лишним не будет – он препятствует накоплению большого количества желудочного сока к моменту пробуждения.
Пить нужно много, но желательно между приемами пищи, чтобы не перегружать желудок. Для этой цели как нельзя лучше подойдет щелочная минеральная вода, соки, растительные чаи — их можно заваривать на водяной бане или купить готовые фильтр-пакетики с мятой, мелиссой, валерианой, чабрецом.
В течение дня облегчить тошноту можно с помощью мятных леденцов или жевательной резинки, а также полосканием рта лимонной водой, отваром мяты, шалфея, ромашки.
Для нормализации работы пищеварительной системы можно использовать такой сбор: 8 частей полыни обыкновенной, 2 части травы зверобоя, 2 части тысячелистника. Одну столовую ложку смеси заливаем стаканом кипятка, настаиваем на водяной бане 15 минут и принимаем по 1/3 стакана 3 раза в день до еды.
Хорошо для борьбы с токсикозом зарекомендовала себя аромотерапия – успокаивают тошноту эфирные масла жасмина, розы, аниса, лимона.
Отлично расслабляют массаж головы и воротниковой области. А если привлечь к этому мужа – лучшего способа выражения солидарности в этот «кризисный момент» беременности и быть не может.
А если привлечь к этому мужа – лучшего способа выражения солидарности в этот «кризисный момент» беременности и быть не может.
Эффективным во время токсикоза является воздействие на специальные противорвотные и метаболические точки путем иглоукалывания или точечного массажа. Иглоукалывание, конечно, должен проводить только специалист, а вот приемам точечного массажа можно обучиться самой под руководством врача.
В любом случае – токсикоз – это только небольшой временной кусочек вашей беременности, который скоро обязательно закончится. И чем спокойнее, оптимистичнее, может быть в какой-то степени даже с юмором, вы отнесетесь к нему, тем легче будет пережить этот «кризис» ваших отношений с беременностью. Ведь главное – это новая, зарождающаяся внутри вас, жизнь!
Токсикоз при беременности — причины, риски, решение проблемы
Многие беременные воспринимают утреннюю тошноту как неизбежный факт: это реакция организма на серьезные процессы, происходящие в нем в первые недели и месяцы беременности. Единственное, что они могут сделать в такой ситуации, это терпеливо ждать, пока она закончится. Что ж, это распространенное мнение не совсем верно, так как токсикоз требует существенного внимания врача.
Единственное, что они могут сделать в такой ситуации, это терпеливо ждать, пока она закончится. Что ж, это распространенное мнение не совсем верно, так как токсикоз требует существенного внимания врача.
Первый триместр беременности – самый важный; в этот период у малыша начинают свое формирование все внутренние системы и органы. Поэтому, если у Матери ребенка возникнут какие-либо проблемы со здоровьем, это может негативно сказаться на столь важном «сроке становления». Кроме того, за токсикозом, тошнотой и рвотой могут скрываться более серьезные проблемы – одни явные, а другие скрытые, выявляемые только с помощью лабораторных исследований. Это могут быть, например, различные поражения кожи, судороги и в наиболее тяжелых случаях — желтуха беременных, бронхиальная астма, нарушения водно-солевого баланса, обмена веществ и др.
Поэтому обязательна тщательная медицинская оценка состояния здоровья женщины, страдающей токсикозом в I триместре беременности. Это самое главное правило, которым ни в коем случае нельзя пренебрегать.
Каковы причины токсикоза в первом триместре?
Единой научно доказанной гипотезы о причинах токсикоза не существует. Некоторые люди считают, что ранний токсикоз – это реакция иммунной системы. Некоторые люди считают, что это состояние может быть вызвано гормонами, а именно – высокой концентрацией гормона ХГЧ в крови.В то же время все причины токсикоза на ранних сроках беременности обусловлены закономерно обусловленными причинами. Почему же тогда у одних женщин бывает токсикоз, а у других нет? Это можно объяснить общим состоянием здоровья: при наличии вредных привычек, хронических заболеваний желудочно-кишечного тракта, печени, щитовидной железы и после искусственных абортов более вероятно возникновение токсикоза.
Как бороться с токсикозом?
При токсикозе врач, наблюдающий Вашу беременность, даст направление на анализ мочи, по результату которого определят степень выраженности токсикоза и обезвоживания, биохимическое и общее исследования крови.В зависимости от результатов анализов и степени токсичности (легкая — рвота не более 5 раз в сутки, тяжелая — 10-20 раз в сутки) врач порекомендует стационарное лечение или соблюдение особых правил в домашних условиях.
Чем может помочь стационарное лечение?
Может потребоваться госпитализация, так как частая рвота может вызвать обезвоживание, нарушение обмена веществ, снижение артериального давления и диуреза, учащение пульса и запор. Без своевременного лечения могут развиться серьезные нарушения водно-солевого, белкового, углеводного и жирового обмена, кислотно-щелочного и витаминного баланса, функции желез внутренней секреции.Все эти условия могут негативно сказаться на развитии малыша.
Какое лечение рекомендуется при легком токсикозе
Легкую форму токсикоза (рвота не более 5 раз в сутки) можно взять под контроль по простой инструкции:
1. Диета – очень важный фактор. Избегайте слишком горячей или слишком холодной пищи – это провоцирует приступ рвоты. Кушайте часто – не менее 5-6 раз в день, но небольшими порциями. Доверьтесь своей интуиции – если вы чувствуете, что соленья или экзотические фрукты – это то, что вам нужно, позвольте себе это.Однако помните, что ваш план питания в этот период должен быть хорошо сбалансирован и содержать достаточное количество белков, жиров и углеводов.
2. Соблюдать питьевой режим. Многие женщины, страдающие от токсикоза, с удовольствием пьют в этот период чай с мятой – он не только утоляет жажду, но и успокаивает.
3. Завтрак — в постель. Если рвота обычно возникает утром, позавтракайте в постели, не вставая. Чай с лимоном и несколько крекеров могут помочь избежать тошноты.
4. Избегать переутомления – как физического, так и нервного. Иногда усталость может спровоцировать тошноту – чаще это бывает во второй половине дня. Успокаивающий чай поможет снять нервное напряжение. По согласованию с врачом можно также использовать пустырник или валериану.
Ранний токсикоз обычно полностью исчезает после 12-й недели беременности, реже может продолжаться до 16-й недели. Наберитесь терпения и будьте предельно внимательны к нюансам своего самочувствия – это очень важно не только для вашего здоровья, но и для здоровья вашего малыша.
Утренняя тошнота: механизм защиты матери и эмбриона
Примерно две трети женщин испытывают тошноту или рвоту в течение первого триместра беременности. Эти симптомы широко известны как утренняя тошнота. Hook (1976) и Profet (1988) предположили, что утренняя тошнота защищает эмбрион, заставляя беременных женщин физически извергать и впоследствии избегать продуктов, содержащих тератогенные и абортивные химические вещества, особенно токсичные химические вещества в овощах с сильным вкусом, напитках с кофеином и алкоголе.Мы проверили эту гипотезу, всесторонне изучив соответствующую медицинскую, психологическую и антропологическую литературу. В подтверждение этому: (i) симптомы достигают пика, когда эмбриональный органогенез наиболее восприимчив к химическому нарушению (6-18 недели), (ii) у женщин, которые испытывают утреннее недомогание, вероятность выкидыша значительно ниже, чем у женщин, которые этого не делают (9 из 9 исследований). , (iii) у женщин, страдающих рвотой, меньше случаев выкидыша, чем у тех, кто испытывает только тошноту, и (iv) многие беременные женщины испытывают отвращение к алкогольным и безалкогольным (в основном кофеиновым) напиткам и овощам с сильным вкусом, особенно в первом триместре.
Эти симптомы широко известны как утренняя тошнота. Hook (1976) и Profet (1988) предположили, что утренняя тошнота защищает эмбрион, заставляя беременных женщин физически извергать и впоследствии избегать продуктов, содержащих тератогенные и абортивные химические вещества, особенно токсичные химические вещества в овощах с сильным вкусом, напитках с кофеином и алкоголе.Мы проверили эту гипотезу, всесторонне изучив соответствующую медицинскую, психологическую и антропологическую литературу. В подтверждение этому: (i) симптомы достигают пика, когда эмбриональный органогенез наиболее восприимчив к химическому нарушению (6-18 недели), (ii) у женщин, которые испытывают утреннее недомогание, вероятность выкидыша значительно ниже, чем у женщин, которые этого не делают (9 из 9 исследований). , (iii) у женщин, страдающих рвотой, меньше случаев выкидыша, чем у тех, кто испытывает только тошноту, и (iv) многие беременные женщины испытывают отвращение к алкогольным и безалкогольным (в основном кофеиновым) напиткам и овощам с сильным вкусом, особенно в первом триместре. Удивительно, однако, что наибольшее отвращение испытывают к мясу, рыбе, птице и яйцам. Кросс-культурный анализ с использованием файлов области человеческих отношений выявил 20 традиционных обществ, в которых наблюдалась утренняя тошнота, и семь, в которых она никогда не наблюдалась. Последние значительно реже использовали продукты животного происхождения в качестве основных продуктов питания и значительно чаще использовали в качестве основных продуктов только растения (в первую очередь кукурузу), чем 20 обществ, в которых наблюдалось утреннее недомогание. Продукты животного происхождения могут быть опасны для беременных женщин и их эмбрионов, поскольку они часто содержат паразитов и болезнетворные микроорганизмы, особенно при хранении при комнатной температуре в теплом климате.Избегание микроорганизмов пищевого происхождения особенно важно для беременных женщин, поскольку у них подавлен иммунитет, предположительно для снижения вероятности отторжения тканей их собственного потомства (Haig, 1993).
Удивительно, однако, что наибольшее отвращение испытывают к мясу, рыбе, птице и яйцам. Кросс-культурный анализ с использованием файлов области человеческих отношений выявил 20 традиционных обществ, в которых наблюдалась утренняя тошнота, и семь, в которых она никогда не наблюдалась. Последние значительно реже использовали продукты животного происхождения в качестве основных продуктов питания и значительно чаще использовали в качестве основных продуктов только растения (в первую очередь кукурузу), чем 20 обществ, в которых наблюдалось утреннее недомогание. Продукты животного происхождения могут быть опасны для беременных женщин и их эмбрионов, поскольку они часто содержат паразитов и болезнетворные микроорганизмы, особенно при хранении при комнатной температуре в теплом климате.Избегание микроорганизмов пищевого происхождения особенно важно для беременных женщин, поскольку у них подавлен иммунитет, предположительно для снижения вероятности отторжения тканей их собственного потомства (Haig, 1993). В результате беременные женщины более уязвимы к серьезным, часто смертельным инфекциям. Мы предполагаем, что утренняя тошнота заставляет женщин избегать продуктов, которые могут быть опасны для них самих или их эмбрионов, особенно продуктов, которые до широко распространенного охлаждения, вероятно, были сильно загружены микроорганизмами и их токсинами.Альтернативные гипотезы о том, что утренняя тошнота является (i) эпифеноменом генетического конфликта между матерью и потомством или гормонами, связанными с жизнеспособной беременностью, или (ii) индикатором для потенциальных сексуальных партнеров и родственников того, что женщина беременна, что приводит к снижению сексуального поведения и увеличению кумовской помощи, не получили должной поддержки. Имеющиеся данные наиболее согласуются с гипотезой о том, что утренняя тошнота выполняет адаптивную профилактическую функцию.
В результате беременные женщины более уязвимы к серьезным, часто смертельным инфекциям. Мы предполагаем, что утренняя тошнота заставляет женщин избегать продуктов, которые могут быть опасны для них самих или их эмбрионов, особенно продуктов, которые до широко распространенного охлаждения, вероятно, были сильно загружены микроорганизмами и их токсинами.Альтернативные гипотезы о том, что утренняя тошнота является (i) эпифеноменом генетического конфликта между матерью и потомством или гормонами, связанными с жизнеспособной беременностью, или (ii) индикатором для потенциальных сексуальных партнеров и родственников того, что женщина беременна, что приводит к снижению сексуального поведения и увеличению кумовской помощи, не получили должной поддержки. Имеющиеся данные наиболее согласуются с гипотезой о том, что утренняя тошнота выполняет адаптивную профилактическую функцию.
Тошнота и рвота во время беременности
Введение
Тошнота и рвота являются обычным явлением во время беременности, которым страдают 70–80% всех беременных женщин. Хотя у большинства женщин тошнота и рвота при беременности (НВП) имеют симптомы, ограниченные первым триместром, у небольшого процента женщин наблюдается длительное течение с симптомами, продолжающимися до родов. У женщин с тяжелой тошнотой и рвотой во время беременности может быть гиперемезис беременных (HG), состояние, отличное от NVP, которое, если его не лечить, может привести к значительной заболеваемости матери и плода.
Хотя у большинства женщин тошнота и рвота при беременности (НВП) имеют симптомы, ограниченные первым триместром, у небольшого процента женщин наблюдается длительное течение с симптомами, продолжающимися до родов. У женщин с тяжелой тошнотой и рвотой во время беременности может быть гиперемезис беременных (HG), состояние, отличное от NVP, которое, если его не лечить, может привести к значительной заболеваемости матери и плода.
Различные метаболические и нервно-мышечные факторы вовлечены в патогенез невирапина и HG; однако их точная причина неизвестна.Следовательно, лечение NVP и HG может быть затруднено, поскольку не известны ни оптимальные цели лечения, ни полные эффекты потенциальных методов лечения на развивающийся плод. В этой статье рассматриваются эпидемиология, патология, диагностика, исходы и лечение невирапина и HG.
Эпидемиология
По оценкам, 70–80% беременных женщин получают невирапин [1]. В Соединенных Штатах и Канаде это означает примерно 4 000 000 и 350 000 женщин, которые страдают каждый год соответственно [2].
НВП чаще встречается в западных странах и у городского населения и редко встречается у африканцев, коренных американцев, эскимосов и большинства азиатских популяций [3]. Лишь в нескольких исследованиях изучалось расовое распределение невирапина в данной популяции. Одно такое исследование, проведенное в Канаде с участием 367 женщин, показало, что азиаты и чернокожие реже сообщали о симптомах невирапина, чем представители европеоидной расы. Социально-демографические факторы не учитывали расовые/этнические различия в распространенности заболевания, что позволяет предположить, что могут играть роль генетические и/или культурные факторы [4].
HG встречается редко по сравнению с NVP и встречается в 0,3–2% всех беременностей [5]. Заболеваемость зависит от этнической принадлежности [6] и колеблется от 3 до 20 на 1000 беременностей [7]. Он чаще диагностируется у женщин в Индии, Пакистане, Азии, Новой Зеландии по сравнению с европейцами, американскими индейцами и эскимосами [8].
Факторы риска
Данные Совместного перинатального проекта, одного из крупнейших на сегодняшний день исследований беременных женщин, показали, что невирапин чаще встречается у молодых женщин, первобеременных, женщин с образованием менее 12 лет, некурящих и женщины с ожирением [9]. О повышенном риске невирапина в первом триместре также сообщалось у женщин с многоплодной беременностью по сравнению с женщинами с одноплодной беременностью (87% против 73%, p<0,01) [10].
О повышенном риске невирапина в первом триместре также сообщалось у женщин с многоплодной беременностью по сравнению с женщинами с одноплодной беременностью (87% против 73%, p<0,01) [10].
НВП был связан с низким уровнем дохода и статусом занятости неполный рабочий день [11]). Было обнаружено, что домохозяйки также подвергаются повышенному риску, в то время как женщины, работающие в качестве белых воротничков, по-видимому, защищены [12]. Однако остается неясным, является ли статус занятости истинным фактором риска для невирапина или искажающим фактором, поскольку затронутые женщины могут прекратить работу из-за своих симптомов.Точно так же их решение не работать вне дома может быть связано с многодетностью и необходимостью заботиться о других детях [13].
Материнская генетика также может служить фактором риска для невирапина. Данные большой популяции норвежских близнецов показывают более широкое использование лекарств от тошноты во время беременности среди монозиготных близнецов женского пола по сравнению с дизиготными близнецами женского пола [14]. Кроме того, более высокие уровни тошноты были обнаружены у женщин, матери которых испытывали тошноту во время беременности [15].Также было показано, что личный анамнез NVP является фактором риска для NVP при последующих беременностях [15]; однако этот вывод не был последовательным в разных исследованиях [16]
Кроме того, более высокие уровни тошноты были обнаружены у женщин, матери которых испытывали тошноту во время беременности [15].Также было показано, что личный анамнез NVP является фактором риска для NVP при последующих беременностях [15]; однако этот вывод не был последовательным в разных исследованиях [16]
Другие факторы риска для невирапина включают личную историю укачивания, возможно, из-за общего вестибулярного механизма [17] и мигреней в анамнезе [18]. Женщины, у которых в анамнезе была тошнота при приеме эстрогенсодержащих пероральных контрацептивов, также подвержены повышенному риску невирапина [19].
Расположение желтого тела также может служить фактором риска невирапина.Ультразвуковые исследования показали, что беременные чаще испытывают тошноту и рвоту при наличии желтого тела в правом яичнике [20]. Это может быть связано с различиями в венозном оттоке между левым и правым яичником и более высокой концентрацией половых стероидов, когда желтое тело находится на правой стороне [21].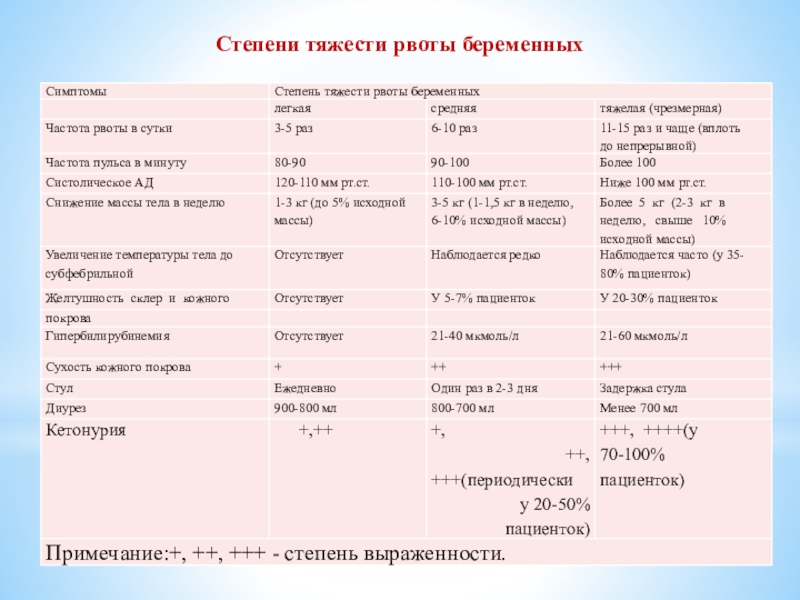
Более высокое суточное потребление общего жира, особенно насыщенных жиров, до беременности увеличивает риск госпитализации по поводу невирапина [22]. Курение до беременности и прием витаминов до и/или на ранних сроках беременности связаны со снижением риска невирапина [23].Также было обнаружено, что употребление алкоголя матерью до зачатия защищает от NVP [24].
Факторы риска HG аналогичны факторам риска NVP. К ним относятся многоплодная беременность, трофобластическая болезнь, HG в предшествующей беременности, аномалии плода, такие как триплоидия, трисомия 21 и водянка плода, а также нерождение плода [25]. Семейный анамнез HG также является фактором риска: примерно 28% женщин сообщают о HG в анамнезе у своих матерей и 19% сообщают, что их сестры имели аналогичные симптомы [26].Дополнительные факторы риска включают семейный или партнерский статус и возраст старше 30 лет. Курение сигарет может быть защитным [27].
Индекс массы тела матери оценивался как фактор риска ГГ с неоднозначными результатами. В исследовании Depue et al ожирение увеличивало риск ГГ на 50% [28]. Работа Cedergren et al. однако обнаружили, что низкий индекс массы тела (<20 кг/м2) был связан с 40% более высоким риском ХГ, а ожирение снижало риск госпитализации по поводу ХГ [29].Более недавнее исследование 33 647 женщин в Норвегии показало, что недостаточный или избыточный вес увеличивает риск ГГ, но только у некурящих [30]. Постулируется, что женщины с недостаточным весом и низкими индексами массы тела имеют низкий уровень эстрогена до беременности и, таким образом, могут иметь преувеличенный ответ в течение первого триместра, когда уровень эстрогена резко возрастает [31]. Напротив, у женщин с ожирением жировые отложения могут нейтрализовать плацентарные факторы, которые, как считается, способствуют патогенезу [29].
В исследовании Depue et al ожирение увеличивало риск ГГ на 50% [28]. Работа Cedergren et al. однако обнаружили, что низкий индекс массы тела (<20 кг/м2) был связан с 40% более высоким риском ХГ, а ожирение снижало риск госпитализации по поводу ХГ [29].Более недавнее исследование 33 647 женщин в Норвегии показало, что недостаточный или избыточный вес увеличивает риск ГГ, но только у некурящих [30]. Постулируется, что женщины с недостаточным весом и низкими индексами массы тела имеют низкий уровень эстрогена до беременности и, таким образом, могут иметь преувеличенный ответ в течение первого триместра, когда уровень эстрогена резко возрастает [31]. Напротив, у женщин с ожирением жировые отложения могут нейтрализовать плацентарные факторы, которые, как считается, способствуют патогенезу [29].
Что касается пола плода, то в нескольких исследованиях была обнаружена связь между ГГ и женским полом плода.Используя данные Шведского медицинского реестра рождений, Kallen et al. обнаружили, что HG был чрезмерно представлен в 3068 беременностях, когда ребенок был девочкой [32]. Точно так же в исследовании беременных женщин, госпитализированных с HG в первом триместре, вероятность рождения девочки была на 50% выше в случаях по сравнению со здоровыми беременными в контрольной группе (ОШ 1,5, 95% ДИ 1,4, 1,7) [33].
Точно так же в исследовании беременных женщин, госпитализированных с HG в первом триместре, вероятность рождения девочки была на 50% выше в случаях по сравнению со здоровыми беременными в контрольной группе (ОШ 1,5, 95% ДИ 1,4, 1,7) [33].
Патогенез
Метаболические и гормональные факторы
Хотя точный патогенез НВП и ГГ неизвестен, общепризнано, что рвота во время беременности является результатом различных метаболических и эндокринных факторов, многие из которых имеют плацентарное происхождение.Наиболее значимым фактором является хорионический гонадотропин человека (ХГЧ). Эта связь между ХГЧ и невирапином в значительной степени основана на временном соотношении между пиком невирапина и пиком продукции ХГЧ, которые происходят между 12 и 14 неделями беременности. Кроме того, тошнота и рвота часто усиливаются у беременных с состояниями, связанными с повышенным уровнем ХГЧ, такими как молярная беременность, многоплодная беременность и синдром Дауна [13]. Более высокие уровни ХГЧ в моче [34] и в сыворотке также были обнаружены у женщин с невирапином по сравнению с бессимптомными [35]. Кроме того, исследование Goodwin et al. обнаружили, что концентрации ХГЧ положительно коррелируют с выраженностью тошноты и рвоты у женщин с ХГ [36].
Кроме того, исследование Goodwin et al. обнаружили, что концентрации ХГЧ положительно коррелируют с выраженностью тошноты и рвоты у женщин с ХГ [36].
Несмотря на множество исследований, связывающих уровень ХГЧ с невирапином и гормоном роста, другие не обнаружили связи между уровнем ХГЧ в сыворотке беременных женщин в течение первого триместра и частотой или интенсивностью тошноты и рвоты. В исследовании Soules et al. даже в подгруппе женщин с пузырным заносом, у которых уровни ХГЧ у женщин были в 5-10 раз выше, чем в контроле, корреляции обнаружено не было [37].Кроме того, исследования показали, что высокие уровни ХГЧ связаны с задержкой роста плода и преждевременными родами [38], в то время как невирапин, по-видимому, защищает от преждевременных родов, что делает маловероятным то, что ХГЧ является единственным фактором патогенеза невирапина.
Предполагается, что различные биологические формы (то есть изоформы) ХГЧ могут объяснить вариабельность между уровнями ХГЧ и тошнотой и рвотой у здоровых и больных людей [39]. Каждая изоформа ХГЧ имеет уникальный период полувыведения и активность в отношении рецепторов лютеинизирующего гормона и тиреотропного гормона (ТТГ).Изоформы без карбоксиконцевой части имеют более короткий период полувыведения, но являются более сильными стимуляторами рецепторов лютеинизирующего гормона и ТТГ. Напротив, гипергликозилированный ХГЧ имеет более длительный период полувыведения и большую продолжительность действия [40]. Эти различные изоформы ХГЧ, вероятно, являются результатом генетических факторов или долгосрочных изменений окружающей среды, которые, таким образом, могут объяснить различия в заболеваемости ХГ, обнаруженные в разных популяциях. Помимо изменчивости изоформ, мутации рецептора ХГЧ также могут объяснить некоторую вариабельность взаимоотношений между невирапином и ХГЧ [39].
Каждая изоформа ХГЧ имеет уникальный период полувыведения и активность в отношении рецепторов лютеинизирующего гормона и тиреотропного гормона (ТТГ).Изоформы без карбоксиконцевой части имеют более короткий период полувыведения, но являются более сильными стимуляторами рецепторов лютеинизирующего гормона и ТТГ. Напротив, гипергликозилированный ХГЧ имеет более длительный период полувыведения и большую продолжительность действия [40]. Эти различные изоформы ХГЧ, вероятно, являются результатом генетических факторов или долгосрочных изменений окружающей среды, которые, таким образом, могут объяснить различия в заболеваемости ХГ, обнаруженные в разных популяциях. Помимо изменчивости изоформ, мутации рецептора ХГЧ также могут объяснить некоторую вариабельность взаимоотношений между невирапином и ХГЧ [39].
Гормоны яичников, эстроген и прогестерон, также участвуют в патогенезе невирапина и гипергидроза. Известно, что некоторые женщины испытывают тошноту при приеме оральных контрацептивов. Кроме того, состояния с высокой концентрацией эстрогена, такие как низкий паритет и высокий индекс массы тела матери, были связаны с более высокой частотой ГГ [28]. Считается, что эстроген вносит свой вклад в HG, стимулируя выработку оксида азота с помощью синтетазы азотоксидазы, которая, в свою очередь, расслабляет гладкие мышцы, замедляя время желудочно-кишечного транзита и опорожнение желудка.
Кроме того, состояния с высокой концентрацией эстрогена, такие как низкий паритет и высокий индекс массы тела матери, были связаны с более высокой частотой ГГ [28]. Считается, что эстроген вносит свой вклад в HG, стимулируя выработку оксида азота с помощью синтетазы азотоксидазы, которая, в свою очередь, расслабляет гладкие мышцы, замедляя время желудочно-кишечного транзита и опорожнение желудка.
Ярнфельт и др. сообщили о значительной связи между рвотой беременных и непереносимостью пероральных контрацептивов в анамнезе [40]. Используя более количественный подход, Depue et al. обнаружили, что средние уровни общего эстрадиола на 26% выше, а средние уровни способности связывания половых гормонов и глобулинов на 37% выше у пациентов с HG, чем в контрольной группе после поправки на гестационный возраст. 28]. Однако важно отметить, что, как и взаимосвязь между ХГЧ и невирапином, взаимосвязь между уровнями эстрогена и невирапином была противоречивой в разных исследованиях [35].Обзор 17 исследований показал положительную связь между невирапином и эстрогеном только в 5 исследованиях [41]. Кроме того, пик уровня эстрогена приходится на третий триместр беременности, в то время как ГГ имеет тенденцию к улучшению на поздних сроках беременности [8].
Кроме того, пик уровня эстрогена приходится на третий триместр беременности, в то время как ГГ имеет тенденцию к улучшению на поздних сроках беременности [8].
Прогестерон в сочетании с эстрогеном также может играть роль в NVP. Прогестерон снижает сократимость гладкой мускулатуры и может изменить опорожнение желудка и привести к усилению тошноты и рвоты. Используя эластогастографию после стандартного приема пищи, Walsh et al. показали, что такое же медленноволновое нарушение желудочного ритма, обнаруженное у женщин с невирапином, может быть вызвано у небеременных женщин монотерапией прогестероном или в комбинации с эстрадиолом в дозах, которые воспроизводят уровни при беременности [42].Другие исследования, однако, не обнаружили существенной разницы между уровнями прогестерона у женщин с невирапином или без него [28].
Роль плацентарного простагландина E2 (PGE2) также оценивалась в патогенезе NVP из-за его влияния на гладкую мускулатуру желудка [43]. ХГЧ стимулирует плацентарный PGE2 и, как и ХГЧ, достигает пика между 9 и 12 неделями беременности. Норт и др. определили количество PGE2 в материнской сыворотке и обнаружили, что уровни были выше во время периодов тошноты и рвоты у 18 женщин на ранних сроках беременности по сравнению с бессимптомными периодами.Они также оценили уровни интерлейкина-1 бета и фактора некроза опухоли альфа у матери и обнаружили, что они были одинаковыми в течение симптоматического и бессимптомного периодов [44].
Норт и др. определили количество PGE2 в материнской сыворотке и обнаружили, что уровни были выше во время периодов тошноты и рвоты у 18 женщин на ранних сроках беременности по сравнению с бессимптомными периодами.Они также оценили уровни интерлейкина-1 бета и фактора некроза опухоли альфа у матери и обнаружили, что они были одинаковыми в течение симптоматического и бессимптомного периодов [44].
В связи с его ролью в вызванных химиотерапией тошноте и рвоте, серотонин также предположительно способствует развитию невирапина. Исследование Borgeat et al. однако не выявили различий в уровне серотонина среди беременных женщин с ХГ, бессимптомных беременных женщин и небеременных женщин [45]. Кроме того, рандомизированное контролируемое исследование, сравнивающее антагонист серотониновых 5-HT3-рецепторов, онданстерон, с прометазином, не выявило существенной разницы в контроле симптомов [46].
Из-за перекрестной реактивности между ХГЧ и рецептором тиреостимулирующего гормона (ТТГ) дисфункция щитовидной железы также изучалась как возможный механизм развития невирапина и ГГ. На самом деле, аномальные результаты функции щитовидной железы обнаруживаются у двух третей женщин с ГГ [36]. Этот «биохимический тиреотоксикоз» характеризуется подавлением ТТГ и слегка повышенным уровнем FT4. Несмотря на эти лабораторные отклонения, женщины с HG, как правило, находятся в эутиреоидном состоянии без предшествующих заболеваний щитовидной железы, отсутствия зоба и отрицательных антитиреоидных антител [47].Кроме того, исследования не выявили взаимосвязи между дисфункцией щитовидной железы и тяжестью симптомов [48], и почти у всех женщин с ХГ уровень ТТГ в норме к 20 нед беременности без какого-либо вмешательства [49].
На самом деле, аномальные результаты функции щитовидной железы обнаруживаются у двух третей женщин с ГГ [36]. Этот «биохимический тиреотоксикоз» характеризуется подавлением ТТГ и слегка повышенным уровнем FT4. Несмотря на эти лабораторные отклонения, женщины с HG, как правило, находятся в эутиреоидном состоянии без предшествующих заболеваний щитовидной железы, отсутствия зоба и отрицательных антитиреоидных антител [47].Кроме того, исследования не выявили взаимосвязи между дисфункцией щитовидной железы и тяжестью симптомов [48], и почти у всех женщин с ХГ уровень ТТГ в норме к 20 нед беременности без какого-либо вмешательства [49].
Недавно была предложена связь между гормоном лептином и HG. Было обнаружено, что повышенный уровень лептина в сыворотке во время беременности, возможно, в результате увеличения общей жировой массы и продукции плаценты, значительно выше у пациенток с HG по сравнению со здоровыми беременными контрольной группой [50, 51].Лептин может способствовать ГГ за счет увеличения секреции ХГЧ за счет паракринного действия плаценты или за счет снижения аппетита и усиления тошноты и рвоты. Примечательно, однако, что другие проспективные когортные исследования не обнаружили аналогичной статистически значимой разницы в уровнях лептина в сыворотке при HG между пациентами и контрольной группой [52, 53].
Примечательно, однако, что другие проспективные когортные исследования не обнаружили аналогичной статистически значимой разницы в уровнях лептина в сыворотке при HG между пациентами и контрольной группой [52, 53].
Также было высказано предположение, что у женщин с HG возникает нарушение регуляции иммунной системы. В сыворотке крови матери были обнаружены повышенные концентрации свободной ДНК клеток плода [54], вызывающие гиперактивный материнский иммунный ответ и повреждение трофобласта.Кроме того, нормальный сдвиг во время беременности, при котором типы Т-хелперов переходят в Т-хелперы типа 1, более преувеличен у женщин с ХГ [55]. Это, в свою очередь, приводит к повышенному высвобождению интерлейкина-4, а также фактора некроза опухоли-альфа, оба из которых были связаны с HG [56]. Также было обнаружено, что аденозин повышен при HG, и его роль заключается в ослаблении TNF-альфа [57]. В проспективном исследовании [58] также было обнаружено, что уровни интерлейкина-6 повышаются при HG, а также повышаются уровни иммуноглобулина G (IgG), IgM, уровни комплемента и количество лимфоцитов [59]. Однако точно определить роль этих иммунологических факторов нельзя, так как при голодании иммунная система обычно угнетается, а не активируется; таким образом, возможно, усиление иммунных факторов, наблюдаемое при HG, может быть попыткой ограничить прогрессирование HG [8].
Однако точно определить роль этих иммунологических факторов нельзя, так как при голодании иммунная система обычно угнетается, а не активируется; таким образом, возможно, усиление иммунных факторов, наблюдаемое при HG, может быть попыткой ограничить прогрессирование HG [8].
Другие гормоны, в том числе тиреотропный гормон, гормон роста, пролактин, адренокортико-стимулирующий гормон, кортизол, лютеинизирующий гормон и фолликулостимулирующий гормон, также оценивались и, как считается, не вносят вклад в патогенез невирапин [60].
Helicobacter pylori
Повышенная частота инфицирования Helicobacter pylori (H. pylori) наблюдалась у женщин с ГГ, и в настоящее время считается, что она играет роль в ее патогенезе. Фриго и др. обнаружили, что 90,5% женщин с HG были H. plyori IgG положительными по сравнению с 46,5% в контрольной группе [61]. Багис и др. использовали золотой стандарт тестирования, гистологическое исследование биопсии слизистой оболочки, и обнаружили, что 95% пациентов с HG дали положительный результат на H. pylori по сравнению с 50% в контрольной группе. Они также обнаружили более высокую плотность H. pylori в антральном отделе и теле желудка у пациентов с HG, что позволяет предположить возможную связь между плотностью H. pylori и тяжестью симптомов [62].
pylori по сравнению с 50% в контрольной группе. Они также обнаружили более высокую плотность H. pylori в антральном отделе и теле желудка у пациентов с HG, что позволяет предположить возможную связь между плотностью H. pylori и тяжестью симптомов [62].
Систематический обзор 2007 г., в котором оценивались 14 исследований типа «случай-контроль» с 1966 по 2007 г., выявил значительную связь между материнской инфекцией H.pylori и HG в 10 исследованиях. Отношение шансов в исследованиях варьировалось от 0.от 55 до 109,33 [63]. Аналогичным образом обновленный систематический обзор и метаанализ 25 исследований 2009 г. показали, что объединенное отношение шансов составляет 3,32 (95% доверительный интервал: 2,25–4,90) для инфекции H. pylori у женщин с HG [64]. Примечательно, что в обоих обзорах была обнаружена высокая гетерогенность исследований.
Инфицирование H. pylori во время беременности может произойти из-за вызванных стероидными гормонами изменений pH желудка [65] и/или повышенной восприимчивости из-за изменений гуморального и клеточно-опосредованного иммунитета [66]. Однако нет четких доказательств того, что беременность предрасполагает к инфекции de novo H. pylori . Напротив, было высказано предположение, что H. pylori может усугубить вызванные гормонами изменения нервной и электрической функции желудка и, таким образом, увеличить риск для инфицированных женщин оказаться в более тяжелой форме тошноты и рвоты. рвота [67].
Однако нет четких доказательств того, что беременность предрасполагает к инфекции de novo H. pylori . Напротив, было высказано предположение, что H. pylori может усугубить вызванные гормонами изменения нервной и электрической функции желудка и, таким образом, увеличить риск для инфицированных женщин оказаться в более тяжелой форме тошноты и рвоты. рвота [67].
Хотя связь между H. pylori и HG интригует, важно отметить, что инфекция не обязательно коррелирует с симптомами.На самом деле у большинства инфицированных женщин заболевание протекает бессимптомно [8]. В исследовании Weyermann et al. 23% из 898 родильниц дали положительный результат на H. pylori при дыхательном тесте с 13C-мочевиной; однако положительный результат не коррелировал с симптомами тошноты, рвоты или рефлюкса во время беременности [68]. Точно так же Wu et al. обнаружили, что 69% беременных женщин являются сероположительными в отношении H. pylori по сравнению с 50% в общей популяции, однако не обнаружили никакой корреляции между статусом антител и желудочно-кишечными симптомами [69].
Почему H. pylori нельзя точно связать с невирапином, а HG связывают с несколькими факторами. Во-первых, в большинстве исследований для оценки наличия инфекции использовалось тестирование на антитела. Однако серологическое тестирование на H. pylori не может отличить активную инфекцию от перенесенной инфекции [70], а активная и перенесенная инфекция могут по-разному влиять на симптомы. Во-вторых, в большинстве исследований не оценивался и/или не учитывался штамм H. pylori . Ассоциированный с цитотоксином белок гена A (CagA) является маркером учащения пептических язв и связан с более агрессивным штаммом H pylori [71].Только одно исследование, включенное в метаанализ 2009 г., оценивало патогенность CagA. В этом исследовании, проведенном Xia et al., положительная реакция на CagA была более распространена у пациентов с HG [72].
Лечение приводит к эрадикации H. pylori у большинства пациенток, однако в настоящее время нет рекомендаций по оценке или лечению H. pylori во время беременности, поскольку последующее облегчение симптомов HG широко не изучалось. Сообщения о клинических случаях и серии случаев позволяют предположить, что лечение и эрадикация 90–105 H.pylori может уменьшить тошноту и рвоту во время беременности, и его следует рассматривать у пациенток с трудноизлечимыми симптомами [73]. Однако необходимы более масштабные исследования, чтобы определить, следует ли и когда начинать лечение во время беременности, учитывая опасения по поводу безопасности лекарств. В настоящее время специалисты рекомендуют после завершения беременности и лактации проводить тройную терапию в течение двух недель [74].
pylori во время беременности, поскольку последующее облегчение симптомов HG широко не изучалось. Сообщения о клинических случаях и серии случаев позволяют предположить, что лечение и эрадикация 90–105 H.pylori может уменьшить тошноту и рвоту во время беременности, и его следует рассматривать у пациенток с трудноизлечимыми симптомами [73]. Однако необходимы более масштабные исследования, чтобы определить, следует ли и когда начинать лечение во время беременности, учитывая опасения по поводу безопасности лекарств. В настоящее время специалисты рекомендуют после завершения беременности и лактации проводить тройную терапию в течение двух недель [74].
Нарушение моторики желудочно-кишечного тракта
Изменения давления в состоянии покоя нижнего пищеводного сфинктера (НПС) и перистальтики пищевода связаны с невирапином.Хотя эти изменения чаще связаны с изжогой во время беременности, гастроэзофагеальная рефлюксная болезнь (ГЭРБ) может вызывать атипичные симптомы, такие как тошнота [75], и способствовать развитию невирапинов. Эстроген и прогестерон являются вероятными медиаторами нарушения моторики пищевода при беременности, при этом эстроген служит праймером, а прогестерон вызывает релаксацию НПС [76].
Эстроген и прогестерон являются вероятными медиаторами нарушения моторики пищевода при беременности, при этом эстроген служит праймером, а прогестерон вызывает релаксацию НПС [76].
Изменения желудочной ритмической активности могут способствовать НВП. Нормальная миоэлектрическая активность желудка приводит к медленному распространению волны от проксимального отдела тела к дистальному отделу антрального отдела со скоростью 3 цикла в минуту (имп/мин).Нарушение ритма в виде увеличения или уменьшения распространения медленных волн связано с тошнотой [74]. Используя эластогастрографию (EGG), Koch et al. продемонстрировали, что лица с нормальной медленноволновой активностью реже жаловались на тошноту во время беременности [77]. Напротив, люди с более высокими или более низкими показателями чаще жаловались на тошноту. Точно так же Riezzo et al. обнаружили, что беременные женщины без симптомов тошноты и рвоты на момент записи ЭГГ имеют нормальную миоэлектрическую активность 3 имп/мин.Они также обнаружили, что беременные женщины с невирапином имели более нестабильную активность EGG по сравнению с женщинами после добровольных абортов и небеременными женщинами из контрольной группы. Они предположили, что это может быть связано с восстановлением нормальной картины медленных волн желудка после аборта после нормализации уровней эстрадиола и прогестерона [78].
Они предположили, что это может быть связано с восстановлением нормальной картины медленных волн желудка после аборта после нормализации уровней эстрадиола и прогестерона [78].
Примечательно, однако, что многие исследования не обнаружили различий в перистальтике желудка между беременными и небеременными женщинами. С помощью сцинтографии желудка не было обнаружено существенных различий в скорости опорожнения жидкости у беременных женщин до добровольного аборта, через 6 недель после аборта и у небеременных женщин контрольной группы [79].Используя методы разбавления красителя феноловым красным, Davison et al. обнаружили задержку опорожнения желудка во время родов, но не в третьем триместре по сравнению с небеременными контрольными женщинами [80]. Точно так же исследования с использованием парацетамола не показали задержки опорожнения желудка в первом, втором или третьем триместре [81].
Изменения моторики желудка при беременности объясняются высоким уровнем прогестерона. Кроме того, на поздних сроках беременности сдавление увеличенной маткой может способствовать симптомам.
Состав пищи также может играть патогенную роль в NVP.Джеднак и др. продемонстрировали, что прием пищи с преобладанием белка был связан с уменьшением симптомов и коррекцией медленноволновой аритмии. Прием пищи с преобладанием углеводов или жиров не влиял на симптомы или медленноволновую аритмию [82].
Наконец, время прохождения по тонкой кишке было оценено в отношении патогенеза NVP. Используя водородный дыхательный тест с лактулозой, косвенный показатель времени прохождения по тонкой кишке, Lawson et al. обнаружили, что время транзита удлиняется во втором и третьем триместре по сравнению с первым триместром, причем самые длинные времена были обнаружены, когда уровни прогестерона были самыми высокими [83].Уолд и др. использовали аналогичные методы и обнаружили, что время транзита увеличивается в третьем триместре, когда уровни прогестерона и эстрогена были высокими по сравнению с послеродовым периодом [84]. Однако в обоих этих исследованиях задержка кишечного транзита не коррелировала с невирапином.
Психосоциальные факторы
Ранние исследования предполагали, что НВП может быть психосоматическим заболеванием, при котором рвота представляет собой интрапсихический конфликт. Некоторые предполагают, что NVP является проявлением подсознательной попытки беременной женщины отказаться от нежелательной беременности [85], поскольку исследования показали, что у женщин с NVP в первом триместре чаще бывают незапланированные или нежелательные беременности [86].
ГГ также ассоциируется с психологическими расстройствами, а именно невротическими наклонностями, истерией, неприятием женственности, неприятием беременности, а также с депрессией и психологическим стрессом, связанным с бедностью и семейными конфликтами [8]. Однако недавние исследования не выявили определенных психогенных причин ГГ [87, 88]. Некоторые, следовательно, утверждают, что социокультурные факторы, а не научные данные, привели к тому, что HG маркируется как психологически обусловленное состояние, и что более вероятно, что психологические нарушения, такие как депрессия, являются результатом, а не причиной HG [89].
Таким образом, хотя NVP и HG, вероятно, не являются результатом конверсионного расстройства или другого психологического расстройства, общепризнано, что у пострадавших женщин возникают психологические реакции, которые переплетаются с их физическими симптомами и, возможно, усугубляют их.
Диагностика и клинические признаки
Анамнез и медицинский осмотр
Несмотря на популярное использование термина «утренняя тошнота», невирапин сохраняется в течение дня у большинства больных женщин и, как было установлено, ограничивается утром менее чем у 2% женщин [90].Он часто начинается в течение нескольких недель после отсутствия менструации и поэтому в большинстве культур карикатурно изображается как начальный признак беременности. Симптомы обычно достигают пика между 10 и 16 неделями беременности и обычно исчезают после 20 недель. Однако до 10% женщин продолжают иметь симптомы после 22 недель [90].
В то время как обезвоживание и ортостаз могут возникать у женщин с HG, у большинства женщин с NVP показатели жизненно важных функций в норме, а физикальный осмотр является благоприятным. Однако следует провести тщательное обследование брюшной полости, чтобы исключить перитонит и другие внутрибрюшные причины тошноты и рвоты.
Однако следует провести тщательное обследование брюшной полости, чтобы исключить перитонит и другие внутрибрюшные причины тошноты и рвоты.
Дифференциальный диагноз
Учитывая высокую распространенность невирапина, тошнота и рвота в первом триместре обычно связаны с невирапином. Однако при наличии изменений в работе кишечника, боли в животе и рвоте желчью следует провести соответствующие исследования для исключения других причин. Дифференциальный диагноз невирапина включает гастроэзофагеальную рефлюксную болезнь, язвенную болезнь, непроходимость тонкой кишки, острый холецистит, желчнокаменную болезнь, панкреатит, а также аппендицит, гастроэнтерит, нефролитиаз, пиелонефрит и гепатит [74]
Диагностические и лабораторные исследования
Для диагностики невирапина не рекомендуются никакие специальные лабораторные исследования, кроме теста на беременность.Однако другие тесты могут быть полезны для исключения других причин тошноты и рвоты. Лейкоцитоз не должен наблюдаться при невирапине и может указывать на инфекционную или воспалительную причину, такую как холецистит, инфекция мочевыводящих путей и панкреатит. Повышение уровня аминотрансфераз может свидетельствовать о хроническом гепатите. Аномальный ТТГ может указывать на гипотиреоз или гипертиреоз, оба из которых могут вызывать тошноту и рвоту. Повышение уровня глюкозы в сыворотке может указывать на диабет и может вызывать тошноту и рвоту за счет снижения сократительной способности антрального отдела и ускорения желудочной аритмии [91].
Повышение уровня аминотрансфераз может свидетельствовать о хроническом гепатите. Аномальный ТТГ может указывать на гипотиреоз или гипертиреоз, оба из которых могут вызывать тошноту и рвоту. Повышение уровня глюкозы в сыворотке может указывать на диабет и может вызывать тошноту и рвоту за счет снижения сократительной способности антрального отдела и ускорения желудочной аритмии [91].
Рентгенография обычно не требуется для диагностики невирапина. УЗИ органов малого таза можно использовать для документирования беременности и оценки состояний, повышающих риск невирапина, таких как многоплодная беременность. Рентген брюшной полости, как правило, бесполезен и, хотя представляет небольшой риск для плода, все еще относительно противоречив в течение первого триместра.
Верхнюю эндоскопию можно безопасно проводить во время беременности и исключить гастрит и ЯБ как причины тошноты и рвоты во время беременности.В одном крупном центре тошнота и рвота были вторым наиболее частым показанием к эндоскопии верхних отделов во время беременности после кровотечения из верхних отделов желудочно-кишечного тракта [92].
Исход
Большинство исследований показали, что невирапин связан с благоприятным исходом для плода. Метаанализ 11 исследований Weigel et al. обнаружили сильную значимую связь между тошнотой и рвотой во время беременности и снижением риска выкидыша (общее отношение шансов = 0,36, 95% ДИ от 0,32 до 0,42) и отсутствие последовательной связи с перинатальной смертностью [93].Кроме того, было обнаружено, что женщины без NVP рожают раньше, чем женщины с NVP [94].
Однако в некоторых исследованиях сообщалось о неблагоприятных исходах, особенно когда невирапин считался тяжелым. Деушар и др. обнаружили повышенный риск задержки внутриутробного развития у женщин с тяжелым НВП, но не смогли объяснить потенциальное влияние противорвотных препаратов на рост плода [95]. Точно так же Zhou et al. обнаружили повышенный риск низкой массы тела при рождении у женщин с тяжелой формой НВП, вероятно, из-за пагубного влияния тошноты и рвоты на питание матери [96].
В проспективном исследовании 16 398 женщин не было обнаружено различий по врожденным аномалиям между женщинами с невирапином и без него [97]. Кроме того, ретроспективное исследование показало более низкий риск врожденных пороков сердца у детей, рожденных от женщин с ранним началом приема невирапина, требующих применения противорвотных средств, по сравнению с женщинами без тошноты [98].
Кроме того, ретроспективное исследование показало более низкий риск врожденных пороков сердца у детей, рожденных от женщин с ранним началом приема невирапина, требующих применения противорвотных средств, по сравнению с женщинами без тошноты [98].
Не совсем ясно, как NVP защищает развивающийся плод, однако было описано несколько теорий. Некоторые утверждают, что тошнота и рвота позволяют беременной женщине избегать или исключать продукты, которые могут быть тератогенными или вызывать аборт.Это может объяснить тесную временную связь между развитием отвращения к еде во время беременности и появлением тошноты [99]. NVP также может снизить потребление энергии и уровень анаболических гормонов, инсулина и фактора роста инсулина, что приводит к шунтированию дефицитных питательных веществ к плаценте и плоду [100].
Несмотря на благоприятное воздействие невирапина на плод, психосоциальные осложнения у беременных с невирапином значительны и, возможно, недооцениваются. В исследовании Smith et al. из 593 австралийских женщин с невирапином большинство сообщили, что их симптомы оказали серьезное негативное влияние на работу, домашние обязанности и воспитание детей, при этом 96% женщин сообщили о легком или умеренном дистрессе из-за тошноты, а 28% сообщили о дистрессе от умеренного до тяжелого [101].Точно так же исследование Mazzotta et al. канадских женщин обнаружили, что более сильная тошнота и рвота связаны с более частым чувством депрессии, рассмотрением вопроса о прерывании беременности, неблагоприятным воздействием на отношения женщин с их партнерами или их повседневную жизнь, а также с предполагаемой вероятностью того, что NVP нанесет вред их ребенку . Примечательно, что женщины с легкими симптомами также сообщали о тех же психосоциальных проблемах, что позволяет предположить, что тяжесть тошноты или рвоты неадекватно отражает дистресс, вызванный невирапином [2].
из 593 австралийских женщин с невирапином большинство сообщили, что их симптомы оказали серьезное негативное влияние на работу, домашние обязанности и воспитание детей, при этом 96% женщин сообщили о легком или умеренном дистрессе из-за тошноты, а 28% сообщили о дистрессе от умеренного до тяжелого [101].Точно так же исследование Mazzotta et al. канадских женщин обнаружили, что более сильная тошнота и рвота связаны с более частым чувством депрессии, рассмотрением вопроса о прерывании беременности, неблагоприятным воздействием на отношения женщин с их партнерами или их повседневную жизнь, а также с предполагаемой вероятностью того, что NVP нанесет вред их ребенку . Примечательно, что женщины с легкими симптомами также сообщали о тех же психосоциальных проблемах, что позволяет предположить, что тяжесть тошноты или рвоты неадекватно отражает дистресс, вызванный невирапином [2].
O’Brien и Naber также выявили значительную психосоциальную заболеваемость у женщин, страдающих невирапином. Они обнаружили, что пострадавшие женщины сообщали о снижении социальных обязательств и ухудшении отношений с супругами и детьми. Женщины с тяжелыми симптомами также сообщали о частой плаксивости, раздражительности, усилении нарушений сна и снижении настроения [102]. Используя краткую форму 36, Attard et al. обнаружили, что женщины с НВП имели более низкие показатели физического функционирования, физической роли, телесной боли, жизнеспособности, социального функционирования и эмоциональной роли в опросе, оценивающем качество жизни, по сравнению со здоровыми беременными контрольной группой на ранних сроках беременности и женщинами с хронической депрессией.Показатели психического здоровья женщин с НВП были аналогичны показателям женщин с депрессией [103].
Они обнаружили, что пострадавшие женщины сообщали о снижении социальных обязательств и ухудшении отношений с супругами и детьми. Женщины с тяжелыми симптомами также сообщали о частой плаксивости, раздражительности, усилении нарушений сна и снижении настроения [102]. Используя краткую форму 36, Attard et al. обнаружили, что женщины с НВП имели более низкие показатели физического функционирования, физической роли, телесной боли, жизнеспособности, социального функционирования и эмоциональной роли в опросе, оценивающем качество жизни, по сравнению со здоровыми беременными контрольной группой на ранних сроках беременности и женщинами с хронической депрессией.Показатели психического здоровья женщин с НВП были аналогичны показателям женщин с депрессией [103].
Помимо того, что невирапин вызывает психосоциальную заболеваемость, он также создает значительное финансовое бремя. В 2002 г. стоимость тяжелого невирапина оценивалась приблизительно в 130 миллионов долларов, исходя из больничных расходов, связанных в среднем с 39 000 госпитализаций. Эта цифра, вероятно, сильно занижена, поскольку она не включает потерю производительности дома, оплату услуг врача или стоимость лечения [104].
Эта цифра, вероятно, сильно занижена, поскольку она не включает потерю производительности дома, оплату услуг врача или стоимость лечения [104].
Подсчитано, что каждая работающая женщина с невирапином теряет 206 рабочих часов [2] и что на невирапин приходится 28% всех отпусков по болезни во время беременности до 28-й недели [19]. Кроме того, работа Vallacott et al. показывает, что 50% пострадавших женщин считают, что эффективность их работы значительно снижена [105].
HYPEREMESIS GRAVDIARUM
Гиперемезис беременных (HG) — это состояние сильной тошноты и рвоты во время беременности, приводящее к водно-электролитному и кислотно-щелочному дисбалансу, дефициту питательных веществ и потере веса [8].Некоторые определяют его как возникновение более трех эпизодов рвоты в день, сопровождающихся кетонурией и потерей веса более 3 кг или 5% массы тела [63]. ГГ является наиболее частой причиной госпитализации на ранних сроках беременности и уступает только преждевременным родам на протяжении всей беременности [106]. В Соединенных Штатах более 36 000 женщин ежегодно госпитализируются по поводу ХГ, и стоимость лечения оценивается более чем в 250 миллионов долларов в год только на госпитализацию [107].В отличие от NVP, который связан с благоприятными исходами для плода, HG представляет значительный риск для здоровья матери и плода.
В Соединенных Штатах более 36 000 женщин ежегодно госпитализируются по поводу ХГ, и стоимость лечения оценивается более чем в 250 миллионов долларов в год только на госпитализацию [107].В отличие от NVP, который связан с благоприятными исходами для плода, HG представляет значительный риск для здоровья матери и плода.
Диагностика и клинические признаки
ГГ проявляется в первом триместре беременности, обычно начиная с 4–5-й недели беременности. В дополнение к сильной тошноте и рвоте у 60% женщин с ГГ также наблюдается избыточное слюноотделение или слюнотечение [108]. Пациенты также могут жаловаться на симптомы гастроэзофагеального рефлюкса, такие как дискомфорт за грудиной и изжога. Уникальная количественная оценка рвоты и тошноты (PUQE) для беременных, которая рассчитывается с использованием количества часов тошноты в день, количества эпизодов рвоты в день и количества эпизодов позывов на рвоту в день, может использоваться для отслеживания тяжести симптомов. [109].
Пациенты могут иметь признаки обезвоживания, такие как сухость слизистых оболочек, тахикардия, плохой тургор кожи и постуральная гипотензия. Тяжело пораженные пациенты могут также иметь мышечную атрофию и слабость и/или изменения психического статуса.
Тяжело пораженные пациенты могут также иметь мышечную атрофию и слабость и/или изменения психического статуса.
Лабораторные нарушения у женщин с HG могут включать повышение азота мочевины в сыворотке крови, креатинина и гематокрита, а также кетонурию и увеличение удельного веса мочи. Кроме того, могут быть обнаружены электролитные нарушения, подтверждающие диагноз либо гипохлоремического метаболического алкалоза, либо метаболического ацидоза с выраженным сокращением объема [39].Уровни преальбумина (транстиретина в плазме) могут быть низкими, отражая плохой статус белкового питания у матери и, возможно, предсказывая более низкую массу тела плода при рождении [110]. Также возможен дефицит витаминов и минералов, таких как витамин B1 (тиамин), железо, кальций и фолиевая кислота [74].
Функциональные пробы печени могут отклоняться от нормы у 50% госпитализированных пациентов с ХГ [111]. Могут наблюдаться умеренная гипербилирубинемия (билирубин < 4 мг на децилитр) и/или повышение уровня щелочной фосфатазы вдвое по сравнению с верхней границей нормы [112]. Умеренный трансаминит является наиболее частым нарушением функции печени, при котором уровни аланинаминотрансферазы (АЛТ) обычно превышают уровни аспартатаминотрансферазы (АСТ). Повышение уровня трансаминаз обычно в два-три раза превышает верхнюю границу нормы; однако сообщалось об уровнях выше 1000 ЕД/мл [113]. Аномальные печеночные пробы исчезают сразу же после прекращения рвоты.
Умеренный трансаминит является наиболее частым нарушением функции печени, при котором уровни аланинаминотрансферазы (АЛТ) обычно превышают уровни аспартатаминотрансферазы (АСТ). Повышение уровня трансаминаз обычно в два-три раза превышает верхнюю границу нормы; однако сообщалось об уровнях выше 1000 ЕД/мл [113]. Аномальные печеночные пробы исчезают сразу же после прекращения рвоты.
Повышение уровня амилазы и липазы в сыворотке наблюдается у 10–15% женщин [39]. Одно исследование выявило повышенный уровень амилазы у 24% пациентов с ХГ [114].Считается, что это связано с избыточной выработкой амилазы слюнными железами, а не с секрецией поджелудочной железы, и является результатом, а не причиной ГГ [8].
Уровни тиреостимулирующего гормона могут быть низкими при ХГ из-за перекрестной реакции между альфа-субъединицей ХГЧ и рецептором ТТГ. В большинстве случаев этот биохимический тиреотоксикоз не имеет клинического значения, так как пациенты находятся в эутиреоидном состоянии. Уровень гормонов щитовидной железы обычно нормализуется без лечения после родов.
HG — это клинический диагноз, основанный на симптомах и исключении других состояний.Как и в случае с невирапином, для диагностики ГГ не требуется специального тестирования; тем не менее, УЗИ брюшной полости и таза может быть полезным для исключения других причин, таких как заболевание желчного пузыря, пузырный занос, а также для оценки многоплодной беременности. Дифференциальный диагноз включает невирапин, острый тиреоидит, расстройства пищевого поведения, заболевания желчевыводящих путей, вирусный гепатит и гастроэзофагеальную рефлюксную болезнь.
Исход
В отличие от NVP, HG связан с неблагоприятными исходами как для матери, так и для плода. В исследовании более 150 000 одноплодных беременностей младенцы, рожденные женщинами с гиперемезисом и низкой прибавкой массы тела при беременности (<7 кг), с большей вероятностью имели низкую массу тела при рождении, маловаты для гестационного возраста, родились до 37 недель беременности и имели мин. Оценка по шкале Апгар < 7 [5].
Общие материнские осложнения включают потерю веса, обезвоживание, дефицит питательных микроэлементов и мышечную слабость. Более тяжелые, хотя и редкие, осложнения включают разрывы Мэллори-Вейса, разрыв пищевода, энцефалопатию Вернике с корсаковским психозом или без него, центральный мостовой миелинолиз из-за быстрой коррекции тяжелой гипонатриемии, кровоизлияние в сетчатку и спонтанный пневмомедиастинум [47]. Также сообщалось о вазоспазме церебральных артерий из-за повышенной симпатической активности [115].
HG способствует возникновению многих психологических проблем и может привести к прерыванию нежелательной беременности и снижению вероятности попытки повторной беременности [116]. Пуршариф и др. обнаружили, что у 15% из 808 женщин с HG было по крайней мере одно прерывание беременности из-за болезни. Интересно, что у тех женщин, которые прервали беременность, не было более тяжелого заболевания, чем у женщин с ГГ, которые сохранили беременность, но в два раза чаще считали, что их врач безразличен или не обратил внимания на тяжесть их заболевания [117].
Долгосрочные последствия HG для матерей неизвестны. Несколько исследований показывают повышенный риск рака молочной железы [118]. Имеются также сообщения о повышенной частоте депрессии, посттравматического стрессового расстройства и различных неврологических расстройств [39].
Некоторые исследования не выявили повышенного риска неблагоприятных исходов для плода у женщин с ГГ. Башири и соавт., например, сообщили о более низкой частоте спонтанных ранних потерь беременности у женщин с ГГ по сравнению с общей популяцией и не обнаружили различий в перинатальных исходах [6].Однако в других исследованиях была обнаружена связь между ГГ и задержкой роста плода, преэклампсией и малым весом для гестационного возраста [119]. В ретроспективном исследовании 3068 женщин ГГ была связана с более ранними родами и меньшей массой тела при рождении. Эти исходы были наиболее вероятны у женщин, которые потеряли более 5% массы тела до беременности [120]. Точно так же Dodds et al. обнаружили более высокие показатели низкой массы тела при рождении, преждевременных родов, гибели плода у женщин с ХГ, которые в целом набрали менее 7 кг во время беременности [5]. Многократные госпитализации по поводу ХГ, по-видимому, являются еще одним фактором риска снижения массы тела новорожденных при рождении [108].
Многократные госпитализации по поводу ХГ, по-видимому, являются еще одним фактором риска снижения массы тела новорожденных при рождении [108].
Различные врожденные пороки развития чаще наблюдаются у женщин с ХГ [32]. К ним относятся синдром Дауна, дисплазия тазобедренного сустава, неопущение яичек, пороки развития скелета, дефекты центральной нервной системы и аномалии кожи. Сообщалось о коагулопатии плода и хондродисплазии из-за дефицита витамина К [121] с внутричерепным кровоизлиянием плода в третьем триместре [122].Некоторые виды рака у детей, такие как рак яичек или лейкемия, также были связаны с ГГ у матери, однако данные противоречивы [39].
ЛЕЧЕНИЕ
Целью лечения является облегчение симптомов при минимизации риска для матери и плода. Для достижения этого обычно необходим мультимодальный подход, адаптированный к каждому человеку. Методы лечения варьируются от простых диетических модификаций до медикаментозной терапии и полного родительского питания. Тяжесть симптомов и потеря веса матери помогают определить агрессивность лечения. PUQEscore и опросник по влиянию гиперемезиса на симптомы (HIS) можно использовать для оценки тяжести симптомов. Обновленная шкала PUQE оценивает симптомы в течение 24 часов [123], в то время как HIS учитывает психосоциальные факторы в дополнение к физическим симптомам [124].
PUQEscore и опросник по влиянию гиперемезиса на симптомы (HIS) можно использовать для оценки тяжести симптомов. Обновленная шкала PUQE оценивает симптомы в течение 24 часов [123], в то время как HIS учитывает психосоциальные факторы в дополнение к физическим симптомам [124].
Текущие исследования показывают, что лечение невирапином является субоптимальным. Одно недавнее проспективное исследование 283 женщин с невирапином в течение первого триместра показало, что только половине из них задавали вопрос об интенсивности и тяжести их симптомов, менее четверти спрашивали, мешают ли их симптомы их повседневным задачам и работе.В этом исследовании Lacasse et al только 27% женщин были предложены противорвотные средства, а еще 14% были рекомендованы немедикаментозные методы лечения [125].
Немедикаментозная терапия
Диетические меры
Начальная терапия невирапина и ГГ должна включать диетические изменения. Пораженные женщины должны избегать больших приемов пищи и вместо этого есть несколько небольших приемов пищи в течение дня, которые должны быть пресными и с низким содержанием жира, поскольку жирная пища может еще больше задержать опорожнение желудка. Употребление белка больше, чем углеводов, и употребление большего количества жидкости, чем твердой пищи, также может уменьшить тошноту, уменьшая желудочные аритмии, связанные с невирапином [82].Рекомендуются небольшие объемы соленых жидкостей, таких как электролитозамещающие спортивные напитки, а если запах горячей пищи является неприятным, следует приготовить холодную пищу [126].
Употребление белка больше, чем углеводов, и употребление большего количества жидкости, чем твердой пищи, также может уменьшить тошноту, уменьшая желудочные аритмии, связанные с невирапином [82].Рекомендуются небольшие объемы соленых жидкостей, таких как электролитозамещающие спортивные напитки, а если запах горячей пищи является неприятным, следует приготовить холодную пищу [126].
Эмоциональная поддержка
Эмоциональную поддержку всегда должен оказывать медицинский работник. Кроме того, поддерживающая психотерапия, поведенческая терапия и гипнотерапия могут быть полезны для женщин с тяжелыми симптомами и/или для тех, у кого играют роль личностные особенности, супружеские или семейные конфликты [60].Цель психотерапии не в том, чтобы углубляться в психологию, которая может способствовать НВП, а в том, чтобы поощрять, объяснять, успокаивать и позволять пациенту выражать стресс [95].
Акупрессура/акупунктура
Акупрессура китайской акупунктурной точки Р6 (Нэйгуань) снижает тошноту у пациентов с тошнотой, вызванной химиотерапией, а также послеоперационной тошнотой и рвотой, и может быть полезна при лечении ГГ. В соответствии с принципом ци, приложение давления к этой точке блокирует аномальное замедление энергии и восстанавливает симптомы, связанные с точкой давления [13].Давление можно оказывать вручную или с помощью эластичных лент на внутренней стороне запястья. Кроме того, ReliefBand, электрический стимулятор нервов с батарейным питанием, который носится на запястье, недавно был одобрен FDA и может также использоваться для стимуляции участка P6 [127].
В соответствии с принципом ци, приложение давления к этой точке блокирует аномальное замедление энергии и восстанавливает симптомы, связанные с точкой давления [13].Давление можно оказывать вручную или с помощью эластичных лент на внутренней стороне запястья. Кроме того, ReliefBand, электрический стимулятор нервов с батарейным питанием, который носится на запястье, недавно был одобрен FDA и может также использоваться для стимуляции участка P6 [127].
Доказательства акупрессуры противоречивы. Один обзор семи испытаний показал, что акупрессура точки Neiguan может облегчить симптомы тошноты [128]. Недавнее плацебо-контролируемое исследование с участием 60 женщин, принимавших невирапин, показало, что в группе лечения наблюдалось облегчение тошноты на следующий день после начала акупрессуры над местом P6, которое продолжалось до конца периода наблюдения.Для сравнения, в группе, получавшей акупрессуру на незначительном участке, наблюдалось первоначальное облегчение симптомов, но к 6-му дню симптомы вернулись и не отличались от группы, не получавшей лечения [129].
Хотя исследования преимуществ акупрессуры не дали окончательных результатов, некоторые эксперты считают, что это вмешательство должно быть предложено, поскольку не существует известных побочных эффектов [130].
Иглоукалывание менее изучено, но одно слепое рандомизированное контролируемое исследование с участием 593 женщин со сроком беременности менее 14 недель показало, что у женщин, получавших еженедельное лечение иглоукалыванием в течение 4 недель, было меньше тошноты и сухих рвотных позывов по сравнению с контрольной группой [131].Однако возможно, что состояние некоторых женщин улучшилось просто с увеличением гестационного возраста [13].
Имбирь
Имбирь — единственное немедикаментозное вмешательство, рекомендованное Американским колледжем акушерства и гинекологии [132]. Считается, что имбирь помогает улучшить НВП, стимулируя моторику желудочно-кишечного тракта и стимулируя выделение слюны, желчи и желудочного секрета. Было показано, что один компонент имбиря обладает такой же активностью, что и антагонист 5-HT3, ондансетрон. Кроме того, было обнаружено, что его экстракт ингибирует рост некоторых штаммов H. pylori [133].
Кроме того, было обнаружено, что его экстракт ингибирует рост некоторых штаммов H. pylori [133].
В двойном слепом рандомизированном перекрестном исследовании 70% женщин с ГГ, получавших 250 мг порошкообразного корня имбиря четыре раза в день, предпочли период приема имбиря по сравнению с периодом приема плацебо. Женщины также сообщали о значительно большем облегчении симптомов при приеме имбиря. 4 дня обнаружили, что у женщин в группе лечения было значительное улучшение симптомов тошноты по сравнению с женщинами в группе плацебо ( P <.001) [135].
Что касается безопасности имбиря во время беременности, исследование случай-контроль с участием 187 беременных женщин не выявило увеличения частоты серьезных пороков развития при употреблении имбиря в первом триместре [136]. Однако существует теоретический риск кровотечения, поскольку имбирь ингибирует тромбоксансинтетазу и может ингибировать функцию тромбоцитов. Таким образом, одновременное использование антикоагулянтов с имбирем не рекомендуется [137].
Фармакологическое лечение
Пиридоксин-доксиламин
Комбинация пиридоксина (витамина В6) (категория А при беременности) и доксиламина (категория В), ранее доступная как бендектин, является единственным лекарственным средством, которое специально маркировано для лечения невирапина Управление по санитарному надзору за качеством пищевых продуктов и медикаментов.Он по-прежнему доступен в Канаде в таблетках с отсроченным высвобождением, содержащих 10 мг пиридоксина и 10 мг доксиламина, под торговым названием Диклектин.
Бенедектин был снят с продажи в 1983 году в США в связи с сообщениями о врожденных пороках развития при применении в первом триместре. Однако до его отмены 30 миллионов женщин принимали его в течение почти 25 лет. Несколько небольших рандомизированных контролируемых исследований подтверждают его эффективность [138]. Кроме того, метаанализ, который включал 170 000 воздействий, показал, что комбинация пиридоксин-доксиламин безопасна и не вызывает побочных эффектов у плода [139]. Другие крупные исследования также не показали увеличения частоты врожденных аномалий по сравнению с фоновой частотой [140]. Тем не менее, Бенедектин остается вне рынка в Соединенных Штатах. Однако женщины могут сделать свой собственный препарат, объединив 10 мг пиридоксина с половинкой таблетки Унисома, который содержит 25 мг доксиламина.
Другие крупные исследования также не показали увеличения частоты врожденных аномалий по сравнению с фоновой частотой [140]. Тем не менее, Бенедектин остается вне рынка в Соединенных Штатах. Однако женщины могут сделать свой собственный препарат, объединив 10 мг пиридоксина с половинкой таблетки Унисома, который содержит 25 мг доксиламина.
В качестве альтернативы пиридоксин можно принимать отдельно. Хотя связи между уровнями пиридоксина и невирапином не обнаружено, в нескольких исследованиях было показано улучшение показателей тошноты у пациентов, принимавших пиридоксин с выраженной тошнотой [141], и уменьшение эпизодов рвоты по сравнению с женщинами, принимавшими плацебо [138].Нет известных доказательств токсичности витамина B6, однако в больших дозах пиридоксин был связан с обратимой периферической нейропатией у небеременных взрослых [13].
Противорвотные средства
Фенотиазины, хлорпромазин (торазин) и прохлорперазин (компазин), являются центральными и периферическими антагонистами дофамина, которые, как было показано, уменьшают симптомы невирапина и ГГ [142]. Они относятся к категории беременности С.
Они относятся к категории беременности С.
Исследование 12 764 беременных женщин показало незначительное повышение риска врожденных дефектов при применении фенотиазинов в первом триместре, особенно при применении хлорпромазина, однако потенциальные смешанные факторы, такие как употребление алкоголя и продолжительность лечения, не были выявлены. 143].Другое исследование показало, что у младенцев от матерей, принимавших хлорпромазин, были экстрапирамидные симптомы и желтуха; значительных нарушений постнатального развития не было [144].
Прометазин (Phenergan) не обладал тератогенными эффектами в одном исследовании [145], но в другом исследовании наблюдалось усиление врожденного вывиха бедра [146].
Активаторы
Метоклопрамид (Реглан) широко используется для лечения невирапина [147]. Это категория беременности B. Считается, что метоклопрамид улучшает симптомы за счет повышения давления в нижнем пищеводном сфинктере и увеличения транзита через желудочный тракт. Он также корректирует желудочные аритмии, стимулируя антральные сокращения и способствуя антродуоденальным сокращениям. Недавнее исследование показало, что 10 мг метоклопрамида, принимаемого каждые 8 часов, столь же эффективны для уменьшения количества эпизодов рвоты и улучшения самочувствия у женщин с ГГ во время их первой госпитализации, как и 25 мг прометазина, принимаемого каждые 8 часов в течение 24 часов. Профиль побочных эффектов был лучше в группе, получавшей метоклопрамид, с меньшей сонливостью, головокружением и дистонией [148].
Он также корректирует желудочные аритмии, стимулируя антральные сокращения и способствуя антродуоденальным сокращениям. Недавнее исследование показало, что 10 мг метоклопрамида, принимаемого каждые 8 часов, столь же эффективны для уменьшения количества эпизодов рвоты и улучшения самочувствия у женщин с ГГ во время их первой госпитализации, как и 25 мг прометазина, принимаемого каждые 8 часов в течение 24 часов. Профиль побочных эффектов был лучше в группе, получавшей метоклопрамид, с меньшей сонливостью, головокружением и дистонией [148].
Что касается безопасности, исследование 81 703 родов в период с 1998 по 2007 год в Израиле, в ходе которого метоклопрамид применялся у 4,2% женщин, не выявило повышенного риска серьезных врожденных пороков развития, низкой массы тела при рождении, преждевременных родов или перинатальной смерти при применении метаклопрамида. использовать [149]. Точно так же датское исследование 309 беременных женщин, принимавших метаклопрамид, не выявило повышенного риска [150].
Несмотря на свою эффективность, использование метоклопрамида ограничено его побочными эффектами, которые включают дистонию, беспокойство и сонливость.В 2009 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) добавило к метоклопрамиду предупреждение «черный ящик» из-за риска поздней дискинезии при хроническом применении.
Другие прокинетики, такие как домперидон и эритромицин, не изучались при применении невирапина [74].
Антигистаминные и антихолинергические препараты
Антигистаминные препараты косвенно влияют на вестибулярную систему, уменьшая стимуляцию рвотного центра [151]. Рандомизированные контролируемые исследования применения антигистаминных препаратов при невирапине ограничены; однако было показано, что меклизин (анитверт), дименгирдинат (драмамин) и дифенгирамин (бенадрил) контролируют симптомы лучше, чем плацебо [142].Кроме того, объединенные данные семи испытаний между 1951 и 1975 годами показали эффективность антигистаминных препаратов [152]. Метаанализ более 24 контролируемых исследований с участием более 200 000 беременных женщин показал, что антигистаминные препараты (в частности блокаторы Н2-рецепторов), назначаемые в течение первого триместра, не повышают риск тератогенного действия [153]. Хотя ранее считалось, что меклизин обладает тератогенным действием, теперь исследования показывают, что его безопасно использовать во время беременности [154]. Дименгидринат и дифенгидрамин имеют противоречивые результаты по безопасности [74].
Метаанализ более 24 контролируемых исследований с участием более 200 000 беременных женщин показал, что антигистаминные препараты (в частности блокаторы Н2-рецепторов), назначаемые в течение первого триместра, не повышают риск тератогенного действия [153]. Хотя ранее считалось, что меклизин обладает тератогенным действием, теперь исследования показывают, что его безопасно использовать во время беременности [154]. Дименгидринат и дифенгидрамин имеют противоречивые результаты по безопасности [74].
В одном исследовании женщин, перенесших плановое кесарево сечение, было обнаружено, что трансдермальный скополамин более эффективен в уменьшении тошноты, рвоты и позывов на рвоту из-за эпидуральной морфиновой анальгезии по сравнению с плацебо [155]. Однако исследования по применению скополамина в первом триместре отсутствуют, поскольку скополамин может вызывать хромосомные аберрации и обмены сестринскими хроматидами в здоровых взрослых лимфоцитах и может приводить к врожденным порокам развития, включая деформацию конечностей и туловища [156].
Другие препараты
Ондансетрон (Зофран) (категория B при беременности) широко используется для лечения послеоперационной и вызванной химиотерапией тошноты и рвоты и в настоящее время является одним из наиболее часто назначаемых противорвотных средств [157].Считается, что он действует как центрально, так и периферически, блокируя серотониновые рецепторы в тонкой кишке и медуллярном рвотном центре [151]. Его безопасность при беременности была определена в недавнем исследовании, которое не показало значительного увеличения числа выкидышей, серьезных пороков развития или массы тела при рождении между младенцами, подвергшимися воздействию ондансетрона, и контрольной группой, не получавшей его [158].
Было проведено одно рандомизированное контролируемое исследование применения ондансетрона для лечения ХГ. В этом небольшом исследовании с участием 30 женщин не было выявлено преимуществ ондансетрона в дозе 10 мг внутривенно каждые 8 часов по мере необходимости по сравнению с прометазином в дозе 50 мг внутривенно каждые 8 часов с точки зрения тошноты, увеличения веса, дней госпитализации или общих доз препарата [46]. .Однако было обнаружено, что прометазин вызывает больший седативный эффект. Тем не менее, сообщения о случаях заболевания и широко распространенный клинический опыт подтверждают эффективность ондансетрона для лечения HG и его лучшую переносимость по сравнению с более ранними противорвотными средствами [159, 160].
.Однако было обнаружено, что прометазин вызывает больший седативный эффект. Тем не менее, сообщения о случаях заболевания и широко распространенный клинический опыт подтверждают эффективность ондансетрона для лечения HG и его лучшую переносимость по сравнению с более ранними противорвотными средствами [159, 160].
Дроперидол (инапсин) является антагонистом дофамина, эффективным противорвотным средством при послеоперационной тошноте и рвоте. Небольшое исследование женщин с HG показало, что комбинация непрерывной инфузии дроперидола и болюсного внутривенного введения дифенгидрамина приводила к более коротким госпитализациям и меньшему количеству повторных госпитализаций по сравнению с исторической контрольной группой, которая получала другие формы парентеральной терапии.Кроме того, не было никаких существенных различий в материнских или перинатальных исходах [161]. Следует отметить, однако, что дроперидол имеет предупреждение черного ящика, поскольку он может вызывать удлинение интервала QT и сердечные аритмии [74].
Пероральные и внутривенные кортикостероиды использовались для рефрактерных случаев HG с переменными результатами. Считается, что они оказывают противорвотное действие на триггерную зону хеморецепторов в стволе головного мозга, а также постулируются для коррекции «относительной надпочечниковой недостаточности», вызванной HG, при которой гипоталамо-гипофизарно-надпочечниковая ось не может реагировать на повышенные потребности в кортизоле. во время ранней беременности.
В рандомизированном контролируемом исследовании 40 женщин с ГГ, получавших метилпреднизолон в дозе 16 мг перорально 3 раза в день в течение 3 дней с последующим 2-недельным снижением дозы, по сравнению с прометазином в дозе 25 мг перорально 3 раза в день в течение 2 недель, — госпитализация была обнаружена в группе, получавшей стероиды [162]. Другие исследования не показали статистически значимого преимущества кортикостероидов. Рандомизированное исследование Yost et al. не обнаружили значительного снижения числа посещений неотложной помощи или повторных госпитализаций при добавлении парентерального и перорального метилпреднизолона к режиму прометазина и метоклопрамида [163].
Нет утвержденных руководств по применению кортикостероидов при ХГ. Однако была предложена возможная схема: 48 мг метилпреднизолона вводят перорально или внутривенно в три приема в течение двух-трех дней. Если в течение трех дней ответа не наблюдается, рекомендуется прекратить лечение, так как ответ через 72 часа маловероятен [151].
Что касается безопасности, то недавний метаанализ показал небольшое увеличение основных пороков развития и 3,4-кратное увеличение расщелины рта у младенцев, матери которых принимали кортикостероиды в первом триместре [164].
В последнее время наблюдается интерес к препаратам, снижающим кислотность при лечении невирапином, поскольку одно недавнее когортное исследование показало, что у женщин с невирапином и изжогой и/или кислотным рефлюксом тошнота и рвота были более выраженными, чем у женщин без изжоги или кислотного рефлюкса [165]. Кроме того, последующие исследования показали, что лечение изжоги и/или рефлюкса приводит к улучшению показателей PUQE и показателей качества жизни [166].
Антациды, содержащие алюминий или кальций, являются терапией первой линии во время беременности при кислотном рефлюксе и изжоге и могут использоваться для лечения женщин с невирапином.Антациды, содержащие магний, связаны с нефролитиазом, гипотонией и респираторным дистресс-синдромом у плода и не рекомендуются во время беременности. Антациды, содержащие бикарбонаты, могут вызывать метаболический ацидоз плода и перегрузку жидкостью и также не рекомендуются [167].
Блокаторы h3 и ингибиторы протонной помпы можно безопасно использовать для лечения кислотного рефлюкса и/или изжоги у женщин с невирапином [168, 169].
Нутритивная поддержка
Женщинам с трудноизлечимыми симптомами, не поддающимися коррекции диеты и фармакологическому лечению и неспособными поддерживать вес за счет перорального приема пищи, может потребоваться пищевая поддержка.В этой популяции следует использовать внутривенную инфузионную терапию, энтеральное или парентеральное питание для предотвращения задержки внутриутробного развития плода, обезвоживания матери и недостаточности питания.
Роль внутривенной гидратации заключается в увеличении объема и восстановлении электролитов. Госпитализированным пациентам при необходимости можно быстро влить физиологический раствор или раствор Рингера с лактатом, а затем откорректировать их для соответствия диурезу. Внутривенно тиамин следует вводить перед любыми жидкостями, содержащими декстрозу, чтобы избежать энцефалопатии Вернике.Женщинам, которым требуется многократная госпитализация, может быть рекомендована внутривенная гидратация в домашних условиях [74].
Энтеральное зондовое питание и полное парентеральное питание следует рассмотреть, если внутривенная терапия не помогает уменьшить симптомы, а дефицит калорий сохраняется. Однако исследования энтерального питания при HG ограничены. В одном небольшом исследовании женщин с HG, получавших энтеральное питание с использованием назогастрального зонда 8-French, сообщалось об улучшении симптомов в течение 24 часов после установки зонда.Через 8 дней пациенты были выписаны в среднем на 43 дополнительных дня амбулаторного энтерального питания, после чего можно было возобновить пероральное питание [170].
Помимо назогастральных зондов, чрескожная эндоскопическая гастростомия (ЧЭГ) [171] успешно использовалась для поддержания питания у женщин с ГГ. Однако оба этих способа кормления ограничены риском усиления тошноты и рвоты, вызванных внутрижелудочным кормлением. Постпилорические зонды для кормления, как назоеюнальные [172, 173], так и чрескожные эндоскопические гастроеюноанастомозы [174] пытались снизить этот риск, однако смещение зондов [175] из-за продолжающейся рвоты, позывов на рвоту и свертывания желудка является частым осложнением. .Кроме того, назоэнтеральные зонды, как назогастральные, так и назоеюнальные, плохо переносятся многими женщинами из-за эстетических соображений и физического дискомфорта. Недавно хирургическая еюностомия была описана как альтернативный способ доставки питания женщинам с HG. В одном небольшом исследовании пяти женщинам с HG была выполнена хирургическая еюностомия во втором триместре. Изотонические кормления через зонд вводили до целевого показателя калорийности. Прибавка в весе матери наблюдалась в 5 из 6 беременностей, и все беременности закончились срочными родами.Серьезных осложнений не произошло, что позволяет предположить, что еюностомия может быть безопасным и эффективным способом нутритивной поддержки у женщин с ХГ [176].
Прибавка в весе матери наблюдалась в 5 из 6 беременностей, и все беременности закончились срочными родами.Серьезных осложнений не произошло, что позволяет предположить, что еюностомия может быть безопасным и эффективным способом нутритивной поддержки у женщин с ХГ [176].
Женщинам, которые не переносят энтеральное питание, следует рассмотреть возможность парентерального питания. Эта терапия, однако, является дорогостоящей и связана со значительной материнской заболеваемостью. Руссо-Стейглиц и др. сообщили о частоте осложнений 9% при парентеральном питании через периферически установленные центральные катетеры во время беременности и о 50% частоте осложнений при центрально вставленных катетерах.Инфекция и тромбоз были двумя наиболее часто встречающимися осложнениями, и предполагалось, что они являются результатом связанной с беременностью гиперкоагуляции и иммунологической супрессии [177]. Holmgren et al. также показали высокую частоту осложнений у женщин, получавших парентеральное питание через PICC. В исследовании 94 женщин с HG 66,4% из тех, кто получал парентеральное питание через PICC, нуждались в лечении тромбоэмболии, инфекции или того и другого. Пациентки на парентеральном питании также имели более высокую частоту неонатальных осложнений, включая госпитализацию в отделение интенсивной терапии новорожденных, малый размер для гестационного возраста, прерывание беременности из-за ГГ и потерю плода по сравнению с женщинами, получавшими энтеральное питание [178].Таким образом, парентеральное питание, хотя оно может быть более переносимым для пациентов, следует зарезервировать для отдельных пациентов с HG.
В исследовании 94 женщин с HG 66,4% из тех, кто получал парентеральное питание через PICC, нуждались в лечении тромбоэмболии, инфекции или того и другого. Пациентки на парентеральном питании также имели более высокую частоту неонатальных осложнений, включая госпитализацию в отделение интенсивной терапии новорожденных, малый размер для гестационного возраста, прерывание беременности из-за ГГ и потерю плода по сравнению с женщинами, получавшими энтеральное питание [178].Таким образом, парентеральное питание, хотя оно может быть более переносимым для пациентов, следует зарезервировать для отдельных пациентов с HG.
Информация для авторов
Ноэль М. Ли, Школа медицины и общественного здравоохранения Университета Висконсина, Медицинский фонд Университета Вашингтона, здание столетия, 1685 Highland Avenue, Madison, WI 53705, телефон: (608) 263-1995, факс: (608) 265-5677.
Сумона Саха, Отделение гастроэнтерологии и гепатологии, Школа медицины и общественного здравоохранения Висконсинского университета, Медицинский фонд Университета Вашингтона, здание столетия, 1685 Хайленд-авеню, комната 4224, Мэдисон, Висконсин 53705, телефон: (608) 263-1995, факс: (608) 265-5677.
Тошнота и рвота при беременности
Введение
Тошнота и рвота являются обычным явлением во время беременности, которым страдают 70–80% всех беременных женщин. Хотя у большинства женщин тошнота и рвота при беременности (НВП) имеют симптомы, ограниченные первым триместром, у небольшого процента женщин наблюдается длительное течение с симптомами, продолжающимися до родов. У женщин с тяжелой тошнотой и рвотой во время беременности может быть гиперемезис беременных (HG), состояние, отличное от NVP, которое, если его не лечить, может привести к значительной заболеваемости матери и плода.
Различные метаболические и нервно-мышечные факторы вовлечены в патогенез невирапина и HG; однако их точная причина неизвестна. Следовательно, лечение NVP и HG может быть затруднено, поскольку не известны ни оптимальные цели лечения, ни полные эффекты потенциальных методов лечения на развивающийся плод. В этой статье рассматриваются эпидемиология, патология, диагностика, исходы и лечение невирапина и HG.
Эпидемиология
По оценкам, 70–80% беременных женщин получают невирапин [1].В Соединенных Штатах и Канаде это означает примерно 4 000 000 и 350 000 женщин, которые страдают каждый год соответственно [2].
НВП чаще встречается в западных странах и у городского населения и редко встречается у африканцев, коренных американцев, эскимосов и большинства азиатских популяций [3]. Лишь в нескольких исследованиях изучалось расовое распределение невирапина в данной популяции. Одно такое исследование, проведенное в Канаде с участием 367 женщин, показало, что азиаты и чернокожие реже сообщали о симптомах невирапина, чем представители европеоидной расы.Социально-демографические факторы не учитывали расовые/этнические различия в распространенности заболевания, что позволяет предположить, что могут играть роль генетические и/или культурные факторы [4].
HG встречается редко по сравнению с NVP и встречается в 0,3–2% всех беременностей [5]. Заболеваемость зависит от этнической принадлежности [6] и колеблется от 3 до 20 на 1000 беременностей [7]. Он чаще диагностируется у женщин в Индии, Пакистане, Азии, Новой Зеландии по сравнению с европейцами, американскими индейцами и эскимосами [8].
Он чаще диагностируется у женщин в Индии, Пакистане, Азии, Новой Зеландии по сравнению с европейцами, американскими индейцами и эскимосами [8].
Факторы риска
Данные Совместного перинатального проекта, одного из крупнейших на сегодняшний день исследований беременных женщин, показали, что невирапин чаще встречается у молодых женщин, первобеременных, женщин с образованием менее 12 лет, некурящих и женщины с ожирением [9]. О повышенном риске невирапина в первом триместре также сообщалось у женщин с многоплодной беременностью по сравнению с женщинами с одноплодной беременностью (87% против 73%, p<0,01) [10].
НВП был связан с низким уровнем дохода и статусом занятости неполный рабочий день [11]).Было обнаружено, что домохозяйки также подвергаются повышенному риску, в то время как женщины, работающие в качестве белых воротничков, по-видимому, защищены [12]. Однако остается неясным, является ли статус занятости истинным фактором риска для невирапина или искажающим фактором, поскольку затронутые женщины могут прекратить работу из-за своих симптомов. Точно так же их решение не работать вне дома может быть связано с многодетностью и необходимостью заботиться о других детях [13].
Точно так же их решение не работать вне дома может быть связано с многодетностью и необходимостью заботиться о других детях [13].
Материнская генетика также может служить фактором риска для невирапина. Данные большой популяции норвежских близнецов показывают более широкое использование лекарств от тошноты во время беременности среди монозиготных близнецов женского пола по сравнению с дизиготными близнецами женского пола [14].Кроме того, более высокие уровни тошноты были обнаружены у женщин, матери которых испытывали тошноту во время беременности [15]. Также было показано, что личный анамнез NVP является фактором риска для NVP при последующих беременностях [15]; однако этот вывод не был последовательным в разных исследованиях [16]
Другие факторы риска для невирапина включают личную историю укачивания, возможно, из-за общего вестибулярного механизма [17] и мигреней в анамнезе [18]. Женщины, у которых в анамнезе была тошнота при приеме эстрогенсодержащих пероральных контрацептивов, также подвержены повышенному риску невирапина [19].
Расположение желтого тела также может служить фактором риска невирапина. Ультразвуковые исследования показали, что беременные чаще испытывают тошноту и рвоту при наличии желтого тела в правом яичнике [20]. Это может быть связано с различиями в венозном оттоке между левым и правым яичником и более высокой концентрацией половых стероидов, когда желтое тело находится на правой стороне [21].
Более высокое суточное потребление общего жира, особенно насыщенных жиров, до беременности увеличивает риск госпитализации по поводу невирапина [22].Курение до беременности и прием витаминов до и/или на ранних сроках беременности связаны со снижением риска невирапина [23]. Также было обнаружено, что употребление алкоголя матерью до зачатия защищает от NVP [24].
Факторы риска HG аналогичны факторам риска NVP. К ним относятся многоплодная беременность, трофобластическая болезнь, HG в предшествующей беременности, аномалии плода, такие как триплоидия, трисомия 21 и водянка плода, а также нерождение плода [25]. Семейный анамнез HG также является фактором риска: примерно 28% женщин сообщают о HG в анамнезе у своих матерей и 19% сообщают, что их сестры имели аналогичные симптомы [26].Дополнительные факторы риска включают семейный или партнерский статус и возраст старше 30 лет. Курение сигарет может быть защитным [27].
Семейный анамнез HG также является фактором риска: примерно 28% женщин сообщают о HG в анамнезе у своих матерей и 19% сообщают, что их сестры имели аналогичные симптомы [26].Дополнительные факторы риска включают семейный или партнерский статус и возраст старше 30 лет. Курение сигарет может быть защитным [27].
Индекс массы тела матери оценивался как фактор риска ГГ с неоднозначными результатами. В исследовании Depue et al ожирение увеличивало риск ГГ на 50% [28]. Работа Cedergren et al. однако обнаружили, что низкий индекс массы тела (<20 кг/м2) был связан с 40% более высоким риском ХГ, а ожирение снижало риск госпитализации по поводу ХГ [29].Более недавнее исследование 33 647 женщин в Норвегии показало, что недостаточный или избыточный вес увеличивает риск ГГ, но только у некурящих [30]. Постулируется, что женщины с недостаточным весом и низкими индексами массы тела имеют низкий уровень эстрогена до беременности и, таким образом, могут иметь преувеличенный ответ в течение первого триместра, когда уровень эстрогена резко возрастает [31]. Напротив, у женщин с ожирением жировые отложения могут нейтрализовать плацентарные факторы, которые, как считается, способствуют патогенезу [29].
Напротив, у женщин с ожирением жировые отложения могут нейтрализовать плацентарные факторы, которые, как считается, способствуют патогенезу [29].
Что касается пола плода, то в нескольких исследованиях была обнаружена связь между ГГ и женским полом плода.Используя данные Шведского медицинского реестра рождений, Kallen et al. обнаружили, что HG был чрезмерно представлен в 3068 беременностях, когда ребенок был девочкой [32]. Точно так же в исследовании беременных женщин, госпитализированных с HG в первом триместре, вероятность рождения девочки была на 50% выше в случаях по сравнению со здоровыми беременными в контрольной группе (ОШ 1,5, 95% ДИ 1,4, 1,7) [33].
Патогенез
Метаболические и гормональные факторы
Хотя точный патогенез НВП и ГГ неизвестен, общепризнано, что рвота во время беременности является результатом различных метаболических и эндокринных факторов, многие из которых имеют плацентарное происхождение.Наиболее значимым фактором является хорионический гонадотропин человека (ХГЧ). Эта связь между ХГЧ и невирапином в значительной степени основана на временном соотношении между пиком невирапина и пиком продукции ХГЧ, которые происходят между 12 и 14 неделями беременности. Кроме того, тошнота и рвота часто усиливаются у беременных с состояниями, связанными с повышенным уровнем ХГЧ, такими как молярная беременность, многоплодная беременность и синдром Дауна [13]. Более высокие уровни ХГЧ в моче [34] и в сыворотке также были обнаружены у женщин с невирапином по сравнению с бессимптомными [35].Кроме того, исследование Goodwin et al. обнаружили, что концентрации ХГЧ положительно коррелируют с выраженностью тошноты и рвоты у женщин с ХГ [36].
Эта связь между ХГЧ и невирапином в значительной степени основана на временном соотношении между пиком невирапина и пиком продукции ХГЧ, которые происходят между 12 и 14 неделями беременности. Кроме того, тошнота и рвота часто усиливаются у беременных с состояниями, связанными с повышенным уровнем ХГЧ, такими как молярная беременность, многоплодная беременность и синдром Дауна [13]. Более высокие уровни ХГЧ в моче [34] и в сыворотке также были обнаружены у женщин с невирапином по сравнению с бессимптомными [35].Кроме того, исследование Goodwin et al. обнаружили, что концентрации ХГЧ положительно коррелируют с выраженностью тошноты и рвоты у женщин с ХГ [36].
Несмотря на множество исследований, связывающих уровень ХГЧ с невирапином и гормоном роста, другие не обнаружили связи между уровнем ХГЧ в сыворотке беременных женщин в течение первого триместра и частотой или интенсивностью тошноты и рвоты. В исследовании Soules et al. даже в подгруппе женщин с пузырным заносом, у которых уровни ХГЧ у женщин были в 5-10 раз выше, чем в контроле, корреляции обнаружено не было [37]. Кроме того, исследования показали, что высокие уровни ХГЧ связаны с задержкой роста плода и преждевременными родами [38], в то время как невирапин, по-видимому, защищает от преждевременных родов, что делает маловероятным то, что ХГЧ является единственным фактором патогенеза невирапина.
Кроме того, исследования показали, что высокие уровни ХГЧ связаны с задержкой роста плода и преждевременными родами [38], в то время как невирапин, по-видимому, защищает от преждевременных родов, что делает маловероятным то, что ХГЧ является единственным фактором патогенеза невирапина.
Предполагается, что различные биологические формы (то есть изоформы) ХГЧ могут объяснить вариабельность между уровнями ХГЧ и тошнотой и рвотой у здоровых и больных людей [39]. Каждая изоформа ХГЧ имеет уникальный период полувыведения и активность в отношении рецепторов лютеинизирующего гормона и тиреотропного гормона (ТТГ).Изоформы без карбоксиконцевой части имеют более короткий период полувыведения, но являются более сильными стимуляторами рецепторов лютеинизирующего гормона и ТТГ. Напротив, гипергликозилированный ХГЧ имеет более длительный период полувыведения и большую продолжительность действия [40]. Эти различные изоформы ХГЧ, вероятно, являются результатом генетических факторов или долгосрочных изменений окружающей среды, которые, таким образом, могут объяснить различия в заболеваемости ХГ, обнаруженные в разных популяциях. Помимо изменчивости изоформ, мутации рецептора ХГЧ также могут объяснить некоторую вариабельность взаимоотношений между невирапином и ХГЧ [39].
Помимо изменчивости изоформ, мутации рецептора ХГЧ также могут объяснить некоторую вариабельность взаимоотношений между невирапином и ХГЧ [39].
Гормоны яичников, эстроген и прогестерон, также участвуют в патогенезе невирапина и гипергидроза. Известно, что некоторые женщины испытывают тошноту при приеме оральных контрацептивов. Кроме того, состояния с высокой концентрацией эстрогена, такие как низкий паритет и высокий индекс массы тела матери, были связаны с более высокой частотой ГГ [28]. Считается, что эстроген вносит свой вклад в HG, стимулируя выработку оксида азота с помощью синтетазы азотоксидазы, которая, в свою очередь, расслабляет гладкие мышцы, замедляя время желудочно-кишечного транзита и опорожнение желудка.
Ярнфельт и др. сообщили о значительной связи между рвотой беременных и непереносимостью пероральных контрацептивов в анамнезе [40]. Используя более количественный подход, Depue et al. обнаружили, что средние уровни общего эстрадиола на 26% выше, а средние уровни способности связывания половых гормонов и глобулинов на 37% выше у пациентов с HG, чем в контрольной группе после поправки на гестационный возраст. 28]. Однако важно отметить, что, как и взаимосвязь между ХГЧ и невирапином, взаимосвязь между уровнями эстрогена и невирапином была противоречивой в разных исследованиях [35].Обзор 17 исследований показал положительную связь между невирапином и эстрогеном только в 5 исследованиях [41]. Кроме того, пик уровня эстрогена приходится на третий триместр беременности, в то время как ГГ имеет тенденцию к улучшению на поздних сроках беременности [8].
28]. Однако важно отметить, что, как и взаимосвязь между ХГЧ и невирапином, взаимосвязь между уровнями эстрогена и невирапином была противоречивой в разных исследованиях [35].Обзор 17 исследований показал положительную связь между невирапином и эстрогеном только в 5 исследованиях [41]. Кроме того, пик уровня эстрогена приходится на третий триместр беременности, в то время как ГГ имеет тенденцию к улучшению на поздних сроках беременности [8].
Прогестерон в сочетании с эстрогеном также может играть роль в NVP. Прогестерон снижает сократимость гладкой мускулатуры и может изменить опорожнение желудка и привести к усилению тошноты и рвоты. Используя эластогастографию после стандартного приема пищи, Walsh et al. показали, что такое же медленноволновое нарушение желудочного ритма, обнаруженное у женщин с невирапином, может быть вызвано у небеременных женщин монотерапией прогестероном или в комбинации с эстрадиолом в дозах, которые воспроизводят уровни при беременности [42].Другие исследования, однако, не обнаружили существенной разницы между уровнями прогестерона у женщин с невирапином или без него [28].
Роль плацентарного простагландина E2 (PGE2) также оценивалась в патогенезе NVP из-за его влияния на гладкую мускулатуру желудка [43]. ХГЧ стимулирует плацентарный PGE2 и, как и ХГЧ, достигает пика между 9 и 12 неделями беременности. Норт и др. определили количество PGE2 в материнской сыворотке и обнаружили, что уровни были выше во время периодов тошноты и рвоты у 18 женщин на ранних сроках беременности по сравнению с бессимптомными периодами.Они также оценили уровни интерлейкина-1 бета и фактора некроза опухоли альфа у матери и обнаружили, что они были одинаковыми в течение симптоматического и бессимптомного периодов [44].
В связи с его ролью в вызванных химиотерапией тошноте и рвоте, серотонин также предположительно способствует развитию невирапина. Исследование Borgeat et al. однако не выявили различий в уровне серотонина среди беременных женщин с ХГ, бессимптомных беременных женщин и небеременных женщин [45]. Кроме того, рандомизированное контролируемое исследование, сравнивающее антагонист серотониновых 5-HT3-рецепторов, онданстерон, с прометазином, не выявило существенной разницы в контроле симптомов [46].
Из-за перекрестной реактивности между ХГЧ и рецептором тиреостимулирующего гормона (ТТГ) дисфункция щитовидной железы также изучалась как возможный механизм развития невирапина и ГГ. На самом деле, аномальные результаты функции щитовидной железы обнаруживаются у двух третей женщин с ГГ [36]. Этот «биохимический тиреотоксикоз» характеризуется подавлением ТТГ и слегка повышенным уровнем FT4. Несмотря на эти лабораторные отклонения, женщины с HG, как правило, находятся в эутиреоидном состоянии без предшествующих заболеваний щитовидной железы, отсутствия зоба и отрицательных антитиреоидных антител [47].Кроме того, исследования не выявили взаимосвязи между дисфункцией щитовидной железы и тяжестью симптомов [48], и почти у всех женщин с ХГ уровень ТТГ в норме к 20 нед беременности без какого-либо вмешательства [49].
Недавно была предложена связь между гормоном лептином и HG. Было обнаружено, что повышенный уровень лептина в сыворотке во время беременности, возможно, в результате увеличения общей жировой массы и продукции плаценты, значительно выше у пациенток с HG по сравнению со здоровыми беременными контрольной группой [50, 51]. Лептин может способствовать ГГ за счет увеличения секреции ХГЧ за счет паракринного действия плаценты или за счет снижения аппетита и усиления тошноты и рвоты. Примечательно, однако, что другие проспективные когортные исследования не обнаружили аналогичной статистически значимой разницы в уровнях лептина в сыворотке при HG между пациентами и контрольной группой [52, 53].
Лептин может способствовать ГГ за счет увеличения секреции ХГЧ за счет паракринного действия плаценты или за счет снижения аппетита и усиления тошноты и рвоты. Примечательно, однако, что другие проспективные когортные исследования не обнаружили аналогичной статистически значимой разницы в уровнях лептина в сыворотке при HG между пациентами и контрольной группой [52, 53].
Также было высказано предположение, что у женщин с HG возникает нарушение регуляции иммунной системы. В сыворотке крови матери были обнаружены повышенные концентрации свободной ДНК клеток плода [54], вызывающие гиперактивный материнский иммунный ответ и повреждение трофобласта.Кроме того, нормальный сдвиг во время беременности, при котором типы Т-хелперов переходят в Т-хелперы типа 1, более преувеличен у женщин с ХГ [55]. Это, в свою очередь, приводит к повышенному высвобождению интерлейкина-4, а также фактора некроза опухоли-альфа, оба из которых были связаны с HG [56]. Также было обнаружено, что аденозин повышен при HG, и его роль заключается в ослаблении TNF-альфа [57]. В проспективном исследовании [58] также было обнаружено, что уровни интерлейкина-6 повышаются при HG, а также повышаются уровни иммуноглобулина G (IgG), IgM, уровни комплемента и количество лимфоцитов [59].Однако точно определить роль этих иммунологических факторов нельзя, так как при голодании иммунная система обычно угнетается, а не активируется; таким образом, возможно, усиление иммунных факторов, наблюдаемое при HG, может быть попыткой ограничить прогрессирование HG [8].
В проспективном исследовании [58] также было обнаружено, что уровни интерлейкина-6 повышаются при HG, а также повышаются уровни иммуноглобулина G (IgG), IgM, уровни комплемента и количество лимфоцитов [59].Однако точно определить роль этих иммунологических факторов нельзя, так как при голодании иммунная система обычно угнетается, а не активируется; таким образом, возможно, усиление иммунных факторов, наблюдаемое при HG, может быть попыткой ограничить прогрессирование HG [8].
Другие гормоны, в том числе тиреотропный гормон, гормон роста, пролактин, адренокортико-стимулирующий гормон, кортизол, лютеинизирующий гормон и фолликулостимулирующий гормон, также оценивались и, как считается, не вносят вклад в патогенез невирапин [60].
Helicobacter pylori
Повышенная частота инфицирования Helicobacter pylori (H. pylori) наблюдалась у женщин с ГГ, и в настоящее время считается, что она играет роль в ее патогенезе. Фриго и др. обнаружили, что 90,5% женщин с HG были H. plyori IgG положительными по сравнению с 46,5% в контрольной группе [61]. Багис и др. использовали золотой стандарт тестирования, гистологическое исследование биопсии слизистой оболочки, и обнаружили, что 95% пациентов с HG дали положительный результат на H.pylori по сравнению с 50% в контрольной группе. Они также обнаружили более высокую плотность H. pylori в антральном отделе и теле желудка у пациентов с HG, что позволяет предположить возможную связь между плотностью H. pylori и тяжестью симптомов [62].
plyori IgG положительными по сравнению с 46,5% в контрольной группе [61]. Багис и др. использовали золотой стандарт тестирования, гистологическое исследование биопсии слизистой оболочки, и обнаружили, что 95% пациентов с HG дали положительный результат на H.pylori по сравнению с 50% в контрольной группе. Они также обнаружили более высокую плотность H. pylori в антральном отделе и теле желудка у пациентов с HG, что позволяет предположить возможную связь между плотностью H. pylori и тяжестью симптомов [62].
Систематический обзор 2007 г., в котором оценивались 14 исследований типа «случай-контроль» с 1966 по 2007 г., выявил значительную связь между материнской инфекцией H.pylori и HG в 10 исследованиях. Отношение шансов в исследованиях варьировалось от 0.от 55 до 109,33 [63]. Аналогичным образом обновленный систематический обзор и метаанализ 25 исследований 2009 г. показали, что объединенное отношение шансов составляет 3,32 (95% доверительный интервал: 2,25–4,90) для инфекции H. pylori у женщин с HG [64]. Примечательно, что в обоих обзорах была обнаружена высокая гетерогенность исследований.
pylori у женщин с HG [64]. Примечательно, что в обоих обзорах была обнаружена высокая гетерогенность исследований.
Инфицирование H. pylori во время беременности может произойти из-за вызванных стероидными гормонами изменений pH желудка [65] и/или повышенной восприимчивости из-за изменений гуморального и клеточно-опосредованного иммунитета [66].Однако нет четких доказательств того, что беременность предрасполагает к инфекции de novo H. pylori . Напротив, было высказано предположение, что H. pylori может усугубить вызванные гормонами изменения нервной и электрической функции желудка и, таким образом, увеличить риск для инфицированных женщин оказаться в более тяжелой форме тошноты и рвоты. рвота [67].
Хотя связь между H. pylori и HG интригует, важно отметить, что инфекция не обязательно коррелирует с симптомами.На самом деле у большинства инфицированных женщин заболевание протекает бессимптомно [8]. В исследовании Weyermann et al. 23% из 898 родильниц дали положительный результат на H. pylori при дыхательном тесте с 13C-мочевиной; однако положительный результат не коррелировал с симптомами тошноты, рвоты или рефлюкса во время беременности [68]. Точно так же Wu et al. обнаружили, что 69% беременных женщин являются сероположительными в отношении H. pylori по сравнению с 50% в общей популяции, однако не обнаружили никакой корреляции между статусом антител и желудочно-кишечными симптомами [69].
23% из 898 родильниц дали положительный результат на H. pylori при дыхательном тесте с 13C-мочевиной; однако положительный результат не коррелировал с симптомами тошноты, рвоты или рефлюкса во время беременности [68]. Точно так же Wu et al. обнаружили, что 69% беременных женщин являются сероположительными в отношении H. pylori по сравнению с 50% в общей популяции, однако не обнаружили никакой корреляции между статусом антител и желудочно-кишечными симптомами [69].
Почему H. pylori нельзя точно связать с невирапином, а HG связывают с несколькими факторами. Во-первых, в большинстве исследований для оценки наличия инфекции использовалось тестирование на антитела. Однако серологическое тестирование на H. pylori не может отличить активную инфекцию от перенесенной инфекции [70], а активная и перенесенная инфекция могут по-разному влиять на симптомы. Во-вторых, в большинстве исследований не оценивался и/или не учитывался штамм H. pylori . Ассоциированный с цитотоксином белок гена A (CagA) является маркером учащения пептических язв и связан с более агрессивным штаммом H pylori [71].Только одно исследование, включенное в метаанализ 2009 г., оценивало патогенность CagA. В этом исследовании, проведенном Xia et al., положительная реакция на CagA была более распространена у пациентов с HG [72].
Ассоциированный с цитотоксином белок гена A (CagA) является маркером учащения пептических язв и связан с более агрессивным штаммом H pylori [71].Только одно исследование, включенное в метаанализ 2009 г., оценивало патогенность CagA. В этом исследовании, проведенном Xia et al., положительная реакция на CagA была более распространена у пациентов с HG [72].
Лечение приводит к эрадикации H. pylori у большинства пациенток, однако в настоящее время нет рекомендаций по оценке или лечению H. pylori во время беременности, поскольку последующее облегчение симптомов HG широко не изучалось. Сообщения о клинических случаях и серии случаев позволяют предположить, что лечение и эрадикация 90–105 H.pylori может уменьшить тошноту и рвоту во время беременности, и его следует рассматривать у пациенток с трудноизлечимыми симптомами [73]. Однако необходимы более масштабные исследования, чтобы определить, следует ли и когда начинать лечение во время беременности, учитывая опасения по поводу безопасности лекарств. В настоящее время специалисты рекомендуют после завершения беременности и лактации проводить тройную терапию в течение двух недель [74].
В настоящее время специалисты рекомендуют после завершения беременности и лактации проводить тройную терапию в течение двух недель [74].
Нарушение моторики желудочно-кишечного тракта
Изменения давления в состоянии покоя нижнего пищеводного сфинктера (НПС) и перистальтики пищевода связаны с невирапином.Хотя эти изменения чаще связаны с изжогой во время беременности, гастроэзофагеальная рефлюксная болезнь (ГЭРБ) может вызывать атипичные симптомы, такие как тошнота [75], и способствовать развитию невирапинов. Эстроген и прогестерон являются вероятными медиаторами нарушения моторики пищевода при беременности, при этом эстроген служит праймером, а прогестерон вызывает релаксацию НПС [76].
Изменения желудочной ритмической активности могут способствовать НВП. Нормальная миоэлектрическая активность желудка приводит к медленному распространению волны от проксимального отдела тела к дистальному отделу антрального отдела со скоростью 3 цикла в минуту (имп/мин).Нарушение ритма в виде увеличения или уменьшения распространения медленных волн связано с тошнотой [74]. Используя эластогастрографию (EGG), Koch et al. продемонстрировали, что лица с нормальной медленноволновой активностью реже жаловались на тошноту во время беременности [77]. Напротив, люди с более высокими или более низкими показателями чаще жаловались на тошноту. Точно так же Riezzo et al. обнаружили, что беременные женщины без симптомов тошноты и рвоты на момент записи ЭГГ имеют нормальную миоэлектрическую активность 3 имп/мин.Они также обнаружили, что беременные женщины с невирапином имели более нестабильную активность EGG по сравнению с женщинами после добровольных абортов и небеременными женщинами из контрольной группы. Они предположили, что это может быть связано с восстановлением нормальной картины медленных волн желудка после аборта после нормализации уровней эстрадиола и прогестерона [78].
Используя эластогастрографию (EGG), Koch et al. продемонстрировали, что лица с нормальной медленноволновой активностью реже жаловались на тошноту во время беременности [77]. Напротив, люди с более высокими или более низкими показателями чаще жаловались на тошноту. Точно так же Riezzo et al. обнаружили, что беременные женщины без симптомов тошноты и рвоты на момент записи ЭГГ имеют нормальную миоэлектрическую активность 3 имп/мин.Они также обнаружили, что беременные женщины с невирапином имели более нестабильную активность EGG по сравнению с женщинами после добровольных абортов и небеременными женщинами из контрольной группы. Они предположили, что это может быть связано с восстановлением нормальной картины медленных волн желудка после аборта после нормализации уровней эстрадиола и прогестерона [78].
Примечательно, однако, что многие исследования не обнаружили различий в перистальтике желудка между беременными и небеременными женщинами. С помощью сцинтографии желудка не было обнаружено существенных различий в скорости опорожнения жидкости у беременных женщин до добровольного аборта, через 6 недель после аборта и у небеременных женщин контрольной группы [79]. Используя методы разбавления красителя феноловым красным, Davison et al. обнаружили задержку опорожнения желудка во время родов, но не в третьем триместре по сравнению с небеременными контрольными женщинами [80]. Точно так же исследования с использованием парацетамола не показали задержки опорожнения желудка в первом, втором или третьем триместре [81].
Используя методы разбавления красителя феноловым красным, Davison et al. обнаружили задержку опорожнения желудка во время родов, но не в третьем триместре по сравнению с небеременными контрольными женщинами [80]. Точно так же исследования с использованием парацетамола не показали задержки опорожнения желудка в первом, втором или третьем триместре [81].
Изменения моторики желудка при беременности объясняются высоким уровнем прогестерона. Кроме того, на поздних сроках беременности сдавление увеличенной маткой может способствовать симптомам.
Состав пищи также может играть патогенную роль в NVP.Джеднак и др. продемонстрировали, что прием пищи с преобладанием белка был связан с уменьшением симптомов и коррекцией медленноволновой аритмии. Прием пищи с преобладанием углеводов или жиров не влиял на симптомы или медленноволновую аритмию [82].
Наконец, время прохождения по тонкой кишке было оценено в отношении патогенеза NVP. Используя водородный дыхательный тест с лактулозой, косвенный показатель времени прохождения по тонкой кишке, Lawson et al. обнаружили, что время транзита удлиняется во втором и третьем триместре по сравнению с первым триместром, причем самые длинные времена были обнаружены, когда уровни прогестерона были самыми высокими [83].Уолд и др. использовали аналогичные методы и обнаружили, что время транзита увеличивается в третьем триместре, когда уровни прогестерона и эстрогена были высокими по сравнению с послеродовым периодом [84]. Однако в обоих этих исследованиях задержка кишечного транзита не коррелировала с невирапином.
обнаружили, что время транзита удлиняется во втором и третьем триместре по сравнению с первым триместром, причем самые длинные времена были обнаружены, когда уровни прогестерона были самыми высокими [83].Уолд и др. использовали аналогичные методы и обнаружили, что время транзита увеличивается в третьем триместре, когда уровни прогестерона и эстрогена были высокими по сравнению с послеродовым периодом [84]. Однако в обоих этих исследованиях задержка кишечного транзита не коррелировала с невирапином.
Психосоциальные факторы
Ранние исследования предполагали, что НВП может быть психосоматическим заболеванием, при котором рвота представляет собой интрапсихический конфликт. Некоторые предполагают, что NVP является проявлением подсознательной попытки беременной женщины отказаться от нежелательной беременности [85], поскольку исследования показали, что у женщин с NVP в первом триместре чаще бывают незапланированные или нежелательные беременности [86].
ГГ также ассоциируется с психологическими расстройствами, а именно невротическими наклонностями, истерией, неприятием женственности, неприятием беременности, а также с депрессией и психологическим стрессом, связанным с бедностью и семейными конфликтами [8]. Однако недавние исследования не выявили определенных психогенных причин ГГ [87, 88]. Некоторые, следовательно, утверждают, что социокультурные факторы, а не научные данные, привели к тому, что HG маркируется как психологически обусловленное состояние, и что более вероятно, что психологические нарушения, такие как депрессия, являются результатом, а не причиной HG [89].
Однако недавние исследования не выявили определенных психогенных причин ГГ [87, 88]. Некоторые, следовательно, утверждают, что социокультурные факторы, а не научные данные, привели к тому, что HG маркируется как психологически обусловленное состояние, и что более вероятно, что психологические нарушения, такие как депрессия, являются результатом, а не причиной HG [89].
Таким образом, хотя NVP и HG, вероятно, не являются результатом конверсионного расстройства или другого психологического расстройства, общепризнано, что у пострадавших женщин возникают психологические реакции, которые переплетаются с их физическими симптомами и, возможно, усугубляют их.
Диагностика и клинические признаки
Анамнез и медицинский осмотр
Несмотря на популярное использование термина «утренняя тошнота», невирапин сохраняется в течение дня у большинства больных женщин и, как было установлено, ограничивается утром менее чем у 2% женщин [90].Он часто начинается в течение нескольких недель после отсутствия менструации и поэтому в большинстве культур карикатурно изображается как начальный признак беременности. Симптомы обычно достигают пика между 10 и 16 неделями беременности и обычно исчезают после 20 недель. Однако до 10% женщин продолжают иметь симптомы после 22 недель [90].
Симптомы обычно достигают пика между 10 и 16 неделями беременности и обычно исчезают после 20 недель. Однако до 10% женщин продолжают иметь симптомы после 22 недель [90].
В то время как обезвоживание и ортостаз могут возникать у женщин с HG, у большинства женщин с NVP показатели жизненно важных функций в норме, а физикальный осмотр является благоприятным. Однако следует провести тщательное обследование брюшной полости, чтобы исключить перитонит и другие внутрибрюшные причины тошноты и рвоты.
Дифференциальный диагноз
Учитывая высокую распространенность невирапина, тошнота и рвота в первом триместре обычно связаны с невирапином. Однако при наличии изменений в работе кишечника, боли в животе и рвоте желчью следует провести соответствующие исследования для исключения других причин. Дифференциальный диагноз невирапина включает гастроэзофагеальную рефлюксную болезнь, язвенную болезнь, непроходимость тонкой кишки, острый холецистит, желчнокаменную болезнь, панкреатит, а также аппендицит, гастроэнтерит, нефролитиаз, пиелонефрит и гепатит [74]
Диагностические и лабораторные исследования
Для диагностики невирапина не рекомендуются никакие специальные лабораторные исследования, кроме теста на беременность. Однако другие тесты могут быть полезны для исключения других причин тошноты и рвоты. Лейкоцитоз не должен наблюдаться при невирапине и может указывать на инфекционную или воспалительную причину, такую как холецистит, инфекция мочевыводящих путей и панкреатит. Повышение уровня аминотрансфераз может свидетельствовать о хроническом гепатите. Аномальный ТТГ может указывать на гипотиреоз или гипертиреоз, оба из которых могут вызывать тошноту и рвоту. Повышение уровня глюкозы в сыворотке может указывать на диабет и может вызывать тошноту и рвоту за счет снижения сократительной способности антрального отдела и ускорения желудочной аритмии [91].
Однако другие тесты могут быть полезны для исключения других причин тошноты и рвоты. Лейкоцитоз не должен наблюдаться при невирапине и может указывать на инфекционную или воспалительную причину, такую как холецистит, инфекция мочевыводящих путей и панкреатит. Повышение уровня аминотрансфераз может свидетельствовать о хроническом гепатите. Аномальный ТТГ может указывать на гипотиреоз или гипертиреоз, оба из которых могут вызывать тошноту и рвоту. Повышение уровня глюкозы в сыворотке может указывать на диабет и может вызывать тошноту и рвоту за счет снижения сократительной способности антрального отдела и ускорения желудочной аритмии [91].
Рентгенография обычно не требуется для диагностики невирапина. УЗИ органов малого таза можно использовать для документирования беременности и оценки состояний, повышающих риск невирапина, таких как многоплодная беременность. Рентген брюшной полости, как правило, бесполезен и, хотя представляет небольшой риск для плода, все еще относительно противоречив в течение первого триместра.
Верхнюю эндоскопию можно безопасно проводить во время беременности и исключить гастрит и ЯБ как причины тошноты и рвоты во время беременности.В одном крупном центре тошнота и рвота были вторым наиболее частым показанием к эндоскопии верхних отделов во время беременности после кровотечения из верхних отделов желудочно-кишечного тракта [92].
Исход
Большинство исследований показали, что невирапин связан с благоприятным исходом для плода. Метаанализ 11 исследований Weigel et al. обнаружили сильную значимую связь между тошнотой и рвотой во время беременности и снижением риска выкидыша (общее отношение шансов = 0,36, 95% ДИ от 0,32 до 0,42) и отсутствие последовательной связи с перинатальной смертностью [93].Кроме того, было обнаружено, что женщины без NVP рожают раньше, чем женщины с NVP [94].
Однако в некоторых исследованиях сообщалось о неблагоприятных исходах, особенно когда невирапин считался тяжелым. Деушар и др. обнаружили повышенный риск задержки внутриутробного развития у женщин с тяжелым НВП, но не смогли объяснить потенциальное влияние противорвотных препаратов на рост плода [95]. Точно так же Zhou et al. обнаружили повышенный риск низкой массы тела при рождении у женщин с тяжелой формой НВП, вероятно, из-за пагубного влияния тошноты и рвоты на питание матери [96].
Точно так же Zhou et al. обнаружили повышенный риск низкой массы тела при рождении у женщин с тяжелой формой НВП, вероятно, из-за пагубного влияния тошноты и рвоты на питание матери [96].
В проспективном исследовании 16 398 женщин не было обнаружено различий по врожденным аномалиям между женщинами с невирапином и без него [97]. Кроме того, ретроспективное исследование показало более низкий риск врожденных пороков сердца у детей, рожденных от женщин с ранним началом приема невирапина, требующих применения противорвотных средств, по сравнению с женщинами без тошноты [98].
Не совсем ясно, как NVP защищает развивающийся плод, однако было описано несколько теорий. Некоторые утверждают, что тошнота и рвота позволяют беременной женщине избегать или исключать продукты, которые могут быть тератогенными или вызывать аборт.Это может объяснить тесную временную связь между развитием отвращения к еде во время беременности и появлением тошноты [99]. NVP также может снизить потребление энергии и уровень анаболических гормонов, инсулина и фактора роста инсулина, что приводит к шунтированию дефицитных питательных веществ к плаценте и плоду [100].
Несмотря на благоприятное воздействие невирапина на плод, психосоциальные осложнения у беременных с невирапином значительны и, возможно, недооцениваются. В исследовании Smith et al. из 593 австралийских женщин с невирапином большинство сообщили, что их симптомы оказали серьезное негативное влияние на работу, домашние обязанности и воспитание детей, при этом 96% женщин сообщили о легком или умеренном дистрессе из-за тошноты, а 28% сообщили о дистрессе от умеренного до тяжелого [101].Точно так же исследование Mazzotta et al. канадских женщин обнаружили, что более сильная тошнота и рвота связаны с более частым чувством депрессии, рассмотрением вопроса о прерывании беременности, неблагоприятным воздействием на отношения женщин с их партнерами или их повседневную жизнь, а также с предполагаемой вероятностью того, что NVP нанесет вред их ребенку . Примечательно, что женщины с легкими симптомами также сообщали о тех же психосоциальных проблемах, что позволяет предположить, что тяжесть тошноты или рвоты неадекватно отражает дистресс, вызванный невирапином [2].
O’Brien и Naber также выявили значительную психосоциальную заболеваемость у женщин, страдающих невирапином. Они обнаружили, что пострадавшие женщины сообщали о снижении социальных обязательств и ухудшении отношений с супругами и детьми. Женщины с тяжелыми симптомами также сообщали о частой плаксивости, раздражительности, усилении нарушений сна и снижении настроения [102]. Используя краткую форму 36, Attard et al. обнаружили, что женщины с НВП имели более низкие показатели физического функционирования, физической роли, телесной боли, жизнеспособности, социального функционирования и эмоциональной роли в опросе, оценивающем качество жизни, по сравнению со здоровыми беременными контрольной группой на ранних сроках беременности и женщинами с хронической депрессией.Показатели психического здоровья женщин с НВП были аналогичны показателям женщин с депрессией [103].
Помимо того, что невирапин вызывает психосоциальную заболеваемость, он также создает значительное финансовое бремя. В 2002 г. стоимость тяжелого невирапина оценивалась приблизительно в 130 миллионов долларов, исходя из больничных расходов, связанных в среднем с 39 000 госпитализаций. Эта цифра, вероятно, сильно занижена, поскольку она не включает потерю производительности дома, оплату услуг врача или стоимость лечения [104].
В 2002 г. стоимость тяжелого невирапина оценивалась приблизительно в 130 миллионов долларов, исходя из больничных расходов, связанных в среднем с 39 000 госпитализаций. Эта цифра, вероятно, сильно занижена, поскольку она не включает потерю производительности дома, оплату услуг врача или стоимость лечения [104].
Подсчитано, что каждая работающая женщина с невирапином теряет 206 рабочих часов [2] и что на невирапин приходится 28% всех отпусков по болезни во время беременности до 28-й недели [19]. Кроме того, работа Vallacott et al. показывает, что 50% пострадавших женщин считают, что эффективность их работы значительно снижена [105].
HYPEREMESIS GRAVDIARUM
Гиперемезис беременных (HG) — это состояние сильной тошноты и рвоты во время беременности, приводящее к водно-электролитному и кислотно-щелочному дисбалансу, дефициту питательных веществ и потере веса [8].Некоторые определяют его как возникновение более трех эпизодов рвоты в день, сопровождающихся кетонурией и потерей веса более 3 кг или 5% массы тела [63]. ГГ является наиболее частой причиной госпитализации на ранних сроках беременности и уступает только преждевременным родам на протяжении всей беременности [106]. В Соединенных Штатах более 36 000 женщин ежегодно госпитализируются по поводу ХГ, и стоимость лечения оценивается более чем в 250 миллионов долларов в год только на госпитализацию [107].В отличие от NVP, который связан с благоприятными исходами для плода, HG представляет значительный риск для здоровья матери и плода.
ГГ является наиболее частой причиной госпитализации на ранних сроках беременности и уступает только преждевременным родам на протяжении всей беременности [106]. В Соединенных Штатах более 36 000 женщин ежегодно госпитализируются по поводу ХГ, и стоимость лечения оценивается более чем в 250 миллионов долларов в год только на госпитализацию [107].В отличие от NVP, который связан с благоприятными исходами для плода, HG представляет значительный риск для здоровья матери и плода.
Диагностика и клинические признаки
ГГ проявляется в первом триместре беременности, обычно начиная с 4–5-й недели беременности. В дополнение к сильной тошноте и рвоте у 60% женщин с ГГ также наблюдается избыточное слюноотделение или слюнотечение [108]. Пациенты также могут жаловаться на симптомы гастроэзофагеального рефлюкса, такие как дискомфорт за грудиной и изжога. Уникальная количественная оценка рвоты и тошноты (PUQE) для беременных, которая рассчитывается с использованием количества часов тошноты в день, количества эпизодов рвоты в день и количества эпизодов позывов на рвоту в день, может использоваться для отслеживания тяжести симптомов. [109].
[109].
Пациенты могут иметь признаки обезвоживания, такие как сухость слизистых оболочек, тахикардия, плохой тургор кожи и постуральная гипотензия. Тяжело пораженные пациенты могут также иметь мышечную атрофию и слабость и/или изменения психического статуса.
Лабораторные нарушения у женщин с HG могут включать повышение азота мочевины в сыворотке крови, креатинина и гематокрита, а также кетонурию и увеличение удельного веса мочи. Кроме того, могут быть обнаружены электролитные нарушения, подтверждающие диагноз либо гипохлоремического метаболического алкалоза, либо метаболического ацидоза с выраженным сокращением объема [39].Уровни преальбумина (транстиретина в плазме) могут быть низкими, отражая плохой статус белкового питания у матери и, возможно, предсказывая более низкую массу тела плода при рождении [110]. Также возможен дефицит витаминов и минералов, таких как витамин B1 (тиамин), железо, кальций и фолиевая кислота [74].
Функциональные пробы печени могут отклоняться от нормы у 50% госпитализированных пациентов с ХГ [111]. Могут наблюдаться умеренная гипербилирубинемия (билирубин < 4 мг на децилитр) и/или повышение уровня щелочной фосфатазы вдвое по сравнению с верхней границей нормы [112].Умеренный трансаминит является наиболее частым нарушением функции печени, при котором уровни аланинаминотрансферазы (АЛТ) обычно превышают уровни аспартатаминотрансферазы (АСТ). Повышение уровня трансаминаз обычно в два-три раза превышает верхнюю границу нормы; однако сообщалось об уровнях выше 1000 ЕД/мл [113]. Аномальные печеночные пробы исчезают сразу же после прекращения рвоты.
Могут наблюдаться умеренная гипербилирубинемия (билирубин < 4 мг на децилитр) и/или повышение уровня щелочной фосфатазы вдвое по сравнению с верхней границей нормы [112].Умеренный трансаминит является наиболее частым нарушением функции печени, при котором уровни аланинаминотрансферазы (АЛТ) обычно превышают уровни аспартатаминотрансферазы (АСТ). Повышение уровня трансаминаз обычно в два-три раза превышает верхнюю границу нормы; однако сообщалось об уровнях выше 1000 ЕД/мл [113]. Аномальные печеночные пробы исчезают сразу же после прекращения рвоты.
Повышение уровня амилазы и липазы в сыворотке наблюдается у 10–15% женщин [39]. Одно исследование выявило повышенный уровень амилазы у 24% пациентов с ХГ [114].Считается, что это связано с избыточной выработкой амилазы слюнными железами, а не с секрецией поджелудочной железы, и является результатом, а не причиной ГГ [8].
Уровни тиреостимулирующего гормона могут быть низкими при ХГ из-за перекрестной реакции между альфа-субъединицей ХГЧ и рецептором ТТГ. В большинстве случаев этот биохимический тиреотоксикоз не имеет клинического значения, так как пациенты находятся в эутиреоидном состоянии. Уровень гормонов щитовидной железы обычно нормализуется без лечения после родов.
В большинстве случаев этот биохимический тиреотоксикоз не имеет клинического значения, так как пациенты находятся в эутиреоидном состоянии. Уровень гормонов щитовидной железы обычно нормализуется без лечения после родов.
HG — это клинический диагноз, основанный на симптомах и исключении других состояний.Как и в случае с невирапином, для диагностики ГГ не требуется специального тестирования; тем не менее, УЗИ брюшной полости и таза может быть полезным для исключения других причин, таких как заболевание желчного пузыря, пузырный занос, а также для оценки многоплодной беременности. Дифференциальный диагноз включает невирапин, острый тиреоидит, расстройства пищевого поведения, заболевания желчевыводящих путей, вирусный гепатит и гастроэзофагеальную рефлюксную болезнь.
Исход
В отличие от NVP, HG связан с неблагоприятными исходами как для матери, так и для плода. В исследовании более 150 000 одноплодных беременностей младенцы, рожденные женщинами с гиперемезисом и низкой прибавкой массы тела при беременности (<7 кг), с большей вероятностью имели низкую массу тела при рождении, маловаты для гестационного возраста, родились до 37 недель беременности и имели мин. Оценка по шкале Апгар < 7 [5].
Оценка по шкале Апгар < 7 [5].
Общие материнские осложнения включают потерю веса, обезвоживание, дефицит питательных микроэлементов и мышечную слабость. Более тяжелые, хотя и редкие, осложнения включают разрывы Мэллори-Вейса, разрыв пищевода, энцефалопатию Вернике с корсаковским психозом или без него, центральный мостовой миелинолиз из-за быстрой коррекции тяжелой гипонатриемии, кровоизлияние в сетчатку и спонтанный пневмомедиастинум [47]. Также сообщалось о вазоспазме церебральных артерий из-за повышенной симпатической активности [115].
HG способствует возникновению многих психологических проблем и может привести к прерыванию нежелательной беременности и снижению вероятности попытки повторной беременности [116]. Пуршариф и др. обнаружили, что у 15% из 808 женщин с HG было по крайней мере одно прерывание беременности из-за болезни. Интересно, что у тех женщин, которые прервали беременность, не было более тяжелого заболевания, чем у женщин с ГГ, которые сохранили беременность, но в два раза чаще считали, что их врач безразличен или не обратил внимания на тяжесть их заболевания [117].
Долгосрочные последствия HG для матерей неизвестны. Несколько исследований показывают повышенный риск рака молочной железы [118]. Имеются также сообщения о повышенной частоте депрессии, посттравматического стрессового расстройства и различных неврологических расстройств [39].
Некоторые исследования не выявили повышенного риска неблагоприятных исходов для плода у женщин с ГГ. Башири и соавт., например, сообщили о более низкой частоте спонтанных ранних потерь беременности у женщин с ГГ по сравнению с общей популяцией и не обнаружили различий в перинатальных исходах [6].Однако в других исследованиях была обнаружена связь между ГГ и задержкой роста плода, преэклампсией и малым весом для гестационного возраста [119]. В ретроспективном исследовании 3068 женщин ГГ была связана с более ранними родами и меньшей массой тела при рождении. Эти исходы были наиболее вероятны у женщин, которые потеряли более 5% массы тела до беременности [120]. Точно так же Dodds et al. обнаружили более высокие показатели низкой массы тела при рождении, преждевременных родов, гибели плода у женщин с ХГ, которые в целом набрали менее 7 кг во время беременности [5]. Многократные госпитализации по поводу ХГ, по-видимому, являются еще одним фактором риска снижения массы тела новорожденных при рождении [108].
Многократные госпитализации по поводу ХГ, по-видимому, являются еще одним фактором риска снижения массы тела новорожденных при рождении [108].
Различные врожденные пороки развития чаще наблюдаются у женщин с ХГ [32]. К ним относятся синдром Дауна, дисплазия тазобедренного сустава, неопущение яичек, пороки развития скелета, дефекты центральной нервной системы и аномалии кожи. Сообщалось о коагулопатии плода и хондродисплазии из-за дефицита витамина К [121] с внутричерепным кровоизлиянием плода в третьем триместре [122].Некоторые виды рака у детей, такие как рак яичек или лейкемия, также были связаны с ГГ у матери, однако данные противоречивы [39].
ЛЕЧЕНИЕ
Целью лечения является облегчение симптомов при минимизации риска для матери и плода. Для достижения этого обычно необходим мультимодальный подход, адаптированный к каждому человеку. Методы лечения варьируются от простых диетических модификаций до медикаментозной терапии и полного родительского питания. Тяжесть симптомов и потеря веса матери помогают определить агрессивность лечения. PUQEscore и опросник по влиянию гиперемезиса на симптомы (HIS) можно использовать для оценки тяжести симптомов. Обновленная шкала PUQE оценивает симптомы в течение 24 часов [123], в то время как HIS учитывает психосоциальные факторы в дополнение к физическим симптомам [124].
PUQEscore и опросник по влиянию гиперемезиса на симптомы (HIS) можно использовать для оценки тяжести симптомов. Обновленная шкала PUQE оценивает симптомы в течение 24 часов [123], в то время как HIS учитывает психосоциальные факторы в дополнение к физическим симптомам [124].
Текущие исследования показывают, что лечение невирапином является субоптимальным. Одно недавнее проспективное исследование 283 женщин с невирапином в течение первого триместра показало, что только половине из них задавали вопрос об интенсивности и тяжести их симптомов, менее четверти спрашивали, мешают ли их симптомы их повседневным задачам и работе.В этом исследовании Lacasse et al только 27% женщин были предложены противорвотные средства, а еще 14% были рекомендованы немедикаментозные методы лечения [125].
Немедикаментозная терапия
Диетические меры
Начальная терапия невирапина и ГГ должна включать диетические изменения. Пораженные женщины должны избегать больших приемов пищи и вместо этого есть несколько небольших приемов пищи в течение дня, которые должны быть пресными и с низким содержанием жира, поскольку жирная пища может еще больше задержать опорожнение желудка. Употребление белка больше, чем углеводов, и употребление большего количества жидкости, чем твердой пищи, также может уменьшить тошноту, уменьшая желудочные аритмии, связанные с невирапином [82].Рекомендуются небольшие объемы соленых жидкостей, таких как электролитозамещающие спортивные напитки, а если запах горячей пищи является неприятным, следует приготовить холодную пищу [126].
Употребление белка больше, чем углеводов, и употребление большего количества жидкости, чем твердой пищи, также может уменьшить тошноту, уменьшая желудочные аритмии, связанные с невирапином [82].Рекомендуются небольшие объемы соленых жидкостей, таких как электролитозамещающие спортивные напитки, а если запах горячей пищи является неприятным, следует приготовить холодную пищу [126].
Эмоциональная поддержка
Эмоциональную поддержку всегда должен оказывать медицинский работник. Кроме того, поддерживающая психотерапия, поведенческая терапия и гипнотерапия могут быть полезны для женщин с тяжелыми симптомами и/или для тех, у кого играют роль личностные особенности, супружеские или семейные конфликты [60].Цель психотерапии не в том, чтобы углубляться в психологию, которая может способствовать НВП, а в том, чтобы поощрять, объяснять, успокаивать и позволять пациенту выражать стресс [95].
Акупрессура/акупунктура
Акупрессура китайской акупунктурной точки Р6 (Нэйгуань) снижает тошноту у пациентов с тошнотой, вызванной химиотерапией, а также послеоперационной тошнотой и рвотой, и может быть полезна при лечении ГГ. В соответствии с принципом ци, приложение давления к этой точке блокирует аномальное замедление энергии и восстанавливает симптомы, связанные с точкой давления [13].Давление можно оказывать вручную или с помощью эластичных лент на внутренней стороне запястья. Кроме того, ReliefBand, электрический стимулятор нервов с батарейным питанием, который носится на запястье, недавно был одобрен FDA и может также использоваться для стимуляции участка P6 [127].
В соответствии с принципом ци, приложение давления к этой точке блокирует аномальное замедление энергии и восстанавливает симптомы, связанные с точкой давления [13].Давление можно оказывать вручную или с помощью эластичных лент на внутренней стороне запястья. Кроме того, ReliefBand, электрический стимулятор нервов с батарейным питанием, который носится на запястье, недавно был одобрен FDA и может также использоваться для стимуляции участка P6 [127].
Доказательства акупрессуры противоречивы. Один обзор семи испытаний показал, что акупрессура точки Neiguan может облегчить симптомы тошноты [128]. Недавнее плацебо-контролируемое исследование с участием 60 женщин, принимавших невирапин, показало, что в группе лечения наблюдалось облегчение тошноты на следующий день после начала акупрессуры над местом P6, которое продолжалось до конца периода наблюдения.Для сравнения, в группе, получавшей акупрессуру на незначительном участке, наблюдалось первоначальное облегчение симптомов, но к 6-му дню симптомы вернулись и не отличались от группы, не получавшей лечения [129].
Хотя исследования преимуществ акупрессуры не дали окончательных результатов, некоторые эксперты считают, что это вмешательство должно быть предложено, поскольку не существует известных побочных эффектов [130].
Иглоукалывание менее изучено, но одно слепое рандомизированное контролируемое исследование с участием 593 женщин со сроком беременности менее 14 недель показало, что у женщин, получавших еженедельное лечение иглоукалыванием в течение 4 недель, было меньше тошноты и сухих рвотных позывов по сравнению с контрольной группой [131].Однако возможно, что состояние некоторых женщин улучшилось просто с увеличением гестационного возраста [13].
Имбирь
Имбирь — единственное немедикаментозное вмешательство, рекомендованное Американским колледжем акушерства и гинекологии [132]. Считается, что имбирь помогает улучшить НВП, стимулируя моторику желудочно-кишечного тракта и стимулируя выделение слюны, желчи и желудочного секрета. Было показано, что один компонент имбиря обладает такой же активностью, что и антагонист 5-HT3, ондансетрон. Кроме того, было обнаружено, что его экстракт ингибирует рост некоторых штаммов H. pylori [133].
Кроме того, было обнаружено, что его экстракт ингибирует рост некоторых штаммов H. pylori [133].
В двойном слепом рандомизированном перекрестном исследовании 70% женщин с ГГ, получавших 250 мг порошкообразного корня имбиря четыре раза в день, предпочли период приема имбиря по сравнению с периодом приема плацебо. Женщины также сообщали о значительно большем облегчении симптомов при приеме имбиря. 4 дня обнаружили, что у женщин в группе лечения было значительное улучшение симптомов тошноты по сравнению с женщинами в группе плацебо ( P <.001) [135].
Что касается безопасности имбиря во время беременности, исследование случай-контроль с участием 187 беременных женщин не выявило увеличения частоты серьезных пороков развития при употреблении имбиря в первом триместре [136]. Однако существует теоретический риск кровотечения, поскольку имбирь ингибирует тромбоксансинтетазу и может ингибировать функцию тромбоцитов. Таким образом, одновременное использование антикоагулянтов с имбирем не рекомендуется [137].
Фармакологическое лечение
Пиридоксин-доксиламин
Комбинация пиридоксина (витамина В6) (категория А при беременности) и доксиламина (категория В), ранее доступная как бендектин, является единственным лекарственным средством, которое специально маркировано для лечения невирапина Управление по санитарному надзору за качеством пищевых продуктов и медикаментов.Он по-прежнему доступен в Канаде в таблетках с отсроченным высвобождением, содержащих 10 мг пиридоксина и 10 мг доксиламина, под торговым названием Диклектин.
Бенедектин был снят с продажи в 1983 году в США в связи с сообщениями о врожденных пороках развития при применении в первом триместре. Однако до его отмены 30 миллионов женщин принимали его в течение почти 25 лет. Несколько небольших рандомизированных контролируемых исследований подтверждают его эффективность [138]. Кроме того, метаанализ, который включал 170 000 воздействий, показал, что комбинация пиридоксин-доксиламин безопасна и не вызывает побочных эффектов у плода [139]. Другие крупные исследования также не показали увеличения частоты врожденных аномалий по сравнению с фоновой частотой [140]. Тем не менее, Бенедектин остается вне рынка в Соединенных Штатах. Однако женщины могут сделать свой собственный препарат, объединив 10 мг пиридоксина с половинкой таблетки Унисома, который содержит 25 мг доксиламина.
Другие крупные исследования также не показали увеличения частоты врожденных аномалий по сравнению с фоновой частотой [140]. Тем не менее, Бенедектин остается вне рынка в Соединенных Штатах. Однако женщины могут сделать свой собственный препарат, объединив 10 мг пиридоксина с половинкой таблетки Унисома, который содержит 25 мг доксиламина.
В качестве альтернативы пиридоксин можно принимать отдельно. Хотя связи между уровнями пиридоксина и невирапином не обнаружено, в нескольких исследованиях было показано улучшение показателей тошноты у пациентов, принимавших пиридоксин с выраженной тошнотой [141], и уменьшение эпизодов рвоты по сравнению с женщинами, принимавшими плацебо [138].Нет известных доказательств токсичности витамина B6, однако в больших дозах пиридоксин был связан с обратимой периферической нейропатией у небеременных взрослых [13].
Противорвотные средства
Фенотиазины, хлорпромазин (торазин) и прохлорперазин (компазин), являются центральными и периферическими антагонистами дофамина, которые, как было показано, уменьшают симптомы невирапина и ГГ [142]. Они относятся к категории беременности С.
Они относятся к категории беременности С.
Исследование 12 764 беременных женщин показало незначительное повышение риска врожденных дефектов при применении фенотиазинов в первом триместре, особенно при применении хлорпромазина, однако потенциальные смешанные факторы, такие как употребление алкоголя и продолжительность лечения, не были выявлены. 143].Другое исследование показало, что у младенцев от матерей, принимавших хлорпромазин, были экстрапирамидные симптомы и желтуха; значительных нарушений постнатального развития не было [144].
Прометазин (Phenergan) не обладал тератогенными эффектами в одном исследовании [145], но в другом исследовании наблюдалось усиление врожденного вывиха бедра [146].
Активаторы
Метоклопрамид (Реглан) широко используется для лечения невирапина [147]. Это категория беременности B. Считается, что метоклопрамид улучшает симптомы за счет повышения давления в нижнем пищеводном сфинктере и увеличения транзита через желудочный тракт. Он также корректирует желудочные аритмии, стимулируя антральные сокращения и способствуя антродуоденальным сокращениям. Недавнее исследование показало, что 10 мг метоклопрамида, принимаемого каждые 8 часов, столь же эффективны для уменьшения количества эпизодов рвоты и улучшения самочувствия у женщин с ГГ во время их первой госпитализации, как и 25 мг прометазина, принимаемого каждые 8 часов в течение 24 часов. Профиль побочных эффектов был лучше в группе, получавшей метоклопрамид, с меньшей сонливостью, головокружением и дистонией [148].
Он также корректирует желудочные аритмии, стимулируя антральные сокращения и способствуя антродуоденальным сокращениям. Недавнее исследование показало, что 10 мг метоклопрамида, принимаемого каждые 8 часов, столь же эффективны для уменьшения количества эпизодов рвоты и улучшения самочувствия у женщин с ГГ во время их первой госпитализации, как и 25 мг прометазина, принимаемого каждые 8 часов в течение 24 часов. Профиль побочных эффектов был лучше в группе, получавшей метоклопрамид, с меньшей сонливостью, головокружением и дистонией [148].
Что касается безопасности, исследование 81 703 родов в период с 1998 по 2007 год в Израиле, в ходе которого метоклопрамид применялся у 4,2% женщин, не выявило повышенного риска серьезных врожденных пороков развития, низкой массы тела при рождении, преждевременных родов или перинатальной смерти при применении метаклопрамида. использовать [149]. Точно так же датское исследование 309 беременных женщин, принимавших метаклопрамид, не выявило повышенного риска [150].
Несмотря на свою эффективность, использование метоклопрамида ограничено его побочными эффектами, которые включают дистонию, беспокойство и сонливость.В 2009 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) добавило к метоклопрамиду предупреждение «черный ящик» из-за риска поздней дискинезии при хроническом применении.
Другие прокинетики, такие как домперидон и эритромицин, не изучались при применении невирапина [74].
Антигистаминные и антихолинергические препараты
Антигистаминные препараты косвенно влияют на вестибулярную систему, уменьшая стимуляцию рвотного центра [151]. Рандомизированные контролируемые исследования применения антигистаминных препаратов при невирапине ограничены; однако было показано, что меклизин (анитверт), дименгирдинат (драмамин) и дифенгирамин (бенадрил) контролируют симптомы лучше, чем плацебо [142].Кроме того, объединенные данные семи испытаний между 1951 и 1975 годами показали эффективность антигистаминных препаратов [152]. Метаанализ более 24 контролируемых исследований с участием более 200 000 беременных женщин показал, что антигистаминные препараты (в частности блокаторы Н2-рецепторов), назначаемые в течение первого триместра, не повышают риск тератогенного действия [153]. Хотя ранее считалось, что меклизин обладает тератогенным действием, теперь исследования показывают, что его безопасно использовать во время беременности [154]. Дименгидринат и дифенгидрамин имеют противоречивые результаты по безопасности [74].
В одном исследовании женщин, перенесших плановое кесарево сечение, было обнаружено, что трансдермальный скополамин более эффективен в уменьшении тошноты, рвоты и позывов на рвоту из-за эпидуральной морфиновой анальгезии по сравнению с плацебо [155]. Однако исследования по применению скополамина в первом триместре отсутствуют, поскольку скополамин может вызывать хромосомные аберрации и обмены сестринскими хроматидами в здоровых взрослых лимфоцитах и может приводить к врожденным порокам развития, включая деформацию конечностей и туловища [156].
Другие препараты
Ондансетрон (Зофран) (категория B при беременности) широко используется для лечения послеоперационной и вызванной химиотерапией тошноты и рвоты и в настоящее время является одним из наиболее часто назначаемых противорвотных средств [157].Считается, что он действует как центрально, так и периферически, блокируя серотониновые рецепторы в тонкой кишке и медуллярном рвотном центре [151]. Его безопасность при беременности была определена в недавнем исследовании, которое не показало значительного увеличения числа выкидышей, серьезных пороков развития или массы тела при рождении между младенцами, подвергшимися воздействию ондансетрона, и контрольной группой, не получавшей его [158].
Было проведено одно рандомизированное контролируемое исследование применения ондансетрона для лечения ХГ. В этом небольшом исследовании с участием 30 женщин не было выявлено преимуществ ондансетрона в дозе 10 мг внутривенно каждые 8 часов по мере необходимости по сравнению с прометазином в дозе 50 мг внутривенно каждые 8 часов с точки зрения тошноты, увеличения веса, дней госпитализации или общих доз препарата [46]. .Однако было обнаружено, что прометазин вызывает больший седативный эффект. Тем не менее, сообщения о случаях заболевания и широко распространенный клинический опыт подтверждают эффективность ондансетрона для лечения HG и его лучшую переносимость по сравнению с более ранними противорвотными средствами [159, 160].
Дроперидол (инапсин) является антагонистом дофамина, эффективным противорвотным средством при послеоперационной тошноте и рвоте. Небольшое исследование женщин с HG показало, что комбинация непрерывной инфузии дроперидола и болюсного внутривенного введения дифенгидрамина приводила к более коротким госпитализациям и меньшему количеству повторных госпитализаций по сравнению с исторической контрольной группой, которая получала другие формы парентеральной терапии.Кроме того, не было никаких существенных различий в материнских или перинатальных исходах [161]. Следует отметить, однако, что дроперидол имеет предупреждение черного ящика, поскольку он может вызывать удлинение интервала QT и сердечные аритмии [74].
Пероральные и внутривенные кортикостероиды использовались для рефрактерных случаев HG с переменными результатами. Считается, что они оказывают противорвотное действие на триггерную зону хеморецепторов в стволе головного мозга, а также постулируются для коррекции «относительной надпочечниковой недостаточности», вызванной HG, при которой гипоталамо-гипофизарно-надпочечниковая ось не может реагировать на повышенные потребности в кортизоле. во время ранней беременности.
В рандомизированном контролируемом исследовании 40 женщин с ГГ, получавших метилпреднизолон в дозе 16 мг перорально 3 раза в день в течение 3 дней с последующим 2-недельным снижением дозы, по сравнению с прометазином в дозе 25 мг перорально 3 раза в день в течение 2 недель, — госпитализация была обнаружена в группе, получавшей стероиды [162]. Другие исследования не показали статистически значимого преимущества кортикостероидов. Рандомизированное исследование Yost et al. не обнаружили значительного снижения числа посещений неотложной помощи или повторных госпитализаций при добавлении парентерального и перорального метилпреднизолона к режиму прометазина и метоклопрамида [163].
Нет утвержденных руководств по применению кортикостероидов при ХГ. Однако была предложена возможная схема: 48 мг метилпреднизолона вводят перорально или внутривенно в три приема в течение двух-трех дней. Если в течение трех дней ответа не наблюдается, рекомендуется прекратить лечение, так как ответ через 72 часа маловероятен [151].
Что касается безопасности, то недавний метаанализ показал небольшое увеличение основных пороков развития и 3,4-кратное увеличение расщелины рта у младенцев, матери которых принимали кортикостероиды в первом триместре [164].
В последнее время наблюдается интерес к препаратам, снижающим кислотность при лечении невирапином, поскольку одно недавнее когортное исследование показало, что у женщин с невирапином и изжогой и/или кислотным рефлюксом тошнота и рвота были более выраженными, чем у женщин без изжоги или кислотного рефлюкса [165]. Кроме того, последующие исследования показали, что лечение изжоги и/или рефлюкса приводит к улучшению показателей PUQE и показателей качества жизни [166].
Антациды, содержащие алюминий или кальций, являются терапией первой линии во время беременности при кислотном рефлюксе и изжоге и могут использоваться для лечения женщин с невирапином.Антациды, содержащие магний, связаны с нефролитиазом, гипотонией и респираторным дистресс-синдромом у плода и не рекомендуются во время беременности. Антациды, содержащие бикарбонаты, могут вызывать метаболический ацидоз плода и перегрузку жидкостью и также не рекомендуются [167].
Блокаторы h3 и ингибиторы протонной помпы можно безопасно использовать для лечения кислотного рефлюкса и/или изжоги у женщин с невирапином [168, 169].
Нутритивная поддержка
Женщинам с трудноизлечимыми симптомами, не поддающимися коррекции диеты и фармакологическому лечению и неспособными поддерживать вес за счет перорального приема пищи, может потребоваться пищевая поддержка.В этой популяции следует использовать внутривенную инфузионную терапию, энтеральное или парентеральное питание для предотвращения задержки внутриутробного развития плода, обезвоживания матери и недостаточности питания.
Роль внутривенной гидратации заключается в увеличении объема и восстановлении электролитов. Госпитализированным пациентам при необходимости можно быстро влить физиологический раствор или раствор Рингера с лактатом, а затем откорректировать их для соответствия диурезу. Внутривенно тиамин следует вводить перед любыми жидкостями, содержащими декстрозу, чтобы избежать энцефалопатии Вернике.Женщинам, которым требуется многократная госпитализация, может быть рекомендована внутривенная гидратация в домашних условиях [74].
Энтеральное зондовое питание и полное парентеральное питание следует рассмотреть, если внутривенная терапия не помогает уменьшить симптомы, а дефицит калорий сохраняется. Однако исследования энтерального питания при HG ограничены. В одном небольшом исследовании женщин с HG, получавших энтеральное питание с использованием назогастрального зонда 8-French, сообщалось об улучшении симптомов в течение 24 часов после установки зонда.Через 8 дней пациенты были выписаны в среднем на 43 дополнительных дня амбулаторного энтерального питания, после чего можно было возобновить пероральное питание [170].
Помимо назогастральных зондов, чрескожная эндоскопическая гастростомия (ЧЭГ) [171] успешно использовалась для поддержания питания у женщин с ГГ. Однако оба этих способа кормления ограничены риском усиления тошноты и рвоты, вызванных внутрижелудочным кормлением. Постпилорические зонды для кормления, как назоеюнальные [172, 173], так и чрескожные эндоскопические гастроеюноанастомозы [174] пытались снизить этот риск, однако смещение зондов [175] из-за продолжающейся рвоты, позывов на рвоту и свертывания желудка является частым осложнением. .Кроме того, назоэнтеральные зонды, как назогастральные, так и назоеюнальные, плохо переносятся многими женщинами из-за эстетических соображений и физического дискомфорта. Недавно хирургическая еюностомия была описана как альтернативный способ доставки питания женщинам с HG. В одном небольшом исследовании пяти женщинам с HG была выполнена хирургическая еюностомия во втором триместре. Изотонические кормления через зонд вводили до целевого показателя калорийности. Прибавка в весе матери наблюдалась в 5 из 6 беременностей, и все беременности закончились срочными родами.Серьезных осложнений не произошло, что позволяет предположить, что еюностомия может быть безопасным и эффективным способом нутритивной поддержки у женщин с ХГ [176].
Женщинам, которые не переносят энтеральное питание, следует рассмотреть возможность парентерального питания. Эта терапия, однако, является дорогостоящей и связана со значительной материнской заболеваемостью. Руссо-Стейглиц и др. сообщили о частоте осложнений 9% при парентеральном питании через периферически установленные центральные катетеры во время беременности и о 50% частоте осложнений при центрально вставленных катетерах.Инфекция и тромбоз были двумя наиболее часто встречающимися осложнениями, и предполагалось, что они являются результатом связанной с беременностью гиперкоагуляции и иммунологической супрессии [177]. Holmgren et al. также показали высокую частоту осложнений у женщин, получавших парентеральное питание через PICC. В исследовании 94 женщин с HG 66,4% из тех, кто получал парентеральное питание через PICC, нуждались в лечении тромбоэмболии, инфекции или того и другого. Пациентки на парентеральном питании также имели более высокую частоту неонатальных осложнений, включая госпитализацию в отделение интенсивной терапии новорожденных, малый размер для гестационного возраста, прерывание беременности из-за ГГ и потерю плода по сравнению с женщинами, получавшими энтеральное питание [178].Таким образом, парентеральное питание, хотя оно может быть более переносимым для пациентов, следует зарезервировать для отдельных пациентов с HG.
Информация для авторов
Ноэль М. Ли, Школа медицины и общественного здравоохранения Университета Висконсина, Медицинский фонд Университета Вашингтона, здание столетия, 1685 Highland Avenue, Madison, WI 53705, телефон: (608) 263-1995, факс: (608) 265-5677.
Сумона Саха, Отделение гастроэнтерологии и гепатологии, Школа медицины и общественного здравоохранения Висконсинского университета, Медицинский фонд Университета Вашингтона, здание столетия, 1685 Хайленд-авеню, комната 4224, Мэдисон, Висконсин 53705, телефон: (608) 263-1995, факс: (608) 265-5677.
Тошнота и рвота при беременности
Введение
Тошнота и рвота являются обычным явлением во время беременности, которым страдают 70–80% всех беременных женщин. Хотя у большинства женщин тошнота и рвота при беременности (НВП) имеют симптомы, ограниченные первым триместром, у небольшого процента женщин наблюдается длительное течение с симптомами, продолжающимися до родов. У женщин с тяжелой тошнотой и рвотой во время беременности может быть гиперемезис беременных (HG), состояние, отличное от NVP, которое, если его не лечить, может привести к значительной заболеваемости матери и плода.
Различные метаболические и нервно-мышечные факторы вовлечены в патогенез невирапина и HG; однако их точная причина неизвестна. Следовательно, лечение NVP и HG может быть затруднено, поскольку не известны ни оптимальные цели лечения, ни полные эффекты потенциальных методов лечения на развивающийся плод. В этой статье рассматриваются эпидемиология, патология, диагностика, исходы и лечение невирапина и HG.
Эпидемиология
По оценкам, 70–80% беременных женщин получают невирапин [1].В Соединенных Штатах и Канаде это означает примерно 4 000 000 и 350 000 женщин, которые страдают каждый год соответственно [2].
НВП чаще встречается в западных странах и у городского населения и редко встречается у африканцев, коренных американцев, эскимосов и большинства азиатских популяций [3]. Лишь в нескольких исследованиях изучалось расовое распределение невирапина в данной популяции. Одно такое исследование, проведенное в Канаде с участием 367 женщин, показало, что азиаты и чернокожие реже сообщали о симптомах невирапина, чем представители европеоидной расы.Социально-демографические факторы не учитывали расовые/этнические различия в распространенности заболевания, что позволяет предположить, что могут играть роль генетические и/или культурные факторы [4].
HG встречается редко по сравнению с NVP и встречается в 0,3–2% всех беременностей [5]. Заболеваемость зависит от этнической принадлежности [6] и колеблется от 3 до 20 на 1000 беременностей [7]. Он чаще диагностируется у женщин в Индии, Пакистане, Азии, Новой Зеландии по сравнению с европейцами, американскими индейцами и эскимосами [8].
Факторы риска
Данные Совместного перинатального проекта, одного из крупнейших на сегодняшний день исследований беременных женщин, показали, что невирапин чаще встречается у молодых женщин, первобеременных, женщин с образованием менее 12 лет, некурящих и женщины с ожирением [9]. О повышенном риске невирапина в первом триместре также сообщалось у женщин с многоплодной беременностью по сравнению с женщинами с одноплодной беременностью (87% против 73%, p<0,01) [10].
НВП был связан с низким уровнем дохода и статусом занятости неполный рабочий день [11]).Было обнаружено, что домохозяйки также подвергаются повышенному риску, в то время как женщины, работающие в качестве белых воротничков, по-видимому, защищены [12]. Однако остается неясным, является ли статус занятости истинным фактором риска для невирапина или искажающим фактором, поскольку затронутые женщины могут прекратить работу из-за своих симптомов. Точно так же их решение не работать вне дома может быть связано с многодетностью и необходимостью заботиться о других детях [13].
Материнская генетика также может служить фактором риска для невирапина. Данные большой популяции норвежских близнецов показывают более широкое использование лекарств от тошноты во время беременности среди монозиготных близнецов женского пола по сравнению с дизиготными близнецами женского пола [14].Кроме того, более высокие уровни тошноты были обнаружены у женщин, матери которых испытывали тошноту во время беременности [15]. Также было показано, что личный анамнез NVP является фактором риска для NVP при последующих беременностях [15]; однако этот вывод не был последовательным в разных исследованиях [16]
Другие факторы риска для невирапина включают личную историю укачивания, возможно, из-за общего вестибулярного механизма [17] и мигреней в анамнезе [18]. Женщины, у которых в анамнезе была тошнота при приеме эстрогенсодержащих пероральных контрацептивов, также подвержены повышенному риску невирапина [19].
Расположение желтого тела также может служить фактором риска невирапина. Ультразвуковые исследования показали, что беременные чаще испытывают тошноту и рвоту при наличии желтого тела в правом яичнике [20]. Это может быть связано с различиями в венозном оттоке между левым и правым яичником и более высокой концентрацией половых стероидов, когда желтое тело находится на правой стороне [21].
Более высокое суточное потребление общего жира, особенно насыщенных жиров, до беременности увеличивает риск госпитализации по поводу невирапина [22].Курение до беременности и прием витаминов до и/или на ранних сроках беременности связаны со снижением риска невирапина [23]. Также было обнаружено, что употребление алкоголя матерью до зачатия защищает от NVP [24].
Факторы риска HG аналогичны факторам риска NVP. К ним относятся многоплодная беременность, трофобластическая болезнь, HG в предшествующей беременности, аномалии плода, такие как триплоидия, трисомия 21 и водянка плода, а также нерождение плода [25]. Семейный анамнез HG также является фактором риска: примерно 28% женщин сообщают о HG в анамнезе у своих матерей и 19% сообщают, что их сестры имели аналогичные симптомы [26].Дополнительные факторы риска включают семейный или партнерский статус и возраст старше 30 лет. Курение сигарет может быть защитным [27].
Индекс массы тела матери оценивался как фактор риска ГГ с неоднозначными результатами. В исследовании Depue et al ожирение увеличивало риск ГГ на 50% [28]. Работа Cedergren et al. однако обнаружили, что низкий индекс массы тела (<20 кг/м2) был связан с 40% более высоким риском ХГ, а ожирение снижало риск госпитализации по поводу ХГ [29].Более недавнее исследование 33 647 женщин в Норвегии показало, что недостаточный или избыточный вес увеличивает риск ГГ, но только у некурящих [30]. Постулируется, что женщины с недостаточным весом и низкими индексами массы тела имеют низкий уровень эстрогена до беременности и, таким образом, могут иметь преувеличенный ответ в течение первого триместра, когда уровень эстрогена резко возрастает [31]. Напротив, у женщин с ожирением жировые отложения могут нейтрализовать плацентарные факторы, которые, как считается, способствуют патогенезу [29].
Что касается пола плода, то в нескольких исследованиях была обнаружена связь между ГГ и женским полом плода.Используя данные Шведского медицинского реестра рождений, Kallen et al. обнаружили, что HG был чрезмерно представлен в 3068 беременностях, когда ребенок был девочкой [32]. Точно так же в исследовании беременных женщин, госпитализированных с HG в первом триместре, вероятность рождения девочки была на 50% выше в случаях по сравнению со здоровыми беременными в контрольной группе (ОШ 1,5, 95% ДИ 1,4, 1,7) [33].
Патогенез
Метаболические и гормональные факторы
Хотя точный патогенез НВП и ГГ неизвестен, общепризнано, что рвота во время беременности является результатом различных метаболических и эндокринных факторов, многие из которых имеют плацентарное происхождение.Наиболее значимым фактором является хорионический гонадотропин человека (ХГЧ). Эта связь между ХГЧ и невирапином в значительной степени основана на временном соотношении между пиком невирапина и пиком продукции ХГЧ, которые происходят между 12 и 14 неделями беременности. Кроме того, тошнота и рвота часто усиливаются у беременных с состояниями, связанными с повышенным уровнем ХГЧ, такими как молярная беременность, многоплодная беременность и синдром Дауна [13]. Более высокие уровни ХГЧ в моче [34] и в сыворотке также были обнаружены у женщин с невирапином по сравнению с бессимптомными [35].Кроме того, исследование Goodwin et al. обнаружили, что концентрации ХГЧ положительно коррелируют с выраженностью тошноты и рвоты у женщин с ХГ [36].
Несмотря на множество исследований, связывающих уровень ХГЧ с невирапином и гормоном роста, другие не обнаружили связи между уровнем ХГЧ в сыворотке беременных женщин в течение первого триместра и частотой или интенсивностью тошноты и рвоты. В исследовании Soules et al. даже в подгруппе женщин с пузырным заносом, у которых уровни ХГЧ у женщин были в 5-10 раз выше, чем в контроле, корреляции обнаружено не было [37].Кроме того, исследования показали, что высокие уровни ХГЧ связаны с задержкой роста плода и преждевременными родами [38], в то время как невирапин, по-видимому, защищает от преждевременных родов, что делает маловероятным то, что ХГЧ является единственным фактором патогенеза невирапина.
Предполагается, что различные биологические формы (то есть изоформы) ХГЧ могут объяснить вариабельность между уровнями ХГЧ и тошнотой и рвотой у здоровых и больных людей [39]. Каждая изоформа ХГЧ имеет уникальный период полувыведения и активность в отношении рецепторов лютеинизирующего гормона и тиреотропного гормона (ТТГ).Изоформы без карбоксиконцевой части имеют более короткий период полувыведения, но являются более сильными стимуляторами рецепторов лютеинизирующего гормона и ТТГ. Напротив, гипергликозилированный ХГЧ имеет более длительный период полувыведения и большую продолжительность действия [40]. Эти различные изоформы ХГЧ, вероятно, являются результатом генетических факторов или долгосрочных изменений окружающей среды, которые, таким образом, могут объяснить различия в заболеваемости ХГ, обнаруженные в разных популяциях. Помимо изменчивости изоформ, мутации рецептора ХГЧ также могут объяснить некоторую вариабельность взаимоотношений между невирапином и ХГЧ [39].
Гормоны яичников, эстроген и прогестерон, также участвуют в патогенезе невирапина и гипергидроза. Известно, что некоторые женщины испытывают тошноту при приеме оральных контрацептивов. Кроме того, состояния с высокой концентрацией эстрогена, такие как низкий паритет и высокий индекс массы тела матери, были связаны с более высокой частотой ГГ [28]. Считается, что эстроген вносит свой вклад в HG, стимулируя выработку оксида азота с помощью синтетазы азотоксидазы, которая, в свою очередь, расслабляет гладкие мышцы, замедляя время желудочно-кишечного транзита и опорожнение желудка.
Ярнфельт и др. сообщили о значительной связи между рвотой беременных и непереносимостью пероральных контрацептивов в анамнезе [40]. Используя более количественный подход, Depue et al. обнаружили, что средние уровни общего эстрадиола на 26% выше, а средние уровни способности связывания половых гормонов и глобулинов на 37% выше у пациентов с HG, чем в контрольной группе после поправки на гестационный возраст. 28]. Однако важно отметить, что, как и взаимосвязь между ХГЧ и невирапином, взаимосвязь между уровнями эстрогена и невирапином была противоречивой в разных исследованиях [35].Обзор 17 исследований показал положительную связь между невирапином и эстрогеном только в 5 исследованиях [41]. Кроме того, пик уровня эстрогена приходится на третий триместр беременности, в то время как ГГ имеет тенденцию к улучшению на поздних сроках беременности [8].
Прогестерон в сочетании с эстрогеном также может играть роль в NVP. Прогестерон снижает сократимость гладкой мускулатуры и может изменить опорожнение желудка и привести к усилению тошноты и рвоты. Используя эластогастографию после стандартного приема пищи, Walsh et al. показали, что такое же медленноволновое нарушение желудочного ритма, обнаруженное у женщин с невирапином, может быть вызвано у небеременных женщин монотерапией прогестероном или в комбинации с эстрадиолом в дозах, которые воспроизводят уровни при беременности [42].Другие исследования, однако, не обнаружили существенной разницы между уровнями прогестерона у женщин с невирапином или без него [28].
Роль плацентарного простагландина E2 (PGE2) также оценивалась в патогенезе NVP из-за его влияния на гладкую мускулатуру желудка [43]. ХГЧ стимулирует плацентарный PGE2 и, как и ХГЧ, достигает пика между 9 и 12 неделями беременности. Норт и др. определили количество PGE2 в материнской сыворотке и обнаружили, что уровни были выше во время периодов тошноты и рвоты у 18 женщин на ранних сроках беременности по сравнению с бессимптомными периодами.Они также оценили уровни интерлейкина-1 бета и фактора некроза опухоли альфа у матери и обнаружили, что они были одинаковыми в течение симптоматического и бессимптомного периодов [44].
В связи с его ролью в вызванных химиотерапией тошноте и рвоте, серотонин также предположительно способствует развитию невирапина. Исследование Borgeat et al. однако не выявили различий в уровне серотонина среди беременных женщин с ХГ, бессимптомных беременных женщин и небеременных женщин [45]. Кроме того, рандомизированное контролируемое исследование, сравнивающее антагонист серотониновых 5-HT3-рецепторов, онданстерон, с прометазином, не выявило существенной разницы в контроле симптомов [46].
Из-за перекрестной реактивности между ХГЧ и рецептором тиреостимулирующего гормона (ТТГ) дисфункция щитовидной железы также изучалась как возможный механизм развития невирапина и ГГ. На самом деле, аномальные результаты функции щитовидной железы обнаруживаются у двух третей женщин с ГГ [36]. Этот «биохимический тиреотоксикоз» характеризуется подавлением ТТГ и слегка повышенным уровнем FT4. Несмотря на эти лабораторные отклонения, женщины с HG, как правило, находятся в эутиреоидном состоянии без предшествующих заболеваний щитовидной железы, отсутствия зоба и отрицательных антитиреоидных антител [47].Кроме того, исследования не выявили взаимосвязи между дисфункцией щитовидной железы и тяжестью симптомов [48], и почти у всех женщин с ХГ уровень ТТГ в норме к 20 нед беременности без какого-либо вмешательства [49].
Недавно была предложена связь между гормоном лептином и HG. Было обнаружено, что повышенный уровень лептина в сыворотке во время беременности, возможно, в результате увеличения общей жировой массы и продукции плаценты, значительно выше у пациенток с HG по сравнению со здоровыми беременными контрольной группой [50, 51].Лептин может способствовать ГГ за счет увеличения секреции ХГЧ за счет паракринного действия плаценты или за счет снижения аппетита и усиления тошноты и рвоты. Примечательно, однако, что другие проспективные когортные исследования не обнаружили аналогичной статистически значимой разницы в уровнях лептина в сыворотке при HG между пациентами и контрольной группой [52, 53].
Также было высказано предположение, что у женщин с HG возникает нарушение регуляции иммунной системы. В сыворотке крови матери были обнаружены повышенные концентрации свободной ДНК клеток плода [54], вызывающие гиперактивный материнский иммунный ответ и повреждение трофобласта.Кроме того, нормальный сдвиг во время беременности, при котором типы Т-хелперов переходят в Т-хелперы типа 1, более преувеличен у женщин с ХГ [55]. Это, в свою очередь, приводит к повышенному высвобождению интерлейкина-4, а также фактора некроза опухоли-альфа, оба из которых были связаны с HG [56]. Также было обнаружено, что аденозин повышен при HG, и его роль заключается в ослаблении TNF-альфа [57]. В проспективном исследовании [58] также было обнаружено, что уровни интерлейкина-6 повышаются при HG, а также повышаются уровни иммуноглобулина G (IgG), IgM, уровни комплемента и количество лимфоцитов [59].Однако точно определить роль этих иммунологических факторов нельзя, так как при голодании иммунная система обычно угнетается, а не активируется; таким образом, возможно, усиление иммунных факторов, наблюдаемое при HG, может быть попыткой ограничить прогрессирование HG [8].
Другие гормоны, в том числе тиреотропный гормон, гормон роста, пролактин, адренокортико-стимулирующий гормон, кортизол, лютеинизирующий гормон и фолликулостимулирующий гормон, также оценивались и, как считается, не вносят вклад в патогенез невирапин [60].
Helicobacter pylori
Повышенная частота инфицирования Helicobacter pylori (H. pylori) наблюдалась у женщин с ГГ, и в настоящее время считается, что она играет роль в ее патогенезе. Фриго и др. обнаружили, что 90,5% женщин с HG были H. plyori IgG положительными по сравнению с 46,5% в контрольной группе [61]. Багис и др. использовали золотой стандарт тестирования, гистологическое исследование биопсии слизистой оболочки, и обнаружили, что 95% пациентов с HG дали положительный результат на H.pylori по сравнению с 50% в контрольной группе. Они также обнаружили более высокую плотность H. pylori в антральном отделе и теле желудка у пациентов с HG, что позволяет предположить возможную связь между плотностью H. pylori и тяжестью симптомов [62].
Систематический обзор 2007 г., в котором оценивались 14 исследований типа «случай-контроль» с 1966 по 2007 г., выявил значительную связь между материнской инфекцией H.pylori и HG в 10 исследованиях. Отношение шансов в исследованиях варьировалось от 0.от 55 до 109,33 [63]. Аналогичным образом обновленный систематический обзор и метаанализ 25 исследований 2009 г. показали, что объединенное отношение шансов составляет 3,32 (95% доверительный интервал: 2,25–4,90) для инфекции H. pylori у женщин с HG [64]. Примечательно, что в обоих обзорах была обнаружена высокая гетерогенность исследований.
Инфицирование H. pylori во время беременности может произойти из-за вызванных стероидными гормонами изменений pH желудка [65] и/или повышенной восприимчивости из-за изменений гуморального и клеточно-опосредованного иммунитета [66].Однако нет четких доказательств того, что беременность предрасполагает к инфекции de novo H. pylori . Напротив, было высказано предположение, что H. pylori может усугубить вызванные гормонами изменения нервной и электрической функции желудка и, таким образом, увеличить риск для инфицированных женщин оказаться в более тяжелой форме тошноты и рвоты. рвота [67].
Хотя связь между H. pylori и HG интригует, важно отметить, что инфекция не обязательно коррелирует с симптомами.На самом деле у большинства инфицированных женщин заболевание протекает бессимптомно [8]. В исследовании Weyermann et al. 23% из 898 родильниц дали положительный результат на H. pylori при дыхательном тесте с 13C-мочевиной; однако положительный результат не коррелировал с симптомами тошноты, рвоты или рефлюкса во время беременности [68]. Точно так же Wu et al. обнаружили, что 69% беременных женщин являются сероположительными в отношении H. pylori по сравнению с 50% в общей популяции, однако не обнаружили никакой корреляции между статусом антител и желудочно-кишечными симптомами [69].
Почему H. pylori нельзя точно связать с невирапином, а HG связывают с несколькими факторами. Во-первых, в большинстве исследований для оценки наличия инфекции использовалось тестирование на антитела. Однако серологическое тестирование на H. pylori не может отличить активную инфекцию от перенесенной инфекции [70], а активная и перенесенная инфекция могут по-разному влиять на симптомы. Во-вторых, в большинстве исследований не оценивался и/или не учитывался штамм H. pylori . Ассоциированный с цитотоксином белок гена A (CagA) является маркером учащения пептических язв и связан с более агрессивным штаммом H pylori [71].Только одно исследование, включенное в метаанализ 2009 г., оценивало патогенность CagA. В этом исследовании, проведенном Xia et al., положительная реакция на CagA была более распространена у пациентов с HG [72].
Лечение приводит к эрадикации H. pylori у большинства пациенток, однако в настоящее время нет рекомендаций по оценке или лечению H. pylori во время беременности, поскольку последующее облегчение симптомов HG широко не изучалось. Сообщения о клинических случаях и серии случаев позволяют предположить, что лечение и эрадикация 90–105 H.pylori может уменьшить тошноту и рвоту во время беременности, и его следует рассматривать у пациенток с трудноизлечимыми симптомами [73]. Однако необходимы более масштабные исследования, чтобы определить, следует ли и когда начинать лечение во время беременности, учитывая опасения по поводу безопасности лекарств. В настоящее время специалисты рекомендуют после завершения беременности и лактации проводить тройную терапию в течение двух недель [74].
Нарушение моторики желудочно-кишечного тракта
Изменения давления в состоянии покоя нижнего пищеводного сфинктера (НПС) и перистальтики пищевода связаны с невирапином.Хотя эти изменения чаще связаны с изжогой во время беременности, гастроэзофагеальная рефлюксная болезнь (ГЭРБ) может вызывать атипичные симптомы, такие как тошнота [75], и способствовать развитию невирапинов. Эстроген и прогестерон являются вероятными медиаторами нарушения моторики пищевода при беременности, при этом эстроген служит праймером, а прогестерон вызывает релаксацию НПС [76].
Изменения желудочной ритмической активности могут способствовать НВП. Нормальная миоэлектрическая активность желудка приводит к медленному распространению волны от проксимального отдела тела к дистальному отделу антрального отдела со скоростью 3 цикла в минуту (имп/мин).Нарушение ритма в виде увеличения или уменьшения распространения медленных волн связано с тошнотой [74]. Используя эластогастрографию (EGG), Koch et al. продемонстрировали, что лица с нормальной медленноволновой активностью реже жаловались на тошноту во время беременности [77]. Напротив, люди с более высокими или более низкими показателями чаще жаловались на тошноту. Точно так же Riezzo et al. обнаружили, что беременные женщины без симптомов тошноты и рвоты на момент записи ЭГГ имеют нормальную миоэлектрическую активность 3 имп/мин.Они также обнаружили, что беременные женщины с невирапином имели более нестабильную активность EGG по сравнению с женщинами после добровольных абортов и небеременными женщинами из контрольной группы. Они предположили, что это может быть связано с восстановлением нормальной картины медленных волн желудка после аборта после нормализации уровней эстрадиола и прогестерона [78].
Примечательно, однако, что многие исследования не обнаружили различий в перистальтике желудка между беременными и небеременными женщинами. С помощью сцинтографии желудка не было обнаружено существенных различий в скорости опорожнения жидкости у беременных женщин до добровольного аборта, через 6 недель после аборта и у небеременных женщин контрольной группы [79].Используя методы разбавления красителя феноловым красным, Davison et al. обнаружили задержку опорожнения желудка во время родов, но не в третьем триместре по сравнению с небеременными контрольными женщинами [80]. Точно так же исследования с использованием парацетамола не показали задержки опорожнения желудка в первом, втором или третьем триместре [81].
Изменения моторики желудка при беременности объясняются высоким уровнем прогестерона. Кроме того, на поздних сроках беременности сдавление увеличенной маткой может способствовать симптомам.
Состав пищи также может играть патогенную роль в NVP.Джеднак и др. продемонстрировали, что прием пищи с преобладанием белка был связан с уменьшением симптомов и коррекцией медленноволновой аритмии. Прием пищи с преобладанием углеводов или жиров не влиял на симптомы или медленноволновую аритмию [82].
Наконец, время прохождения по тонкой кишке было оценено в отношении патогенеза NVP. Используя водородный дыхательный тест с лактулозой, косвенный показатель времени прохождения по тонкой кишке, Lawson et al. обнаружили, что время транзита удлиняется во втором и третьем триместре по сравнению с первым триместром, причем самые длинные времена были обнаружены, когда уровни прогестерона были самыми высокими [83].Уолд и др. использовали аналогичные методы и обнаружили, что время транзита увеличивается в третьем триместре, когда уровни прогестерона и эстрогена были высокими по сравнению с послеродовым периодом [84]. Однако в обоих этих исследованиях задержка кишечного транзита не коррелировала с невирапином.
Психосоциальные факторы
Ранние исследования предполагали, что НВП может быть психосоматическим заболеванием, при котором рвота представляет собой интрапсихический конфликт. Некоторые предполагают, что NVP является проявлением подсознательной попытки беременной женщины отказаться от нежелательной беременности [85], поскольку исследования показали, что у женщин с NVP в первом триместре чаще бывают незапланированные или нежелательные беременности [86].
ГГ также ассоциируется с психологическими расстройствами, а именно невротическими наклонностями, истерией, неприятием женственности, неприятием беременности, а также с депрессией и психологическим стрессом, связанным с бедностью и семейными конфликтами [8]. Однако недавние исследования не выявили определенных психогенных причин ГГ [87, 88]. Некоторые, следовательно, утверждают, что социокультурные факторы, а не научные данные, привели к тому, что HG маркируется как психологически обусловленное состояние, и что более вероятно, что психологические нарушения, такие как депрессия, являются результатом, а не причиной HG [89].
Таким образом, хотя NVP и HG, вероятно, не являются результатом конверсионного расстройства или другого психологического расстройства, общепризнано, что у пострадавших женщин возникают психологические реакции, которые переплетаются с их физическими симптомами и, возможно, усугубляют их.
Диагностика и клинические признаки
Анамнез и медицинский осмотр
Несмотря на популярное использование термина «утренняя тошнота», невирапин сохраняется в течение дня у большинства больных женщин и, как было установлено, ограничивается утром менее чем у 2% женщин [90].Он часто начинается в течение нескольких недель после отсутствия менструации и поэтому в большинстве культур карикатурно изображается как начальный признак беременности. Симптомы обычно достигают пика между 10 и 16 неделями беременности и обычно исчезают после 20 недель. Однако до 10% женщин продолжают иметь симптомы после 22 недель [90].
В то время как обезвоживание и ортостаз могут возникать у женщин с HG, у большинства женщин с NVP показатели жизненно важных функций в норме, а физикальный осмотр является благоприятным. Однако следует провести тщательное обследование брюшной полости, чтобы исключить перитонит и другие внутрибрюшные причины тошноты и рвоты.
Дифференциальный диагноз
Учитывая высокую распространенность невирапина, тошнота и рвота в первом триместре обычно связаны с невирапином. Однако при наличии изменений в работе кишечника, боли в животе и рвоте желчью следует провести соответствующие исследования для исключения других причин. Дифференциальный диагноз невирапина включает гастроэзофагеальную рефлюксную болезнь, язвенную болезнь, непроходимость тонкой кишки, острый холецистит, желчнокаменную болезнь, панкреатит, а также аппендицит, гастроэнтерит, нефролитиаз, пиелонефрит и гепатит [74]
Диагностические и лабораторные исследования
Для диагностики невирапина не рекомендуются никакие специальные лабораторные исследования, кроме теста на беременность.Однако другие тесты могут быть полезны для исключения других причин тошноты и рвоты. Лейкоцитоз не должен наблюдаться при невирапине и может указывать на инфекционную или воспалительную причину, такую как холецистит, инфекция мочевыводящих путей и панкреатит. Повышение уровня аминотрансфераз может свидетельствовать о хроническом гепатите. Аномальный ТТГ может указывать на гипотиреоз или гипертиреоз, оба из которых могут вызывать тошноту и рвоту. Повышение уровня глюкозы в сыворотке может указывать на диабет и может вызывать тошноту и рвоту за счет снижения сократительной способности антрального отдела и ускорения желудочной аритмии [91].
Рентгенография обычно не требуется для диагностики невирапина. УЗИ органов малого таза можно использовать для документирования беременности и оценки состояний, повышающих риск невирапина, таких как многоплодная беременность. Рентген брюшной полости, как правило, бесполезен и, хотя представляет небольшой риск для плода, все еще относительно противоречив в течение первого триместра.
Верхнюю эндоскопию можно безопасно проводить во время беременности и исключить гастрит и ЯБ как причины тошноты и рвоты во время беременности.В одном крупном центре тошнота и рвота были вторым наиболее частым показанием к эндоскопии верхних отделов во время беременности после кровотечения из верхних отделов желудочно-кишечного тракта [92].
Исход
Большинство исследований показали, что невирапин связан с благоприятным исходом для плода. Метаанализ 11 исследований Weigel et al. обнаружили сильную значимую связь между тошнотой и рвотой во время беременности и снижением риска выкидыша (общее отношение шансов = 0,36, 95% ДИ от 0,32 до 0,42) и отсутствие последовательной связи с перинатальной смертностью [93].Кроме того, было обнаружено, что женщины без NVP рожают раньше, чем женщины с NVP [94].
Однако в некоторых исследованиях сообщалось о неблагоприятных исходах, особенно когда невирапин считался тяжелым. Деушар и др. обнаружили повышенный риск задержки внутриутробного развития у женщин с тяжелым НВП, но не смогли объяснить потенциальное влияние противорвотных препаратов на рост плода [95]. Точно так же Zhou et al. обнаружили повышенный риск низкой массы тела при рождении у женщин с тяжелой формой НВП, вероятно, из-за пагубного влияния тошноты и рвоты на питание матери [96].
В проспективном исследовании 16 398 женщин не было обнаружено различий по врожденным аномалиям между женщинами с невирапином и без него [97]. Кроме того, ретроспективное исследование показало более низкий риск врожденных пороков сердца у детей, рожденных от женщин с ранним началом приема невирапина, требующих применения противорвотных средств, по сравнению с женщинами без тошноты [98].
Не совсем ясно, как NVP защищает развивающийся плод, однако было описано несколько теорий. Некоторые утверждают, что тошнота и рвота позволяют беременной женщине избегать или исключать продукты, которые могут быть тератогенными или вызывать аборт.Это может объяснить тесную временную связь между развитием отвращения к еде во время беременности и появлением тошноты [99]. NVP также может снизить потребление энергии и уровень анаболических гормонов, инсулина и фактора роста инсулина, что приводит к шунтированию дефицитных питательных веществ к плаценте и плоду [100].
Несмотря на благоприятное воздействие невирапина на плод, психосоциальные осложнения у беременных с невирапином значительны и, возможно, недооцениваются. В исследовании Smith et al. из 593 австралийских женщин с невирапином большинство сообщили, что их симптомы оказали серьезное негативное влияние на работу, домашние обязанности и воспитание детей, при этом 96% женщин сообщили о легком или умеренном дистрессе из-за тошноты, а 28% сообщили о дистрессе от умеренного до тяжелого [101].Точно так же исследование Mazzotta et al. канадских женщин обнаружили, что более сильная тошнота и рвота связаны с более частым чувством депрессии, рассмотрением вопроса о прерывании беременности, неблагоприятным воздействием на отношения женщин с их партнерами или их повседневную жизнь, а также с предполагаемой вероятностью того, что NVP нанесет вред их ребенку . Примечательно, что женщины с легкими симптомами также сообщали о тех же психосоциальных проблемах, что позволяет предположить, что тяжесть тошноты или рвоты неадекватно отражает дистресс, вызванный невирапином [2].
O’Brien и Naber также выявили значительную психосоциальную заболеваемость у женщин, страдающих невирапином. Они обнаружили, что пострадавшие женщины сообщали о снижении социальных обязательств и ухудшении отношений с супругами и детьми. Женщины с тяжелыми симптомами также сообщали о частой плаксивости, раздражительности, усилении нарушений сна и снижении настроения [102]. Используя краткую форму 36, Attard et al. обнаружили, что женщины с НВП имели более низкие показатели физического функционирования, физической роли, телесной боли, жизнеспособности, социального функционирования и эмоциональной роли в опросе, оценивающем качество жизни, по сравнению со здоровыми беременными контрольной группой на ранних сроках беременности и женщинами с хронической депрессией.Показатели психического здоровья женщин с НВП были аналогичны показателям женщин с депрессией [103].
Помимо того, что невирапин вызывает психосоциальную заболеваемость, он также создает значительное финансовое бремя. В 2002 г. стоимость тяжелого невирапина оценивалась приблизительно в 130 миллионов долларов, исходя из больничных расходов, связанных в среднем с 39 000 госпитализаций. Эта цифра, вероятно, сильно занижена, поскольку она не включает потерю производительности дома, оплату услуг врача или стоимость лечения [104].
Подсчитано, что каждая работающая женщина с невирапином теряет 206 рабочих часов [2] и что на невирапин приходится 28% всех отпусков по болезни во время беременности до 28-й недели [19]. Кроме того, работа Vallacott et al. показывает, что 50% пострадавших женщин считают, что эффективность их работы значительно снижена [105].
HYPEREMESIS GRAVDIARUM
Гиперемезис беременных (HG) — это состояние сильной тошноты и рвоты во время беременности, приводящее к водно-электролитному и кислотно-щелочному дисбалансу, дефициту питательных веществ и потере веса [8].Некоторые определяют его как возникновение более трех эпизодов рвоты в день, сопровождающихся кетонурией и потерей веса более 3 кг или 5% массы тела [63]. ГГ является наиболее частой причиной госпитализации на ранних сроках беременности и уступает только преждевременным родам на протяжении всей беременности [106]. В Соединенных Штатах более 36 000 женщин ежегодно госпитализируются по поводу ХГ, и стоимость лечения оценивается более чем в 250 миллионов долларов в год только на госпитализацию [107].В отличие от NVP, который связан с благоприятными исходами для плода, HG представляет значительный риск для здоровья матери и плода.
Диагностика и клинические признаки
ГГ проявляется в первом триместре беременности, обычно начиная с 4–5-й недели беременности. В дополнение к сильной тошноте и рвоте у 60% женщин с ГГ также наблюдается избыточное слюноотделение или слюнотечение [108]. Пациенты также могут жаловаться на симптомы гастроэзофагеального рефлюкса, такие как дискомфорт за грудиной и изжога. Уникальная количественная оценка рвоты и тошноты (PUQE) для беременных, которая рассчитывается с использованием количества часов тошноты в день, количества эпизодов рвоты в день и количества эпизодов позывов на рвоту в день, может использоваться для отслеживания тяжести симптомов. [109].
Пациенты могут иметь признаки обезвоживания, такие как сухость слизистых оболочек, тахикардия, плохой тургор кожи и постуральная гипотензия. Тяжело пораженные пациенты могут также иметь мышечную атрофию и слабость и/или изменения психического статуса.
Лабораторные нарушения у женщин с HG могут включать повышение азота мочевины в сыворотке крови, креатинина и гематокрита, а также кетонурию и увеличение удельного веса мочи. Кроме того, могут быть обнаружены электролитные нарушения, подтверждающие диагноз либо гипохлоремического метаболического алкалоза, либо метаболического ацидоза с выраженным сокращением объема [39].Уровни преальбумина (транстиретина в плазме) могут быть низкими, отражая плохой статус белкового питания у матери и, возможно, предсказывая более низкую массу тела плода при рождении [110]. Также возможен дефицит витаминов и минералов, таких как витамин B1 (тиамин), железо, кальций и фолиевая кислота [74].
Функциональные пробы печени могут отклоняться от нормы у 50% госпитализированных пациентов с ХГ [111]. Могут наблюдаться умеренная гипербилирубинемия (билирубин < 4 мг на децилитр) и/или повышение уровня щелочной фосфатазы вдвое по сравнению с верхней границей нормы [112].Умеренный трансаминит является наиболее частым нарушением функции печени, при котором уровни аланинаминотрансферазы (АЛТ) обычно превышают уровни аспартатаминотрансферазы (АСТ). Повышение уровня трансаминаз обычно в два-три раза превышает верхнюю границу нормы; однако сообщалось об уровнях выше 1000 ЕД/мл [113]. Аномальные печеночные пробы исчезают сразу же после прекращения рвоты.
Повышение уровня амилазы и липазы в сыворотке наблюдается у 10–15% женщин [39]. Одно исследование выявило повышенный уровень амилазы у 24% пациентов с ХГ [114].Считается, что это связано с избыточной выработкой амилазы слюнными железами, а не с секрецией поджелудочной железы, и является результатом, а не причиной ГГ [8].
Уровни тиреостимулирующего гормона могут быть низкими при ХГ из-за перекрестной реакции между альфа-субъединицей ХГЧ и рецептором ТТГ. В большинстве случаев этот биохимический тиреотоксикоз не имеет клинического значения, так как пациенты находятся в эутиреоидном состоянии. Уровень гормонов щитовидной железы обычно нормализуется без лечения после родов.
HG — это клинический диагноз, основанный на симптомах и исключении других состояний.Как и в случае с невирапином, для диагностики ГГ не требуется специального тестирования; тем не менее, УЗИ брюшной полости и таза может быть полезным для исключения других причин, таких как заболевание желчного пузыря, пузырный занос, а также для оценки многоплодной беременности. Дифференциальный диагноз включает невирапин, острый тиреоидит, расстройства пищевого поведения, заболевания желчевыводящих путей, вирусный гепатит и гастроэзофагеальную рефлюксную болезнь.
Исход
В отличие от NVP, HG связан с неблагоприятными исходами как для матери, так и для плода. В исследовании более 150 000 одноплодных беременностей младенцы, рожденные женщинами с гиперемезисом и низкой прибавкой массы тела при беременности (<7 кг), с большей вероятностью имели низкую массу тела при рождении, маловаты для гестационного возраста, родились до 37 недель беременности и имели мин. Оценка по шкале Апгар < 7 [5].
Общие материнские осложнения включают потерю веса, обезвоживание, дефицит питательных микроэлементов и мышечную слабость. Более тяжелые, хотя и редкие, осложнения включают разрывы Мэллори-Вейса, разрыв пищевода, энцефалопатию Вернике с корсаковским психозом или без него, центральный мостовой миелинолиз из-за быстрой коррекции тяжелой гипонатриемии, кровоизлияние в сетчатку и спонтанный пневмомедиастинум [47]. Также сообщалось о вазоспазме церебральных артерий из-за повышенной симпатической активности [115].
HG способствует возникновению многих психологических проблем и может привести к прерыванию нежелательной беременности и снижению вероятности попытки повторной беременности [116]. Пуршариф и др. обнаружили, что у 15% из 808 женщин с HG было по крайней мере одно прерывание беременности из-за болезни. Интересно, что у тех женщин, которые прервали беременность, не было более тяжелого заболевания, чем у женщин с ГГ, которые сохранили беременность, но в два раза чаще считали, что их врач безразличен или не обратил внимания на тяжесть их заболевания [117].
Долгосрочные последствия HG для матерей неизвестны. Несколько исследований показывают повышенный риск рака молочной железы [118]. Имеются также сообщения о повышенной частоте депрессии, посттравматического стрессового расстройства и различных неврологических расстройств [39].
Некоторые исследования не выявили повышенного риска неблагоприятных исходов для плода у женщин с ГГ. Башири и соавт., например, сообщили о более низкой частоте спонтанных ранних потерь беременности у женщин с ГГ по сравнению с общей популяцией и не обнаружили различий в перинатальных исходах [6].Однако в других исследованиях была обнаружена связь между ГГ и задержкой роста плода, преэклампсией и малым весом для гестационного возраста [119]. В ретроспективном исследовании 3068 женщин ГГ была связана с более ранними родами и меньшей массой тела при рождении. Эти исходы были наиболее вероятны у женщин, которые потеряли более 5% массы тела до беременности [120]. Точно так же Dodds et al. обнаружили более высокие показатели низкой массы тела при рождении, преждевременных родов, гибели плода у женщин с ХГ, которые в целом набрали менее 7 кг во время беременности [5].Многократные госпитализации по поводу ХГ, по-видимому, являются еще одним фактором риска снижения массы тела новорожденных при рождении [108].
Различные врожденные пороки развития чаще наблюдаются у женщин с ХГ [32]. К ним относятся синдром Дауна, дисплазия тазобедренного сустава, неопущение яичек, пороки развития скелета, дефекты центральной нервной системы и аномалии кожи. Сообщалось о коагулопатии плода и хондродисплазии из-за дефицита витамина К [121] с внутричерепным кровоизлиянием плода в третьем триместре [122].Некоторые виды рака у детей, такие как рак яичек или лейкемия, также были связаны с ГГ у матери, однако данные противоречивы [39].
ЛЕЧЕНИЕ
Целью лечения является облегчение симптомов при минимизации риска для матери и плода. Для достижения этого обычно необходим мультимодальный подход, адаптированный к каждому человеку. Методы лечения варьируются от простых диетических модификаций до медикаментозной терапии и полного родительского питания. Тяжесть симптомов и потеря веса матери помогают определить агрессивность лечения.PUQEscore и опросник по влиянию гиперемезиса на симптомы (HIS) можно использовать для оценки тяжести симптомов. Обновленная шкала PUQE оценивает симптомы в течение 24 часов [123], в то время как HIS учитывает психосоциальные факторы в дополнение к физическим симптомам [124].
Текущие исследования показывают, что лечение невирапином является субоптимальным. Одно недавнее проспективное исследование 283 женщин с невирапином в течение первого триместра показало, что только половине из них задавали вопрос об интенсивности и тяжести их симптомов, менее четверти спрашивали, мешают ли их симптомы их повседневным задачам и работе.В этом исследовании Lacasse et al только 27% женщин были предложены противорвотные средства, а еще 14% были рекомендованы немедикаментозные методы лечения [125].
Немедикаментозная терапия
Диетические меры
Начальная терапия невирапина и ГГ должна включать диетические изменения. Пораженные женщины должны избегать больших приемов пищи и вместо этого есть несколько небольших приемов пищи в течение дня, которые должны быть пресными и с низким содержанием жира, поскольку жирная пища может еще больше задержать опорожнение желудка. Употребление белка больше, чем углеводов, и употребление большего количества жидкости, чем твердой пищи, также может уменьшить тошноту, уменьшая желудочные аритмии, связанные с невирапином [82].Рекомендуются небольшие объемы соленых жидкостей, таких как электролитозамещающие спортивные напитки, а если запах горячей пищи является неприятным, следует приготовить холодную пищу [126].
Эмоциональная поддержка
Эмоциональную поддержку всегда должен оказывать медицинский работник. Кроме того, поддерживающая психотерапия, поведенческая терапия и гипнотерапия могут быть полезны для женщин с тяжелыми симптомами и/или для тех, у кого играют роль личностные особенности, супружеские или семейные конфликты [60].Цель психотерапии не в том, чтобы углубляться в психологию, которая может способствовать НВП, а в том, чтобы поощрять, объяснять, успокаивать и позволять пациенту выражать стресс [95].
Акупрессура/акупунктура
Акупрессура китайской акупунктурной точки Р6 (Нэйгуань) снижает тошноту у пациентов с тошнотой, вызванной химиотерапией, а также послеоперационной тошнотой и рвотой, и может быть полезна при лечении ГГ. В соответствии с принципом ци, приложение давления к этой точке блокирует аномальное замедление энергии и восстанавливает симптомы, связанные с точкой давления [13].Давление можно оказывать вручную или с помощью эластичных лент на внутренней стороне запястья. Кроме того, ReliefBand, электрический стимулятор нервов с батарейным питанием, который носится на запястье, недавно был одобрен FDA и может также использоваться для стимуляции участка P6 [127].
Доказательства акупрессуры противоречивы. Один обзор семи испытаний показал, что акупрессура точки Neiguan может облегчить симптомы тошноты [128]. Недавнее плацебо-контролируемое исследование с участием 60 женщин, принимавших невирапин, показало, что в группе лечения наблюдалось облегчение тошноты на следующий день после начала акупрессуры над местом P6, которое продолжалось до конца периода наблюдения.Для сравнения, в группе, получавшей акупрессуру на незначительном участке, наблюдалось первоначальное облегчение симптомов, но к 6-му дню симптомы вернулись и не отличались от группы, не получавшей лечения [129].
Хотя исследования преимуществ акупрессуры не дали окончательных результатов, некоторые эксперты считают, что это вмешательство должно быть предложено, поскольку не существует известных побочных эффектов [130].
Иглоукалывание менее изучено, но одно слепое рандомизированное контролируемое исследование с участием 593 женщин со сроком беременности менее 14 недель показало, что у женщин, получавших еженедельное лечение иглоукалыванием в течение 4 недель, было меньше тошноты и сухих рвотных позывов по сравнению с контрольной группой [131].Однако возможно, что состояние некоторых женщин улучшилось просто с увеличением гестационного возраста [13].
Имбирь
Имбирь — единственное немедикаментозное вмешательство, рекомендованное Американским колледжем акушерства и гинекологии [132]. Считается, что имбирь помогает улучшить НВП, стимулируя моторику желудочно-кишечного тракта и стимулируя выделение слюны, желчи и желудочного секрета. Было показано, что один компонент имбиря обладает такой же активностью, что и антагонист 5-HT3, ондансетрон.Кроме того, было обнаружено, что его экстракт ингибирует рост некоторых штаммов H. pylori [133].
В двойном слепом рандомизированном перекрестном исследовании 70% женщин с ГГ, получавших 250 мг порошкообразного корня имбиря четыре раза в день, предпочли период приема имбиря по сравнению с периодом приема плацебо. Женщины также сообщали о значительно большем облегчении симптомов при приеме имбиря. 4 дня обнаружили, что у женщин в группе лечения было значительное улучшение симптомов тошноты по сравнению с женщинами в группе плацебо ( P <.001) [135].
Что касается безопасности имбиря во время беременности, исследование случай-контроль с участием 187 беременных женщин не выявило увеличения частоты серьезных пороков развития при употреблении имбиря в первом триместре [136]. Однако существует теоретический риск кровотечения, поскольку имбирь ингибирует тромбоксансинтетазу и может ингибировать функцию тромбоцитов. Таким образом, одновременное использование антикоагулянтов с имбирем не рекомендуется [137].
Фармакологическое лечение
Пиридоксин-доксиламин
Комбинация пиридоксина (витамина В6) (категория А при беременности) и доксиламина (категория В), ранее доступная как бендектин, является единственным лекарственным средством, которое специально маркировано для лечения невирапина Управление по санитарному надзору за качеством пищевых продуктов и медикаментов.Он по-прежнему доступен в Канаде в таблетках с отсроченным высвобождением, содержащих 10 мг пиридоксина и 10 мг доксиламина, под торговым названием Диклектин.
Бенедектин был снят с продажи в 1983 году в США в связи с сообщениями о врожденных пороках развития при применении в первом триместре. Однако до его отмены 30 миллионов женщин принимали его в течение почти 25 лет. Несколько небольших рандомизированных контролируемых исследований подтверждают его эффективность [138]. Кроме того, метаанализ, который включал 170 000 воздействий, показал, что комбинация пиридоксин-доксиламин безопасна и не вызывает побочных эффектов у плода [139].Другие крупные исследования также не показали увеличения частоты врожденных аномалий по сравнению с фоновой частотой [140]. Тем не менее, Бенедектин остается вне рынка в Соединенных Штатах. Однако женщины могут сделать свой собственный препарат, объединив 10 мг пиридоксина с половинкой таблетки Унисома, который содержит 25 мг доксиламина.
В качестве альтернативы пиридоксин можно принимать отдельно. Хотя связи между уровнями пиридоксина и невирапином не обнаружено, в нескольких исследованиях было показано улучшение показателей тошноты у пациентов, принимавших пиридоксин с выраженной тошнотой [141], и уменьшение эпизодов рвоты по сравнению с женщинами, принимавшими плацебо [138].Нет известных доказательств токсичности витамина B6, однако в больших дозах пиридоксин был связан с обратимой периферической нейропатией у небеременных взрослых [13].
Противорвотные средства
Фенотиазины, хлорпромазин (торазин) и прохлорперазин (компазин), являются центральными и периферическими антагонистами дофамина, которые, как было показано, уменьшают симптомы невирапина и ГГ [142]. Они относятся к категории беременности С.
Исследование 12 764 беременных женщин показало незначительное повышение риска врожденных дефектов при применении фенотиазинов в первом триместре, особенно при применении хлорпромазина, однако потенциальные смешанные факторы, такие как употребление алкоголя и продолжительность лечения, не были выявлены. 143].Другое исследование показало, что у младенцев от матерей, принимавших хлорпромазин, были экстрапирамидные симптомы и желтуха; значительных нарушений постнатального развития не было [144].
Прометазин (Phenergan) не обладал тератогенными эффектами в одном исследовании [145], но в другом исследовании наблюдалось усиление врожденного вывиха бедра [146].
Активаторы
Метоклопрамид (Реглан) широко используется для лечения невирапина [147]. Это категория беременности B. Считается, что метоклопрамид улучшает симптомы за счет повышения давления в нижнем пищеводном сфинктере и увеличения транзита через желудочный тракт.Он также корректирует желудочные аритмии, стимулируя антральные сокращения и способствуя антродуоденальным сокращениям. Недавнее исследование показало, что 10 мг метоклопрамида, принимаемого каждые 8 часов, столь же эффективны для уменьшения количества эпизодов рвоты и улучшения самочувствия у женщин с ГГ во время их первой госпитализации, как и 25 мг прометазина, принимаемого каждые 8 часов в течение 24 часов. Профиль побочных эффектов был лучше в группе, получавшей метоклопрамид, с меньшей сонливостью, головокружением и дистонией [148].
Что касается безопасности, исследование 81 703 родов в период с 1998 по 2007 год в Израиле, в ходе которого метоклопрамид применялся у 4,2% женщин, не выявило повышенного риска серьезных врожденных пороков развития, низкой массы тела при рождении, преждевременных родов или перинатальной смерти при применении метаклопрамида. использовать [149]. Точно так же датское исследование 309 беременных женщин, принимавших метаклопрамид, не выявило повышенного риска [150].
Несмотря на свою эффективность, использование метоклопрамида ограничено его побочными эффектами, которые включают дистонию, беспокойство и сонливость.В 2009 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) добавило к метоклопрамиду предупреждение «черный ящик» из-за риска поздней дискинезии при хроническом применении.
Другие прокинетики, такие как домперидон и эритромицин, не изучались при применении невирапина [74].
Антигистаминные и антихолинергические препараты
Антигистаминные препараты косвенно влияют на вестибулярную систему, уменьшая стимуляцию рвотного центра [151]. Рандомизированные контролируемые исследования применения антигистаминных препаратов при невирапине ограничены; однако было показано, что меклизин (анитверт), дименгирдинат (драмамин) и дифенгирамин (бенадрил) контролируют симптомы лучше, чем плацебо [142].Кроме того, объединенные данные семи испытаний между 1951 и 1975 годами показали эффективность антигистаминных препаратов [152]. Метаанализ более 24 контролируемых исследований с участием более 200 000 беременных женщин показал, что антигистаминные препараты (в частности блокаторы Н2-рецепторов), назначаемые в течение первого триместра, не повышают риск тератогенного действия [153]. Хотя ранее считалось, что меклизин обладает тератогенным действием, теперь исследования показывают, что его безопасно использовать во время беременности [154]. Дименгидринат и дифенгидрамин имеют противоречивые результаты по безопасности [74].
В одном исследовании женщин, перенесших плановое кесарево сечение, было обнаружено, что трансдермальный скополамин более эффективен в уменьшении тошноты, рвоты и позывов на рвоту из-за эпидуральной морфиновой анальгезии по сравнению с плацебо [155]. Однако исследования по применению скополамина в первом триместре отсутствуют, поскольку скополамин может вызывать хромосомные аберрации и обмены сестринскими хроматидами в здоровых взрослых лимфоцитах и может приводить к врожденным порокам развития, включая деформацию конечностей и туловища [156].
Другие препараты
Ондансетрон (Зофран) (категория B при беременности) широко используется для лечения послеоперационной и вызванной химиотерапией тошноты и рвоты и в настоящее время является одним из наиболее часто назначаемых противорвотных средств [157].Считается, что он действует как центрально, так и периферически, блокируя серотониновые рецепторы в тонкой кишке и медуллярном рвотном центре [151]. Его безопасность при беременности была определена в недавнем исследовании, которое не показало значительного увеличения числа выкидышей, серьезных пороков развития или массы тела при рождении между младенцами, подвергшимися воздействию ондансетрона, и контрольной группой, не получавшей его [158].
Было проведено одно рандомизированное контролируемое исследование применения ондансетрона для лечения ХГ. В этом небольшом исследовании с участием 30 женщин не было выявлено преимуществ ондансетрона в дозе 10 мг внутривенно каждые 8 часов по мере необходимости по сравнению с прометазином в дозе 50 мг внутривенно каждые 8 часов с точки зрения тошноты, увеличения веса, дней госпитализации или общих доз препарата [46]. .Однако было обнаружено, что прометазин вызывает больший седативный эффект. Тем не менее, сообщения о случаях заболевания и широко распространенный клинический опыт подтверждают эффективность ондансетрона для лечения HG и его лучшую переносимость по сравнению с более ранними противорвотными средствами [159, 160].
Дроперидол (инапсин) является антагонистом дофамина, эффективным противорвотным средством при послеоперационной тошноте и рвоте. Небольшое исследование женщин с HG показало, что комбинация непрерывной инфузии дроперидола и болюсного внутривенного введения дифенгидрамина приводила к более коротким госпитализациям и меньшему количеству повторных госпитализаций по сравнению с исторической контрольной группой, которая получала другие формы парентеральной терапии.Кроме того, не было никаких существенных различий в материнских или перинатальных исходах [161]. Следует отметить, однако, что дроперидол имеет предупреждение черного ящика, поскольку он может вызывать удлинение интервала QT и сердечные аритмии [74].
Пероральные и внутривенные кортикостероиды использовались для рефрактерных случаев HG с переменными результатами. Считается, что они оказывают противорвотное действие на триггерную зону хеморецепторов в стволе головного мозга, а также постулируются для коррекции «относительной надпочечниковой недостаточности», вызванной HG, при которой гипоталамо-гипофизарно-надпочечниковая ось не может реагировать на повышенные потребности в кортизоле. во время ранней беременности.
В рандомизированном контролируемом исследовании 40 женщин с ГГ, получавших метилпреднизолон в дозе 16 мг перорально 3 раза в день в течение 3 дней с последующим 2-недельным снижением дозы, по сравнению с прометазином в дозе 25 мг перорально 3 раза в день в течение 2 недель, — госпитализация была обнаружена в группе, получавшей стероиды [162]. Другие исследования не показали статистически значимого преимущества кортикостероидов. Рандомизированное исследование Yost et al. не обнаружили значительного снижения числа посещений неотложной помощи или повторных госпитализаций при добавлении парентерального и перорального метилпреднизолона к режиму прометазина и метоклопрамида [163].
Нет утвержденных руководств по применению кортикостероидов при ХГ. Однако была предложена возможная схема: 48 мг метилпреднизолона вводят перорально или внутривенно в три приема в течение двух-трех дней. Если в течение трех дней ответа не наблюдается, рекомендуется прекратить лечение, так как ответ через 72 часа маловероятен [151].
Что касается безопасности, то недавний метаанализ показал небольшое увеличение основных пороков развития и 3,4-кратное увеличение расщелины рта у младенцев, матери которых принимали кортикостероиды в первом триместре [164].
В последнее время наблюдается интерес к препаратам, снижающим кислотность при лечении невирапином, поскольку одно недавнее когортное исследование показало, что у женщин с невирапином и изжогой и/или кислотным рефлюксом тошнота и рвота были более выраженными, чем у женщин без изжоги или кислотного рефлюкса [165]. Кроме того, последующие исследования показали, что лечение изжоги и/или рефлюкса приводит к улучшению показателей PUQE и показателей качества жизни [166].
Антациды, содержащие алюминий или кальций, являются терапией первой линии во время беременности при кислотном рефлюксе и изжоге и могут использоваться для лечения женщин с невирапином.Антациды, содержащие магний, связаны с нефролитиазом, гипотонией и респираторным дистресс-синдромом у плода и не рекомендуются во время беременности. Антациды, содержащие бикарбонаты, могут вызывать метаболический ацидоз плода и перегрузку жидкостью и также не рекомендуются [167].
Блокаторы h3 и ингибиторы протонной помпы можно безопасно использовать для лечения кислотного рефлюкса и/или изжоги у женщин с невирапином [168, 169].
Нутритивная поддержка
Женщинам с трудноизлечимыми симптомами, не поддающимися коррекции диеты и фармакологическому лечению и неспособными поддерживать вес за счет перорального приема пищи, может потребоваться пищевая поддержка.В этой популяции следует использовать внутривенную инфузионную терапию, энтеральное или парентеральное питание для предотвращения задержки внутриутробного развития плода, обезвоживания матери и недостаточности питания.
Роль внутривенной гидратации заключается в увеличении объема и восстановлении электролитов. Госпитализированным пациентам при необходимости можно быстро влить физиологический раствор или раствор Рингера с лактатом, а затем откорректировать их для соответствия диурезу. Внутривенно тиамин следует вводить перед любыми жидкостями, содержащими декстрозу, чтобы избежать энцефалопатии Вернике.Женщинам, которым требуется многократная госпитализация, может быть рекомендована внутривенная гидратация в домашних условиях [74].
Энтеральное зондовое питание и полное парентеральное питание следует рассмотреть, если внутривенная терапия не помогает уменьшить симптомы, а дефицит калорий сохраняется. Однако исследования энтерального питания при HG ограничены. В одном небольшом исследовании женщин с HG, получавших энтеральное питание с использованием назогастрального зонда 8-French, сообщалось об улучшении симптомов в течение 24 часов после установки зонда.Через 8 дней пациенты были выписаны в среднем на 43 дополнительных дня амбулаторного энтерального питания, после чего можно было возобновить пероральное питание [170].
Помимо назогастральных зондов, чрескожная эндоскопическая гастростомия (ЧЭГ) [171] успешно использовалась для поддержания питания у женщин с ГГ. Однако оба этих способа кормления ограничены риском усиления тошноты и рвоты, вызванных внутрижелудочным кормлением. Постпилорические зонды для кормления, как назоеюнальные [172, 173], так и чрескожные эндоскопические гастроеюноанастомозы [174] пытались снизить этот риск, однако смещение зондов [175] из-за продолжающейся рвоты, позывов на рвоту и свертывания желудка является частым осложнением. .Кроме того, назоэнтеральные зонды, как назогастральные, так и назоеюнальные, плохо переносятся многими женщинами из-за эстетических соображений и физического дискомфорта. Недавно хирургическая еюностомия была описана как альтернативный способ доставки питания женщинам с HG. В одном небольшом исследовании пяти женщинам с HG была выполнена хирургическая еюностомия во втором триместре. Изотонические кормления через зонд вводили до целевого показателя калорийности. Прибавка в весе матери наблюдалась в 5 из 6 беременностей, и все беременности закончились срочными родами.Серьезных осложнений не произошло, что позволяет предположить, что еюностомия может быть безопасным и эффективным способом нутритивной поддержки у женщин с ХГ [176].
Женщинам, которые не переносят энтеральное питание, следует рассмотреть возможность парентерального питания. Эта терапия, однако, является дорогостоящей и связана со значительной материнской заболеваемостью. Руссо-Стейглиц и др. сообщили о частоте осложнений 9% при парентеральном питании через периферически установленные центральные катетеры во время беременности и о 50% частоте осложнений при центрально вставленных катетерах.Инфекция и тромбоз были двумя наиболее часто встречающимися осложнениями, и предполагалось, что они являются результатом связанной с беременностью гиперкоагуляции и иммунологической супрессии [177]. Holmgren et al. также показали высокую частоту осложнений у женщин, получавших парентеральное питание через PICC. В исследовании 94 женщин с HG 66,4% из тех, кто получал парентеральное питание через PICC, нуждались в лечении тромбоэмболии, инфекции или того и другого. Пациентки на парентеральном питании также имели более высокую частоту неонатальных осложнений, включая госпитализацию в отделение интенсивной терапии новорожденных, малый размер для гестационного возраста, прерывание беременности из-за ГГ и потерю плода по сравнению с женщинами, получавшими энтеральное питание [178].Таким образом, парентеральное питание, хотя оно может быть более переносимым для пациентов, следует зарезервировать для отдельных пациентов с HG.
Информация для авторов
Ноэль М. Ли, Школа медицины и общественного здравоохранения Университета Висконсина, Медицинский фонд Университета Вашингтона, здание столетия, 1685 Highland Avenue, Madison, WI 53705, телефон: (608) 263-1995, факс: (608) 265-5677.
Сумона Саха, Отделение гастроэнтерологии и гепатологии, Школа медицины и общественного здравоохранения Висконсинского университета, Медицинский фонд Университета Вашингтона, здание столетия, 1685 Хайленд-авеню, комната 4224, Мэдисон, Висконсин 53705, телефон: (608) 263-1995, факс: (608) 265-5677.
Тошнота и рвота при беременности
Введение
Тошнота и рвота являются обычным явлением во время беременности, которым страдают 70–80% всех беременных женщин. Хотя у большинства женщин тошнота и рвота при беременности (НВП) имеют симптомы, ограниченные первым триместром, у небольшого процента женщин наблюдается длительное течение с симптомами, продолжающимися до родов. У женщин с тяжелой тошнотой и рвотой во время беременности может быть гиперемезис беременных (HG), состояние, отличное от NVP, которое, если его не лечить, может привести к значительной заболеваемости матери и плода.
Различные метаболические и нервно-мышечные факторы вовлечены в патогенез невирапина и HG; однако их точная причина неизвестна. Следовательно, лечение NVP и HG может быть затруднено, поскольку не известны ни оптимальные цели лечения, ни полные эффекты потенциальных методов лечения на развивающийся плод. В этой статье рассматриваются эпидемиология, патология, диагностика, исходы и лечение невирапина и HG.
Эпидемиология
По оценкам, 70–80% беременных женщин получают невирапин [1].В Соединенных Штатах и Канаде это означает примерно 4 000 000 и 350 000 женщин, которые страдают каждый год соответственно [2].
НВП чаще встречается в западных странах и у городского населения и редко встречается у африканцев, коренных американцев, эскимосов и большинства азиатских популяций [3]. Лишь в нескольких исследованиях изучалось расовое распределение невирапина в данной популяции. Одно такое исследование, проведенное в Канаде с участием 367 женщин, показало, что азиаты и чернокожие реже сообщали о симптомах невирапина, чем представители европеоидной расы.Социально-демографические факторы не учитывали расовые/этнические различия в распространенности заболевания, что позволяет предположить, что могут играть роль генетические и/или культурные факторы [4].
HG встречается редко по сравнению с NVP и встречается в 0,3–2% всех беременностей [5]. Заболеваемость зависит от этнической принадлежности [6] и колеблется от 3 до 20 на 1000 беременностей [7]. Он чаще диагностируется у женщин в Индии, Пакистане, Азии, Новой Зеландии по сравнению с европейцами, американскими индейцами и эскимосами [8].
Факторы риска
Данные Совместного перинатального проекта, одного из крупнейших на сегодняшний день исследований беременных женщин, показали, что невирапин чаще встречается у молодых женщин, первобеременных, женщин с образованием менее 12 лет, некурящих и женщины с ожирением [9]. О повышенном риске невирапина в первом триместре также сообщалось у женщин с многоплодной беременностью по сравнению с женщинами с одноплодной беременностью (87% против 73%, p<0,01) [10].
НВП был связан с низким уровнем дохода и статусом занятости неполный рабочий день [11]).Было обнаружено, что домохозяйки также подвергаются повышенному риску, в то время как женщины, работающие в качестве белых воротничков, по-видимому, защищены [12]. Однако остается неясным, является ли статус занятости истинным фактором риска для невирапина или искажающим фактором, поскольку затронутые женщины могут прекратить работу из-за своих симптомов. Точно так же их решение не работать вне дома может быть связано с многодетностью и необходимостью заботиться о других детях [13].
Материнская генетика также может служить фактором риска для невирапина. Данные большой популяции норвежских близнецов показывают более широкое использование лекарств от тошноты во время беременности среди монозиготных близнецов женского пола по сравнению с дизиготными близнецами женского пола [14].Кроме того, более высокие уровни тошноты были обнаружены у женщин, матери которых испытывали тошноту во время беременности [15]. Также было показано, что личный анамнез NVP является фактором риска для NVP при последующих беременностях [15]; однако этот вывод не был последовательным в разных исследованиях [16]
Другие факторы риска для невирапина включают личную историю укачивания, возможно, из-за общего вестибулярного механизма [17] и мигреней в анамнезе [18]. Женщины, у которых в анамнезе была тошнота при приеме эстрогенсодержащих пероральных контрацептивов, также подвержены повышенному риску невирапина [19].
Расположение желтого тела также может служить фактором риска невирапина. Ультразвуковые исследования показали, что беременные чаще испытывают тошноту и рвоту при наличии желтого тела в правом яичнике [20]. Это может быть связано с различиями в венозном оттоке между левым и правым яичником и более высокой концентрацией половых стероидов, когда желтое тело находится на правой стороне [21].
Более высокое суточное потребление общего жира, особенно насыщенных жиров, до беременности увеличивает риск госпитализации по поводу невирапина [22].Курение до беременности и прием витаминов до и/или на ранних сроках беременности связаны со снижением риска невирапина [23]. Также было обнаружено, что употребление алкоголя матерью до зачатия защищает от NVP [24].
Факторы риска HG аналогичны факторам риска NVP. К ним относятся многоплодная беременность, трофобластическая болезнь, HG в предшествующей беременности, аномалии плода, такие как триплоидия, трисомия 21 и водянка плода, а также нерождение плода [25]. Семейный анамнез HG также является фактором риска: примерно 28% женщин сообщают о HG в анамнезе у своих матерей и 19% сообщают, что их сестры имели аналогичные симптомы [26].Дополнительные факторы риска включают семейный или партнерский статус и возраст старше 30 лет. Курение сигарет может быть защитным [27].
Индекс массы тела матери оценивался как фактор риска ГГ с неоднозначными результатами. В исследовании Depue et al ожирение увеличивало риск ГГ на 50% [28]. Работа Cedergren et al. однако обнаружили, что низкий индекс массы тела (<20 кг/м2) был связан с 40% более высоким риском ХГ, а ожирение снижало риск госпитализации по поводу ХГ [29].Более недавнее исследование 33 647 женщин в Норвегии показало, что недостаточный или избыточный вес увеличивает риск ГГ, но только у некурящих [30]. Постулируется, что женщины с недостаточным весом и низкими индексами массы тела имеют низкий уровень эстрогена до беременности и, таким образом, могут иметь преувеличенный ответ в течение первого триместра, когда уровень эстрогена резко возрастает [31]. Напротив, у женщин с ожирением жировые отложения могут нейтрализовать плацентарные факторы, которые, как считается, способствуют патогенезу [29].
Что касается пола плода, то в нескольких исследованиях была обнаружена связь между ГГ и женским полом плода.Используя данные Шведского медицинского реестра рождений, Kallen et al. обнаружили, что HG был чрезмерно представлен в 3068 беременностях, когда ребенок был девочкой [32]. Точно так же в исследовании беременных женщин, госпитализированных с HG в первом триместре, вероятность рождения девочки была на 50% выше в случаях по сравнению со здоровыми беременными в контрольной группе (ОШ 1,5, 95% ДИ 1,4, 1,7) [33].
Патогенез
Метаболические и гормональные факторы
Хотя точный патогенез НВП и ГГ неизвестен, общепризнано, что рвота во время беременности является результатом различных метаболических и эндокринных факторов, многие из которых имеют плацентарное происхождение.Наиболее значимым фактором является хорионический гонадотропин человека (ХГЧ). Эта связь между ХГЧ и невирапином в значительной степени основана на временном соотношении между пиком невирапина и пиком продукции ХГЧ, которые происходят между 12 и 14 неделями беременности. Кроме того, тошнота и рвота часто усиливаются у беременных с состояниями, связанными с повышенным уровнем ХГЧ, такими как молярная беременность, многоплодная беременность и синдром Дауна [13]. Более высокие уровни ХГЧ в моче [34] и в сыворотке также были обнаружены у женщин с невирапином по сравнению с бессимптомными [35].Кроме того, исследование Goodwin et al. обнаружили, что концентрации ХГЧ положительно коррелируют с выраженностью тошноты и рвоты у женщин с ХГ [36].
Несмотря на множество исследований, связывающих уровень ХГЧ с невирапином и гормоном роста, другие не обнаружили связи между уровнем ХГЧ в сыворотке беременных женщин в течение первого триместра и частотой или интенсивностью тошноты и рвоты. В исследовании Soules et al. даже в подгруппе женщин с пузырным заносом, у которых уровни ХГЧ у женщин были в 5-10 раз выше, чем в контроле, корреляции обнаружено не было [37].Кроме того, исследования показали, что высокие уровни ХГЧ связаны с задержкой роста плода и преждевременными родами [38], в то время как невирапин, по-видимому, защищает от преждевременных родов, что делает маловероятным то, что ХГЧ является единственным фактором патогенеза невирапина.
Предполагается, что различные биологические формы (то есть изоформы) ХГЧ могут объяснить вариабельность между уровнями ХГЧ и тошнотой и рвотой у здоровых и больных людей [39]. Каждая изоформа ХГЧ имеет уникальный период полувыведения и активность в отношении рецепторов лютеинизирующего гормона и тиреотропного гормона (ТТГ).Изоформы без карбоксиконцевой части имеют более короткий период полувыведения, но являются более сильными стимуляторами рецепторов лютеинизирующего гормона и ТТГ. Напротив, гипергликозилированный ХГЧ имеет более длительный период полувыведения и большую продолжительность действия [40]. Эти различные изоформы ХГЧ, вероятно, являются результатом генетических факторов или долгосрочных изменений окружающей среды, которые, таким образом, могут объяснить различия в заболеваемости ХГ, обнаруженные в разных популяциях. Помимо изменчивости изоформ, мутации рецептора ХГЧ также могут объяснить некоторую вариабельность взаимоотношений между невирапином и ХГЧ [39].
Гормоны яичников, эстроген и прогестерон, также участвуют в патогенезе невирапина и гипергидроза. Известно, что некоторые женщины испытывают тошноту при приеме оральных контрацептивов. Кроме того, состояния с высокой концентрацией эстрогена, такие как низкий паритет и высокий индекс массы тела матери, были связаны с более высокой частотой ГГ [28]. Считается, что эстроген вносит свой вклад в HG, стимулируя выработку оксида азота с помощью синтетазы азотоксидазы, которая, в свою очередь, расслабляет гладкие мышцы, замедляя время желудочно-кишечного транзита и опорожнение желудка.
Ярнфельт и др. сообщили о значительной связи между рвотой беременных и непереносимостью пероральных контрацептивов в анамнезе [40]. Используя более количественный подход, Depue et al. обнаружили, что средние уровни общего эстрадиола на 26% выше, а средние уровни способности связывания половых гормонов и глобулинов на 37% выше у пациентов с HG, чем в контрольной группе после поправки на гестационный возраст. 28]. Однако важно отметить, что, как и взаимосвязь между ХГЧ и невирапином, взаимосвязь между уровнями эстрогена и невирапином была противоречивой в разных исследованиях [35].Обзор 17 исследований показал положительную связь между невирапином и эстрогеном только в 5 исследованиях [41]. Кроме того, пик уровня эстрогена приходится на третий триместр беременности, в то время как ГГ имеет тенденцию к улучшению на поздних сроках беременности [8].
Прогестерон в сочетании с эстрогеном также может играть роль в NVP. Прогестерон снижает сократимость гладкой мускулатуры и может изменить опорожнение желудка и привести к усилению тошноты и рвоты. Используя эластогастографию после стандартного приема пищи, Walsh et al. показали, что такое же медленноволновое нарушение желудочного ритма, обнаруженное у женщин с невирапином, может быть вызвано у небеременных женщин монотерапией прогестероном или в комбинации с эстрадиолом в дозах, которые воспроизводят уровни при беременности [42].Другие исследования, однако, не обнаружили существенной разницы между уровнями прогестерона у женщин с невирапином или без него [28].
Роль плацентарного простагландина E2 (PGE2) также оценивалась в патогенезе NVP из-за его влияния на гладкую мускулатуру желудка [43]. ХГЧ стимулирует плацентарный PGE2 и, как и ХГЧ, достигает пика между 9 и 12 неделями беременности. Норт и др. определили количество PGE2 в материнской сыворотке и обнаружили, что уровни были выше во время периодов тошноты и рвоты у 18 женщин на ранних сроках беременности по сравнению с бессимптомными периодами.Они также оценили уровни интерлейкина-1 бета и фактора некроза опухоли альфа у матери и обнаружили, что они были одинаковыми в течение симптоматического и бессимптомного периодов [44].
В связи с его ролью в вызванных химиотерапией тошноте и рвоте, серотонин также предположительно способствует развитию невирапина. Исследование Borgeat et al. однако не выявили различий в уровне серотонина среди беременных женщин с ХГ, бессимптомных беременных женщин и небеременных женщин [45]. Кроме того, рандомизированное контролируемое исследование, сравнивающее антагонист серотониновых 5-HT3-рецепторов, онданстерон, с прометазином, не выявило существенной разницы в контроле симптомов [46].
Из-за перекрестной реактивности между ХГЧ и рецептором тиреостимулирующего гормона (ТТГ) дисфункция щитовидной железы также изучалась как возможный механизм развития невирапина и ГГ. На самом деле, аномальные результаты функции щитовидной железы обнаруживаются у двух третей женщин с ГГ [36]. Этот «биохимический тиреотоксикоз» характеризуется подавлением ТТГ и слегка повышенным уровнем FT4. Несмотря на эти лабораторные отклонения, женщины с HG, как правило, находятся в эутиреоидном состоянии без предшествующих заболеваний щитовидной железы, отсутствия зоба и отрицательных антитиреоидных антител [47].Кроме того, исследования не выявили взаимосвязи между дисфункцией щитовидной железы и тяжестью симптомов [48], и почти у всех женщин с ХГ уровень ТТГ в норме к 20 нед беременности без какого-либо вмешательства [49].
Недавно была предложена связь между гормоном лептином и HG. Было обнаружено, что повышенный уровень лептина в сыворотке во время беременности, возможно, в результате увеличения общей жировой массы и продукции плаценты, значительно выше у пациенток с HG по сравнению со здоровыми беременными контрольной группой [50, 51].Лептин может способствовать ГГ за счет увеличения секреции ХГЧ за счет паракринного действия плаценты или за счет снижения аппетита и усиления тошноты и рвоты. Примечательно, однако, что другие проспективные когортные исследования не обнаружили аналогичной статистически значимой разницы в уровнях лептина в сыворотке при HG между пациентами и контрольной группой [52, 53].
Также было высказано предположение, что у женщин с HG возникает нарушение регуляции иммунной системы. В сыворотке крови матери были обнаружены повышенные концентрации свободной ДНК клеток плода [54], вызывающие гиперактивный материнский иммунный ответ и повреждение трофобласта.Кроме того, нормальный сдвиг во время беременности, при котором типы Т-хелперов переходят в Т-хелперы типа 1, более преувеличен у женщин с ХГ [55]. Это, в свою очередь, приводит к повышенному высвобождению интерлейкина-4, а также фактора некроза опухоли-альфа, оба из которых были связаны с HG [56]. Также было обнаружено, что аденозин повышен при HG, и его роль заключается в ослаблении TNF-альфа [57]. В проспективном исследовании [58] также было обнаружено, что уровни интерлейкина-6 повышаются при HG, а также повышаются уровни иммуноглобулина G (IgG), IgM, уровни комплемента и количество лимфоцитов [59].Однако точно определить роль этих иммунологических факторов нельзя, так как при голодании иммунная система обычно угнетается, а не активируется; таким образом, возможно, усиление иммунных факторов, наблюдаемое при HG, может быть попыткой ограничить прогрессирование HG [8].
Другие гормоны, в том числе тиреотропный гормон, гормон роста, пролактин, адренокортико-стимулирующий гормон, кортизол, лютеинизирующий гормон и фолликулостимулирующий гормон, также оценивались и, как считается, не вносят вклад в патогенез невирапин [60].
Helicobacter pylori
Повышенная частота инфицирования Helicobacter pylori (H. pylori) наблюдалась у женщин с ГГ, и в настоящее время считается, что она играет роль в ее патогенезе. Фриго и др. обнаружили, что 90,5% женщин с HG были H. plyori IgG положительными по сравнению с 46,5% в контрольной группе [61]. Багис и др. использовали золотой стандарт тестирования, гистологическое исследование биопсии слизистой оболочки, и обнаружили, что 95% пациентов с HG дали положительный результат на H.pylori по сравнению с 50% в контрольной группе. Они также обнаружили более высокую плотность H. pylori в антральном отделе и теле желудка у пациентов с HG, что позволяет предположить возможную связь между плотностью H. pylori и тяжестью симптомов [62].
Систематический обзор 2007 г., в котором оценивались 14 исследований типа «случай-контроль» с 1966 по 2007 г., выявил значительную связь между материнской инфекцией H.pylori и HG в 10 исследованиях. Отношение шансов в исследованиях варьировалось от 0.от 55 до 109,33 [63]. Аналогичным образом обновленный систематический обзор и метаанализ 25 исследований 2009 г. показали, что объединенное отношение шансов составляет 3,32 (95% доверительный интервал: 2,25–4,90) для инфекции H. pylori у женщин с HG [64]. Примечательно, что в обоих обзорах была обнаружена высокая гетерогенность исследований.
Инфицирование H. pylori во время беременности может произойти из-за вызванных стероидными гормонами изменений pH желудка [65] и/или повышенной восприимчивости из-за изменений гуморального и клеточно-опосредованного иммунитета [66].Однако нет четких доказательств того, что беременность предрасполагает к инфекции de novo H. pylori . Напротив, было высказано предположение, что H. pylori может усугубить вызванные гормонами изменения нервной и электрической функции желудка и, таким образом, увеличить риск для инфицированных женщин оказаться в более тяжелой форме тошноты и рвоты. рвота [67].
Хотя связь между H. pylori и HG интригует, важно отметить, что инфекция не обязательно коррелирует с симптомами.На самом деле у большинства инфицированных женщин заболевание протекает бессимптомно [8]. В исследовании Weyermann et al. 23% из 898 родильниц дали положительный результат на H. pylori при дыхательном тесте с 13C-мочевиной; однако положительный результат не коррелировал с симптомами тошноты, рвоты или рефлюкса во время беременности [68]. Точно так же Wu et al. обнаружили, что 69% беременных женщин являются сероположительными в отношении H. pylori по сравнению с 50% в общей популяции, однако не обнаружили никакой корреляции между статусом антител и желудочно-кишечными симптомами [69].
Почему H. pylori нельзя точно связать с невирапином, а HG связывают с несколькими факторами. Во-первых, в большинстве исследований для оценки наличия инфекции использовалось тестирование на антитела. Однако серологическое тестирование на H. pylori не может отличить активную инфекцию от перенесенной инфекции [70], а активная и перенесенная инфекция могут по-разному влиять на симптомы. Во-вторых, в большинстве исследований не оценивался и/или не учитывался штамм H. pylori . Ассоциированный с цитотоксином белок гена A (CagA) является маркером учащения пептических язв и связан с более агрессивным штаммом H pylori [71].Только одно исследование, включенное в метаанализ 2009 г., оценивало патогенность CagA. В этом исследовании, проведенном Xia et al., положительная реакция на CagA была более распространена у пациентов с HG [72].
Лечение приводит к эрадикации H. pylori у большинства пациенток, однако в настоящее время нет рекомендаций по оценке или лечению H. pylori во время беременности, поскольку последующее облегчение симптомов HG широко не изучалось. Сообщения о клинических случаях и серии случаев позволяют предположить, что лечение и эрадикация 90–105 H.pylori может уменьшить тошноту и рвоту во время беременности, и его следует рассматривать у пациенток с трудноизлечимыми симптомами [73]. Однако необходимы более масштабные исследования, чтобы определить, следует ли и когда начинать лечение во время беременности, учитывая опасения по поводу безопасности лекарств. В настоящее время специалисты рекомендуют после завершения беременности и лактации проводить тройную терапию в течение двух недель [74].
Нарушение моторики желудочно-кишечного тракта
Изменения давления в состоянии покоя нижнего пищеводного сфинктера (НПС) и перистальтики пищевода связаны с невирапином.Хотя эти изменения чаще связаны с изжогой во время беременности, гастроэзофагеальная рефлюксная болезнь (ГЭРБ) может вызывать атипичные симптомы, такие как тошнота [75], и способствовать развитию невирапинов. Эстроген и прогестерон являются вероятными медиаторами нарушения моторики пищевода при беременности, при этом эстроген служит праймером, а прогестерон вызывает релаксацию НПС [76].
Изменения желудочной ритмической активности могут способствовать НВП. Нормальная миоэлектрическая активность желудка приводит к медленному распространению волны от проксимального отдела тела к дистальному отделу антрального отдела со скоростью 3 цикла в минуту (имп/мин).Нарушение ритма в виде увеличения или уменьшения распространения медленных волн связано с тошнотой [74]. Используя эластогастрографию (EGG), Koch et al. продемонстрировали, что лица с нормальной медленноволновой активностью реже жаловались на тошноту во время беременности [77]. Напротив, люди с более высокими или более низкими показателями чаще жаловались на тошноту. Точно так же Riezzo et al. обнаружили, что беременные женщины без симптомов тошноты и рвоты на момент записи ЭГГ имеют нормальную миоэлектрическую активность 3 имп/мин.Они также обнаружили, что беременные женщины с невирапином имели более нестабильную активность EGG по сравнению с женщинами после добровольных абортов и небеременными женщинами из контрольной группы. Они предположили, что это может быть связано с восстановлением нормальной картины медленных волн желудка после аборта после нормализации уровней эстрадиола и прогестерона [78].
Примечательно, однако, что многие исследования не обнаружили различий в перистальтике желудка между беременными и небеременными женщинами. С помощью сцинтографии желудка не было обнаружено существенных различий в скорости опорожнения жидкости у беременных женщин до добровольного аборта, через 6 недель после аборта и у небеременных женщин контрольной группы [79].Используя методы разбавления красителя феноловым красным, Davison et al. обнаружили задержку опорожнения желудка во время родов, но не в третьем триместре по сравнению с небеременными контрольными женщинами [80]. Точно так же исследования с использованием парацетамола не показали задержки опорожнения желудка в первом, втором или третьем триместре [81].
Изменения моторики желудка при беременности объясняются высоким уровнем прогестерона. Кроме того, на поздних сроках беременности сдавление увеличенной маткой может способствовать симптомам.
Состав пищи также может играть патогенную роль в NVP.Джеднак и др. продемонстрировали, что прием пищи с преобладанием белка был связан с уменьшением симптомов и коррекцией медленноволновой аритмии. Прием пищи с преобладанием углеводов или жиров не влиял на симптомы или медленноволновую аритмию [82].
Наконец, время прохождения по тонкой кишке было оценено в отношении патогенеза NVP. Используя водородный дыхательный тест с лактулозой, косвенный показатель времени прохождения по тонкой кишке, Lawson et al. обнаружили, что время транзита удлиняется во втором и третьем триместре по сравнению с первым триместром, причем самые длинные времена были обнаружены, когда уровни прогестерона были самыми высокими [83].Уолд и др. использовали аналогичные методы и обнаружили, что время транзита увеличивается в третьем триместре, когда уровни прогестерона и эстрогена были высокими по сравнению с послеродовым периодом [84]. Однако в обоих этих исследованиях задержка кишечного транзита не коррелировала с невирапином.
Психосоциальные факторы
Ранние исследования предполагали, что НВП может быть психосоматическим заболеванием, при котором рвота представляет собой интрапсихический конфликт. Некоторые предполагают, что NVP является проявлением подсознательной попытки беременной женщины отказаться от нежелательной беременности [85], поскольку исследования показали, что у женщин с NVP в первом триместре чаще бывают незапланированные или нежелательные беременности [86].
ГГ также ассоциируется с психологическими расстройствами, а именно невротическими наклонностями, истерией, неприятием женственности, неприятием беременности, а также с депрессией и психологическим стрессом, связанным с бедностью и семейными конфликтами [8]. Однако недавние исследования не выявили определенных психогенных причин ГГ [87, 88]. Некоторые, следовательно, утверждают, что социокультурные факторы, а не научные данные, привели к тому, что HG маркируется как психологически обусловленное состояние, и что более вероятно, что психологические нарушения, такие как депрессия, являются результатом, а не причиной HG [89].
Таким образом, хотя NVP и HG, вероятно, не являются результатом конверсионного расстройства или другого психологического расстройства, общепризнано, что у пострадавших женщин возникают психологические реакции, которые переплетаются с их физическими симптомами и, возможно, усугубляют их.
Диагностика и клинические признаки
Анамнез и медицинский осмотр
Несмотря на популярное использование термина «утренняя тошнота», невирапин сохраняется в течение дня у большинства больных женщин и, как было установлено, ограничивается утром менее чем у 2% женщин [90].Он часто начинается в течение нескольких недель после отсутствия менструации и поэтому в большинстве культур карикатурно изображается как начальный признак беременности. Симптомы обычно достигают пика между 10 и 16 неделями беременности и обычно исчезают после 20 недель. Однако до 10% женщин продолжают иметь симптомы после 22 недель [90].
В то время как обезвоживание и ортостаз могут возникать у женщин с HG, у большинства женщин с NVP показатели жизненно важных функций в норме, а физикальный осмотр является благоприятным. Однако следует провести тщательное обследование брюшной полости, чтобы исключить перитонит и другие внутрибрюшные причины тошноты и рвоты.
Дифференциальный диагноз
Учитывая высокую распространенность невирапина, тошнота и рвота в первом триместре обычно связаны с невирапином. Однако при наличии изменений в работе кишечника, боли в животе и рвоте желчью следует провести соответствующие исследования для исключения других причин. Дифференциальный диагноз невирапина включает гастроэзофагеальную рефлюксную болезнь, язвенную болезнь, непроходимость тонкой кишки, острый холецистит, желчнокаменную болезнь, панкреатит, а также аппендицит, гастроэнтерит, нефролитиаз, пиелонефрит и гепатит [74]
Диагностические и лабораторные исследования
Для диагностики невирапина не рекомендуются никакие специальные лабораторные исследования, кроме теста на беременность.Однако другие тесты могут быть полезны для исключения других причин тошноты и рвоты. Лейкоцитоз не должен наблюдаться при невирапине и может указывать на инфекционную или воспалительную причину, такую как холецистит, инфекция мочевыводящих путей и панкреатит. Повышение уровня аминотрансфераз может свидетельствовать о хроническом гепатите. Аномальный ТТГ может указывать на гипотиреоз или гипертиреоз, оба из которых могут вызывать тошноту и рвоту. Повышение уровня глюкозы в сыворотке может указывать на диабет и может вызывать тошноту и рвоту за счет снижения сократительной способности антрального отдела и ускорения желудочной аритмии [91].
Рентгенография обычно не требуется для диагностики невирапина. УЗИ органов малого таза можно использовать для документирования беременности и оценки состояний, повышающих риск невирапина, таких как многоплодная беременность. Рентген брюшной полости, как правило, бесполезен и, хотя представляет небольшой риск для плода, все еще относительно противоречив в течение первого триместра.
Верхнюю эндоскопию можно безопасно проводить во время беременности и исключить гастрит и ЯБ как причины тошноты и рвоты во время беременности.В одном крупном центре тошнота и рвота были вторым наиболее частым показанием к эндоскопии верхних отделов во время беременности после кровотечения из верхних отделов желудочно-кишечного тракта [92].
Исход
Большинство исследований показали, что невирапин связан с благоприятным исходом для плода. Метаанализ 11 исследований Weigel et al. обнаружили сильную значимую связь между тошнотой и рвотой во время беременности и снижением риска выкидыша (общее отношение шансов = 0,36, 95% ДИ от 0,32 до 0,42) и отсутствие последовательной связи с перинатальной смертностью [93].Кроме того, было обнаружено, что женщины без NVP рожают раньше, чем женщины с NVP [94].
Однако в некоторых исследованиях сообщалось о неблагоприятных исходах, особенно когда невирапин считался тяжелым. Деушар и др. обнаружили повышенный риск задержки внутриутробного развития у женщин с тяжелым НВП, но не смогли объяснить потенциальное влияние противорвотных препаратов на рост плода [95]. Точно так же Zhou et al. обнаружили повышенный риск низкой массы тела при рождении у женщин с тяжелой формой НВП, вероятно, из-за пагубного влияния тошноты и рвоты на питание матери [96].
В проспективном исследовании 16 398 женщин не было обнаружено различий по врожденным аномалиям между женщинами с невирапином и без него [97]. Кроме того, ретроспективное исследование показало более низкий риск врожденных пороков сердца у детей, рожденных от женщин с ранним началом приема невирапина, требующих применения противорвотных средств, по сравнению с женщинами без тошноты [98].
Не совсем ясно, как NVP защищает развивающийся плод, однако было описано несколько теорий. Некоторые утверждают, что тошнота и рвота позволяют беременной женщине избегать или исключать продукты, которые могут быть тератогенными или вызывать аборт.Это может объяснить тесную временную связь между развитием отвращения к еде во время беременности и появлением тошноты [99]. NVP также может снизить потребление энергии и уровень анаболических гормонов, инсулина и фактора роста инсулина, что приводит к шунтированию дефицитных питательных веществ к плаценте и плоду [100].
Несмотря на благоприятное воздействие невирапина на плод, психосоциальные осложнения у беременных с невирапином значительны и, возможно, недооцениваются. В исследовании Smith et al. из 593 австралийских женщин с невирапином большинство сообщили, что их симптомы оказали серьезное негативное влияние на работу, домашние обязанности и воспитание детей, при этом 96% женщин сообщили о легком или умеренном дистрессе из-за тошноты, а 28% сообщили о дистрессе от умеренного до тяжелого [101].Точно так же исследование Mazzotta et al. канадских женщин обнаружили, что более сильная тошнота и рвота связаны с более частым чувством депрессии, рассмотрением вопроса о прерывании беременности, неблагоприятным воздействием на отношения женщин с их партнерами или их повседневную жизнь, а также с предполагаемой вероятностью того, что NVP нанесет вред их ребенку . Примечательно, что женщины с легкими симптомами также сообщали о тех же психосоциальных проблемах, что позволяет предположить, что тяжесть тошноты или рвоты неадекватно отражает дистресс, вызванный невирапином [2].
O’Brien и Naber также выявили значительную психосоциальную заболеваемость у женщин, страдающих невирапином. Они обнаружили, что пострадавшие женщины сообщали о снижении социальных обязательств и ухудшении отношений с супругами и детьми. Женщины с тяжелыми симптомами также сообщали о частой плаксивости, раздражительности, усилении нарушений сна и снижении настроения [102]. Используя краткую форму 36, Attard et al. обнаружили, что женщины с НВП имели более низкие показатели физического функционирования, физической роли, телесной боли, жизнеспособности, социального функционирования и эмоциональной роли в опросе, оценивающем качество жизни, по сравнению со здоровыми беременными контрольной группой на ранних сроках беременности и женщинами с хронической депрессией.Показатели психического здоровья женщин с НВП были аналогичны показателям женщин с депрессией [103].
Помимо того, что невирапин вызывает психосоциальную заболеваемость, он также создает значительное финансовое бремя. В 2002 г. стоимость тяжелого невирапина оценивалась приблизительно в 130 миллионов долларов, исходя из больничных расходов, связанных в среднем с 39 000 госпитализаций. Эта цифра, вероятно, сильно занижена, поскольку она не включает потерю производительности дома, оплату услуг врача или стоимость лечения [104].
Подсчитано, что каждая работающая женщина с невирапином теряет 206 рабочих часов [2] и что на невирапин приходится 28% всех отпусков по болезни во время беременности до 28-й недели [19]. Кроме того, работа Vallacott et al. показывает, что 50% пострадавших женщин считают, что эффективность их работы значительно снижена [105].
HYPEREMESIS GRAVDIARUM
Гиперемезис беременных (HG) — это состояние сильной тошноты и рвоты во время беременности, приводящее к водно-электролитному и кислотно-щелочному дисбалансу, дефициту питательных веществ и потере веса [8].Некоторые определяют его как возникновение более трех эпизодов рвоты в день, сопровождающихся кетонурией и потерей веса более 3 кг или 5% массы тела [63]. ГГ является наиболее частой причиной госпитализации на ранних сроках беременности и уступает только преждевременным родам на протяжении всей беременности [106]. В Соединенных Штатах более 36 000 женщин ежегодно госпитализируются по поводу ХГ, и стоимость лечения оценивается более чем в 250 миллионов долларов в год только на госпитализацию [107].В отличие от NVP, который связан с благоприятными исходами для плода, HG представляет значительный риск для здоровья матери и плода.
Диагностика и клинические признаки
ГГ проявляется в первом триместре беременности, обычно начиная с 4–5-й недели беременности. В дополнение к сильной тошноте и рвоте у 60% женщин с ГГ также наблюдается избыточное слюноотделение или слюнотечение [108]. Пациенты также могут жаловаться на симптомы гастроэзофагеального рефлюкса, такие как дискомфорт за грудиной и изжога. Уникальная количественная оценка рвоты и тошноты (PUQE) для беременных, которая рассчитывается с использованием количества часов тошноты в день, количества эпизодов рвоты в день и количества эпизодов позывов на рвоту в день, может использоваться для отслеживания тяжести симптомов. [109].
Пациенты могут иметь признаки обезвоживания, такие как сухость слизистых оболочек, тахикардия, плохой тургор кожи и постуральная гипотензия. Тяжело пораженные пациенты могут также иметь мышечную атрофию и слабость и/или изменения психического статуса.
Лабораторные нарушения у женщин с HG могут включать повышение азота мочевины в сыворотке крови, креатинина и гематокрита, а также кетонурию и увеличение удельного веса мочи. Кроме того, могут быть обнаружены электролитные нарушения, подтверждающие диагноз либо гипохлоремического метаболического алкалоза, либо метаболического ацидоза с выраженным сокращением объема [39].Уровни преальбумина (транстиретина в плазме) могут быть низкими, отражая плохой статус белкового питания у матери и, возможно, предсказывая более низкую массу тела плода при рождении [110]. Также возможен дефицит витаминов и минералов, таких как витамин B1 (тиамин), железо, кальций и фолиевая кислота [74].
Функциональные пробы печени могут отклоняться от нормы у 50% госпитализированных пациентов с ХГ [111]. Могут наблюдаться умеренная гипербилирубинемия (билирубин < 4 мг на децилитр) и/или повышение уровня щелочной фосфатазы вдвое по сравнению с верхней границей нормы [112].Умеренный трансаминит является наиболее частым нарушением функции печени, при котором уровни аланинаминотрансферазы (АЛТ) обычно превышают уровни аспартатаминотрансферазы (АСТ). Повышение уровня трансаминаз обычно в два-три раза превышает верхнюю границу нормы; однако сообщалось об уровнях выше 1000 ЕД/мл [113]. Аномальные печеночные пробы исчезают сразу же после прекращения рвоты.
Повышение уровня амилазы и липазы в сыворотке наблюдается у 10–15% женщин [39]. Одно исследование выявило повышенный уровень амилазы у 24% пациентов с ХГ [114].Считается, что это связано с избыточной выработкой амилазы слюнными железами, а не с секрецией поджелудочной железы, и является результатом, а не причиной ГГ [8].
Уровни тиреостимулирующего гормона могут быть низкими при ХГ из-за перекрестной реакции между альфа-субъединицей ХГЧ и рецептором ТТГ. В большинстве случаев этот биохимический тиреотоксикоз не имеет клинического значения, так как пациенты находятся в эутиреоидном состоянии. Уровень гормонов щитовидной железы обычно нормализуется без лечения после родов.
HG — это клинический диагноз, основанный на симптомах и исключении других состояний.Как и в случае с невирапином, для диагностики ГГ не требуется специального тестирования; тем не менее, УЗИ брюшной полости и таза может быть полезным для исключения других причин, таких как заболевание желчного пузыря, пузырный занос, а также для оценки многоплодной беременности. Дифференциальный диагноз включает невирапин, острый тиреоидит, расстройства пищевого поведения, заболевания желчевыводящих путей, вирусный гепатит и гастроэзофагеальную рефлюксную болезнь.
Исход
В отличие от NVP, HG связан с неблагоприятными исходами как для матери, так и для плода. В исследовании более 150 000 одноплодных беременностей младенцы, рожденные женщинами с гиперемезисом и низкой прибавкой массы тела при беременности (<7 кг), с большей вероятностью имели низкую массу тела при рождении, маловаты для гестационного возраста, родились до 37 недель беременности и имели мин. Оценка по шкале Апгар < 7 [5].
Общие материнские осложнения включают потерю веса, обезвоживание, дефицит питательных микроэлементов и мышечную слабость. Более тяжелые, хотя и редкие, осложнения включают разрывы Мэллори-Вейса, разрыв пищевода, энцефалопатию Вернике с корсаковским психозом или без него, центральный мостовой миелинолиз из-за быстрой коррекции тяжелой гипонатриемии, кровоизлияние в сетчатку и спонтанный пневмомедиастинум [47]. Также сообщалось о вазоспазме церебральных артерий из-за повышенной симпатической активности [115].
HG способствует возникновению многих психологических проблем и может привести к прерыванию нежелательной беременности и снижению вероятности попытки повторной беременности [116]. Пуршариф и др. обнаружили, что у 15% из 808 женщин с HG было по крайней мере одно прерывание беременности из-за болезни. Интересно, что у тех женщин, которые прервали беременность, не было более тяжелого заболевания, чем у женщин с ГГ, которые сохранили беременность, но в два раза чаще считали, что их врач безразличен или не обратил внимания на тяжесть их заболевания [117].
Долгосрочные последствия HG для матерей неизвестны. Несколько исследований показывают повышенный риск рака молочной железы [118]. Имеются также сообщения о повышенной частоте депрессии, посттравматического стрессового расстройства и различных неврологических расстройств [39].
Некоторые исследования не выявили повышенного риска неблагоприятных исходов для плода у женщин с ГГ. Башири и соавт., например, сообщили о более низкой частоте спонтанных ранних потерь беременности у женщин с ГГ по сравнению с общей популяцией и не обнаружили различий в перинатальных исходах [6].Однако в других исследованиях была обнаружена связь между ГГ и задержкой роста плода, преэклампсией и малым весом для гестационного возраста [119]. В ретроспективном исследовании 3068 женщин ГГ была связана с более ранними родами и меньшей массой тела при рождении. Эти исходы были наиболее вероятны у женщин, которые потеряли более 5% массы тела до беременности [120]. Точно так же Dodds et al. обнаружили более высокие показатели низкой массы тела при рождении, преждевременных родов, гибели плода у женщин с ХГ, которые в целом набрали менее 7 кг во время беременности [5].Многократные госпитализации по поводу ХГ, по-видимому, являются еще одним фактором риска снижения массы тела новорожденных при рождении [108].
Различные врожденные пороки развития чаще наблюдаются у женщин с ХГ [32]. К ним относятся синдром Дауна, дисплазия тазобедренного сустава, неопущение яичек, пороки развития скелета, дефекты центральной нервной системы и аномалии кожи. Сообщалось о коагулопатии плода и хондродисплазии из-за дефицита витамина К [121] с внутричерепным кровоизлиянием плода в третьем триместре [122].Некоторые виды рака у детей, такие как рак яичек или лейкемия, также были связаны с ГГ у матери, однако данные противоречивы [39].
ЛЕЧЕНИЕ
Целью лечения является облегчение симптомов при минимизации риска для матери и плода. Для достижения этого обычно необходим мультимодальный подход, адаптированный к каждому человеку. Методы лечения варьируются от простых диетических модификаций до медикаментозной терапии и полного родительского питания. Тяжесть симптомов и потеря веса матери помогают определить агрессивность лечения.PUQEscore и опросник по влиянию гиперемезиса на симптомы (HIS) можно использовать для оценки тяжести симптомов. Обновленная шкала PUQE оценивает симптомы в течение 24 часов [123], в то время как HIS учитывает психосоциальные факторы в дополнение к физическим симптомам [124].
Текущие исследования показывают, что лечение невирапином является субоптимальным. Одно недавнее проспективное исследование 283 женщин с невирапином в течение первого триместра показало, что только половине из них задавали вопрос об интенсивности и тяжести их симптомов, менее четверти спрашивали, мешают ли их симптомы их повседневным задачам и работе.В этом исследовании Lacasse et al только 27% женщин были предложены противорвотные средства, а еще 14% были рекомендованы немедикаментозные методы лечения [125].
Немедикаментозная терапия
Диетические меры
Начальная терапия невирапина и ГГ должна включать диетические изменения. Пораженные женщины должны избегать больших приемов пищи и вместо этого есть несколько небольших приемов пищи в течение дня, которые должны быть пресными и с низким содержанием жира, поскольку жирная пища может еще больше задержать опорожнение желудка. Употребление белка больше, чем углеводов, и употребление большего количества жидкости, чем твердой пищи, также может уменьшить тошноту, уменьшая желудочные аритмии, связанные с невирапином [82].Рекомендуются небольшие объемы соленых жидкостей, таких как электролитозамещающие спортивные напитки, а если запах горячей пищи является неприятным, следует приготовить холодную пищу [126].
Эмоциональная поддержка
Эмоциональную поддержку всегда должен оказывать медицинский работник. Кроме того, поддерживающая психотерапия, поведенческая терапия и гипнотерапия могут быть полезны для женщин с тяжелыми симптомами и/или для тех, у кого играют роль личностные особенности, супружеские или семейные конфликты [60].Цель психотерапии не в том, чтобы углубляться в психологию, которая может способствовать НВП, а в том, чтобы поощрять, объяснять, успокаивать и позволять пациенту выражать стресс [95].
Акупрессура/акупунктура
Акупрессура китайской акупунктурной точки Р6 (Нэйгуань) снижает тошноту у пациентов с тошнотой, вызванной химиотерапией, а также послеоперационной тошнотой и рвотой, и может быть полезна при лечении ГГ. В соответствии с принципом ци, приложение давления к этой точке блокирует аномальное замедление энергии и восстанавливает симптомы, связанные с точкой давления [13].Давление можно оказывать вручную или с помощью эластичных лент на внутренней стороне запястья. Кроме того, ReliefBand, электрический стимулятор нервов с батарейным питанием, который носится на запястье, недавно был одобрен FDA и может также использоваться для стимуляции участка P6 [127].
Доказательства акупрессуры противоречивы. Один обзор семи испытаний показал, что акупрессура точки Neiguan может облегчить симптомы тошноты [128]. Недавнее плацебо-контролируемое исследование с участием 60 женщин, принимавших невирапин, показало, что в группе лечения наблюдалось облегчение тошноты на следующий день после начала акупрессуры над местом P6, которое продолжалось до конца периода наблюдения.Для сравнения, в группе, получавшей акупрессуру на незначительном участке, наблюдалось первоначальное облегчение симптомов, но к 6-му дню симптомы вернулись и не отличались от группы, не получавшей лечения [129].
Хотя исследования преимуществ акупрессуры не дали окончательных результатов, некоторые эксперты считают, что это вмешательство должно быть предложено, поскольку не существует известных побочных эффектов [130].
Иглоукалывание менее изучено, но одно слепое рандомизированное контролируемое исследование с участием 593 женщин со сроком беременности менее 14 недель показало, что у женщин, получавших еженедельное лечение иглоукалыванием в течение 4 недель, было меньше тошноты и сухих рвотных позывов по сравнению с контрольной группой [131].Однако возможно, что состояние некоторых женщин улучшилось просто с увеличением гестационного возраста [13].
Имбирь
Имбирь — единственное немедикаментозное вмешательство, рекомендованное Американским колледжем акушерства и гинекологии [132]. Считается, что имбирь помогает улучшить НВП, стимулируя моторику желудочно-кишечного тракта и стимулируя выделение слюны, желчи и желудочного секрета. Было показано, что один компонент имбиря обладает такой же активностью, что и антагонист 5-HT3, ондансетрон.Кроме того, было обнаружено, что его экстракт ингибирует рост некоторых штаммов H. pylori [133].
В двойном слепом рандомизированном перекрестном исследовании 70% женщин с ГГ, получавших 250 мг порошкообразного корня имбиря четыре раза в день, предпочли период приема имбиря по сравнению с периодом приема плацебо. Женщины также сообщали о значительно большем облегчении симптомов при приеме имбиря. 4 дня обнаружили, что у женщин в группе лечения было значительное улучшение симптомов тошноты по сравнению с женщинами в группе плацебо ( P <.001) [135].
Что касается безопасности имбиря во время беременности, исследование случай-контроль с участием 187 беременных женщин не выявило увеличения частоты серьезных пороков развития при употреблении имбиря в первом триместре [136]. Однако существует теоретический риск кровотечения, поскольку имбирь ингибирует тромбоксансинтетазу и может ингибировать функцию тромбоцитов. Таким образом, одновременное использование антикоагулянтов с имбирем не рекомендуется [137].
Фармакологическое лечение
Пиридоксин-доксиламин
Комбинация пиридоксина (витамина В6) (категория А при беременности) и доксиламина (категория В), ранее доступная как бендектин, является единственным лекарственным средством, которое специально маркировано для лечения невирапина Управление по санитарному надзору за качеством пищевых продуктов и медикаментов.Он по-прежнему доступен в Канаде в таблетках с отсроченным высвобождением, содержащих 10 мг пиридоксина и 10 мг доксиламина, под торговым названием Диклектин.
Бенедектин был снят с продажи в 1983 году в США в связи с сообщениями о врожденных пороках развития при применении в первом триместре. Однако до его отмены 30 миллионов женщин принимали его в течение почти 25 лет. Несколько небольших рандомизированных контролируемых исследований подтверждают его эффективность [138]. Кроме того, метаанализ, который включал 170 000 воздействий, показал, что комбинация пиридоксин-доксиламин безопасна и не вызывает побочных эффектов у плода [139].Другие крупные исследования также не показали увеличения частоты врожденных аномалий по сравнению с фоновой частотой [140]. Тем не менее, Бенедектин остается вне рынка в Соединенных Штатах. Однако женщины могут сделать свой собственный препарат, объединив 10 мг пиридоксина с половинкой таблетки Унисома, который содержит 25 мг доксиламина.
В качестве альтернативы пиридоксин можно принимать отдельно. Хотя связи между уровнями пиридоксина и невирапином не обнаружено, в нескольких исследованиях было показано улучшение показателей тошноты у пациентов, принимавших пиридоксин с выраженной тошнотой [141], и уменьшение эпизодов рвоты по сравнению с женщинами, принимавшими плацебо [138].Нет известных доказательств токсичности витамина B6, однако в больших дозах пиридоксин был связан с обратимой периферической нейропатией у небеременных взрослых [13].
Противорвотные средства
Фенотиазины, хлорпромазин (торазин) и прохлорперазин (компазин), являются центральными и периферическими антагонистами дофамина, которые, как было показано, уменьшают симптомы невирапина и ГГ [142]. Они относятся к категории беременности С.
Исследование 12 764 беременных женщин показало незначительное повышение риска врожденных дефектов при применении фенотиазинов в первом триместре, особенно при применении хлорпромазина, однако потенциальные смешанные факторы, такие как употребление алкоголя и продолжительность лечения, не были выявлены. 143].Другое исследование показало, что у младенцев от матерей, принимавших хлорпромазин, были экстрапирамидные симптомы и желтуха; значительных нарушений постнатального развития не было [144].
Прометазин (Phenergan) не обладал тератогенными эффектами в одном исследовании [145], но в другом исследовании наблюдалось усиление врожденного вывиха бедра [146].
Активаторы
Метоклопрамид (Реглан) широко используется для лечения невирапина [147]. Это категория беременности B. Считается, что метоклопрамид улучшает симптомы за счет повышения давления в нижнем пищеводном сфинктере и увеличения транзита через желудочный тракт.Он также корректирует желудочные аритмии, стимулируя антральные сокращения и способствуя антродуоденальным сокращениям. Недавнее исследование показало, что 10 мг метоклопрамида, принимаемого каждые 8 часов, столь же эффективны для уменьшения количества эпизодов рвоты и улучшения самочувствия у женщин с ГГ во время их первой госпитализации, как и 25 мг прометазина, принимаемого каждые 8 часов в течение 24 часов. Профиль побочных эффектов был лучше в группе, получавшей метоклопрамид, с меньшей сонливостью, головокружением и дистонией [148].
Что касается безопасности, исследование 81 703 родов в период с 1998 по 2007 год в Израиле, в ходе которого метоклопрамид применялся у 4,2% женщин, не выявило повышенного риска серьезных врожденных пороков развития, низкой массы тела при рождении, преждевременных родов или перинатальной смерти при применении метаклопрамида. использовать [149]. Точно так же датское исследование 309 беременных женщин, принимавших метаклопрамид, не выявило повышенного риска [150].
Несмотря на свою эффективность, использование метоклопрамида ограничено его побочными эффектами, которые включают дистонию, беспокойство и сонливость.В 2009 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) добавило к метоклопрамиду предупреждение «черный ящик» из-за риска поздней дискинезии при хроническом применении.
Другие прокинетики, такие как домперидон и эритромицин, не изучались при применении невирапина [74].
Антигистаминные и антихолинергические препараты
Антигистаминные препараты косвенно влияют на вестибулярную систему, уменьшая стимуляцию рвотного центра [151]. Рандомизированные контролируемые исследования применения антигистаминных препаратов при невирапине ограничены; однако было показано, что меклизин (анитверт), дименгирдинат (драмамин) и дифенгирамин (бенадрил) контролируют симптомы лучше, чем плацебо [142].Кроме того, объединенные данные семи испытаний между 1951 и 1975 годами показали эффективность антигистаминных препаратов [152]. Метаанализ более 24 контролируемых исследований с участием более 200 000 беременных женщин показал, что антигистаминные препараты (в частности блокаторы Н2-рецепторов), назначаемые в течение первого триместра, не повышают риск тератогенного действия [153]. Хотя ранее считалось, что меклизин обладает тератогенным действием, теперь исследования показывают, что его безопасно использовать во время беременности [154]. Дименгидринат и дифенгидрамин имеют противоречивые результаты по безопасности [74].
В одном исследовании женщин, перенесших плановое кесарево сечение, было обнаружено, что трансдермальный скополамин более эффективен в уменьшении тошноты, рвоты и позывов на рвоту из-за эпидуральной морфиновой анальгезии по сравнению с плацебо [155]. Однако исследования по применению скополамина в первом триместре отсутствуют, поскольку скополамин может вызывать хромосомные аберрации и обмены сестринскими хроматидами в здоровых взрослых лимфоцитах и может приводить к врожденным порокам развития, включая деформацию конечностей и туловища [156].
Другие препараты
Ондансетрон (Зофран) (категория B при беременности) широко используется для лечения послеоперационной и вызванной химиотерапией тошноты и рвоты и в настоящее время является одним из наиболее часто назначаемых противорвотных средств [157].Считается, что он действует как центрально, так и периферически, блокируя серотониновые рецепторы в тонкой кишке и медуллярном рвотном центре [151]. Его безопасность при беременности была определена в недавнем исследовании, которое не показало значительного увеличения числа выкидышей, серьезных пороков развития или массы тела при рождении между младенцами, подвергшимися воздействию ондансетрона, и контрольной группой, не получавшей его [158].
Было проведено одно рандомизированное контролируемое исследование применения ондансетрона для лечения ХГ. В этом небольшом исследовании с участием 30 женщин не было выявлено преимуществ ондансетрона в дозе 10 мг внутривенно каждые 8 часов по мере необходимости по сравнению с прометазином в дозе 50 мг внутривенно каждые 8 часов с точки зрения тошноты, увеличения веса, дней госпитализации или общих доз препарата [46]. .Однако было обнаружено, что прометазин вызывает больший седативный эффект. Тем не менее, сообщения о случаях заболевания и широко распространенный клинический опыт подтверждают эффективность ондансетрона для лечения HG и его лучшую переносимость по сравнению с более ранними противорвотными средствами [159, 160].
Дроперидол (инапсин) является антагонистом дофамина, эффективным противорвотным средством при послеоперационной тошноте и рвоте. Небольшое исследование женщин с HG показало, что комбинация непрерывной инфузии дроперидола и болюсного внутривенного введения дифенгидрамина приводила к более коротким госпитализациям и меньшему количеству повторных госпитализаций по сравнению с исторической контрольной группой, которая получала другие формы парентеральной терапии.Кроме того, не было никаких существенных различий в материнских или перинатальных исходах [161]. Следует отметить, однако, что дроперидол имеет предупреждение черного ящика, поскольку он может вызывать удлинение интервала QT и сердечные аритмии [74].
Пероральные и внутривенные кортикостероиды использовались для рефрактерных случаев HG с переменными результатами. Считается, что они оказывают противорвотное действие на триггерную зону хеморецепторов в стволе головного мозга, а также постулируются для коррекции «относительной надпочечниковой недостаточности», вызванной HG, при которой гипоталамо-гипофизарно-надпочечниковая ось не может реагировать на повышенные потребности в кортизоле. во время ранней беременности.
В рандомизированном контролируемом исследовании 40 женщин с ГГ, получавших метилпреднизолон в дозе 16 мг перорально 3 раза в день в течение 3 дней с последующим 2-недельным снижением дозы, по сравнению с прометазином в дозе 25 мг перорально 3 раза в день в течение 2 недель, — госпитализация была обнаружена в группе, получавшей стероиды [162]. Другие исследования не показали статистически значимого преимущества кортикостероидов. Рандомизированное исследование Yost et al. не обнаружили значительного снижения числа посещений неотложной помощи или повторных госпитализаций при добавлении парентерального и перорального метилпреднизолона к режиму прометазина и метоклопрамида [163].
Нет утвержденных руководств по применению кортикостероидов при ХГ. Однако была предложена возможная схема: 48 мг метилпреднизолона вводят перорально или внутривенно в три приема в течение двух-трех дней. Если в течение трех дней ответа не наблюдается, рекомендуется прекратить лечение, так как ответ через 72 часа маловероятен [151].
Что касается безопасности, то недавний метаанализ показал небольшое увеличение основных пороков развития и 3,4-кратное увеличение расщелины рта у младенцев, матери которых принимали кортикостероиды в первом триместре [164].
В последнее время наблюдается интерес к препаратам, снижающим кислотность при лечении невирапином, поскольку одно недавнее когортное исследование показало, что у женщин с невирапином и изжогой и/или кислотным рефлюксом тошнота и рвота были более выраженными, чем у женщин без изжоги или кислотного рефлюкса [165]. Кроме того, последующие исследования показали, что лечение изжоги и/или рефлюкса приводит к улучшению показателей PUQE и показателей качества жизни [166].
Антациды, содержащие алюминий или кальций, являются терапией первой линии во время беременности при кислотном рефлюксе и изжоге и могут использоваться для лечения женщин с невирапином.Антациды, содержащие магний, связаны с нефролитиазом, гипотонией и респираторным дистресс-синдромом у плода и не рекомендуются во время беременности. Антациды, содержащие бикарбонаты, могут вызывать метаболический ацидоз плода и перегрузку жидкостью и также не рекомендуются [167].
Блокаторы h3 и ингибиторы протонной помпы можно безопасно использовать для лечения кислотного рефлюкса и/или изжоги у женщин с невирапином [168, 169].
Нутритивная поддержка
Женщинам с трудноизлечимыми симптомами, не поддающимися коррекции диеты и фармакологическому лечению и неспособными поддерживать вес за счет перорального приема пищи, может потребоваться пищевая поддержка.В этой популяции следует использовать внутривенную инфузионную терапию, энтеральное или парентеральное питание для предотвращения задержки внутриутробного развития плода, обезвоживания матери и недостаточности питания.
Роль внутривенной гидратации заключается в увеличении объема и восстановлении электролитов. Госпитализированным пациентам при необходимости можно быстро влить физиологический раствор или раствор Рингера с лактатом, а затем откорректировать их для соответствия диурезу. Внутривенно тиамин следует вводить перед любыми жидкостями, содержащими декстрозу, чтобы избежать энцефалопатии Вернике.Женщинам, которым требуется многократная госпитализация, может быть рекомендована внутривенная гидратация в домашних условиях [74].
Энтеральное зондовое питание и полное парентеральное питание следует рассмотреть, если внутривенная терапия не помогает уменьшить симптомы, а дефицит калорий сохраняется. Однако исследования энтерального питания при HG ограничены. В одном небольшом исследовании женщин с HG, получавших энтеральное питание с использованием назогастрального зонда 8-French, сообщалось об улучшении симптомов в течение 24 часов после установки зонда.Через 8 дней пациенты были выписаны в среднем на 43 дополнительных дня амбулаторного энтерального питания, после чего можно было возобновить пероральное питание [170].
Помимо назогастральных зондов, чрескожная эндоскопическая гастростомия (ЧЭГ) [171] успешно использовалась для поддержания питания у женщин с ГГ. Однако оба этих способа кормления ограничены риском усиления тошноты и рвоты, вызванных внутрижелудочным кормлением. Постпилорические зонды для кормления, как назоеюнальные [172, 173], так и чрескожные эндоскопические гастроеюноанастомозы [174] пытались снизить этот риск, однако смещение зондов [175] из-за продолжающейся рвоты, позывов на рвоту и свертывания желудка является частым осложнением. .Кроме того, назоэнтеральные зонды, как назогастральные, так и назоеюнальные, плохо переносятся многими женщинами из-за эстетических соображений и физического дискомфорта. Недавно хирургическая еюностомия была описана как альтернативный способ доставки питания женщинам с HG. В одном небольшом исследовании пяти женщинам с HG была выполнена хирургическая еюностомия во втором триместре. Изотонические кормления через зонд вводили до целевого показателя калорийности. Прибавка в весе матери наблюдалась в 5 из 6 беременностей, и все беременности закончились срочными родами.Серьезных осложнений не произошло, что позволяет предположить, что еюностомия может быть безопасным и эффективным способом нутритивной поддержки у женщин с ХГ [176].
Женщинам, которые не переносят энтеральное питание, следует рассмотреть возможность парентерального питания. Эта терапия, однако, является дорогостоящей и связана со значительной материнской заболеваемостью. Руссо-Стейглиц и др. сообщили о частоте осложнений 9% при парентеральном питании через периферически установленные центральные катетеры во время беременности и о 50% частоте осложнений при центрально вставленных катетерах.Инфекция и тромбоз были двумя наиболее часто встречающимися осложнениями, и предполагалось, что они являются результатом связанной с беременностью гиперкоагуляции и иммунологической супрессии [177]. Holmgren et al. также показали высокую частоту осложнений у женщин, получавших парентеральное питание через PICC. В исследовании 94 женщин с HG 66,4% из тех, кто получал парентеральное питание через PICC, нуждались в лечении тромбоэмболии, инфекции или того и другого. Пациентки на парентеральном питании также имели более высокую частоту неонатальных осложнений, включая госпитализацию в отделение интенсивной терапии новорожденных, малый размер для гестационного возраста, прерывание беременности из-за ГГ и потерю плода по сравнению с женщинами, получавшими энтеральное питание [178].Таким образом, парентеральное питание, хотя оно может быть более переносимым для пациентов, следует зарезервировать для отдельных пациентов с HG.
Информация для авторов
Ноэль М. Ли, Школа медицины и общественного здравоохранения Университета Висконсина, Медицинский фонд Университета Вашингтона, здание столетия, 1685 Highland Avenue, Madison, WI 53705, телефон: (608) 263-1995, факс: (608) 265-5677.
Сумона Саха, Отделение гастроэнтерологии и гепатологии, Школа медицины и общественного здравоохранения Висконсинского университета, Медицинский фонд Университета Вашингтона, здание столетия, 1685 Хайленд-авеню, комната 4224, Мэдисон, Висконсин 53705, телефон: (608) 263-1995, факс: (608) 265-5677.
Тошнота и рвота при беременности
Введение
Тошнота и рвота являются обычным явлением во время беременности, которым страдают 70–80% всех беременных женщин. Хотя у большинства женщин тошнота и рвота при беременности (НВП) имеют симптомы, ограниченные первым триместром, у небольшого процента женщин наблюдается длительное течение с симптомами, продолжающимися до родов. У женщин с тяжелой тошнотой и рвотой во время беременности может быть гиперемезис беременных (HG), состояние, отличное от NVP, которое, если его не лечить, может привести к значительной заболеваемости матери и плода.
Различные метаболические и нервно-мышечные факторы вовлечены в патогенез невирапина и HG; однако их точная причина неизвестна. Следовательно, лечение NVP и HG может быть затруднено, поскольку не известны ни оптимальные цели лечения, ни полные эффекты потенциальных методов лечения на развивающийся плод. В этой статье рассматриваются эпидемиология, патология, диагностика, исходы и лечение невирапина и HG.
Эпидемиология
По оценкам, 70–80% беременных женщин получают невирапин [1].В Соединенных Штатах и Канаде это означает примерно 4 000 000 и 350 000 женщин, которые страдают каждый год соответственно [2].
НВП чаще встречается в западных странах и у городского населения и редко встречается у африканцев, коренных американцев, эскимосов и большинства азиатских популяций [3]. Лишь в нескольких исследованиях изучалось расовое распределение невирапина в данной популяции. Одно такое исследование, проведенное в Канаде с участием 367 женщин, показало, что азиаты и чернокожие реже сообщали о симптомах невирапина, чем представители европеоидной расы.Социально-демографические факторы не учитывали расовые/этнические различия в распространенности заболевания, что позволяет предположить, что могут играть роль генетические и/или культурные факторы [4].
HG встречается редко по сравнению с NVP и встречается в 0,3–2% всех беременностей [5]. Заболеваемость зависит от этнической принадлежности [6] и колеблется от 3 до 20 на 1000 беременностей [7]. Он чаще диагностируется у женщин в Индии, Пакистане, Азии, Новой Зеландии по сравнению с европейцами, американскими индейцами и эскимосами [8].
Факторы риска
Данные Совместного перинатального проекта, одного из крупнейших на сегодняшний день исследований беременных женщин, показали, что невирапин чаще встречается у молодых женщин, первобеременных, женщин с образованием менее 12 лет, некурящих и женщины с ожирением [9]. О повышенном риске невирапина в первом триместре также сообщалось у женщин с многоплодной беременностью по сравнению с женщинами с одноплодной беременностью (87% против 73%, p<0,01) [10].
НВП был связан с низким уровнем дохода и статусом занятости неполный рабочий день [11]).Было обнаружено, что домохозяйки также подвергаются повышенному риску, в то время как женщины, работающие в качестве белых воротничков, по-видимому, защищены [12]. Однако остается неясным, является ли статус занятости истинным фактором риска для невирапина или искажающим фактором, поскольку затронутые женщины могут прекратить работу из-за своих симптомов. Точно так же их решение не работать вне дома может быть связано с многодетностью и необходимостью заботиться о других детях [13].
Материнская генетика также может служить фактором риска для невирапина. Данные большой популяции норвежских близнецов показывают более широкое использование лекарств от тошноты во время беременности среди монозиготных близнецов женского пола по сравнению с дизиготными близнецами женского пола [14].Кроме того, более высокие уровни тошноты были обнаружены у женщин, матери которых испытывали тошноту во время беременности [15]. Также было показано, что личный анамнез NVP является фактором риска для NVP при последующих беременностях [15]; однако этот вывод не был последовательным в разных исследованиях [16]
Другие факторы риска для невирапина включают личную историю укачивания, возможно, из-за общего вестибулярного механизма [17] и мигреней в анамнезе [18]. Женщины, у которых в анамнезе была тошнота при приеме эстрогенсодержащих пероральных контрацептивов, также подвержены повышенному риску невирапина [19].
Расположение желтого тела также может служить фактором риска невирапина. Ультразвуковые исследования показали, что беременные чаще испытывают тошноту и рвоту при наличии желтого тела в правом яичнике [20]. Это может быть связано с различиями в венозном оттоке между левым и правым яичником и более высокой концентрацией половых стероидов, когда желтое тело находится на правой стороне [21].
Более высокое суточное потребление общего жира, особенно насыщенных жиров, до беременности увеличивает риск госпитализации по поводу невирапина [22].Курение до беременности и прием витаминов до и/или на ранних сроках беременности связаны со снижением риска невирапина [23]. Также было обнаружено, что употребление алкоголя матерью до зачатия защищает от NVP [24].
Факторы риска HG аналогичны факторам риска NVP. К ним относятся многоплодная беременность, трофобластическая болезнь, HG в предшествующей беременности, аномалии плода, такие как триплоидия, трисомия 21 и водянка плода, а также нерождение плода [25]. Семейный анамнез HG также является фактором риска: примерно 28% женщин сообщают о HG в анамнезе у своих матерей и 19% сообщают, что их сестры имели аналогичные симптомы [26].Дополнительные факторы риска включают семейный или партнерский статус и возраст старше 30 лет. Курение сигарет может быть защитным [27].
Индекс массы тела матери оценивался как фактор риска ГГ с неоднозначными результатами. В исследовании Depue et al ожирение увеличивало риск ГГ на 50% [28]. Работа Cedergren et al. однако обнаружили, что низкий индекс массы тела (<20 кг/м2) был связан с 40% более высоким риском ХГ, а ожирение снижало риск госпитализации по поводу ХГ [29].Более недавнее исследование 33 647 женщин в Норвегии показало, что недостаточный или избыточный вес увеличивает риск ГГ, но только у некурящих [30]. Постулируется, что женщины с недостаточным весом и низкими индексами массы тела имеют низкий уровень эстрогена до беременности и, таким образом, могут иметь преувеличенный ответ в течение первого триместра, когда уровень эстрогена резко возрастает [31]. Напротив, у женщин с ожирением жировые отложения могут нейтрализовать плацентарные факторы, которые, как считается, способствуют патогенезу [29].
Что касается пола плода, то в нескольких исследованиях была обнаружена связь между ГГ и женским полом плода.Используя данные Шведского медицинского реестра рождений, Kallen et al. обнаружили, что HG был чрезмерно представлен в 3068 беременностях, когда ребенок был девочкой [32]. Точно так же в исследовании беременных женщин, госпитализированных с HG в первом триместре, вероятность рождения девочки была на 50% выше в случаях по сравнению со здоровыми беременными в контрольной группе (ОШ 1,5, 95% ДИ 1,4, 1,7) [33].
Патогенез
Метаболические и гормональные факторы
Хотя точный патогенез НВП и ГГ неизвестен, общепризнано, что рвота во время беременности является результатом различных метаболических и эндокринных факторов, многие из которых имеют плацентарное происхождение.Наиболее значимым фактором является хорионический гонадотропин человека (ХГЧ). Эта связь между ХГЧ и невирапином в значительной степени основана на временном соотношении между пиком невирапина и пиком продукции ХГЧ, которые происходят между 12 и 14 неделями беременности. Кроме того, тошнота и рвота часто усиливаются у беременных с состояниями, связанными с повышенным уровнем ХГЧ, такими как молярная беременность, многоплодная беременность и синдром Дауна [13]. Более высокие уровни ХГЧ в моче [34] и в сыворотке также были обнаружены у женщин с невирапином по сравнению с бессимптомными [35].Кроме того, исследование Goodwin et al. обнаружили, что концентрации ХГЧ положительно коррелируют с выраженностью тошноты и рвоты у женщин с ХГ [36].
Несмотря на множество исследований, связывающих уровень ХГЧ с невирапином и гормоном роста, другие не обнаружили связи между уровнем ХГЧ в сыворотке беременных женщин в течение первого триместра и частотой или интенсивностью тошноты и рвоты. В исследовании Soules et al. даже в подгруппе женщин с пузырным заносом, у которых уровни ХГЧ у женщин были в 5-10 раз выше, чем в контроле, корреляции обнаружено не было [37].Кроме того, исследования показали, что высокие уровни ХГЧ связаны с задержкой роста плода и преждевременными родами [38], в то время как невирапин, по-видимому, защищает от преждевременных родов, что делает маловероятным то, что ХГЧ является единственным фактором патогенеза невирапина.
Предполагается, что различные биологические формы (то есть изоформы) ХГЧ могут объяснить вариабельность между уровнями ХГЧ и тошнотой и рвотой у здоровых и больных людей [39]. Каждая изоформа ХГЧ имеет уникальный период полувыведения и активность в отношении рецепторов лютеинизирующего гормона и тиреотропного гормона (ТТГ).Изоформы без карбоксиконцевой части имеют более короткий период полувыведения, но являются более сильными стимуляторами рецепторов лютеинизирующего гормона и ТТГ. Напротив, гипергликозилированный ХГЧ имеет более длительный период полувыведения и большую продолжительность действия [40]. Эти различные изоформы ХГЧ, вероятно, являются результатом генетических факторов или долгосрочных изменений окружающей среды, которые, таким образом, могут объяснить различия в заболеваемости ХГ, обнаруженные в разных популяциях. Помимо изменчивости изоформ, мутации рецептора ХГЧ также могут объяснить некоторую вариабельность взаимоотношений между невирапином и ХГЧ [39].
Гормоны яичников, эстроген и прогестерон, также участвуют в патогенезе невирапина и гипергидроза. Известно, что некоторые женщины испытывают тошноту при приеме оральных контрацептивов. Кроме того, состояния с высокой концентрацией эстрогена, такие как низкий паритет и высокий индекс массы тела матери, были связаны с более высокой частотой ГГ [28]. Считается, что эстроген вносит свой вклад в HG, стимулируя выработку оксида азота с помощью синтетазы азотоксидазы, которая, в свою очередь, расслабляет гладкие мышцы, замедляя время желудочно-кишечного транзита и опорожнение желудка.
Ярнфельт и др. сообщили о значительной связи между рвотой беременных и непереносимостью пероральных контрацептивов в анамнезе [40]. Используя более количественный подход, Depue et al. обнаружили, что средние уровни общего эстрадиола на 26% выше, а средние уровни способности связывания половых гормонов и глобулинов на 37% выше у пациентов с HG, чем в контрольной группе после поправки на гестационный возраст. 28]. Однако важно отметить, что, как и взаимосвязь между ХГЧ и невирапином, взаимосвязь между уровнями эстрогена и невирапином была противоречивой в разных исследованиях [35].Обзор 17 исследований показал положительную связь между невирапином и эстрогеном только в 5 исследованиях [41]. Кроме того, пик уровня эстрогена приходится на третий триместр беременности, в то время как ГГ имеет тенденцию к улучшению на поздних сроках беременности [8].
Прогестерон в сочетании с эстрогеном также может играть роль в NVP. Прогестерон снижает сократимость гладкой мускулатуры и может изменить опорожнение желудка и привести к усилению тошноты и рвоты. Используя эластогастографию после стандартного приема пищи, Walsh et al. показали, что такое же медленноволновое нарушение желудочного ритма, обнаруженное у женщин с невирапином, может быть вызвано у небеременных женщин монотерапией прогестероном или в комбинации с эстрадиолом в дозах, которые воспроизводят уровни при беременности [42].Другие исследования, однако, не обнаружили существенной разницы между уровнями прогестерона у женщин с невирапином или без него [28].
Роль плацентарного простагландина E2 (PGE2) также оценивалась в патогенезе NVP из-за его влияния на гладкую мускулатуру желудка [43]. ХГЧ стимулирует плацентарный PGE2 и, как и ХГЧ, достигает пика между 9 и 12 неделями беременности. Норт и др. определили количество PGE2 в материнской сыворотке и обнаружили, что уровни были выше во время периодов тошноты и рвоты у 18 женщин на ранних сроках беременности по сравнению с бессимптомными периодами.Они также оценили уровни интерлейкина-1 бета и фактора некроза опухоли альфа у матери и обнаружили, что они были одинаковыми в течение симптоматического и бессимптомного периодов [44].
В связи с его ролью в вызванных химиотерапией тошноте и рвоте, серотонин также предположительно способствует развитию невирапина. Исследование Borgeat et al. однако не выявили различий в уровне серотонина среди беременных женщин с ХГ, бессимптомных беременных женщин и небеременных женщин [45]. Кроме того, рандомизированное контролируемое исследование, сравнивающее антагонист серотониновых 5-HT3-рецепторов, онданстерон, с прометазином, не выявило существенной разницы в контроле симптомов [46].
Из-за перекрестной реактивности между ХГЧ и рецептором тиреостимулирующего гормона (ТТГ) дисфункция щитовидной железы также изучалась как возможный механизм развития невирапина и ГГ. На самом деле, аномальные результаты функции щитовидной железы обнаруживаются у двух третей женщин с ГГ [36]. Этот «биохимический тиреотоксикоз» характеризуется подавлением ТТГ и слегка повышенным уровнем FT4. Несмотря на эти лабораторные отклонения, женщины с HG, как правило, находятся в эутиреоидном состоянии без предшествующих заболеваний щитовидной железы, отсутствия зоба и отрицательных антитиреоидных антител [47].Кроме того, исследования не выявили взаимосвязи между дисфункцией щитовидной железы и тяжестью симптомов [48], и почти у всех женщин с ХГ уровень ТТГ в норме к 20 нед беременности без какого-либо вмешательства [49].
Недавно была предложена связь между гормоном лептином и HG. Было обнаружено, что повышенный уровень лептина в сыворотке во время беременности, возможно, в результате увеличения общей жировой массы и продукции плаценты, значительно выше у пациенток с HG по сравнению со здоровыми беременными контрольной группой [50, 51].Лептин может способствовать ГГ за счет увеличения секреции ХГЧ за счет паракринного действия плаценты или за счет снижения аппетита и усиления тошноты и рвоты. Примечательно, однако, что другие проспективные когортные исследования не обнаружили аналогичной статистически значимой разницы в уровнях лептина в сыворотке при HG между пациентами и контрольной группой [52, 53].
Также было высказано предположение, что у женщин с HG возникает нарушение регуляции иммунной системы. В сыворотке крови матери были обнаружены повышенные концентрации свободной ДНК клеток плода [54], вызывающие гиперактивный материнский иммунный ответ и повреждение трофобласта.Кроме того, нормальный сдвиг во время беременности, при котором типы Т-хелперов переходят в Т-хелперы типа 1, более преувеличен у женщин с ХГ [55]. Это, в свою очередь, приводит к повышенному высвобождению интерлейкина-4, а также фактора некроза опухоли-альфа, оба из которых были связаны с HG [56]. Также было обнаружено, что аденозин повышен при HG, и его роль заключается в ослаблении TNF-альфа [57]. В проспективном исследовании [58] также было обнаружено, что уровни интерлейкина-6 повышаются при HG, а также повышаются уровни иммуноглобулина G (IgG), IgM, уровни комплемента и количество лимфоцитов [59].Однако точно определить роль этих иммунологических факторов нельзя, так как при голодании иммунная система обычно угнетается, а не активируется; таким образом, возможно, усиление иммунных факторов, наблюдаемое при HG, может быть попыткой ограничить прогрессирование HG [8].
Другие гормоны, в том числе тиреотропный гормон, гормон роста, пролактин, адренокортико-стимулирующий гормон, кортизол, лютеинизирующий гормон и фолликулостимулирующий гормон, также оценивались и, как считается, не вносят вклад в патогенез невирапин [60].
Helicobacter pylori
Повышенная частота инфицирования Helicobacter pylori (H. pylori) наблюдалась у женщин с ГГ, и в настоящее время считается, что она играет роль в ее патогенезе. Фриго и др. обнаружили, что 90,5% женщин с HG были H. plyori IgG положительными по сравнению с 46,5% в контрольной группе [61]. Багис и др. использовали золотой стандарт тестирования, гистологическое исследование биопсии слизистой оболочки, и обнаружили, что 95% пациентов с HG дали положительный результат на H.pylori по сравнению с 50% в контрольной группе. Они также обнаружили более высокую плотность H. pylori в антральном отделе и теле желудка у пациентов с HG, что позволяет предположить возможную связь между плотностью H. pylori и тяжестью симптомов [62].
Систематический обзор 2007 г., в котором оценивались 14 исследований типа «случай-контроль» с 1966 по 2007 г., выявил значительную связь между материнской инфекцией H.pylori и HG в 10 исследованиях. Отношение шансов в исследованиях варьировалось от 0.от 55 до 109,33 [63]. Аналогичным образом обновленный систематический обзор и метаанализ 25 исследований 2009 г. показали, что объединенное отношение шансов составляет 3,32 (95% доверительный интервал: 2,25–4,90) для инфекции H. pylori у женщин с HG [64]. Примечательно, что в обоих обзорах была обнаружена высокая гетерогенность исследований.
Инфицирование H. pylori во время беременности может произойти из-за вызванных стероидными гормонами изменений pH желудка [65] и/или повышенной восприимчивости из-за изменений гуморального и клеточно-опосредованного иммунитета [66].Однако нет четких доказательств того, что беременность предрасполагает к инфекции de novo H. pylori . Напротив, было высказано предположение, что H. pylori может усугубить вызванные гормонами изменения нервной и электрической функции желудка и, таким образом, увеличить риск для инфицированных женщин оказаться в более тяжелой форме тошноты и рвоты. рвота [67].
Хотя связь между H. pylori и HG интригует, важно отметить, что инфекция не обязательно коррелирует с симптомами.На самом деле у большинства инфицированных женщин заболевание протекает бессимптомно [8]. В исследовании Weyermann et al. 23% из 898 родильниц дали положительный результат на H. pylori при дыхательном тесте с 13C-мочевиной; однако положительный результат не коррелировал с симптомами тошноты, рвоты или рефлюкса во время беременности [68]. Точно так же Wu et al. обнаружили, что 69% беременных женщин являются сероположительными в отношении H. pylori по сравнению с 50% в общей популяции, однако не обнаружили никакой корреляции между статусом антител и желудочно-кишечными симптомами [69].
Почему H. pylori нельзя точно связать с невирапином, а HG связывают с несколькими факторами. Во-первых, в большинстве исследований для оценки наличия инфекции использовалось тестирование на антитела. Однако серологическое тестирование на H. pylori не может отличить активную инфекцию от перенесенной инфекции [70], а активная и перенесенная инфекция могут по-разному влиять на симптомы. Во-вторых, в большинстве исследований не оценивался и/или не учитывался штамм H. pylori . Ассоциированный с цитотоксином белок гена A (CagA) является маркером учащения пептических язв и связан с более агрессивным штаммом H pylori [71].Только одно исследование, включенное в метаанализ 2009 г., оценивало патогенность CagA. В этом исследовании, проведенном Xia et al., положительная реакция на CagA была более распространена у пациентов с HG [72].
Лечение приводит к эрадикации H. pylori у большинства пациенток, однако в настоящее время нет рекомендаций по оценке или лечению H. pylori во время беременности, поскольку последующее облегчение симптомов HG широко не изучалось. Сообщения о клинических случаях и серии случаев позволяют предположить, что лечение и эрадикация 90–105 H.pylori может уменьшить тошноту и рвоту во время беременности, и его следует рассматривать у пациенток с трудноизлечимыми симптомами [73]. Однако необходимы более масштабные исследования, чтобы определить, следует ли и когда начинать лечение во время беременности, учитывая опасения по поводу безопасности лекарств. В настоящее время специалисты рекомендуют после завершения беременности и лактации проводить тройную терапию в течение двух недель [74].
Нарушение моторики желудочно-кишечного тракта
Изменения давления в состоянии покоя нижнего пищеводного сфинктера (НПС) и перистальтики пищевода связаны с невирапином.Хотя эти изменения чаще связаны с изжогой во время беременности, гастроэзофагеальная рефлюксная болезнь (ГЭРБ) может вызывать атипичные симптомы, такие как тошнота [75], и способствовать развитию невирапинов. Эстроген и прогестерон являются вероятными медиаторами нарушения моторики пищевода при беременности, при этом эстроген служит праймером, а прогестерон вызывает релаксацию НПС [76].
Изменения желудочной ритмической активности могут способствовать НВП. Нормальная миоэлектрическая активность желудка приводит к медленному распространению волны от проксимального отдела тела к дистальному отделу антрального отдела со скоростью 3 цикла в минуту (имп/мин).Нарушение ритма в виде увеличения или уменьшения распространения медленных волн связано с тошнотой [74]. Используя эластогастрографию (EGG), Koch et al. продемонстрировали, что лица с нормальной медленноволновой активностью реже жаловались на тошноту во время беременности [77]. Напротив, люди с более высокими или более низкими показателями чаще жаловались на тошноту. Точно так же Riezzo et al. обнаружили, что беременные женщины без симптомов тошноты и рвоты на момент записи ЭГГ имеют нормальную миоэлектрическую активность 3 имп/мин.Они также обнаружили, что беременные женщины с невирапином имели более нестабильную активность EGG по сравнению с женщинами после добровольных абортов и небеременными женщинами из контрольной группы. Они предположили, что это может быть связано с восстановлением нормальной картины медленных волн желудка после аборта после нормализации уровней эстрадиола и прогестерона [78].
Примечательно, однако, что многие исследования не обнаружили различий в перистальтике желудка между беременными и небеременными женщинами. С помощью сцинтографии желудка не было обнаружено существенных различий в скорости опорожнения жидкости у беременных женщин до добровольного аборта, через 6 недель после аборта и у небеременных женщин контрольной группы [79].Используя методы разбавления красителя феноловым красным, Davison et al. обнаружили задержку опорожнения желудка во время родов, но не в третьем триместре по сравнению с небеременными контрольными женщинами [80]. Точно так же исследования с использованием парацетамола не показали задержки опорожнения желудка в первом, втором или третьем триместре [81].
Изменения моторики желудка при беременности объясняются высоким уровнем прогестерона. Кроме того, на поздних сроках беременности сдавление увеличенной маткой может способствовать симптомам.
Состав пищи также может играть патогенную роль в NVP.Джеднак и др. продемонстрировали, что прием пищи с преобладанием белка был связан с уменьшением симптомов и коррекцией медленноволновой аритмии. Прием пищи с преобладанием углеводов или жиров не влиял на симптомы или медленноволновую аритмию [82].
Наконец, время прохождения по тонкой кишке было оценено в отношении патогенеза NVP. Используя водородный дыхательный тест с лактулозой, косвенный показатель времени прохождения по тонкой кишке, Lawson et al. обнаружили, что время транзита удлиняется во втором и третьем триместре по сравнению с первым триместром, причем самые длинные времена были обнаружены, когда уровни прогестерона были самыми высокими [83].Уолд и др. использовали аналогичные методы и обнаружили, что время транзита увеличивается в третьем триместре, когда уровни прогестерона и эстрогена были высокими по сравнению с послеродовым периодом [84]. Однако в обоих этих исследованиях задержка кишечного транзита не коррелировала с невирапином.
Психосоциальные факторы
Ранние исследования предполагали, что НВП может быть психосоматическим заболеванием, при котором рвота представляет собой интрапсихический конфликт. Некоторые предполагают, что NVP является проявлением подсознательной попытки беременной женщины отказаться от нежелательной беременности [85], поскольку исследования показали, что у женщин с NVP в первом триместре чаще бывают незапланированные или нежелательные беременности [86].
ГГ также ассоциируется с психологическими расстройствами, а именно невротическими наклонностями, истерией, неприятием женственности, неприятием беременности, а также с депрессией и психологическим стрессом, связанным с бедностью и семейными конфликтами [8]. Однако недавние исследования не выявили определенных психогенных причин ГГ [87, 88]. Некоторые, следовательно, утверждают, что социокультурные факторы, а не научные данные, привели к тому, что HG маркируется как психологически обусловленное состояние, и что более вероятно, что психологические нарушения, такие как депрессия, являются результатом, а не причиной HG [89].
Таким образом, хотя NVP и HG, вероятно, не являются результатом конверсионного расстройства или другого психологического расстройства, общепризнано, что у пострадавших женщин возникают психологические реакции, которые переплетаются с их физическими симптомами и, возможно, усугубляют их.
Диагностика и клинические признаки
Анамнез и медицинский осмотр
Несмотря на популярное использование термина «утренняя тошнота», невирапин сохраняется в течение дня у большинства больных женщин и, как было установлено, ограничивается утром менее чем у 2% женщин [90].Он часто начинается в течение нескольких недель после отсутствия менструации и поэтому в большинстве культур карикатурно изображается как начальный признак беременности. Симптомы обычно достигают пика между 10 и 16 неделями беременности и обычно исчезают после 20 недель. Однако до 10% женщин продолжают иметь симптомы после 22 недель [90].
В то время как обезвоживание и ортостаз могут возникать у женщин с HG, у большинства женщин с NVP показатели жизненно важных функций в норме, а физикальный осмотр является благоприятным. Однако следует провести тщательное обследование брюшной полости, чтобы исключить перитонит и другие внутрибрюшные причины тошноты и рвоты.
Дифференциальный диагноз
Учитывая высокую распространенность невирапина, тошнота и рвота в первом триместре обычно связаны с невирапином. Однако при наличии изменений в работе кишечника, боли в животе и рвоте желчью следует провести соответствующие исследования для исключения других причин. Дифференциальный диагноз невирапина включает гастроэзофагеальную рефлюксную болезнь, язвенную болезнь, непроходимость тонкой кишки, острый холецистит, желчнокаменную болезнь, панкреатит, а также аппендицит, гастроэнтерит, нефролитиаз, пиелонефрит и гепатит [74]
Диагностические и лабораторные исследования
Для диагностики невирапина не рекомендуются никакие специальные лабораторные исследования, кроме теста на беременность.Однако другие тесты могут быть полезны для исключения других причин тошноты и рвоты. Лейкоцитоз не должен наблюдаться при невирапине и может указывать на инфекционную или воспалительную причину, такую как холецистит, инфекция мочевыводящих путей и панкреатит. Повышение уровня аминотрансфераз может свидетельствовать о хроническом гепатите. Аномальный ТТГ может указывать на гипотиреоз или гипертиреоз, оба из которых могут вызывать тошноту и рвоту. Повышение уровня глюкозы в сыворотке может указывать на диабет и может вызывать тошноту и рвоту за счет снижения сократительной способности антрального отдела и ускорения желудочной аритмии [91].
Рентгенография обычно не требуется для диагностики невирапина. УЗИ органов малого таза можно использовать для документирования беременности и оценки состояний, повышающих риск невирапина, таких как многоплодная беременность. Рентген брюшной полости, как правило, бесполезен и, хотя представляет небольшой риск для плода, все еще относительно противоречив в течение первого триместра.
Верхнюю эндоскопию можно безопасно проводить во время беременности и исключить гастрит и ЯБ как причины тошноты и рвоты во время беременности.В одном крупном центре тошнота и рвота были вторым наиболее частым показанием к эндоскопии верхних отделов во время беременности после кровотечения из верхних отделов желудочно-кишечного тракта [92].
Исход
Большинство исследований показали, что невирапин связан с благоприятным исходом для плода. Метаанализ 11 исследований Weigel et al. обнаружили сильную значимую связь между тошнотой и рвотой во время беременности и снижением риска выкидыша (общее отношение шансов = 0,36, 95% ДИ от 0,32 до 0,42) и отсутствие последовательной связи с перинатальной смертностью [93].Кроме того, было обнаружено, что женщины без NVP рожают раньше, чем женщины с NVP [94].
Однако в некоторых исследованиях сообщалось о неблагоприятных исходах, особенно когда невирапин считался тяжелым. Деушар и др. обнаружили повышенный риск задержки внутриутробного развития у женщин с тяжелым НВП, но не смогли объяснить потенциальное влияние противорвотных препаратов на рост плода [95]. Точно так же Zhou et al. обнаружили повышенный риск низкой массы тела при рождении у женщин с тяжелой формой НВП, вероятно, из-за пагубного влияния тошноты и рвоты на питание матери [96].
В проспективном исследовании 16 398 женщин не было обнаружено различий по врожденным аномалиям между женщинами с невирапином и без него [97]. Кроме того, ретроспективное исследование показало более низкий риск врожденных пороков сердца у детей, рожденных от женщин с ранним началом приема невирапина, требующих применения противорвотных средств, по сравнению с женщинами без тошноты [98].
Не совсем ясно, как NVP защищает развивающийся плод, однако было описано несколько теорий. Некоторые утверждают, что тошнота и рвота позволяют беременной женщине избегать или исключать продукты, которые могут быть тератогенными или вызывать аборт.Это может объяснить тесную временную связь между развитием отвращения к еде во время беременности и появлением тошноты [99]. NVP также может снизить потребление энергии и уровень анаболических гормонов, инсулина и фактора роста инсулина, что приводит к шунтированию дефицитных питательных веществ к плаценте и плоду [100].
Несмотря на благоприятное воздействие невирапина на плод, психосоциальные осложнения у беременных с невирапином значительны и, возможно, недооцениваются. В исследовании Smith et al. из 593 австралийских женщин с невирапином большинство сообщили, что их симптомы оказали серьезное негативное влияние на работу, домашние обязанности и воспитание детей, при этом 96% женщин сообщили о легком или умеренном дистрессе из-за тошноты, а 28% сообщили о дистрессе от умеренного до тяжелого [101].Точно так же исследование Mazzotta et al. канадских женщин обнаружили, что более сильная тошнота и рвота связаны с более частым чувством депрессии, рассмотрением вопроса о прерывании беременности, неблагоприятным воздействием на отношения женщин с их партнерами или их повседневную жизнь, а также с предполагаемой вероятностью того, что NVP нанесет вред их ребенку . Примечательно, что женщины с легкими симптомами также сообщали о тех же психосоциальных проблемах, что позволяет предположить, что тяжесть тошноты или рвоты неадекватно отражает дистресс, вызванный невирапином [2].
O’Brien и Naber также выявили значительную психосоциальную заболеваемость у женщин, страдающих невирапином. Они обнаружили, что пострадавшие женщины сообщали о снижении социальных обязательств и ухудшении отношений с супругами и детьми. Женщины с тяжелыми симптомами также сообщали о частой плаксивости, раздражительности, усилении нарушений сна и снижении настроения [102]. Используя краткую форму 36, Attard et al. обнаружили, что женщины с НВП имели более низкие показатели физического функционирования, физической роли, телесной боли, жизнеспособности, социального функционирования и эмоциональной роли в опросе, оценивающем качество жизни, по сравнению со здоровыми беременными контрольной группой на ранних сроках беременности и женщинами с хронической депрессией.Показатели психического здоровья женщин с НВП были аналогичны показателям женщин с депрессией [103].
Помимо того, что невирапин вызывает психосоциальную заболеваемость, он также создает значительное финансовое бремя. В 2002 г. стоимость тяжелого невирапина оценивалась приблизительно в 130 миллионов долларов, исходя из больничных расходов, связанных в среднем с 39 000 госпитализаций. Эта цифра, вероятно, сильно занижена, поскольку она не включает потерю производительности дома, оплату услуг врача или стоимость лечения [104].
Подсчитано, что каждая работающая женщина с невирапином теряет 206 рабочих часов [2] и что на невирапин приходится 28% всех отпусков по болезни во время беременности до 28-й недели [19]. Кроме того, работа Vallacott et al. показывает, что 50% пострадавших женщин считают, что эффективность их работы значительно снижена [105].
HYPEREMESIS GRAVDIARUM
Гиперемезис беременных (HG) — это состояние сильной тошноты и рвоты во время беременности, приводящее к водно-электролитному и кислотно-щелочному дисбалансу, дефициту питательных веществ и потере веса [8].Некоторые определяют его как возникновение более трех эпизодов рвоты в день, сопровождающихся кетонурией и потерей веса более 3 кг или 5% массы тела [63]. ГГ является наиболее частой причиной госпитализации на ранних сроках беременности и уступает только преждевременным родам на протяжении всей беременности [106]. В Соединенных Штатах более 36 000 женщин ежегодно госпитализируются по поводу ХГ, и стоимость лечения оценивается более чем в 250 миллионов долларов в год только на госпитализацию [107].В отличие от NVP, который связан с благоприятными исходами для плода, HG представляет значительный риск для здоровья матери и плода.
Диагностика и клинические признаки
ГГ проявляется в первом триместре беременности, обычно начиная с 4–5-й недели беременности. В дополнение к сильной тошноте и рвоте у 60% женщин с ГГ также наблюдается избыточное слюноотделение или слюнотечение [108]. Пациенты также могут жаловаться на симптомы гастроэзофагеального рефлюкса, такие как дискомфорт за грудиной и изжога. Уникальная количественная оценка рвоты и тошноты (PUQE) для беременных, которая рассчитывается с использованием количества часов тошноты в день, количества эпизодов рвоты в день и количества эпизодов позывов на рвоту в день, может использоваться для отслеживания тяжести симптомов. [109].
Пациенты могут иметь признаки обезвоживания, такие как сухость слизистых оболочек, тахикардия, плохой тургор кожи и постуральная гипотензия. Тяжело пораженные пациенты могут также иметь мышечную атрофию и слабость и/или изменения психического статуса.
Лабораторные нарушения у женщин с HG могут включать повышение азота мочевины в сыворотке крови, креатинина и гематокрита, а также кетонурию и увеличение удельного веса мочи. Кроме того, могут быть обнаружены электролитные нарушения, подтверждающие диагноз либо гипохлоремического метаболического алкалоза, либо метаболического ацидоза с выраженным сокращением объема [39].Уровни преальбумина (транстиретина в плазме) могут быть низкими, отражая плохой статус белкового питания у матери и, возможно, предсказывая более низкую массу тела плода при рождении [110]. Также возможен дефицит витаминов и минералов, таких как витамин B1 (тиамин), железо, кальций и фолиевая кислота [74].
Функциональные пробы печени могут отклоняться от нормы у 50% госпитализированных пациентов с ХГ [111]. Могут наблюдаться умеренная гипербилирубинемия (билирубин < 4 мг на децилитр) и/или повышение уровня щелочной фосфатазы вдвое по сравнению с верхней границей нормы [112].Умеренный трансаминит является наиболее частым нарушением функции печени, при котором уровни аланинаминотрансферазы (АЛТ) обычно превышают уровни аспартатаминотрансферазы (АСТ). Повышение уровня трансаминаз обычно в два-три раза превышает верхнюю границу нормы; однако сообщалось об уровнях выше 1000 ЕД/мл [113]. Аномальные печеночные пробы исчезают сразу же после прекращения рвоты.
Повышение уровня амилазы и липазы в сыворотке наблюдается у 10–15% женщин [39]. Одно исследование выявило повышенный уровень амилазы у 24% пациентов с ХГ [114].Считается, что это связано с избыточной выработкой амилазы слюнными железами, а не с секрецией поджелудочной железы, и является результатом, а не причиной ГГ [8].
Уровни тиреостимулирующего гормона могут быть низкими при ХГ из-за перекрестной реакции между альфа-субъединицей ХГЧ и рецептором ТТГ. В большинстве случаев этот биохимический тиреотоксикоз не имеет клинического значения, так как пациенты находятся в эутиреоидном состоянии. Уровень гормонов щитовидной железы обычно нормализуется без лечения после родов.
HG — это клинический диагноз, основанный на симптомах и исключении других состояний.Как и в случае с невирапином, для диагностики ГГ не требуется специального тестирования; тем не менее, УЗИ брюшной полости и таза может быть полезным для исключения других причин, таких как заболевание желчного пузыря, пузырный занос, а также для оценки многоплодной беременности. Дифференциальный диагноз включает невирапин, острый тиреоидит, расстройства пищевого поведения, заболевания желчевыводящих путей, вирусный гепатит и гастроэзофагеальную рефлюксную болезнь.
Исход
В отличие от NVP, HG связан с неблагоприятными исходами как для матери, так и для плода. В исследовании более 150 000 одноплодных беременностей младенцы, рожденные женщинами с гиперемезисом и низкой прибавкой массы тела при беременности (<7 кг), с большей вероятностью имели низкую массу тела при рождении, маловаты для гестационного возраста, родились до 37 недель беременности и имели мин. Оценка по шкале Апгар < 7 [5].
Общие материнские осложнения включают потерю веса, обезвоживание, дефицит питательных микроэлементов и мышечную слабость. Более тяжелые, хотя и редкие, осложнения включают разрывы Мэллори-Вейса, разрыв пищевода, энцефалопатию Вернике с корсаковским психозом или без него, центральный мостовой миелинолиз из-за быстрой коррекции тяжелой гипонатриемии, кровоизлияние в сетчатку и спонтанный пневмомедиастинум [47]. Также сообщалось о вазоспазме церебральных артерий из-за повышенной симпатической активности [115].
HG способствует возникновению многих психологических проблем и может привести к прерыванию нежелательной беременности и снижению вероятности попытки повторной беременности [116]. Пуршариф и др. обнаружили, что у 15% из 808 женщин с HG было по крайней мере одно прерывание беременности из-за болезни. Интересно, что у тех женщин, которые прервали беременность, не было более тяжелого заболевания, чем у женщин с ГГ, которые сохранили беременность, но в два раза чаще считали, что их врач безразличен или не обратил внимания на тяжесть их заболевания [117].
Долгосрочные последствия HG для матерей неизвестны. Несколько исследований показывают повышенный риск рака молочной железы [118]. Имеются также сообщения о повышенной частоте депрессии, посттравматического стрессового расстройства и различных неврологических расстройств [39].
Некоторые исследования не выявили повышенного риска неблагоприятных исходов для плода у женщин с ГГ. Башири и соавт., например, сообщили о более низкой частоте спонтанных ранних потерь беременности у женщин с ГГ по сравнению с общей популяцией и не обнаружили различий в перинатальных исходах [6].Однако в других исследованиях была обнаружена связь между ГГ и задержкой роста плода, преэклампсией и малым весом для гестационного возраста [119]. В ретроспективном исследовании 3068 женщин ГГ была связана с более ранними родами и меньшей массой тела при рождении. Эти исходы были наиболее вероятны у женщин, которые потеряли более 5% массы тела до беременности [120]. Точно так же Dodds et al. обнаружили более высокие показатели низкой массы тела при рождении, преждевременных родов, гибели плода у женщин с ХГ, которые в целом набрали менее 7 кг во время беременности [5].Многократные госпитализации по поводу ХГ, по-видимому, являются еще одним фактором риска снижения массы тела новорожденных при рождении [108].
Различные врожденные пороки развития чаще наблюдаются у женщин с ХГ [32]. К ним относятся синдром Дауна, дисплазия тазобедренного сустава, неопущение яичек, пороки развития скелета, дефекты центральной нервной системы и аномалии кожи. Сообщалось о коагулопатии плода и хондродисплазии из-за дефицита витамина К [121] с внутричерепным кровоизлиянием плода в третьем триместре [122].Некоторые виды рака у детей, такие как рак яичек или лейкемия, также были связаны с ГГ у матери, однако данные противоречивы [39].
ЛЕЧЕНИЕ
Целью лечения является облегчение симптомов при минимизации риска для матери и плода. Для достижения этого обычно необходим мультимодальный подход, адаптированный к каждому человеку. Методы лечения варьируются от простых диетических модификаций до медикаментозной терапии и полного родительского питания. Тяжесть симптомов и потеря веса матери помогают определить агрессивность лечения.PUQEscore и опросник по влиянию гиперемезиса на симптомы (HIS) можно использовать для оценки тяжести симптомов. Обновленная шкала PUQE оценивает симптомы в течение 24 часов [123], в то время как HIS учитывает психосоциальные факторы в дополнение к физическим симптомам [124].
Текущие исследования показывают, что лечение невирапином является субоптимальным. Одно недавнее проспективное исследование 283 женщин с невирапином в течение первого триместра показало, что только половине из них задавали вопрос об интенсивности и тяжести их симптомов, менее четверти спрашивали, мешают ли их симптомы их повседневным задачам и работе.В этом исследовании Lacasse et al только 27% женщин были предложены противорвотные средства, а еще 14% были рекомендованы немедикаментозные методы лечения [125].
Немедикаментозная терапия
Диетические меры
Начальная терапия невирапина и ГГ должна включать диетические изменения. Пораженные женщины должны избегать больших приемов пищи и вместо этого есть несколько небольших приемов пищи в течение дня, которые должны быть пресными и с низким содержанием жира, поскольку жирная пища может еще больше задержать опорожнение желудка. Употребление белка больше, чем углеводов, и употребление большего количества жидкости, чем твердой пищи, также может уменьшить тошноту, уменьшая желудочные аритмии, связанные с невирапином [82].Рекомендуются небольшие объемы соленых жидкостей, таких как электролитозамещающие спортивные напитки, а если запах горячей пищи является неприятным, следует приготовить холодную пищу [126].
Эмоциональная поддержка
Эмоциональную поддержку всегда должен оказывать медицинский работник. Кроме того, поддерживающая психотерапия, поведенческая терапия и гипнотерапия могут быть полезны для женщин с тяжелыми симптомами и/или для тех, у кого играют роль личностные особенности, супружеские или семейные конфликты [60].Цель психотерапии не в том, чтобы углубляться в психологию, которая может способствовать НВП, а в том, чтобы поощрять, объяснять, успокаивать и позволять пациенту выражать стресс [95].
Акупрессура/акупунктура
Акупрессура китайской акупунктурной точки Р6 (Нэйгуань) снижает тошноту у пациентов с тошнотой, вызванной химиотерапией, а также послеоперационной тошнотой и рвотой, и может быть полезна при лечении ГГ. В соответствии с принципом ци, приложение давления к этой точке блокирует аномальное замедление энергии и восстанавливает симптомы, связанные с точкой давления [13].Давление можно оказывать вручную или с помощью эластичных лент на внутренней стороне запястья. Кроме того, ReliefBand, электрический стимулятор нервов с батарейным питанием, который носится на запястье, недавно был одобрен FDA и может также использоваться для стимуляции участка P6 [127].
Доказательства акупрессуры противоречивы. Один обзор семи испытаний показал, что акупрессура точки Neiguan может облегчить симптомы тошноты [128]. Недавнее плацебо-контролируемое исследование с участием 60 женщин, принимавших невирапин, показало, что в группе лечения наблюдалось облегчение тошноты на следующий день после начала акупрессуры над местом P6, которое продолжалось до конца периода наблюдения.Для сравнения, в группе, получавшей акупрессуру на незначительном участке, наблюдалось первоначальное облегчение симптомов, но к 6-му дню симптомы вернулись и не отличались от группы, не получавшей лечения [129].
Хотя исследования преимуществ акупрессуры не дали окончательных результатов, некоторые эксперты считают, что это вмешательство должно быть предложено, поскольку не существует известных побочных эффектов [130].
Иглоукалывание менее изучено, но одно слепое рандомизированное контролируемое исследование с участием 593 женщин со сроком беременности менее 14 недель показало, что у женщин, получавших еженедельное лечение иглоукалыванием в течение 4 недель, было меньше тошноты и сухих рвотных позывов по сравнению с контрольной группой [131].Однако возможно, что состояние некоторых женщин улучшилось просто с увеличением гестационного возраста [13].
Имбирь
Имбирь — единственное немедикаментозное вмешательство, рекомендованное Американским колледжем акушерства и гинекологии [132]. Считается, что имбирь помогает улучшить НВП, стимулируя моторику желудочно-кишечного тракта и стимулируя выделение слюны, желчи и желудочного секрета. Было показано, что один компонент имбиря обладает такой же активностью, что и антагонист 5-HT3, ондансетрон.Кроме того, было обнаружено, что его экстракт ингибирует рост некоторых штаммов H. pylori [133].
В двойном слепом рандомизированном перекрестном исследовании 70% женщин с ГГ, получавших 250 мг порошкообразного корня имбиря четыре раза в день, предпочли период приема имбиря по сравнению с периодом приема плацебо. Женщины также сообщали о значительно большем облегчении симптомов при приеме имбиря. 4 дня обнаружили, что у женщин в группе лечения было значительное улучшение симптомов тошноты по сравнению с женщинами в группе плацебо ( P <.001) [135].
Что касается безопасности имбиря во время беременности, исследование случай-контроль с участием 187 беременных женщин не выявило увеличения частоты серьезных пороков развития при употреблении имбиря в первом триместре [136]. Однако существует теоретический риск кровотечения, поскольку имбирь ингибирует тромбоксансинтетазу и может ингибировать функцию тромбоцитов. Таким образом, одновременное использование антикоагулянтов с имбирем не рекомендуется [137].
Фармакологическое лечение
Пиридоксин-доксиламин
Комбинация пиридоксина (витамина В6) (категория А при беременности) и доксиламина (категория В), ранее доступная как бендектин, является единственным лекарственным средством, которое специально маркировано для лечения невирапина Управление по санитарному надзору за качеством пищевых продуктов и медикаментов.Он по-прежнему доступен в Канаде в таблетках с отсроченным высвобождением, содержащих 10 мг пиридоксина и 10 мг доксиламина, под торговым названием Диклектин.
Бенедектин был снят с продажи в 1983 году в США в связи с сообщениями о врожденных пороках развития при применении в первом триместре. Однако до его отмены 30 миллионов женщин принимали его в течение почти 25 лет. Несколько небольших рандомизированных контролируемых исследований подтверждают его эффективность [138]. Кроме того, метаанализ, который включал 170 000 воздействий, показал, что комбинация пиридоксин-доксиламин безопасна и не вызывает побочных эффектов у плода [139].Другие крупные исследования также не показали увеличения частоты врожденных аномалий по сравнению с фоновой частотой [140]. Тем не менее, Бенедектин остается вне рынка в Соединенных Штатах. Однако женщины могут сделать свой собственный препарат, объединив 10 мг пиридоксина с половинкой таблетки Унисома, который содержит 25 мг доксиламина.
В качестве альтернативы пиридоксин можно принимать отдельно. Хотя связи между уровнями пиридоксина и невирапином не обнаружено, в нескольких исследованиях было показано улучшение показателей тошноты у пациентов, принимавших пиридоксин с выраженной тошнотой [141], и уменьшение эпизодов рвоты по сравнению с женщинами, принимавшими плацебо [138].Нет известных доказательств токсичности витамина B6, однако в больших дозах пиридоксин был связан с обратимой периферической нейропатией у небеременных взрослых [13].
Противорвотные средства
Фенотиазины, хлорпромазин (торазин) и прохлорперазин (компазин), являются центральными и периферическими антагонистами дофамина, которые, как было показано, уменьшают симптомы невирапина и ГГ [142]. Они относятся к категории беременности С.
Исследование 12 764 беременных женщин показало незначительное повышение риска врожденных дефектов при применении фенотиазинов в первом триместре, особенно при применении хлорпромазина, однако потенциальные смешанные факторы, такие как употребление алкоголя и продолжительность лечения, не были выявлены. 143].Другое исследование показало, что у младенцев от матерей, принимавших хлорпромазин, были экстрапирамидные симптомы и желтуха; значительных нарушений постнатального развития не было [144].
Прометазин (Phenergan) не обладал тератогенными эффектами в одном исследовании [145], но в другом исследовании наблюдалось усиление врожденного вывиха бедра [146].
Активаторы
Метоклопрамид (Реглан) широко используется для лечения невирапина [147]. Это категория беременности B. Считается, что метоклопрамид улучшает симптомы за счет повышения давления в нижнем пищеводном сфинктере и увеличения транзита через желудочный тракт.Он также корректирует желудочные аритмии, стимулируя антральные сокращения и способствуя антродуоденальным сокращениям. Недавнее исследование показало, что 10 мг метоклопрамида, принимаемого каждые 8 часов, столь же эффективны для уменьшения количества эпизодов рвоты и улучшения самочувствия у женщин с ГГ во время их первой госпитализации, как и 25 мг прометазина, принимаемого каждые 8 часов в течение 24 часов. Профиль побочных эффектов был лучше в группе, получавшей метоклопрамид, с меньшей сонливостью, головокружением и дистонией [148].
Что касается безопасности, исследование 81 703 родов в период с 1998 по 2007 год в Израиле, в ходе которого метоклопрамид применялся у 4,2% женщин, не выявило повышенного риска серьезных врожденных пороков развития, низкой массы тела при рождении, преждевременных родов или перинатальной смерти при применении метаклопрамида. использовать [149]. Точно так же датское исследование 309 беременных женщин, принимавших метаклопрамид, не выявило повышенного риска [150].
Несмотря на свою эффективность, использование метоклопрамида ограничено его побочными эффектами, которые включают дистонию, беспокойство и сонливость.В 2009 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) добавило к метоклопрамиду предупреждение «черный ящик» из-за риска поздней дискинезии при хроническом применении.
Другие прокинетики, такие как домперидон и эритромицин, не изучались при применении невирапина [74].
Антигистаминные и антихолинергические препараты
Антигистаминные препараты косвенно влияют на вестибулярную систему, уменьшая стимуляцию рвотного центра [151]. Рандомизированные контролируемые исследования применения антигистаминных препаратов при невирапине ограничены; однако было показано, что меклизин (анитверт), дименгирдинат (драмамин) и дифенгирамин (бенадрил) контролируют симптомы лучше, чем плацебо [142].Кроме того, объединенные данные семи испытаний между 1951 и 1975 годами показали эффективность антигистаминных препаратов [152]. Метаанализ более 24 контролируемых исследований с участием более 200 000 беременных женщин показал, что антигистаминные препараты (в частности блокаторы Н2-рецепторов), назначаемые в течение первого триместра, не повышают риск тератогенного действия [153]. Хотя ранее считалось, что меклизин обладает тератогенным действием, теперь исследования показывают, что его безопасно использовать во время беременности [154]. Дименгидринат и дифенгидрамин имеют противоречивые результаты по безопасности [74].
В одном исследовании женщин, перенесших плановое кесарево сечение, было обнаружено, что трансдермальный скополамин более эффективен в уменьшении тошноты, рвоты и позывов на рвоту из-за эпидуральной морфиновой анальгезии по сравнению с плацебо [155]. Однако исследования по применению скополамина в первом триместре отсутствуют, поскольку скополамин может вызывать хромосомные аберрации и обмены сестринскими хроматидами в здоровых взрослых лимфоцитах и может приводить к врожденным порокам развития, включая деформацию конечностей и туловища [156].
Другие препараты
Ондансетрон (Зофран) (категория B при беременности) широко используется для лечения послеоперационной и вызванной химиотерапией тошноты и рвоты и в настоящее время является одним из наиболее часто назначаемых противорвотных средств [157].Считается, что он действует как центрально, так и периферически, блокируя серотониновые рецепторы в тонкой кишке и медуллярном рвотном центре [151]. Его безопасность при беременности была определена в недавнем исследовании, которое не показало значительного увеличения числа выкидышей, серьезных пороков развития или массы тела при рождении между младенцами, подвергшимися воздействию ондансетрона, и контрольной группой, не получавшей его [158].
Было проведено одно рандомизированное контролируемое исследование применения ондансетрона для лечения ХГ. В этом небольшом исследовании с участием 30 женщин не было выявлено преимуществ ондансетрона в дозе 10 мг внутривенно каждые 8 часов по мере необходимости по сравнению с прометазином в дозе 50 мг внутривенно каждые 8 часов с точки зрения тошноты, увеличения веса, дней госпитализации или общих доз препарата [46]. .Однако было обнаружено, что прометазин вызывает больший седативный эффект. Тем не менее, сообщения о случаях заболевания и широко распространенный клинический опыт подтверждают эффективность ондансетрона для лечения HG и его лучшую переносимость по сравнению с более ранними противорвотными средствами [159, 160].
Дроперидол (инапсин) является антагонистом дофамина, эффективным противорвотным средством при послеоперационной тошноте и рвоте. Небольшое исследование женщин с HG показало, что комбинация непрерывной инфузии дроперидола и болюсного внутривенного введения дифенгидрамина приводила к более коротким госпитализациям и меньшему количеству повторных госпитализаций по сравнению с исторической контрольной группой, которая получала другие формы парентеральной терапии.Кроме того, не было никаких существенных различий в материнских или перинатальных исходах [161]. Следует отметить, однако, что дроперидол имеет предупреждение черного ящика, поскольку он может вызывать удлинение интервала QT и сердечные аритмии [74].
Пероральные и внутривенные кортикостероиды использовались для рефрактерных случаев HG с переменными результатами. Считается, что они оказывают противорвотное действие на триггерную зону хеморецепторов в стволе головного мозга, а также постулируются для коррекции «относительной надпочечниковой недостаточности», вызванной HG, при которой гипоталамо-гипофизарно-надпочечниковая ось не может реагировать на повышенные потребности в кортизоле. во время ранней беременности.
В рандомизированном контролируемом исследовании 40 женщин с ГГ, получавших метилпреднизолон в дозе 16 мг перорально 3 раза в день в течение 3 дней с последующим 2-недельным снижением дозы, по сравнению с прометазином в дозе 25 мг перорально 3 раза в день в течение 2 недель, — госпитализация была обнаружена в группе, получавшей стероиды [162]. Другие исследования не показали статистически значимого преимущества кортикостероидов. Рандомизированное исследование Yost et al. не обнаружили значительного снижения числа посещений неотложной помощи или повторных госпитализаций при добавлении парентерального и перорального метилпреднизолона к режиму прометазина и метоклопрамида [163].
Нет утвержденных руководств по применению кортикостероидов при ХГ. Однако была предложена возможная схема: 48 мг метилпреднизолона вводят перорально или внутривенно в три приема в течение двух-трех дней. Если в течение трех дней ответа не наблюдается, рекомендуется прекратить лечение, так как ответ через 72 часа маловероятен [151].
Что касается безопасности, то недавний метаанализ показал небольшое увеличение основных пороков развития и 3,4-кратное увеличение расщелины рта у младенцев, матери которых принимали кортикостероиды в первом триместре [164].
В последнее время наблюдается интерес к препаратам, снижающим кислотность при лечении невирапином, поскольку одно недавнее когортное исследование показало, что у женщин с невирапином и изжогой и/или кислотным рефлюксом тошнота и рвота были более выраженными, чем у женщин без изжоги или кислотного рефлюкса [165]. Кроме того, последующие исследования показали, что лечение изжоги и/или рефлюкса приводит к улучшению показателей PUQE и показателей качества жизни [166].
Антациды, содержащие алюминий или кальций, являются терапией первой линии во время беременности при кислотном рефлюксе и изжоге и могут использоваться для лечения женщин с невирапином.Антациды, содержащие магний, связаны с нефролитиазом, гипотонией и респираторным дистресс-синдромом у плода и не рекомендуются во время беременности. Антациды, содержащие бикарбонаты, могут вызывать метаболический ацидоз плода и перегрузку жидкостью и также не рекомендуются [167].
Блокаторы h3 и ингибиторы протонной помпы можно безопасно использовать для лечения кислотного рефлюкса и/или изжоги у женщин с невирапином [168, 169].
Нутритивная поддержка
Женщинам с трудноизлечимыми симптомами, не поддающимися коррекции диеты и фармакологическому лечению и неспособными поддерживать вес за счет перорального приема пищи, может потребоваться пищевая поддержка.В этой популяции следует использовать внутривенную инфузионную терапию, энтеральное или парентеральное питание для предотвращения задержки внутриутробного развития плода, обезвоживания матери и недостаточности питания.
Роль внутривенной гидратации заключается в увеличении объема и восстановлении электролитов. Госпитализированным пациентам при необходимости можно быстро влить физиологический раствор или раствор Рингера с лактатом, а затем откорректировать их для соответствия диурезу. Внутривенно тиамин следует вводить перед любыми жидкостями, содержащими декстрозу, чтобы избежать энцефалопатии Вернике.Женщинам, которым требуется многократная госпитализация, может быть рекомендована внутривенная гидратация в домашних условиях [74].
Энтеральное зондовое питание и полное парентеральное питание следует рассмотреть, если внутривенная терапия не помогает уменьшить симптомы, а дефицит калорий сохраняется. Однако исследования энтерального питания при HG ограничены. В одном небольшом исследовании женщин с HG, получавших энтеральное питание с использованием назогастрального зонда 8-French, сообщалось об улучшении симптомов в течение 24 часов после установки зонда.Через 8 дней пациенты были выписаны в среднем на 43 дополнительных дня амбулаторного энтерального питания, после чего можно было возобновить пероральное питание [170].
Помимо назогастральных зондов, чрескожная эндоскопическая гастростомия (ЧЭГ) [171] успешно использовалась для поддержания питания у женщин с ГГ. Однако оба этих способа кормления ограничены риском усиления тошноты и рвоты, вызванных внутрижелудочным кормлением. Постпилорические зонды для кормления, как назоеюнальные [172, 173], так и чрескожные эндоскопические гастроеюноанастомозы [174] пытались снизить этот риск, однако смещение зондов [175] из-за продолжающейся рвоты, позывов на рвоту и свертывания желудка является частым осложнением. .Кроме того, назоэнтеральные зонды, как назогастральные, так и назоеюнальные, плохо переносятся многими женщинами из-за эстетических соображений и физического дискомфорта. Недавно хирургическая еюностомия была описана как альтернативный способ доставки питания женщинам с HG. В одном небольшом исследовании пяти женщинам с HG была выполнена хирургическая еюностомия во втором триместре. Изотонические кормления через зонд вводили до целевого показателя калорийности. Прибавка в весе матери наблюдалась в 5 из 6 беременностей, и все беременности закончились срочными родами.Серьезных осложнений не произошло, что позволяет предположить, что еюностомия может быть безопасным и эффективным способом нутритивной поддержки у женщин с ХГ [176].
Женщинам, которые не переносят энтеральное питание, следует рассмотреть возможность парентерального питания. Эта терапия, однако, является дорогостоящей и связана со значительной материнской заболеваемостью. Руссо-Стейглиц и др. сообщили о частоте осложнений 9% при парентеральном питании через периферически установленные центральные катетеры во время беременности и о 50% частоте осложнений при центрально вставленных катетерах.Инфекция и тромбоз были двумя наиболее часто встречающимися осложнениями, и предполагалось, что они являются результатом связанной с беременностью гиперкоагуляции и иммунологической супрессии [177]. Holmgren et al. также показали высокую частоту осложнений у женщин, получавших парентеральное питание через PICC. В исследовании 94 женщин с HG 66,4% из тех, кто получал парентеральное питание через PICC, нуждались в лечении тромбоэмболии, инфекции или того и другого. Пациентки на парентеральном питании также имели более высокую частоту неонатальных осложнений, включая госпитализацию в отделение интенсивной терапии новорожденных, малый размер для гестационного возраста, прерывание беременности из-за ГГ и потерю плода по сравнению с женщинами, получавшими энтеральное питание [178].Таким образом, парентеральное питание, хотя оно может быть более переносимым для пациентов, следует зарезервировать для отдельных пациентов с HG.
Информация для авторов
Ноэль М. Ли, Школа медицины и общественного здравоохранения Университета Висконсина, Медицинский фонд Университета Вашингтона, здание столетия, 1685 Highland Avenue, Madison, WI 53705, телефон: (608) 263-1995, факс: (608) 265-5677.
Сумона Саха, Отделение гастроэнтерологии и гепатологии, Школа медицины и общественного здравоохранения Висконсинского университета, Медицинский фонд Университета Вашингтона, здание столетия, 1685 Хайленд-авеню, комната 4224, Мэдисон, Висконсин 53705, телефон: (608) 263-1995, факс: (608) 265-5677.

 Vomiting During Pregnancy Treatment // WebMD. — 2020. — 14 January.
Vomiting During Pregnancy Treatment // WebMD. — 2020. — 14 January.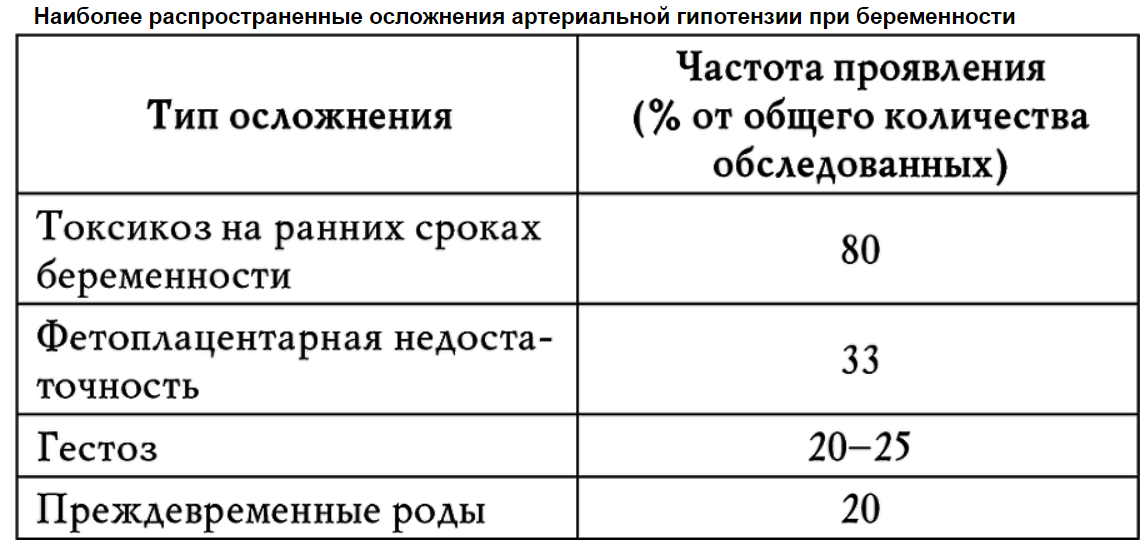 Чтобы он не избавился от плода, за счет особого механизма угнетается работа иммунной системы. Это тоже тесно связано с работой гормонов. А следовательно, любую простуду вы будете переносить намного тяжелей.
Чтобы он не избавился от плода, за счет особого механизма угнетается работа иммунной системы. Это тоже тесно связано с работой гормонов. А следовательно, любую простуду вы будете переносить намного тяжелей. Не все, но большинство из них способствует утренней слабости и тошноте.
Не все, но большинство из них способствует утренней слабости и тошноте.
 Возникает в результате сильного переутомления и недостаточного приема пищи. Побороть его можно, если разнообразить питание и совершать прогулки перед сном.
Возникает в результате сильного переутомления и недостаточного приема пищи. Побороть его можно, если разнообразить питание и совершать прогулки перед сном.