Релатокс инструкция по применению: показания, противопоказания, побочное действие – описание Relatox лиофилизат д/пригот. р-ра д/инъекций 100 ЕД: фл. или банка в компл. с растворителем или без него (33947)
Перед разведением препарата центральную часть пробки флакона обрабатывают спиртом этиловым. Препарат растворяют, вводя во флакон 1-8 мл 0.9% раствора натрия хлорида для инъекций путем прокола пробки стерильной иглой длиной 23 или 25 мм. Запрещается открывать флакон и удалять пробку. Раствор препарата представляет собой прозрачную бесцветную жидкость.
Приготовленный инъекционный раствор вводят инсулиновым шприцем с несъемной иглой диаметром 0.27-0.29 мм. Положение пациента при введении препарата в мышцы лица — сидя на стуле, затылок зафиксирован.
Таблица 1. Концентрации препарата, получаемые при разведении Релатокс® Токсин ботулинический типа А в комплексе с гемагглютинином 50 ЕД
| Объем 0.9% раствора натрия хлорида для инъекций, мл | Активность препарата (ЕД в 0. 1 мл) 1 мл) |
| 1 | 5 |
| 2 | 2.5 |
| 2.5 | 2.0 |
| 4 | 1.25 |
Таблица 2. Концентрации препарата, получаемые при разведении Релатокс® Токсин ботулинический типа А в комплексе с гемагглютинином 100 ЕД
| Объем 0.9% раствора натрия хлорида для инъекций, мл | Активность препарата (ЕД в 0.1 мл) |
| 2 | 5 |
| 4 | 2.5 |
| 5 | 2.0 |
| 8 | 1.25 |
Дозы, схемы и способы введения препарата при коррекции мимических морщин
Сглаживание межбровных морщин
В процессе формирования межбровных морщин участвуют musculus corrugator supercilii (мышца, сморщивающая бровь) и musculus procerus (мышца гордецов).
Для определения места инъекций с целью устранения межбровных морщин пациента просят нахмуриться, в этот момент хорошо пальпируется musculus corrugator supercilii, при этом точка наиболее выраженной мышечной активности должна находиться на 0. 5 см вверх от верхнего медиального края брови. Аналогичным образом производят разметку на другой стороне. Игла вводится в толщу брюшка, направление иглы — либо под углом 45° спереди назад, медиально, либо под углом 90°. Глубина введения иглы — 7-10 мм. Если игла упрется в надкостницу, ее надо вытянуть на 1 мм и после этого ввести препарат. Точка введения препарата в musculus procerus располагается в центре линии, соединяющей медиальные края бровей. Положение иглы — спереди назад, глубина введения иглы — 2-3 мм.
5 см вверх от верхнего медиального края брови. Аналогичным образом производят разметку на другой стороне. Игла вводится в толщу брюшка, направление иглы — либо под углом 45° спереди назад, медиально, либо под углом 90°. Глубина введения иглы — 7-10 мм. Если игла упрется в надкостницу, ее надо вытянуть на 1 мм и после этого ввести препарат. Точка введения препарата в musculus procerus располагается в центре линии, соединяющей медиальные края бровей. Положение иглы — спереди назад, глубина введения иглы — 2-3 мм.
В каждую отмеченную точку вводят препарат Релатокс® Токсин ботулинический типа А в комплексе с гемагглютинином от 2.5 до 7.5 ЕД в зависимости от выраженности морщин, возраста и пола. Общее количество препарата, введенного в эту область, не должно превышать 25 ЕД.
Сглаживание горизонтальных морщин в области лба.
В образовании горизонтальных морщин в области лба участвует musculus epicranius (мышца надчерепная). Для сглаживания лобных морщин пациента просят поднять брови и на максимуме амплитуды отмечают точки с наиболее выраженной мимической активностью.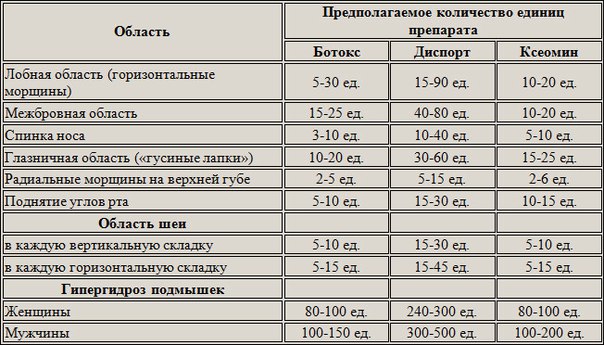
Сглаживание морщин в периорбитальной области
Морщины, расходящиеся радиально вокруг глаз, так называемые «гусиные лапки», возникают в результате активности круговой мышцы глаза. Для выбора дозы надо попросить пациента рассмеяться и в это время очертить примерные границы области кожи с максимальным количеством складок.
Для уменьшения «гусиных лапок» необходимо произвести несколько инъекций (от 2 до 4 с каждой стороны) в область проекции musculus orbicularis oculi (мышца глаза круговая) на расстоянии не менее чем 1 см от наружного угла глаза, а также в область латеральной части нижнего века в местах максимальной мышечной активности. Расчет дозы производится исходя из площади этой поверхности в покое: в каждую точку вводится 2.0-2.5 ЕД препарата, диффузия из одной точки имеет радиус 0.5-1.0 см, следовательно, расстояние между точками введения должно составлять в среднем 1.0-2.0 см. Максимально допустимое количество вводимых в периорбитальную область единиц не более 25 ЕД на одну сторону. Чтобы не нарушать пропорции лица, необходимо тщательно следить за симметричностью расположения точек введения. Препарат в области «гусиных лапок» не вводится очень низко, т.к. возможно нарушение симметричности углов рта и носогубной складки вследствие диффузии препарата в область musculus zygomaticus major (мышца скуловая большая).
Сглаживание морщин в области спинки носа
При наличии выраженных морщин в области спинки носа препарат вводится непосредственно в musculus nasalis (мышца носовая) с каждой стороны по 2.5 ЕД препарата.
Сглаживание морщин в нижней части лица
Крылья носа. Препарат вводится непосредственно в крыльную часть musculus nasalis по 2.5 ЕД с каждой стороны.
Верхняя губа. Инъекции производятся вдоль красной каймы верхней губы в/к непосредственно в морщины, отступая от края на 2 мм, по 1.25 ЕД в каждую точку, количество точек от 4 до 6.
Углы рта. Препарат вводится п/к в количестве 2.5 ЕД непосредственно в musculus depressor anguli oris (мышца, опускающая угол рта).
Подбородок. Препарат вводится п/к в количестве 2.5 ЕД непосредственно в musculus mentalis (мышца подбородочная).
Дозы, схемы и способ введения препарата при лечении блефароспазма
При лечении блефароспазма препарат вводится поверхностно в/м шприцем с иглой калибром 28-30 в следующие точки: две точки на верхнем веке, одна точка на латеральной половине нижнего века и одна точка у латерального угла глаза.
Максимально допустимое количество вводимых в периорбитальную область единиц не более 25 ЕД на одну сторону.
Выраженный клинический эффект от введения препарата проявляется в интервале от 2 до 14 дней после инъекции, в зависимости от индивидуальных особенностей организма, и длится в течение 4-6 месяцев.
При неэффективности первой процедуры при любом выше описанном лечении, т.е. отсутствия значительного клинического улучшения, по сравнению с исходным состоянием, через 1 месяц после введения препарата, необходимо:
- клиническое подтверждение действия токсина на инъецированную мышцу (мышцы), которое может включать электромиографическое (ЭМГ) исследование, выполняемое опытным специалистом в специализированном отделении;
- анализ причин неэффективности процедуры, например, неадекватный выбор точек для инъекции, недостаточная доза, неправильная техника инъекции, признаки фиксированной контрактуры, слабость мышц-антагонистов, формирование токсиннейтрализующих антител;
- повторная оценка целесообразности лечения ботулиническим токсином типа А;
- при отсутствии каких-либо нежелательных эффектов, связанных с первым введением препарата, при повторной процедуре должны быть соблюдены следующие условия: коррекция дозы с учетом анализа причин неэффективности предыдущей процедуры; ЭМГ-контроль; интервал между процедурами должен составлять не менее 3 месяцев.

При отсутствии эффекта от введения препарата или снижении его выраженности после повторных инъекций, следует рекомендовать другие методы лечения.
Дозы и способ введения препарата при лечении спастичности мышц верхней конечности после ишемического инсульта
Раствор препарата вводят иглой размером 25G, 27G или 30G в поверхностные мышцы и более длинной иглой в глубокие мышцы верхней конечности.
Раствор препарата можно вводить под электромиографическим контролем для установления мышц, вовлеченных в патологический процесс с использованием иглы для ЭМГ-контроля.
Расчет дозы препарата и определение числа точек для инъекций проводится индивидуально для каждого пациента с учетом размера мышц, числа и локализации вовлеченных в патологический процесс мышц, выраженности спастичности.
Таблица 3. Дозы препарата Релатокс® Токсин ботулинический типа А в комплексе с гемагглютинином при введении в мышцы верхней конечности
| Мышца | Суммарная доза |
| Сгибатели пальцев | |
| musculus flexor digitorum profundus (Глубокий сгибатель пальцев) | 15-50 ЕД |
| musculus flexor digitorum superficialis (Поверхностный сгибатель пальцев) | 15-50 ЕД |
| musculus adductor pollicis (Мышца, приводящая большой палец кисти) | 20 ЕД |
| musculus flexor pollicis longus (Длинный сгибатель большого пальца кисти) | 20 ЕД |
| Сгибатели кисти | |
| musculus flexor carpi radialis (Лучевой сгибатель запястья) | 15-60 ЕД |
| musculus flexor carpi ulnaris (Локтевой сгибатель запястья) | 10-50 ЕД |
| Сгибатели локтевого сустава | |
| musculus biceps brachii (Двуглавая мышца плеча) | 100-150 ЕД |
| musculus brachialis (Плечевая мышца) | 20-60 ЕД |
| musculus brachioradialis (Плече-лучевая мышца) | 20-100 ЕД |
| musculus pronator teres (Круглый вращатель предплечья) | 10-30 ЕД |
| Мышцы, приводящие плечевой сустав к туловищу | |
| musculus pectoralis major (Большая грудная мышца) | 20-100 ЕД |
| musculus teres major (Большая круглая мышца) | 5-40 ЕД |
| musculus latissimus dorsi (Широчайшая мышца спины) | 20-100 ЕД |
Максимальная суммарная разовая доза на один курс лечения, использованная в клинических исследованиях, составила не более 400 ЕД, распределенная между выбранными мышцами.
В клинических исследованиях период наблюдения за пациентами составил 12 недель после инъекции. Уменьшение мышечного тонуса отмечалось через неделю после инъекции, достигая максимума в течение 4-8 недель. На 12 неделе также отмечалось снижение уровня спастичности по сравнению с исходным уровнем.
Целесообразно применять инъекции препаратом Релатокс® Токсин ботулинический типа А в комплексе с гемагглютинином в комбинации со стандартной схемой лечения и реабилитации постинсультной спастичности.
Дозы и способ введения препарата при лечении спастичности верхней и нижней конечностей у детей 2-17 лет с детским церебральным параличом
Раствор препарата вводят иглой размером 23-26G.
Раствор препарата возможно вводить под электромиографическим (ЭМГ) контролем для установления мышц, вовлеченных в патологический процесс, с использованием иглы для ЭМГ-контроля.
Расчет дозы препарата и определение числа точек для инъекций проводится индивидуально для каждого пациента с учетом размера мышц, числом и локализацией вовлеченных в патологический процесс мышц, выраженности спастичности.
Таблица 4. Дозы препарата Релатокс® Токсин ботулинический типа А в комплексе с гемагглютинином при введении в мышцы верхней и нижней конечностей при лечении спастичности у детей с ДЦП в возрасте 2-17 лет
| Мышца | Суммарная доза |
| Синдромы спастичности с преимущественным вовлечением мышц нижней конечности | |
| - Спастическая эквинусная установка стопы (динамический эквинус или трицепс-синдром): | |
| musculus gastrocnemius (Икроножная мышца) | 4-6 ЕД/кг |
| musculus soleus (Камбаловидная мышца) | 6-8 ЕД/кг |
| musculus soleus tibialis posterior (Задняя большеберцовая мышца) | 2-4 ЕД/кг |
| — Аддукторный синдром: | |
| musculus adductor longus (Длинная приводящая мышца бедра) | 4-6 ЕД/кг |
| musculus adductor brevis (Короткая приводящая мышца бедра) | 4-6 ЕД/кг |
| musculus adductor magnus (Большая приводящая мышца бедра) | 4-6 ЕД/кг |
| — Синдром, сопровождающийся повышением тонуса в заднемедиальной группе мышц бедра (Hamstring-синдром): | |
| musculus biceps femoris (Двуглавая мышца бедра) | 6-10 ЕД/кг |
| musculus semimembranosus (Полуперепончатая мышца) | 4-6 ЕД/кг |
| musculus semitendinosus (Полусухожильная мышца) | 6-10 ЕД/кг |
| — Повышение спастичности в четырехглавой мышце бедра (Rectus-синдром)**: | |
| musculus rectus femoris (Прямая мышца бедра) | 4-6 ЕД/кг |
| musculus vastus lateralis (Латеральная порция четырехглавой мышцы бедра) | 4-6 ЕД/кг |
| Синдромы спастичности с преимущественным вовлечением мышц верхней конечности | |
| — Сгибательно-пронаторная установка предплечья: | |
| musculus pronator teres (Круглый вращатель предплечья) | 0. 8-1.6 ЕД/кг 8-1.6 ЕД/кг |
| musculus pronator quadratus (Квадратный вращатель предплечья) | 0.8-1.6 ЕД/кг |
| musculus biceps brachii (Двуглавая мышца плеча) | 1.6-3.2 ЕД/кг |
| musculus brachialis (Плечевая мышца) | 1.6-3.2 ЕД/кг |
| — Синдром приведения плеча и его внутренней ротации: | |
| musculus pectoralis major (Большая грудная мышца) | 4-6 ЕД/кг |
| — Сгибательная установка кисти: | |
| musculus flexor carpi ulnaris (Локтевой сгибатель запястья) | 0.8-1.6 ЕД/кг* |
| musculus flexor carpi radialis (Лучевой сгибатель запястья) | 0.8-1.6 ЕД/кг* |
| — Сгибательная установка 2-5 пальцев кисти, сгибательная установка первого пальца кисти, установка приведения первого пальца кисти: | |
| musculus flexor digitorum superficialis (Поверхностный сгибатель пальцев) | 0.8-1.6 ЕД/кг* |
| musculus flexor digitorum profundus (Глубокий сгибатель пальцев) | 0. 8-1.6 ЕД/кг* 8-1.6 ЕД/кг* |
| musculus flexor pollicis longus (Длинный сгибатель большого пальца кисти) | 0.8-1.6 ЕД/кг* |
| musculus flexor pollicis brevis (Короткий сгибатель большого пальца кисти) | 0.8-1.6 ЕД/кг* |
| musculus adductor pollicis (Мышца, приводящая большой палец кисти) | 0.8-1.6 ЕД/кг* |
| musculus opponens pollicis (Мышца, противопоставляющая большой палец кисти) | 0.4-0.8 ЕД/кг* |
* Максимальная суммарная разовая доза при сгибательной установке кисти и при сгибательной установке пальцев кисти, которая использовалась в клинических исследованиях препарата, не превышала 80 ЕД.
** Детям до 7 лет проведение инъекций в четырехглавую мышцу бедра противопоказано.
Максимальная суммарная разовая доза на один курс лечения, использованная в клинических исследованиях, составила не более 200 ЕД, распределенная между выбранными мышцами.
В клинических исследованиях период наблюдения за пациентами составил 12 недель после инъекции. Уменьшение мышечного тонуса отмечалось через неделю после инъекции, достигая максимума в течение 4-8 недель. На 12 неделе также отмечалось снижение уровня спастичности по сравнению с исходным уровнем.
Уменьшение мышечного тонуса отмечалось через неделю после инъекции, достигая максимума в течение 4-8 недель. На 12 неделе также отмечалось снижение уровня спастичности по сравнению с исходным уровнем.
При ДЦП целесообразно применять инъекции препаратом Релатокс® Токсин ботулинический типа А в комплексе с гемагглютинином в комбинации со стандартной схемой лечения и комплексом реабилитационных процедур.
Дозы и способ введения препарата при лечении аксиллярного гипергидроза
Инъекции раствора препарата производят в/к при помощи инсулинового шприца с иглой 30G. Инъекции могут быть сделаны в 10-20 точек в зависимости от степени выраженности гипергидроза. Для уменьшения болезненности ощущений перед процедурой допускается применение местных анестезирующих средств.
Область введения препарата определяют пробой Минора.
Проба проводится до лечения и, при необходимости, в динамике, при комнатной температуре после 15-минутного отдыха.
Для проведения пробы необходимо:
- 5% спиртовой раствор йода;
- картофельный крахмал;
- маркер;
- антисептик;
- кисточка;
- марлевые салфетки.

Пациент находится в положении лежа, руки под головой. Область потоотделения обрабатывают 5% спиртовым раствором йода и через 1 мин на эту зону салфеткой или кисточкой наносят тонким слоем картофельный крахмал. Результаты теста оценивают через 5 мин. При наличии потоотделения визуально наблюдается окрашивание обработанной поверхности в синий цвет. Интенсивность окраски (от бледно-синего до сине-черного) коррелирует с активностью потоотделения. После проведенной пробы площадь гипергидроза отмечают маркером, затем крахмал смывают спиртом или другим антисептиком.
Общая доза вводимого в одну подмышечную область препарата составляет 30-50 ЕД. Точки инъекции располагаются на расстоянии 1-6 см друг от друга. Таким образом, 50 ЕД могут вводиться в 10-20 точек, по 5 ЕД на точку. Если желаемый эффект не достигается, то возможно последующее увеличение дозы до 100 ЕД в каждую подмышечную область.
13 отзывов, инструкция по применению
Перед разведением препарата центральную часть пробки флакона обрабатывают спиртом этиловым. Препарат растворяют, вводя во флакон 1-8 мл 0,9%-ного раствора натрия хлорида для инъекций путем прокола пробки стерильной иглой длиной 23 или 25 мм. Запрещается открывать флакон и удалять пробку. Раствор препарата представляет собой прозрачную бесцветную жидкость.
Препарат растворяют, вводя во флакон 1-8 мл 0,9%-ного раствора натрия хлорида для инъекций путем прокола пробки стерильной иглой длиной 23 или 25 мм. Запрещается открывать флакон и удалять пробку. Раствор препарата представляет собой прозрачную бесцветную жидкость.
Приготовленный инъекционный раствор вводят инсулиновым шприцем с несъемной иглой диаметром 0,27-0,29 мм. Положение пациента при введении препарата в мышцы лица — сидя на стуле, затылок зафиксирован.
Таблица 1. Концентрации препарата, получаемые при разведении Релатокс 50 ЕД
| №№ пп | Объем 0,9%-ного раствора натрия хлорида для инъекций, мл | Активность препарата (ЕД в 0,1 мл) |
| 1 | 1 | 5 |
| 2 | 2 | 2,5 |
| 3 | 2,5 | 2,0 |
| 4 | 4 | 1,25 |
Таблица 2. Концентрации препарата, получаемые при разведении РЕЛАТОКС 100 ЕД
| №№ пп | Объем 0,9%-ного раствора натрия хлорида для инъекций, мл | Активность препарата (ЕД в 0,1 мл) |
| 1 | 2 | 5 |
| 2 | 4 | 2,5 |
| 3 | 5 | 2,0 |
| 4 | 8 | 1,25 |
Единицы действия ботулинического токсина в различных препаратах не взаимозаменяемы. Рекомендованные дозы, выраженные в единицах действия, для препарата Релатокс отличаются от таковых у других препаратов ботулотоксина.
Рекомендованные дозы, выраженные в единицах действия, для препарата Релатокс отличаются от таковых у других препаратов ботулотоксина.
Дозы и способы введения препарата при коррекции мимических морщин
Сглаживание межбровных морщин.
В процессе формирования межбровных морщин участвуют m. corrugator supercilii (мышца, сморщивающая бровь) и m. procerus (мышца гордецов).
Для определения места инъекций с целью устранения межбровных морщин пациента просят нахмуриться, в этот момент хорошо пальпируется m. corrugator supercilii (мышца, сморщивающая бровь), при этом точка наиболее выраженной мышечной активности должна находиться на 0,5 см вверх от верхнего медиального края брови. Аналогичным образом производят разметку на другой стороне. Игла вводится в толщу брюшка, направление иглы — либо под углом 45° спереди назад, медиально, либо под углом 90°. Глубина введения иглы — 7-10 мм. Если игла упрется в надкостницу, ее надо вытянуть на 1 мм и после этого ввести препарат. Точка введения препарата в m. procerus (мышца гордецов) располагается в центре линии, соединяющей медиальные края бровей. Положение иглы — спереди назад, глубина введения иглы — 2-3 мм.
procerus (мышца гордецов) располагается в центре линии, соединяющей медиальные края бровей. Положение иглы — спереди назад, глубина введения иглы — 2-3 мм.
В каждую точку вводят препарат Релатокс от 2,5 до 7,5 ЕД в зависимости от выраженности морщин, возраста и пола. Общее количество препарата, введенного в эту область, не должно превышать 25 ЕД.
Сглаживание горизонтальных морщин в области лба.
В образовании горизонтальных морщин в области лба участвует m. epicranius (мышца надчерепная). Для сглаживания лобных морщин пациента просят поднять брови и на максимуме амплитуды отмечают точки с наиболее выраженной мимической активностью. С целью исключения птоза брови, расстояние между точкой инъекции и верхним краем брови должно составлять не менее 2 см. Используется 5-10 точек и в каждую вводят от 1,25 ЕД до 2,5 ЕД препарата РЕЛАТОКС. При незначительно выраженных морщинах вводится по 2,0-2,5 ЕД в середину лобной области правой и левой стороны. При желании пациента сохранить движение кончиков бровей, точки инъекции можно расположить V- образно. Если у пациента очень высокий лоб и складки образуются близко под линией волос, можно дополнительно ввести по 1,25-2,5 ЕД в 2-3 точки параллельно линии роста волос. Общее количество препарата на данную область не должно превышать 20 ЕД.
Если у пациента очень высокий лоб и складки образуются близко под линией волос, можно дополнительно ввести по 1,25-2,5 ЕД в 2-3 точки параллельно линии роста волос. Общее количество препарата на данную область не должно превышать 20 ЕД.
Сглаживание морщин в периорбитальной области.
Морщины, расходящиеся радиально вокруг глаз, так называемые «гусиные лапки», возникают в результате активности круговой мышцы глаза. Для выбора дозы надо попросить пациента рассмеяться и в это время очертить примерные границы области кожи с максимальным количеством складок.
Для уменьшения «гусиных лапок» необходимо произвести несколько инъекций (от 2 до 4 с каждой стороны) в область проекции m. orbicularis oculi(мышца глаза круговая) на расстоянии не менее чем 1 см от наружного угла глаза, а также в область латеральной части нижнего века в местах максимальной мышечной активности. Расчет дозы производится исходя из площади этой поверхности в покое: в каждую точку вводится 2,0-2,5 ЕД препарата, диффузия из одной точки имеет радиус 0,5-1,0 см, следовательно, расстояние между точками введения должно составлять в среднем 1,0-2,0 см. Максимально допустимое количество вводимых в периорбитальную область единиц не более 25 ЕД на одну сторону. Чтобы не нарушать пропорции лица, необходимо тщательно следить за симметричностью расположения точек введения. Препарат в области «гусиных лапок» не вводится очень низко, так как возможно нарушение симметричности углов рта и носогубной складки вследствие диффузии препарата в область m. zygomaticus major (мышца скуловая большая).
Максимально допустимое количество вводимых в периорбитальную область единиц не более 25 ЕД на одну сторону. Чтобы не нарушать пропорции лица, необходимо тщательно следить за симметричностью расположения точек введения. Препарат в области «гусиных лапок» не вводится очень низко, так как возможно нарушение симметричности углов рта и носогубной складки вследствие диффузии препарата в область m. zygomaticus major (мышца скуловая большая).
Сглаживание морщин в области спинки носа.
При наличии выраженных морщин в области спинки носа препарат вводится непосредственно в m. nasalis (мышца носовая) с каждой стороны по 2,5 ЕД препарата.
Сглаживание морщин в нижней части лица.
Крылья носа. Препарат вводится непосредственно в крыльную часть m. nasalis (мышца носовая) по 2,5 ЕД с каждой стороны.
Верхняя губа. Инъекции производятся вдоль красной каймы верхней губы внутрикожно непосредственно в морщины, отступая от края на 2 мм, по 1,25 ЕД в каждую точку, количество точек от 4 до 6.
Углы рта. Препарат вводится подкожно в количестве 2,5 ЕД непосредственно в m. depressor anguli oris (мышца, опускающая угол рта).
Подбородок. Препарат вводится подкожно в количестве 2,5 ЕД непосредственно в m. mentalis (мышца подбородочная).
Дозы, схемы и способ введения препарата при лечении блефароспазма
При лечении блефароспазма препарат вводится поверхностно внутримышечно шприцем с иглой калибром 28-30 в следующие точки: две точки на верхнем веке, одна точка на латеральной половине нижнего века и одна точка у латерального угла глаза. В каждую точку следует вводить 2,5-5,0 ЕД. Средняя начальная доза 15-25 ЕД на одну сторону.
Максимально допустимое количество вводимых в периорбитальную область единиц не более 25 ЕД на одну сторону.
Выраженный клинический эффект от введения препарата проявляется в интервале от 2 до 14 дней после инъекции, в зависимости от индивидуальных особенностей организма, и длиться в течение 4-6 месяцев.
При неэффективности первой процедуры при любом выше описанном лечении, т. е. отсутствия значительного клинического улучшения, по сравнению с исходным состоянием, через 1 месяц после введения препарата, необходимо:
е. отсутствия значительного клинического улучшения, по сравнению с исходным состоянием, через 1 месяц после введения препарата, необходимо:
— клиническое подтверждение действия токсина на инъецированную мышцу (мышцы), которое может включать электромиграфическое (ЭМГ) исследование, выполняемое опытным специалистом в специализированном отделении;
— анализ причин неэффективности процедуры, например, неадекватный выбор точек для ииъещии, недостаточная доза, неправильная техника инъекции, признаки фиксированной контрактуры, слабость мышц-антагонистов, формирование токсин нейтрализующих антител;
— повторная оценка целесообразности лечения ботулиническим токсином типа А;
— при отсутствии каких-либо нежелательных эффектов, связанных с первым введением препарата, при повторной процедуре должны быть соблюдены следующие условия: коррекция дозы с учетом анализа причин неэффективности предыдущей процедуры; ЭМГ-контроль; интервал между процедурами должен составлять не менее 3- х месяцев.
При отсутствии эффекта от введения препарата или снижении его выраженности после повторных инъекции, следует рекомендовать другие методы лечения.
Передозировка
Больные с симптомами отравления ботулиническим токсином А (общая слабость, птоз, диплопия, затруднение глотания и расстройство речи, парез дыхательной мускулатуры) должны быть госпитализированы.
При параличе дыхательных мышц необходимо проведение интубации и перевод на искусственную вентиляцию легких до улучшения состояния больного.
ГЕПОН | ОАО «Авексима»
Показания к применению
В составе комбинированной терапии: лечение инфекций слизистых оболочек и кожи, вызванных грибами Candida; снижения интенсивности воспаления (покраснение, отек, зуд, жжение, боль) слизистых оболочек и кожи, сухости слизистых оболочек. Профилактика кандидоза слизистых оболочек и кожи на фоне терапии антибиотиками.
Способ применения и дозы
Применяют местно, наружно.
Перед применением препарат растворяют в воде для инъекций (при наружном применении препарата, т.е. для обработки кожи) или в 0,9 % растворе натрия хлорида (при местном применении препарата, т.е. для обработки слизистых оболочек). Способ приготовления препарата перед применением:
-
Удалить защитную часть алюминиевого колпачка с резиновой пробки флакона с лекарственным препаратом. Если лекарственный препарат в ампуле, вскрыть ампулу.
-
Вскрыть ампулу с растворителем (вода для инъекций). В качестве растворителя также может использоваться 0,9 % раствор натрия хлорида.
-
Надеть иглу на одноразовый шприц (объемом 5/10 мл — см. табл. 1)
-
Набрать в шприц растворитель (объем растворителя указан в табл. 1).
-
Проколоть иглой со шприцем резиновую пробку флакона с лекарственным препаратом и влить во флакон 2 — 2,5 мл растворителя.
 Если лекарственный препарат в ампуле, влить во вскрытую ампулу также 2—2,5 мл растворителя.
Если лекарственный препарат в ампуле, влить во вскрытую ампулу также 2—2,5 мл растворителя.
-
Не извлекая иглу, легкими колебательными движениями в течение примерно 1 минуты, полностью растворить содержимое флакона (ампулы).
-
Набрать полученный раствор в шприц с остатком растворителя. Конечный объем раствора в шприце должен соответствовать объему указанному в Таблице 1.
-
Извлечь шприц с иглой из флакона (ампулы), легкими колебательными движениями в течение примерно 1 минуты, полностью перемешать раствор в шприце.
-
Снять иглу со шприца.
-
Использовать шприц в качестве дозирующего устройства для инстилляций, нанесения на кожу и слизистые оболочки или смачивания марлевых салфеток.
Таблица 1
|
Гепон, мг |
Способ применения |
Гепон 0,02 % раствор |
Гепон 0,04 % раствор |
||
|
1 |
2 |
1 |
2 |
||
|
Вода для инъекций |
наружно |
− |
− |
2,5 |
5 |
|
0,9 % раствор хлорида натрия, мл |
местно |
5 |
10 |
− |
− |
Рекондуемая доза для взрослых и детей 12 лет и старше составляет 1-2 мг в виде 0,02 % раствора для местной обработки слизистых оболочек один раз в день.
Рекомендуемая доза для взрослых и детей 12 лет и старше составляет 1-2 мг в виде 0,04 % раствора для обработки кожи один раз в день.
Для лечения инфекций слизистых оболочек, вызванных грибами Candida, рекомендуется местное применение Гепона путем нанесения на пораженные участки слизистых оболочек (вульвы, влагалища, уретры) 0,02 % раствором, курсом в 3 применения (один раз в сутки) с интервалом 1-3 дня между нанесениями.
Для лечения инфекций кожи, вызванных грибами Candida, рекомендуется наружное применение Гепона путем нанесения на пораженные участки кожи 0,04 % раствором, курсом в 3 применения (один раз в сутки) с интервалом 1-3 дня между нанесениями.
При вульвовагините, уретрите у женщин применяют обработку 0,02 % раствором Гепона слизистой вульвы, влагалища, а также примочки на пораженные участки кожи, прилегающие ко входу во влагалище 0,04 % раствором Гепона.
При уретрите и баланопостите у мужчин применяют инстилляции 0,02 % раствором Гепона в уретру и примочки на пораженные участки кожи 0,04 % раствором Гепона.
Обработку слизистых оболочек и кожи проводят курсом в 3 приема (один раз в сутки) с интервалом 1 -3 дня.
Профилактика кандидоза слизистых оболочек на фоне терапии антибиотиками: рекомендуется проводить примочки 0,02 % раствором Гепона во время курса лечения антибиотиком. Обработку слизистых оболочек проводят курсом в 3 приема (один раз в сутки) с интервалом 1-3 дня.
Профилактика кандидоза кожи на фоне терапии антибиотиками: рекомендуется проводить примочки 0,04 % раствором Гепона во время курса лечения антибиотиком. Обработку кожи проводят курсом в 3 приема (один раз в сутки) с интервалом 1-3 дня.
Для снижения интенсивности воспаления и сухости слизистые оболочки следует обрабатывать 0,02 % раствором Гепона. Обработку слизистых оболочек проводят курсом в 3 приема (один раз в сутки) с интервалом 1 -3 дня.
Для снижения интенсивности воспаления кожи: накладывать марлевые салфетки, смоченные 0,04 % раствором Гепона.
Обработку кожи проводят курсом в 3 приема (один раз в сутки) с интервалом 1 -3 дня.
состав, побочные действия, показания, дозировка
Регистрационный номер
П N015890/01
Торговое название
Кальцемин®
Лекарственная форма
Таблетки, покрытые пленочной оболочкой.
Состав
1 таблетка содержит Действующие вещества: кальций (кальция цитрата тетрагидрат и кальция карбонат) 250 мг, витамин D3 (колекальциферол) 50 МЕ, цинк (цинка оксид) 2 мг, медь (меди оксид) 0,5 мг, марганец (марганца сульфат) 0,5 мг, бор (натрия борат декагидрат) 50 мкг.
Вспомогательные вещества: сои полисахарид 10 мг, натрия лаурилсульфат 5 мг, кремния диоксид коллоидный 3,9 мг, кроскармеллоза натрия 28 мг, микрокристаллическая целлюлоза 199,45 мг, стеариновая кислота 35 мг, магния стеарат 10 мг.
Оболочка: гипромеллоза 11,71 мг, триацетин 2,53 мг, минеральное масло 1,27 мг, натрия лаурилсульфат 0,004 мг, титана диоксид 7,03 мг, магния силикат 5 мг.
Описание
Таблетки двояковыпуклые овальной формы, покрытые пленочной оболочкой белого цвета с риской на одной стороне.
Фармакотерапевтическая группа
Кальциево-фосфорного обмена регулятор.
Код АТХ
A12AX
Фармакологические свойства
Комбинированный препарат, содержащий кальций, витамин D3, остеотропные минералы, регулирующие обмен кальция. Фармакологическое действие препарата определяется свойствами входящих в его состав ингредиентов.
Кальций участвует в формировании костной ткани, снижает резорбцию (рассасывание) и увеличивает плотность костной ткани, предупреждает заболевания опорно-двигательного аппарата, способствует укреплению костной системы и суставов. Кальций цитрат обеспечивает усвоение кальция вне зависимости от функционального состояния ЖКТ, что применимо для лечения пациентов со сниженной секреторной функцией ЖКТ, а также на фоне лечения препаратами для снижения секреции; снижает уровень маркеров резорбции костной ткани, что свидетельствует о замедлении процессов разрушения костной ткани; регулирует уровень паратгормона, что приводит к улучшению регуляции кальциевого гомеостаза; не увеличивает содержание оксалатов и кальция в моче, следовательно не вызывает риска образования камней в почках; не блокирует усвоение железа, что снижает риск развития железодефицитной анемии.
Колекальциферол (витамин D3) регулирует обмен кальция и фосфора в организме, участвует в формировании костного скелета, способствует сохранению структуры костей, усиливает всасывание кальция в кишечнике и реабсорбцию фосфора в почечных канальцах. Цинк способствует синтезу половых гормонов, что препятствует разрушению костной ткани.
Марганец участвует в образовании протеогликанов, что улучшает качество костной ткани и формирует протеиновый матрикс костной ткани. Медь участвует в синтезе коллагена и эластина, входящего в состав костной и соединительной ткани, что оказывает влияние на процессы образования костной массы.
Бор снижает избыточную активность паратгормона, улучшает абсорбцию кальция, уменьшает риск развития дефицита холекальциферола, способствует предотвращению остеопороза.
Показания к применению
Профилактика и комплексное лечение остеопороза различного генеза.
Для восполнения дефицита кальция и микроэлементов у детей, подростков и у женщин в период беременности и грудного вскармливания.
Противопоказания
Гиперчувствительность к любому из действующих или вспомогательных веществ в составе препарата. Гиперкальциемия и/или состояния, сопровождающиеся гиперкальциемией, такие как саркоидоз, злокачественные опухоли (в том числе, миелома), метастазы в кости и первичный гипертиреоидизм.
Гиперкальциурия. Нефролитиаз.
Гипервитаминоз витамина D3.
Почечная недостаточность.
Почечнокаменная болезнь.
Активная форма туберкулеза.
Детский возраст до 5 лет.
Если у Вас есть одно из перечисленных выше заболеваний/состояний или факторов риска, перед применением препарата необходимо проконсультироваться с врачом.
С осторожностью
Доброкачественный гранулематоз, у пациентов, получающих терапию сердечными гликозидами, блокаторами кальциевых каналов и/или тиазидными диуретиками, у иммобилизованных (лежачих) пациентов в связи с повышенным риском развития гиперкальциемии, у пожилых пациентов, беременность, период грудного вскармливания.
Если у Вас есть одно из перечисленных выше заболеваний/состояний или факторов риска, перед применением препарата необходимо проконсультироваться с врачом.
Применение в период беременности и грудного вскармливания
В период беременности и грудного вскармливания прием препарата следует согласовать с врачом.
Суточная доза не должна превышать 1500 мг кальция и 600 МЕ витамина D3, гиперкальциемия, развивающаяся на фоне передозировки в период беременности может вызвать дефекты умственного и физического развития у плода.
У кормящих женщин следует учитывать, что колекальциферол и его метаболиты проникают в грудное молоко, поэтому необходимо учитывать поступление кальция и витамина D3.
Способ применения и дозы
Принимать внутрь во время еды, запивая достаточным количеством воды (200 мл).
Детям от 5 до 12 лет принимать по 1 таблетке 1 раз в день во время еды.
Взрослым и детям старше 12 лет — по 1 таблетке 2 раза в день во время еды.
В период беременности и грудного вскармливания: с 20-й недели беременности и весь период грудного вскармливания — по 1 таблетке 2 раза в день.
Минимальный курс приема препарата для лечения остеопороза в составе комплексной терапии для взрослых составляет 3 месяца, более продолжительный курс — после консультации с врачом.
Минимальный курс приема препарата для профилактики остеопороза для взрослых составляет 1 месяц, более продолжительный курс — после консультации с врачом. Минимальный курс приема препарата для детей и взрослых при дефиците кальция и микроэлементов составляет 2-3 месяца, более продолжительный курс — после консультации с врачом. Повторный курс приема препарата возможен через 1 месяц после окончания лечения.
Применяйте препарат только согласно тем показаниям, тому способу применения и в тех дозах, которые указаны в инструкции.
Побочное действие
Были выявлены следующие нежелательные реакции в ходе пострегистрационного применения препарата. В связи с тем, что данные по нежелательным реакциям представляют собой разрозненные сообщения от пациентов или различных групп, не всегда достоверно можно установить их частоту или причинно-следственную взаимосвязь с применением препарата.
Нарушения со стороны желудочно-кишечного тракта: боли в области живота, запор, диарея, метеоризм, тошнота и рвота.
Нарушения со стороны иммунной системы: аллергические реакции, анафилактические реакции, анафилактический шок.
Редкие реакции гиперчувствительности с соответствующими лабораторными и клиническими проявлениями, включая астматический синдром, от легких до умеренных умеренных реакций кожи и/или дыхательных путей, и/или желудочно-кишечного тракта и/или сердечно-сосудистой системы. Симптомы могут включать сыпь, крапивницу, отек, зуд, респираторный дистресс-синдром и, очень редко, тяжелые реакции, включая анафилактический шок.
Если у Вас отмечаются нежелательные реакции, указанные в инструкции или они усугубляются, или Вы заметили любые другие нежелательные реакции, неуказанные в инструкции, сообщите об этом врачу.
Передозировка
Гипервитаминоз витамина D, гиперкальциемия, гиперкальциурия и гиперфосфатемия.
Симптомы: снижение аппетита, жажда, полиурия, головокружение, обморочные состояния, запор, тошнота и рвота, нарушение функции почек, «молочно-щелочной синдром», повышение активности «печеночных» ферментов (АЛТ и АСТ). При длительном применении избыточных доз — кальциноз сосудов и тканей. В случае передозировки препарата Кальцемин® следует немедленно обратиться к врачу. Лечение: симптоматическое.
При длительном применении избыточных доз — кальциноз сосудов и тканей. В случае передозировки препарата Кальцемин® следует немедленно обратиться к врачу. Лечение: симптоматическое.
Взаимодействие с другими лекарственными средствами
Соли кальция.
Соли кальция могут взаимодействовать со многими веществами из-за изменений рН желудочного сока, влияния на опорожнение желудкаили образования комплексов с определенными веществами, что приводит к снижению всасывания обоих веществ.
Поскольку указанные взаимодействия происходят в желудочно-кишечном тракте, для минимизации возможности взаимодействия препараты кальция следует принимать отдельно от других лекарственных средств. Как правило, достаточно соблюдения интервала между приемом препаратов, по крайней мере, за 2 часа до или через 4-6 часов после приема препарата кальция, если не указано иное.
Антибиотики и противовирусные препараты (например, тетрациклины, фторхинолоны) Кальций снижает всасывание тетрациклиновых антибиотиков путем образования нерастворимых комплексов. Пациенты должны принимать данные препараты, по крайней мере, за два часа до или от 4 до 6 часов после приема препарата кальция.
Пациенты должны принимать данные препараты, по крайней мере, за два часа до или от 4 до 6 часов после приема препарата кальция.
Левотироксин
Кальций уменьшает всасывание левотироксина, вероятно, за счет формирования нерастворимых комплексов. Пациентам следует принимать левотироксин, по крайней мере, за 4 часа до или через 4 часа после приема препаратов кальция.
Фосфаты, бисфосфонаты и фториды
Препараты кальция уменьшают всасывание бисфосфонатов. Пациенты должны принимать бисфосфонаты, по крайней мере, за 30 минут до применения кальция, но предпочтительно в разное время суток.
Элтромбопаг
Наблюдалось снижение уровня в плазме элтромбопага на 59 % при потреблении завтрака с высоким содержанием жиров и высоким содержанием кальция (427 мг), в то время как питание с низким уровнем кальция (<50 мг) не оказывает существенного влияния на уровень элтромбопага в плазме. Богатые кальцием продукты и антациды, содержащие алюминий, кальций и магний демонстрировали значительное снижение системного воздействия.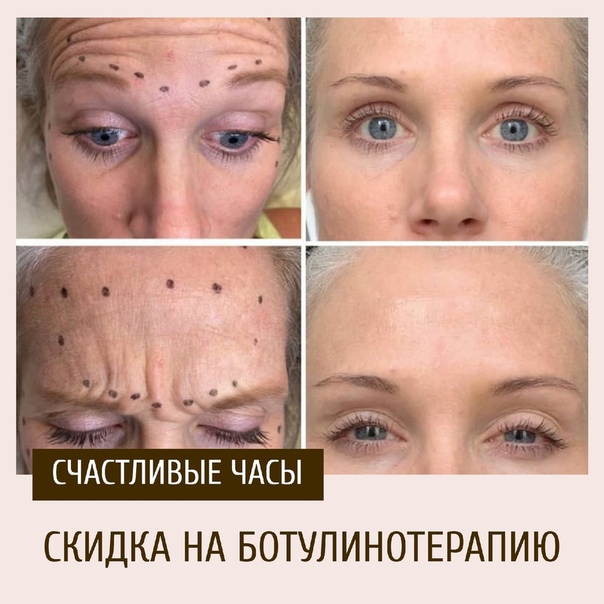
Фторид натрия
Препараты кальция ухудшают всасывание фторида натрия. Пациентам следует принимать фторид натрия, по крайней мере, за 2 часа до или через 2 часа после приема препаратов кальция.
Сердечные гликозиды и блокаторы кальциевых каналов
Гиперкальциемия увеличивает вероятность сердечных аритмий с летальным исходом при применении сердечных гликозидов, таких как дигоксин и снижает эффективность блокаторов кальциевых канальцев, таких как верапамил при фибрилляции предсердий. Рекомендуется контролировать концентрацию кальция в плазме крови у людей, принимающих кальций и/или витамин D или эти препараты одновременно.
Ингибиторы протеазы
Если продукты, содержащие кальций или магний, в том числе буферизированные препараты, вводят вместе с некоторыми ингибиторами протеазы, возможно снижение концентрации в плазме всех этих веществ. Поэтому рекомендуется применять ингибитор протеазы за 2 часа до или через 1 час после приема препаратов, содержащих алюминий, кальций или магний. Такой эффект был замечен со следующими препаратами: ампренавир, атазанавир и типранавир.
Такой эффект был замечен со следующими препаратами: ампренавир, атазанавир и типранавир.
Тиазидные диуретики
Тиазидные диуретики уменьшают экскрецию кальция. В связи с повышенным риском гиперкальциемии, следует регулярно контролировать концентрацию кальция в плазме крови во время сопутствующего применения тиазидных диуретиков.
Некоторые лекарственные препараты могут уменьшить желудочно-кишечную абсорбцию витамина D. Для минимизации такого взаимодействия необходимо раздельное применение этих препаратов и витамина D, по крайней мере, 2 часа до или через 4-6 часов после приема витамина D. К данным препаратам относятся: ионобменные смолы (например, колестирамин), слабительные средства.
Орлистат, карбамазепин, фенитоин и барбитураты увеличивают превращение витамина D в его неактивный метаболит, уменьшая эффект витамина D3.
Взаимодействие с компонентами пищи
Щавелевая кислота, фитиновая кислота
Щавелевая кислота, находящаяся в шпинате и ревене, и фитиновая кислота, находящаяся в зерновых культурах, может препятствовать всасыванию кальция. Не рекомендуется принимать препараты кальция в течение 2 часов после приема пищи, содержащей высокую концентрацию щавелевой и фитиновой кислот.
Не рекомендуется принимать препараты кальция в течение 2 часов после приема пищи, содержащей высокую концентрацию щавелевой и фитиновой кислот.
Железо, цинк, магний
Препараты кальция могут уменьшить всасывание из пищи железа, цинка и магния. Однако у людей с нормальной обеспеченностью этими минералами это не имеет клинического значения в долгосрочной перспективе. Пациенты с риском дефицита железа, цинка или магния должны принимать препараты кальция перед сном, а не во время еды, чтобы избежать замедления всасывания микроэлементов.
Пищевые волокна
Некоторые компоненты пищевых волокон могут замедлять всасывание кальция. К ним относятся фитиновая кислота (содержится в пшеничных отрубях), щавелевая кислота (содержится в шпинате и ревене) и уроновая кислота (общий компонент растительных волокон). Если Вы применяете вышеперечисленные или другие лекарственные препараты (в том числе безрецептурные), перед применением препарата Кальцемин® проконсультируйтесь с врачом.
Особые указания
Доза не должна превышать ту, которая указана в инструкции, так как повышенное потребление кальция может угнетать всасывание в кишечнике железа, цинка и других необходимых минералов.
Пациентам, принимающим другие моно либо мультивитаминные препараты, содержащие витамин D и/или кальций, другие препараты, а также пациентам, находящимся под медицинским наблюдением, перед приемом данного лекарственного средства следует проконсультироваться с врачом. У пожилых пациентов, а также пациентов, принимающих сердечные гликозиды, блокаторы кальциевых каналов и/или тиазидные диуретики, при длительной терапии комбинированным препаратом кальция и витамина D следует следить за уровнем кальция в крови и моче, функциональным состоянием почек посредством определения содержания креатинина крови.
Препарат содержит натрий. Следует принять к сведению пациентам, находящимся на контролируемой натриевой диете.
Влияние на способность управлять автомобилем и движущими механизмами
Не влияет.
Форма выпуска
Таблетки, покрытые пленочной оболочкой.
По 30, 60 и 120 таблеток во флаконе из полиэтилена высокой плотности с завинчивающейся крышкой из полипропилена, опечатанной защитной полимерной пленкой. Под крышкой горлышко флакона опечатано многослойной мембраной. Свободное пространство флакона заполнено хлопковой ватой. Флакон вместе с инструкцией по медицинскому применению препарата помещают в картонную пачку.
Условия хранения
При температуре не выше 25 ºС. Хранить в недоступном для детей месте.
Срок годности
3 года. Не использовать по истечении срока годности.
Условия отпуска
Без рецепта.
Производитель
Владелец регистрационного удостоверения: АО «БАЙЕР», Россия Производство готовой лекарственной формы: Контракт Фармакал Корпорейшн, 150 и 160 Коммерс Драйв, Хоппог, Нью-Йорк 11788, США Первичная, вторичная упаковка и выпускающий контроль качества: Контракт Фармакал Корпорейшн, 135 Адамс Авеню, Хоппог, Нью-Йорк 11788, США
Организация, принимающая претензии потребителей:
АО «БАЙЕР», Россия 107113, г. Москва, ул. 3-я Рыбинская, д. 18, стр. 2 Тел.: +7 (495) 231-12-00
Москва, ул. 3-я Рыбинская, д. 18, стр. 2 Тел.: +7 (495) 231-12-00
www.bayer.ru
Сравнение препаратов ботулинического нейротоксина типа А в Азии
Clin Cosmet Investig Dermatol. 2018; 11: 327–331.
Ки Ён Ан
2 Клиника пластической и эстетической хирургии доктора Ана, Тэгу, Южная Корея
Ми Янг Парк
3 Кафедра неврологии, Медицинский факультет Университета Йонгнам, Тэгу, Южная Корея
Owen Sunga
4 Merz Asia Pacific, Сингапур
2 Др.Клиника пластической и эстетической хирургии Ана, Тэгу, Южная Корея
3 Кафедра неврологии, Медицинский факультет Университета Йонгнам, Тэгу, Южная Корея
4 Merz Asia Pacific, Singapore
Для корреспонденции: Jürgen Frevert Merz, Pharmaceuticals GmbH, Hermannswerder 15, 14473 Potsdam, Germany, тел. Фреверт и др. Эта работа опубликована и лицензирована Dove Medical Press Limited. Полные условия этой лицензии доступны по адресу https://www.dovepress.com/terms.php и включите лицензию Creative Commons Attribution — некоммерческая (непортированная, версия 3.0) (http://creativecommons.org/licenses/by-nc/3.0/). Получая доступ к работе, вы тем самым принимаете Условия. Некоммерческое использование работы разрешено без какого-либо дополнительного разрешения от Dove Medical Press Limited при условии, что работа правильно указана. Эта статья цитировалась в других статьях в PMC.
Полные условия этой лицензии доступны по адресу https://www.dovepress.com/terms.php и включите лицензию Creative Commons Attribution — некоммерческая (непортированная, версия 3.0) (http://creativecommons.org/licenses/by-nc/3.0/). Получая доступ к работе, вы тем самым принимаете Условия. Некоммерческое использование работы разрешено без какого-либо дополнительного разрешения от Dove Medical Press Limited при условии, что работа правильно указана. Эта статья цитировалась в других статьях в PMC.Abstract
Results
Все терапевтические препараты на основе белков, такие как ботулинический нейротоксин типа A (BoNT/A), являются потенциально иммуногенными и могут привести к анафилаксии, аутоиммунитету или снижению или полному отсутствию терапевтической эффективности, особенно при повторном введении.Таким образом, количество белка в продуктах BoNT/A является важным фактором при выборе продуктов для лечения. Однако основные данные о составе не всегда общедоступны.
Материалы и методы
Содержание белка нейротоксина в продуктах, впервые представленных в Азии, таких как (перечислены в алфавитном порядке) Botulax ® , Meditoxin ® , Nabota ® и Relatox ® , было измерено ферментным сэндвичем. Связанный иммуносорбентный анализ с антисыворотками, направленными против BoNT/A, по сравнению с Xeomin ® .
Связанный иммуносорбентный анализ с антисыворотками, направленными против BoNT/A, по сравнению с Xeomin ® .
Результаты
По сравнению с Ксеомином без неактивного нейротоксина, хотя Ботулакс и Набота содержали 844 и 754 пг белка нейротоксина соответственно, процент неактивного нейротоксина составил 103 и 81, соответственно, в то время как эффективность на пг нейротоксина составило 0,118 и 0,133 ед. соответственно. Медитоксин и Релатокс содержали 575 и 578 пг нейротоксинов соответственно, что немного выше, чем у Ксеомина, в то время как процент неактивных нейротоксинов составлял 38 и 33 соответственно, а эффективность на пг нейротоксина равнялась 0.174 и 0,173 ед. соответственно. Однако Ксеомин, который содержит 416 мкг/флакон очищенного нейротоксина и 0,240 ЕД эффективности на мкг нейротоксина, имеет самое низкое содержание белка нейротоксина и, следовательно, самую высокую удельную эффективность по сравнению с четырьмя азиатскими препаратами ботулинического токсина/А в этом исследовании.
Заключение
Хотя Ботулакс и Набота содержали больше нейротоксина, чем Ксеомин в эквивалентном объеме, они содержали большее количество неактивного нейротоксина. Кроме того, хотя Медитоксин и Релатокс содержали немного больше нейротоксина, чем Ксеомин, оба препарата содержали большее количество неактивного нейротоксина.
Ключевые слова: ботулинический нейротоксин типа А, чистота, эффективность, иммуногенность, Азия
Введение
Ботулинический нейротоксин типа А (BoNT/A) является ведущим средством в лечении нервно-мышечных заболеваний, а также используется в косметических целях. длительное время. Во время иммуногенных реакций вырабатываются «нейтрализующие» антитела против токсина, ингибирующие взаимодействие между БоНТ/А и его местом связывания с пресинаптической мембраной, 1 – 3 , вызывая неадекватную реакцию или отсутствие реакции на БоНТ/А. 4 Продукты BoNT/A, особенно новые составы токсинов, обычно проходят тщательную оценку для использования в качестве лекарств, отпускаемых только по рецепту. Поэтому клиницисты должны выбирать менее иммуногенные высокоочищенные токсины для получения успешных результатов при длительном повторном лечении. 5
Поэтому клиницисты должны выбирать менее иммуногенные высокоочищенные токсины для получения успешных результатов при длительном повторном лечении. 5
Недавно в Азии появились новые составы токсинов, но исследования по количественной оценке этих нейротоксинов, таких как их чистота (определяемая как комплексообразование без белка), влияние их дозы на эффективность или побочные эффекты, были ограничены. 6 Поэтому мы проанализировали состав нейротоксинового компонента каждого продукта по сравнению с Xeomin ® , используя сэндвич-иммуноферментный анализ (ELISA) с антисыворотками, направленными против очищенного BoNT/A, чтобы лучше понять эти новые составы. Мы стремимся предоставить клиницистам ценную информацию для обеспечения безопасного и эффективного лечения с помощью BoNT/A.
Материалы и методы
Материалы
Различное содержание белка и нейротоксина в Botulax ® (партия HUA 15133; Hugel Inc., Сеул, Корея), Innotox ® (серия LAE 1401; Medytox Inc. , Сеул, Корея), Meditoxin ® (серия FAA 1587; Medytox Inc., Сеул, Корея), Nabota ® (серия 084962; Daewoong Pharmaceutical Co. Ltd., Сеул, Корея), Релатокс ® (серия 0615; «Микроген», Россия), а также Ксеомин (серия 31149; Merz Pharmaceuticals GmbH, Райнхайм, Германия) измеряли с помощью сэндвич-ИФА с антисыворотками. (). Поскольку производственный процесс биологического терапевтического средства должен быть последовательным, а каждая партия должна быть репрезентативной, поэтому партии были выбраны произвольно.Партии были приобретены в южнокорейской аптеке (ShinOn Pharmacy Co. Ltd., Сеул, Южная Корея). Были приняты меры по транспортировке и хранению образцов при температуре 2–8 °C, за исключением образцов Ксеомина, которые можно хранить при комнатной температуре. Состав элементов нейротоксина каждого продукта по сравнению с составом Xeomin затем анализировали в двух экземплярах для определения среднего количества белка нейротоксина.
, Сеул, Корея), Meditoxin ® (серия FAA 1587; Medytox Inc., Сеул, Корея), Nabota ® (серия 084962; Daewoong Pharmaceutical Co. Ltd., Сеул, Корея), Релатокс ® (серия 0615; «Микроген», Россия), а также Ксеомин (серия 31149; Merz Pharmaceuticals GmbH, Райнхайм, Германия) измеряли с помощью сэндвич-ИФА с антисыворотками. (). Поскольку производственный процесс биологического терапевтического средства должен быть последовательным, а каждая партия должна быть репрезентативной, поэтому партии были выбраны произвольно.Партии были приобретены в южнокорейской аптеке (ShinOn Pharmacy Co. Ltd., Сеул, Южная Корея). Были приняты меры по транспортировке и хранению образцов при температуре 2–8 °C, за исключением образцов Ксеомина, которые можно хранить при комнатной температуре. Состав элементов нейротоксина каждого продукта по сравнению с составом Xeomin затем анализировали в двух экземплярах для определения среднего количества белка нейротоксина.
Таблица 1
Свойства Botulinum Neurotoxin Тип продуктов Анализируется в этом исследовании
| NinoTox ® | Botulax | Meditoxin ® / Neuronox ® | Nabota ® | Relatox ® | Xeomin ® | | ||||
|---|---|---|---|---|---|---|---|---|---|---|
| Производитель | Medytox | Hugel Инк | Medytox Inc | Daewong | Микроген | Merz | ||||
| Дозировка (U) | 25 | 25 | 100 | 100 | 100 | 100 | 100 | 100 | 100 | 100 |
| Комплекс | ||||||||||
| Комплекс | Комплекс | Комплекс | Комплекс (900 KDA) | Комплекс (900 KDA) | Очищенный токсин (150 кДа) | |||||
| Внешний вид | Жидкость | Лиофилизированный | Лиофилизат | Лиофилизат | Лиофилизат | Лиофилизат | ||||
| Лекарственная форма | Полисорбат (без ЧСА) | 0. 5 мг ЧСА; 0,9 мг NaCl 5 мг ЧСА; 0,9 мг NaCl | 0,5 мг ЧСА; 0,9 мг NaCl | 0,5 мг ЧСА; 0,9 мг NaCl | 6 мг желатина; 12 мг мальтозы | 4,7 мг сахарозы; 1 мг ЧСА | ||||
| Хранение | 2°C–8°C | 2°C–8°C | 2°C–8°C | 2°C–8°C | 2°C– 8 ° C | Комнатная температура (20 ° C-25 ° C) | ||||
| CloseTridial белок на 100 U (PG) | N / A | 5000 12 | N / | N / | Н/Д | 416 |
Методы
Все анализы проводились с помощью ИФА, одобренного FDA (Food and Drug Administration, Silver Spring, MD, USA) и несколькими другими органами здравоохранения. Учреждение, в котором анализировались образцы, регулярно инспектировалось FDA и соответствовало текущим требованиям надлежащей производственной практики.
Учреждение, в котором анализировались образцы, регулярно инспектировалось FDA и соответствовало текущим требованиям надлежащей производственной практики.
Для инкубации: PBS + 0,1% бычий сывороточный альбумин (раствор 1) и PBS + 6% гелафусал (Serumwerke Bernburg, Бернбург, Германия; раствор 2) (Merck, Дармштадт, Германия, или Riedel-de-Haen, Seelze, Германия ) были использованы. Дополнительные реагенты включали дигидрохлорид О-фенилендиамина (Sigma-Aldrich Corp, Сент-Луис, Миссури, США) и лошадиную антисыворотку, реагирующую с нейротоксиновым комплексом BoNT/A (Национальный институт биологических стандартов и контроля Великобритании, NIBSC).Следуя модифицированному протоколу, 7 нейротоксин массой 150 кДа, выделенный из «штамма Холла», C. botulinum тип A, штамм ATCC 3502, был подтвержден вестерн-блоттингом как комплексообразующий, не содержащий белка и детоксицированный обработкой 0,4% формальдегидом до производят нетоксичный антиген для приготовления антител. Комплексообразующие белки (за исключением белка ботулинического нейротоксина) готовили, как было опубликовано ранее. 8 Очищенный токсин подвергали диализу против 50 мМ TRIS (трис[гидроксиметил]аминометан)/HCl, pH = 7.9, элюировали колоночную хроматографию с Q-сефарозой (GE Healthcare, Мюнхен, Германия) и связанные с колонкой комплексообразующие белки. Антитела против BoNT/A иммобилизовали на сефарозной матрице CNBr (GE Healthcare). BoNT/A удаляли с помощью аффинной хроматографии, элюировали и проверяли его состав на целостность.
Комплексообразующие белки (за исключением белка ботулинического нейротоксина) готовили, как было опубликовано ранее. 8 Очищенный токсин подвергали диализу против 50 мМ TRIS (трис[гидроксиметил]аминометан)/HCl, pH = 7.9, элюировали колоночную хроматографию с Q-сефарозой (GE Healthcare, Мюнхен, Германия) и связанные с колонкой комплексообразующие белки. Антитела против BoNT/A иммобилизовали на сефарозной матрице CNBr (GE Healthcare). BoNT/A удаляли с помощью аффинной хроматографии, элюировали и проверяли его состав на целостность.
ELISA
Количество BoNT/A в фармацевтических составах Botulax, Meditoxin, Nabota или Relatox измеряли параллельно с Xeomin с помощью чувствительного сэндвич-ELISA с антисыворотками против нейротоксина 150 кДа, полученными на кроликах и морских свинках.Покрытые микротитровальные планшеты инкубировали с антисывороткой, разведенной 1:1000 в 100 ммоль/л карбоната натрия, рН 9,5. За исключением жидкой формы Иннотокс, два флакона из одной партии Ботулакса, Медитоксина, Набота, Релатокса и Ксеомина (по 100 ЕД каждый) разбавляли 1 мл раствора 1. Сто мкл каждого препарата анализировали в антисыворотках. пластины с покрытием. Innotox был дополнен человеческим сывороточным альбумином, чтобы установить условия реакции, подтвержденные для ELISA. Каждый флакон с восстановленным Ботулаксом, Медитоксином, Наботой, Релатоксом или жидким Иннотоксом анализировали в двух повторностях.После инкубации лунки промывали раствором 1 и инкубировали с антисывороткой морской свинки (разведение 1:2000 в растворе 2). Несвязавшиеся антитела против нейротоксина массой 150 кДа отмывали. Конъюгат пероксидазы G иммуноглобулина морской свинки (1:5000; Sigma, A7289) использовали для обнаружения связанных антител колориметрическим количественным определением с о-фенилендиамином (16 ммоль/л) в 10 ммоль/л цитратного буфера (pH = 5,0). Оптическую плотность измеряли при 490 нм с использованием устройства для чтения микротитрационных планшетов и SoftMax Pro GxP (Spectra-Max Plus, Molecular Devices, Сан-Хосе, Калифорния, США).Стандартная кривая между 0,2 и 1,6 нг/мл нейротоксина была получена с интервалами 0,2 нг/мл (см.
Сто мкл каждого препарата анализировали в антисыворотках. пластины с покрытием. Innotox был дополнен человеческим сывороточным альбумином, чтобы установить условия реакции, подтвержденные для ELISA. Каждый флакон с восстановленным Ботулаксом, Медитоксином, Наботой, Релатоксом или жидким Иннотоксом анализировали в двух повторностях.После инкубации лунки промывали раствором 1 и инкубировали с антисывороткой морской свинки (разведение 1:2000 в растворе 2). Несвязавшиеся антитела против нейротоксина массой 150 кДа отмывали. Конъюгат пероксидазы G иммуноглобулина морской свинки (1:5000; Sigma, A7289) использовали для обнаружения связанных антител колориметрическим количественным определением с о-фенилендиамином (16 ммоль/л) в 10 ммоль/л цитратного буфера (pH = 5,0). Оптическую плотность измеряли при 490 нм с использованием устройства для чтения микротитрационных планшетов и SoftMax Pro GxP (Spectra-Max Plus, Molecular Devices, Сан-Хосе, Калифорния, США).Стандартная кривая между 0,2 и 1,6 нг/мл нейротоксина была получена с интервалами 0,2 нг/мл (см. Frevert 2010 8 для репрезентативных стандартных кривых). Внутренние контроли были выполнены для каждого планшета, чтобы гарантировать достоверность анализа. Линейность стандартной кривой и специфичность, точность и надежность ELISA определяли в соответствии с рекомендациями Международной конференции по гармонизации. 9 Было показано, что ELISA является специфичным для нейротоксина BoNT/A и не обнаруживает комплексообразующие белки.
Frevert 2010 8 для репрезентативных стандартных кривых). Внутренние контроли были выполнены для каждого планшета, чтобы гарантировать достоверность анализа. Линейность стандартной кривой и специфичность, точность и надежность ELISA определяли в соответствии с рекомендациями Международной конференции по гармонизации. 9 Было показано, что ELISA является специфичным для нейротоксина BoNT/A и не обнаруживает комплексообразующие белки.
Результаты
описывает свойства Innotox, Botulax, Meditoxin, Nabota и Relatox. 10
Для количественного определения количества белка BoNT/A в препаратах Botulax, Meditoxin, Nabota и Relatox был использован высокочувствительный сэндвич-ELISA (). Ксеомин был проанализирован независимо параллельно в качестве контроля, и было обнаружено, что среднее содержание токсина составляет 416 пг/флакон, что сравнимо с отчетами из другой партии. 8 Следует отметить, что это отклонение от опубликованных значений связано с тем, что эти партии токсина больше не доступны для настоящего анализа и с использованием другой партии Ксеомина, а также с 5-процентной межсерийной изменчивостью в процессе производства. (неопубликованные данные 2018 г., Merz Pharmaceuticals GmbH).
(неопубликованные данные 2018 г., Merz Pharmaceuticals GmbH).
Таблица 2
Определение содержания ботулинового нейротоксина типа белок в продуктах ELISA
| Название продукта | Название партии | Дозировка | Количество невротоксин белок на 100 единиц (PG) | Специальная потенция (PG) | U / PG Neurotoxin) | Рассчитанная пропорция (%) неактивного нейротоксина * | | |
|---|---|---|---|---|---|---|---|---|
| Botulax ® ® | HUA 15133 | 100 U / VIAL (LYO) | 844 ± 43 ‡ | 0. 118 118 | 103 | |||
| Meditoxin ® / Neuronox ® | АВС 1587 | 100 Ед / флакон (Лио) | 575 ± 6 | 0,174 | 38 | |||
| Nabota ® | 084962 | 4 | 100 U / Vial (Lyo) 754 | ± 11 ‡ | 0. 133 133 | 0.133 | 81 | |
| Relatox ® | 41 0615100 U / Plaial (лио) | 578 ± 48 | 0.173 | 3 | ||||
| Xeomin ® | 31149 | 100 U / Vial (Lyo) 416 | ± 6 | 0. 240 240 | 0.240 | не найден |
Botulax and Nabota содержали 844 и 754 пг нейротоксинов, соответственно, что почти в два раза превышает содержание нейротоксинов в Ксеомине (416 пг) в эквивалентном флаконе на 100 ЕД. Тем не менее, процент неактивных нейротоксинов также был подсчитан, что он был намного выше, 103 и 81, соответственно, чем у Ксеомина без неактивного нейротоксина.Активность на мкг нейротоксина в Ботулаксе и Наботе составила 0,118 и 0,133 ЕД соответственно. Это было менее эффективно, чем 0,240 ЕД Ксеомина на мкг нейротоксина. Медитоксин и Релатокс содержали 575 и 578 пг нейротоксинов соответственно, что было несколько выше, чем у Ксеомина, как и рассчитанный процент неактивных нейротоксинов при 38 и 33 соответственно. Было обнаружено, что эффективность медитоксина и релатокса на пг нейротоксина составляет 0,174 и 0,173 ЕД соответственно, что также ниже, чем 0 у Ксеомина. 240 ЕД эффективности на пг нейротоксина.
240 ЕД эффективности на пг нейротоксина.
Обсуждение
Все препараты BoNT/A содержат нейротоксин с молекулярной массой 150 кДа, который является активной молекулой. Однако ксеомин состоит исключительно из нейротоксина молекулярной массой 150 кДа. Все продукты основаны на комплексе ботулинического токсина с примерно в шесть раз большим количеством дополнительных бактериальных белков, при условии, что молекулярная масса комплекса составляет ≈900 кДа. Некоторые из комплексообразующих белков представляют собой гемагглютинины, которые представляют собой белки, связывающие гликопротеины (так называемые лектины).В отличие от нейротоксина с молекулярной массой 150 кДа, эти комплексообразующие белки обладают способностью связываться с дендритными клетками, 11 , 14 сигнальными клетками иммунной системы. Эти клетки должны быть активированы в качестве первого шага инициации иммунного ответа. 12 , 14 В связи с этим комплексообразующие белоксодержащие продукты обладают более высоким потенциалом вызывать иммунный ответ. Действительно, сообщалось об образовании антител у пациентов, получавших в эстетической медицине комплексообразующие белоксодержащие продукты. 7 Напротив, у пациентов, получавших Ксеомин, не содержащий комплексообразующих белков, образование антител не наблюдалось. Еще одним важным фактором, определяющим потенциальную иммуногенность композиций ботулотоксина/А и последующую неэффективность лечения, является количество присутствующего белка нейротоксина. 5 , 15 Это связано с повышенным уровнем антигена и, следовательно, повышенным риском образования антител. 16 У пациентов с цервикальной дистонией, получавших препараты ботулинического токсина, было продемонстрировано, что удельная эффективность (Ед на пг нейротоксина) коррелирует с неэффективностью терапии, вызванной антителами. 17 Таким образом, врачам будет полезно получить информацию о специфической эффективности различных препаратов ботулинического токсина.
Действительно, сообщалось об образовании антител у пациентов, получавших в эстетической медицине комплексообразующие белоксодержащие продукты. 7 Напротив, у пациентов, получавших Ксеомин, не содержащий комплексообразующих белков, образование антител не наблюдалось. Еще одним важным фактором, определяющим потенциальную иммуногенность композиций ботулотоксина/А и последующую неэффективность лечения, является количество присутствующего белка нейротоксина. 5 , 15 Это связано с повышенным уровнем антигена и, следовательно, повышенным риском образования антител. 16 У пациентов с цервикальной дистонией, получавших препараты ботулинического токсина, было продемонстрировано, что удельная эффективность (Ед на пг нейротоксина) коррелирует с неэффективностью терапии, вызванной антителами. 17 Таким образом, врачам будет полезно получить информацию о специфической эффективности различных препаратов ботулинического токсина.
В настоящее время препараты ботулотоксина/А, одобренные для применения по нескольким показаниям у взрослых в Азии, Европе и США, включают онаботулотоксин А (Allergan Inc. , Ирвин, Калифорния, США; также известный как Ботокс ® или Vistabel ® ), абоботулотоксин А (Ipsen Ltd, Слау, Великобритания/Галдерма, Париж, Франция; также известен как Dysport ® или Azzalure ® ) и инкоботулотоксин A (Merz Pharmaceuticals GmbH, Рейнхайм, Германия; также известен как Xeomin или Bocouture ® ), каждый из которых уникален.Эти различные процессы производства, рецептуры и тестирования позволили получить препараты с различной активностью, дозировкой, составом и иммуногенностью. 18 , 19
, Ирвин, Калифорния, США; также известный как Ботокс ® или Vistabel ® ), абоботулотоксин А (Ipsen Ltd, Слау, Великобритания/Галдерма, Париж, Франция; также известен как Dysport ® или Azzalure ® ) и инкоботулотоксин A (Merz Pharmaceuticals GmbH, Рейнхайм, Германия; также известен как Xeomin или Bocouture ® ), каждый из которых уникален.Эти различные процессы производства, рецептуры и тестирования позволили получить препараты с различной активностью, дозировкой, составом и иммуногенностью. 18 , 19
Поскольку в процессе производства Ксеомина выделяется только активный нейротоксин с молекулярной массой 150 кДа, Ксеомин полностью свободен от комплексообразующего белка. 20 Помимо активного нейротоксина с молекулярной массой 150 кДа, Ботокс и Диспорт содержат белки-комплексообразователи, образующие высокомолекулярный комплекс с нейротоксином с молекулярной массой 150 кДа.То есть Ботокс включает одну молекулу нейротоксина массой 150 кДа в белковом комплексе массой 900 кДа. 21 Хотя точный биохимический состав Диспорта остается неустановленным, он, вероятно, также содержит белок L-комплекса массой 500–600 кДа в комплексе белка массой 900 кДа. 22 Xeomin/Bocouture остается единственным продуктом BoNT/A, продаваемым как содержащий «очищенный нейротоксин», который был зарегистрирован регулирующими органами в США и Европе.
21 Хотя точный биохимический состав Диспорта остается неустановленным, он, вероятно, также содержит белок L-комплекса массой 500–600 кДа в комплексе белка массой 900 кДа. 22 Xeomin/Bocouture остается единственным продуктом BoNT/A, продаваемым как содержащий «очищенный нейротоксин», который был зарегистрирован регулирующими органами в США и Европе.
Как сообщалось, Ботокс содержит 5000 пг токсина на 100 ЕД флакона 23 (включая комплексообразующие белки), Диспорт содержит 4350 пг токсина (включая комплексообразующие белки) на 500 ЕД флакона, 24 и Ксеомин содержит 440 пг нейротоксина на 100 ед. флакона. 8 Здесь средняя концентрация нейротоксина BoNT/A составила 730 пг во флаконе 100 ЕД Ботокса (серии C2344C3, C2384C3, C2419 и C2385), 650 пг во флаконе 100 ЕД Диспорта (серии 678F и 689X). и 440 пг во флаконах по 100 ед. Ксеомина (партии 61 111, 70 604 и 81 208). 8 Удельная активность, определяемая как активность в единицах, связанная с определенным количеством токсина с молекулярной массой 150 кДа в каждом продукте, составляла 0,137 ЕД/пг для Ботокса, 0,154 ЕД/пг для Диспорта и 0,227 ЕД/пг для Ксеомина, 8 , что свидетельствует о том, что Ксеомин был наиболее сильнодействующим, потому что он содержит наибольшее количество токсинного белка среди протестированных.
При сравнении различных продуктов Ботулакс и Набота продемонстрировали одинаковую удельную активность с 0,118 и 0,133 ЕД/пг соответственно. Meditoxin и Relatox содержат меньше белка нейротоксина, чем Botulax и Nabota, но более высокую удельную активность (0,174 и 0,173 ЕД/пг). Однако их удельная активность ниже, чем у Ксеомина (0,240 ЕД/пг). Можно сделать вывод, что более низкая удельная активность ботулакса, набота, медитоксина и релатокса может фактически свидетельствовать о наличии значительных количеств неактивного, а не активного нейротоксина.Таким образом, высокие уровни белка нейротоксина, обнаруженные в этом исследовании, были связаны не с биологически эффективным нейротоксином, а с неактивным токсином при условии, что все продукты были равноэффективны при содержании 100 ЕД на флакон. Этот неактивный нейротоксин не может поглощаться нейронами, но может представлять собой иммуногенную примесь. 17 Эти неактивные компоненты, которые сами по себе не обладают клинической эффективностью, могут стимулировать выработку антител. 11 Они могут снижать эффективность нейротоксина, вызывая иммунные реакции у пациентов, которым затем необходимо получать более высокие дозы на более поздних сеансах, что в конечном итоге увеличивает риск невосприимчивости.
11 Они могут снижать эффективность нейротоксина, вызывая иммунные реакции у пациентов, которым затем необходимо получать более высокие дозы на более поздних сеансах, что в конечном итоге увеличивает риск невосприимчивости.
Заключение
В этом исследовании четыре препарата BoNT/A, используемые в Азии, показали более низкую чистоту нейротоксина и удельную эффективность, но более высокие концентрации белка нейротоксина, чем Xeomin. Хотя Ботулакс и Набота содержали больше нейротоксина, чем Ксеомин в эквивалентном объеме, они содержали большее количество неактивного нейротоксина. Кроме того, хотя Медитоксин и Релатокс содержали немного больше нейротоксина, чем Ксеомин, оба препарата содержали большее количество неактивного нейротоксина. В будущем необходимо будет провести сравнительное исследование эффективности, продолжительности действия и профиля безопасности всех продуктов нейротоксинов, в частности частоты вторичных неудач лечения из-за образования антител у пациентов, подвергающихся длительному лечению ботулотоксинами. А.
А.
Сноски
Вклад авторов
Все авторы внесли свой вклад в анализ данных, подготовку и редактирование документа и соглашаются нести ответственность за все аспекты работы.
Раскрытие информации
JF и OS являются сотрудниками Merz Pharmaceuticals. Авторы сообщают об отсутствии других конфликтов интересов в этой работе.
Ссылки
1. Baker MP, Reynolds HM, Lumicisi B, Bryson CJ. Иммуногенность белковой терапии: основные причины, последствия и проблемы.Сам Не Я. 2010;1(4):314–322. [Бесплатная статья PMC] [PubMed] [Google Scholar]2. Джоши С.Г., Элиас М., Сингх А. и др. Модуляция вызванных ботулиническим токсином изменений нервно-мышечной функции антителами, направленными против рекомбинантных полипептидов или их фрагментов. Неврология. 2011; 179: 208–222. [PubMed] [Google Scholar]3. Pless DD, Torres ER, Reinke EK, Bavari S. Высокоаффинные защитные антитела к домену связывания ботулинического нейротоксина типа A. Infect Immun. 2001;69(1):570–574. [Бесплатная статья PMC] [PubMed] [Google Scholar]4.Янкович Дж., Шварц К. Реакция и иммунорезистентность на инъекции ботулинического токсина. Неврология. 1995; 45: 1743–1746. [PubMed] [Google Scholar]5. Торрес С., Гамильтон М., Санчес Э., Староватова П., Губанова Е., Решетникова Т. Нейтрализующие антитела к ботулиническому нейротоксину типа А в эстетической медицине: пять историй болезни. Clin Cosmet Investig Dermatol. 2014;7:11–17. [Бесплатная статья PMC] [PubMed] [Google Scholar]7. DasGupta BR, Sathyamoorthy V. Очистка и аминокислотный состав ботулинического нейротоксина типа А.Токсикон. 1984; 22: 415–424. [PubMed] [Google Scholar]8. Frevert J. Содержание ботулинического нейротоксина в препаратах Ботокс ® /Vistabel ® , Диспорт ® /Azzalure ® и Ксеомин ® /Bocouture ® (60 D ® ): –73. [Бесплатная статья PMC] [PubMed] [Google Scholar]10. Ян ГХ, Юнг ХХ. Новый ботулинический токсин, потенциально биоэквивалентный онаботулотоксину А: есть ли вообще отличия? Дерматол Хирург.
Infect Immun. 2001;69(1):570–574. [Бесплатная статья PMC] [PubMed] [Google Scholar]4.Янкович Дж., Шварц К. Реакция и иммунорезистентность на инъекции ботулинического токсина. Неврология. 1995; 45: 1743–1746. [PubMed] [Google Scholar]5. Торрес С., Гамильтон М., Санчес Э., Староватова П., Губанова Е., Решетникова Т. Нейтрализующие антитела к ботулиническому нейротоксину типа А в эстетической медицине: пять историй болезни. Clin Cosmet Investig Dermatol. 2014;7:11–17. [Бесплатная статья PMC] [PubMed] [Google Scholar]7. DasGupta BR, Sathyamoorthy V. Очистка и аминокислотный состав ботулинического нейротоксина типа А.Токсикон. 1984; 22: 415–424. [PubMed] [Google Scholar]8. Frevert J. Содержание ботулинического нейротоксина в препаратах Ботокс ® /Vistabel ® , Диспорт ® /Azzalure ® и Ксеомин ® /Bocouture ® (60 D ® ): –73. [Бесплатная статья PMC] [PubMed] [Google Scholar]10. Ян ГХ, Юнг ХХ. Новый ботулинический токсин, потенциально биоэквивалентный онаботулотоксину А: есть ли вообще отличия? Дерматол Хирург. 2013; 39: 165–170. [PubMed] [Google Scholar] 11.Лам СМ. Фундаментальная наука о ботулиническом токсине. Пластмасса для лица Surg Clin N Am. 2003; 11: 431–438. [PubMed] [Google Scholar] 12. Хугель Фарма. Брошюра о ботулиническом токсине типа А Ботулакс. Корея: 2014. 6 ноября, н.п. [Google Академия] 13. Шарон Н., Лис Х. История лектинов: от гемагглютининов до молекул биологического распознавания. Гликобиология. 2004; 14:53р–62р. [PubMed] [Google Scholar] 14. Ван Л., Сунь Ю., Ян В. и др. Белки комплекса ботулинического нейротоксина типа А по-разному модулируют реакцию нейронов хозяина.Токсикон. 2014;82:52–60. [PubMed] [Google Scholar] 15. Стенгель Г., Би Э. Вторичная неудача лечения, вызванная антителами, у пациента, получавшего ботулинический токсин типа А от межбровных морщин. Clin Interv Старение. 2011;6:281–284. [Бесплатная статья PMC] [PubMed] [Google Scholar]17. Дресслер Д. IncobotulinumtoxinA (Xeomin ® ) В: Stacy MA, редактор. Справочник по дистонии. Нью-Йорк (Нью-Йорк): Informa Healthcare; 2012. С. 469–476. [Google Академия] 18. Dessy LA, Fallico N, Mazzocchi M, Scuderi N. Ботулинический токсин для межбровных морщин: обзор эффективности и безопасности доступных в настоящее время продуктов.Am J Clin Дерматол. 2011;12:377–388. [PubMed] [Google Scholar] 19. Брин М.Ф., Джеймс С., Мальтман Дж. Продукты ботулинического токсина типа А не являются взаимозаменяемыми: обзор доказательств. Биопрепараты. 2014; 8: 227–241. [Бесплатная статья PMC] [PubMed] [Google Scholar]20. Хименес-Шахед Дж. Новое лечение фокальной дистонии: инкоботулотоксин А (Ксеомин ® ), ботулинический нейротоксин типа А, свободный от комплексообразующих белков. Нейропсихиатр Dis Treat. 2012; 8:13–25. [Бесплатная статья PMC] [PubMed] [Google Scholar]21.Шанц Э.Дж., Джонсон Э.А. Свойства и применение ботулотоксина и других микробных нейротоксинов в медицине. Microbiol Rev. 1992;56(1):80–99. [Бесплатная статья PMC] [PubMed] [Google Scholar]22. Hambleton P. Ботулинические токсины Clostridium: общий обзор участия в заболевании, структура, способ действия и подготовка к клиническому применению. Дж Нейрол. 1992;239(1):16–20. [PubMed] [Google Scholar] 24. Панджвани Н., О’Киф Р., Пикетт А. Биохимические, функциональные и силовые характеристики ботулинического токсина типа А при клиническом применении.The Botulinum J. 2008;1(1):153–166. [Google Академия] 25. Сео КК. Innotox ® : «Ботулинический токсин, одобренный BOTOX ® » В: Seo KK, редактор. Ботулинический токсин для азиатов. 1-е изд. Сингапур: Springer Science+Business Media; 2017. с. 19. [Google Scholar]
2013; 39: 165–170. [PubMed] [Google Scholar] 11.Лам СМ. Фундаментальная наука о ботулиническом токсине. Пластмасса для лица Surg Clin N Am. 2003; 11: 431–438. [PubMed] [Google Scholar] 12. Хугель Фарма. Брошюра о ботулиническом токсине типа А Ботулакс. Корея: 2014. 6 ноября, н.п. [Google Академия] 13. Шарон Н., Лис Х. История лектинов: от гемагглютининов до молекул биологического распознавания. Гликобиология. 2004; 14:53р–62р. [PubMed] [Google Scholar] 14. Ван Л., Сунь Ю., Ян В. и др. Белки комплекса ботулинического нейротоксина типа А по-разному модулируют реакцию нейронов хозяина.Токсикон. 2014;82:52–60. [PubMed] [Google Scholar] 15. Стенгель Г., Би Э. Вторичная неудача лечения, вызванная антителами, у пациента, получавшего ботулинический токсин типа А от межбровных морщин. Clin Interv Старение. 2011;6:281–284. [Бесплатная статья PMC] [PubMed] [Google Scholar]17. Дресслер Д. IncobotulinumtoxinA (Xeomin ® ) В: Stacy MA, редактор. Справочник по дистонии. Нью-Йорк (Нью-Йорк): Informa Healthcare; 2012. С. 469–476. [Google Академия] 18. Dessy LA, Fallico N, Mazzocchi M, Scuderi N. Ботулинический токсин для межбровных морщин: обзор эффективности и безопасности доступных в настоящее время продуктов.Am J Clin Дерматол. 2011;12:377–388. [PubMed] [Google Scholar] 19. Брин М.Ф., Джеймс С., Мальтман Дж. Продукты ботулинического токсина типа А не являются взаимозаменяемыми: обзор доказательств. Биопрепараты. 2014; 8: 227–241. [Бесплатная статья PMC] [PubMed] [Google Scholar]20. Хименес-Шахед Дж. Новое лечение фокальной дистонии: инкоботулотоксин А (Ксеомин ® ), ботулинический нейротоксин типа А, свободный от комплексообразующих белков. Нейропсихиатр Dis Treat. 2012; 8:13–25. [Бесплатная статья PMC] [PubMed] [Google Scholar]21.Шанц Э.Дж., Джонсон Э.А. Свойства и применение ботулотоксина и других микробных нейротоксинов в медицине. Microbiol Rev. 1992;56(1):80–99. [Бесплатная статья PMC] [PubMed] [Google Scholar]22. Hambleton P. Ботулинические токсины Clostridium: общий обзор участия в заболевании, структура, способ действия и подготовка к клиническому применению. Дж Нейрол. 1992;239(1):16–20. [PubMed] [Google Scholar] 24. Панджвани Н., О’Киф Р., Пикетт А. Биохимические, функциональные и силовые характеристики ботулинического токсина типа А при клиническом применении.The Botulinum J. 2008;1(1):153–166. [Google Академия] 25. Сео КК. Innotox ® : «Ботулинический токсин, одобренный BOTOX ® » В: Seo KK, редактор. Ботулинический токсин для азиатов. 1-е изд. Сингапур: Springer Science+Business Media; 2017. с. 19. [Google Scholar]Как закапывать глазные капли
Существует много видов глазных капель, и попадание любого из них в глаза может быть проблемой. Но с несколькими советами и некоторой практикой вы освоитесь в этом процессе.Чем более знакомым и уверенным вы будете, тем легче будет закапывать глазные капли, не пропуская, не проливая и не используя слишком много.
Шаг 1: прочтите инструкции своего врача
Время и дозировка ваших глазных капель могут иметь большое значение в вашем лечении. Используете ли вы капли от глаукомы, сухости глаз, инфекции или аллергии, вы должны использовать капли правильно, чтобы получить максимальную пользу. Если у вас возникли проблемы с приемом капель или их использованием по правильному графику, поговорите со своим офтальмологом о возможных вариантах.
- Используйте капли именно тогда и так, как вам скажет врач.
- Если вам нужно принять более одного типа глазных капель одновременно, подождите от 3 до 5 минут между различными видами лекарств.
- Спросите своего офтальмолога или фармацевта, можно ли хранить капли в холодильнике. Когда капли холодные, может быть легче почувствовать каплю при попадании в глаз, чтобы вы могли сказать, куда она попала.
Шаг 2: Подготовьтесь
- Всегда мойте руки перед тем, как прикасаться к глазным каплям или прикасаться к глазам.
- Если вы носите контактные линзы, снимите их, если только ваш офтальмолог не сказал вам не снимать их.
- Энергично встряхните капли перед использованием.
- Снимите колпачок с глазных капель, но не прикасайтесь к кончику капельницы . Если вы это сделаете, пипетка может забрать бактерии с ваших пальцев и загрязнить флакон с лекарством.
Шаг 3: закапайте капли в глаза
- Слегка наклоните голову назад и посмотрите вверх.Некоторые люди считают полезным сосредоточиться на определенной точке на потолке. Может быть полезно прикрепить фотографию или вырезку из журнала к потолку, чтобы ваши глаза могли сфокусироваться на них.
- Одной рукой оттяните нижнее веко вниз от глаза. Это формирует карман для ловли капли.
- Держите наконечник пипетки прямо над карманом для век.
- Не прикасайтесь флаконом к глазу или веку. Это может привести к размножению бактерий или других загрязнителей в ваших глазных каплях.
- Аккуратно сожмите флакон и дайте глазной капле упасть в карман.
Если вам не терпится закапать глазные капли
Дети и люди с сильной реакцией на что-либо вблизи глаз могут с трудом держать глаза открытыми. Если это так, попробуйте этот метод:
- Откиньте голову назад, насколько это удобно, или лягте на кровать или кушетку.
- Держите глаза закрытыми.
- Держите флакон с глазными каплями большим и двумя первыми пальцами.
- Положите два других пальца руки на нос для устойчивости.
- Не касаясь флаконом века, закапайте глазную каплю в уголок глаза возле носа.
- Пока ваша голова все еще запрокинута, откройте глаза и несколько раз поморгайте, пока капля не скатится в глаз.
Если проблема не устранена
- Если возможно, попросите члена семьи, соседа или друга помочь вам ввести капли альтернативным методом, описанным выше.
- Спросите своего врача о вспомогательных устройствах для глазных капель. Эти устройства могут помочь вам направить каплю, сжать бутылку и держать глаза открытыми.
Шаг 4: Закройте глаза и не моргайте!
- Осторожно надавите на слезные протоки в месте соединения век с носом. Держите слезные протоки закрытыми в течение минуты или двух или столько, сколько рекомендует ваш офтальмолог, прежде чем открывать глаза. Это даст капле время, чтобы она впиталась в глаза, а не попала в нос.
- Если какие-либо капли вытекли, вытрите их салфеткой с закрытых век.
- При необходимости повторите шаги 3 и 4 для другого глаза.
Шаг 5: Мойте руки
Важно мыть руки водой с мылом после контакта с лекарствами и прикосновения к лицу.
| Руководство по отчетности предусмотрено? (т.е. именно то, что утверждают авторы в статье) | Для полноты, прозрачности и анализа данных в отчетах о случаях болезни и данных с места оказания медицинской помощи.
Контрольный список CARE (PDF)
|
| Полная библиографическая ссылка | Ганье Дж.Дж., Кинле Г., Альтман Д.Г., Мохер Д., Сокс Х., Райли Д.; Группа ЗАБОТА. Руководство CARE: Разработка руководства по отчетности о клинических случаях на основе консенсуса. Это руководство было опубликовано одновременно в 7 журналах.Вы можете прочитать руководство в любом из этих журналов, используя приведенные ниже ссылки. BMJ Case Rep. 2013; doi: 10.1136/bcr-2013-201554 PMID: 24155002
|
| Язык | Английский |
| Релевантные URL-адреса (полный текст, если доступен) | Контрольный список CARE доступен для загрузки на английском языке в виде файла PDF.
|
| Пояснения и доработки | Райли Д.С., Барбер М.С., Кинле Г.С., Аронсон Дж.К., фон Шен-Ангерер Т., Тагвелл П., Киен Х., Хелфанд М., Альтман Д.Г., Сокс Х., Вертманн П.Г., Мохер Д., Рисон Р.А., Шамсир Л., Кох К.А., Сун GH, Hanaway P, Sudak NL, Kaszkin-Bettag M, Carpenter JE, Gagnier JJ.Руководящие принципы CARE для отчетов о случаях заболевания: документ с пояснениями и уточнениями. Дж. Клин Эпидемиол. 2017. pii: S0895-4356(17)30037-9. PMID: 28529185 |
| Доступность на дополнительных языках | Бесплатный контрольный список CARE и план написания отчета о клиническом случае для авторов переведены на различные языки и доступны по адресу: https://swihm.com/resources/ Руководство CARE переведено на итальянский язык: CARE Italian (PDF)
|
| Соответствующие более общие/специализированные инструкции по отчетности (т.е. основное общее руководство или дополнение к общему правилу) | Специализированный Терапевтический массаж и работа с телом : Munk N, Boulanger K. Адаптация рекомендаций CARE для публикаций по терапевтическому массажу и работе с телом: усилия по улучшению воздействия отчетов о случаях заболевания. Int J Ther Массаж тела. 2014;7(3):32-40. PMID: 25184013
|
| URL веб-сайта руководства по отчетности | http://www.care-statement.орг/ |
| Аббревиатура руководства по отчетности | УХОД |
| Дизайн исследования | Наблюдательные исследования |
| Относится ко всему отчету или к отдельным разделам отчета? | Весь отчет |
| Дополнительная информация | Руководящая группа CARE разработала блок-схему того, как клиницист должен рассмотреть подход к сбору данных при осмотре пациента или при просмотре карты, чтобы ее можно было систематически собирать и записывать в соответствии с рекомендациями CARE.Блок-схема доступна для загрузки: Блок-схема CARE (PDF) Статьи CARE 2013 и 2017, а также другие бесплатные публикации доступны для загрузки по адресу https://www.care-statement.org/publications .Дополнительная бесплатная онлайн-информация, включая примеры временных шкал и инструкции по созданию временных шкал, доступна по адресу https://swihm.com/resources
| .
| Последнее обновление записи | 13 января 2022 г. |
Микроволновая печь Радиация | FDA
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) регулирует производство микроволновых печей с 1971 года.Производители микроволновых печей обязаны сертифицировать свою продукцию и соответствовать стандартам безопасности, установленным и введенным в действие FDA для защиты здоровья населения. Основываясь на современных знаниях о микроволновом излучении, Агентство считает, что печи, соответствующие стандарту FDA и используемые в соответствии с инструкциями производителя, безопасны для использования.
Что такое микроволновое излучение?
Микроволны представляют собой форму «электромагнитного» излучения; то есть это волны электрической и магнитной энергии, движущиеся вместе в пространстве.Электромагнитное излучение охватывает широкий спектр от очень длинных радиоволн до очень коротких гамма-лучей. Человеческий глаз может обнаружить только небольшую часть этого спектра, называемого видимым светом. Радио обнаруживает другую часть спектра, а рентгеновский аппарат использует еще одну часть.
Видимый свет, микроволны и радиочастотное (РЧ) излучение являются формами неионизирующего излучения. У неионизирующего излучения недостаточно энергии, чтобы выбить электроны из атомов. Рентгеновские лучи являются формой ионизирующего излучения.Воздействие ионизирующего излучения может изменить атомы и молекулы и вызвать повреждение клеток в органическом веществе.
Микроволны используются для обнаружения движущихся автомобилей, а также для передачи телефонных и телевизионных сообщений. Промышленность использует микроволны для сушки и отверждения фанеры, отверждения резины и смол, для выращивания хлеба и пончиков, а также для приготовления картофельных чипсов. Но чаще всего микроволновая энергия используется потребителями в микроволновых печах. Микроволны имеют три характеристики, позволяющие использовать их в кулинарии: они отражаются металлом; они проходят через стекло, бумагу, пластик и подобные материалы; и они усваиваются пищей.
Приготовление пищи в микроволновой печи
Микроволны производятся внутри духовки с помощью электронной трубки, называемой магнетроном. Микроволны отражаются внутри металлической внутренней части духовки, где они поглощаются пищей. Микроволны заставляют молекулы воды в пище колебаться, выделяя тепло, которое готовит пищу. Вот почему продукты с высоким содержанием воды, такие как свежие овощи, можно приготовить быстрее, чем другие продукты. Энергия микроволн превращается в тепло по мере того, как она поглощается пищей, и не делает пищу «радиоактивной» или «загрязненной».»
Хотя тепло вырабатывается непосредственно в пище, микроволновые печи не готовят пищу «изнутри наружу». Когда толстые продукты готовятся, внешние слои нагреваются и готовятся в основном за счет микроволн, в то время как внутренняя часть готовится в основном за счет теплопроводности от горячих внешних слоев.
Приготовление в микроволновой печи может быть более энергоэффективным, чем обычное приготовление пищи, потому что продукты готовятся быстрее, а энергия нагревает только продукты, а не всю камеру духового шкафа. Приготовление в микроволновой печи снижает питательную ценность продуктов не больше, чем при обычном приготовлении.На самом деле, продукты, приготовленные в микроволновой печи, могут сохранить больше витаминов и минералов, потому что микроволновые печи могут готовить быстрее и без добавления воды.
Стеклянные, бумажные, керамические или пластиковые контейнеры используются для приготовления пищи в микроволновой печи, поскольку микроволны проходят через эти материалы. Хотя такие контейнеры нельзя нагревать микроволнами, они могут нагреваться от тепла пищи, готовящейся внутри. Некоторые пластиковые контейнеры нельзя использовать в микроволновой печи, поскольку они могут расплавиться от тепла пищи внутри.Как правило, металлические кастрюли или алюминиевую фольгу также нельзя использовать в микроволновой печи, так как микроволны отражаются от этих материалов, что приводит к неравномерному приготовлению пищи и может привести к повреждению печи. В инструкциях, прилагаемых к каждой микроволновой печи, указаны типы используемых контейнеров. Они также рассказывают, как проверять контейнеры, чтобы определить, можно ли их использовать в микроволновых печах.
Предотвращение травм от перегретой воды в микроволновых печах
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) в прошлом получало сообщения о серьезных ожогах кожи или обвариваниях рук и лиц людей в результате выплескивания горячей воды из чашки после ее перегрева в микроволновой печи.Перегретая вода (вода, нагретая выше температуры кипения) не кажется кипящей и возникает, когда вода нагревается сама по себе в чистой чашке. Если произошел перегрев, небольшое возмущение или движение, например, поднятие чашки или наливание полной ложки растворимого кофе, может привести к сильному извержению кипятка, вырывающемуся из чашки. Добавление таких веществ, как растворимый кофе или сахар , перед нагреванием значительно снижает этот риск.
Пользователи должны строго соблюдать меры предосторожности и рекомендации, содержащиеся в руководствах по эксплуатации микроволновых печей, особенно в отношении времени нагрева.Пользователи должны следить за тем, чтобы они не превышали рекомендуемое время нагрева при определении оптимальных настроек времени для нагрева воды до желаемой температуры.
Стандарт безопасности для микроволновой печи
Через свой Центр устройств и радиологического здоровья (CDRH) FDA устанавливает и обеспечивает соблюдение стандартов производительности электронных продуктов, чтобы гарантировать, что излучение не представляет опасности для здоровья населения.
Федеральный стандарт (21 CFR 1030.10) ограничивает количество микроволн, которые могут выходить из духовки в течение всего срока ее службы, до 5 милливатт (мВт) микроволнового излучения на квадратный сантиметр на расстоянии примерно 2 дюйма от поверхности духовки. Этот предел намного ниже уровня, который, как известно, вредит людям. Энергия микроволн также резко уменьшается по мере удаления от источника излучения. Измерение, сделанное на расстоянии 20 дюймов от духовки, будет составлять примерно 1/100 значения, измеренного на расстоянии 2 дюймов от духовки.
Стандарт также требует, чтобы все духовки имели две независимые системы блокировки, которые останавливают производство микроволн в тот момент, когда защелка освобождается или открывается дверца.Кроме того, система контроля останавливает работу печи в случае выхода из строя одной или обеих систем блокировки.
Все печи должны иметь этикетку, указывающую, что они соответствуют стандарту безопасности. Кроме того, FDA требует, чтобы все печи имели этикетку с разъяснением мер предосторожности при использовании. Это требование может быть снято, если изготовитель доказал, что печь не превысит допустимый предел утечки, даже если она будет использоваться в условиях, предостерегаемых на этикетке.
Чтобы убедиться в соблюдении стандарта, FDA тестирует микроволновые печи в собственной лаборатории.FDA также оценивает программы производителей радиационных испытаний и контроля качества на их заводах.
Микроволновые печи и здоровье
Микроволновое излучение может нагревать ткани тела так же, как оно нагревает пищу. Воздействие высоких уровней микроволн может вызвать болезненный ожог. Две области тела, глаза и яички, особенно уязвимы для РЧ-нагрева, потому что в них относительно небольшой кровоток для отвода избыточного тепла. Кроме того, хрусталик глаза особенно чувствителен к сильному нагреву, а воздействие высоких уровней микроволн может вызвать катаракту.Но такие виды травм — ожоги и катаракта — могут быть вызваны только воздействием большого количества микроволнового излучения.
Потребители должны принимать разумные меры предосторожности при обращении с горячими продуктами и напитками. Дополнительные рекомендации по безопасности см. в разделе этой страницы под названием «Советы по безопасной эксплуатации микроволновой печи».
Были ли радиационные поражения в результате использования микроволновых печей?
Большинство травм, связанных с микроволновыми печами, являются результатом тепловых ожогов от горячих контейнеров, перегретых продуктов или взрывающихся жидкостей.Большинство травм не связаны с радиацией. Тем не менее, были очень редкие случаи радиационного поражения из-за необычных обстоятельств или неправильного обслуживания. Как правило, радиационные поражения микроволновой печи вызываются воздействием большого количества микроволнового излучения, просачивающегося через отверстия, такие как зазоры в уплотнителях микроволновой печи. Однако правила FDA требуют, чтобы микроволновые печи были спроектированы таким образом, чтобы предотвращать эти утечки радиации высокого уровня.
Микроволновые печи и кардиостимуляторы
Одно время высказывались опасения, что утечка излучения из микроволновых печей может мешать работе некоторых электронных кардиостимуляторов.Аналогичные опасения высказывались по поводу помех кардиостимуляторам от электробритв, систем автоматического зажигания и других электронных продуктов. Хотя Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) специально не требует, чтобы микроволновые печи содержали предупреждения для людей с кардиостимуляторами, эта проблема в значительной степени решена, поскольку современные кардиостимуляторы предназначены для защиты от таких электрических помех. Тем не менее, пациентам с кардиостимуляторами рекомендуется проконсультироваться со своими врачами, если у них есть проблемы.
Проверка печей на утечки и другие проблемы радиационной безопасности
Мало причин для беспокойства по поводу чрезмерной утечки микроволн из духовок, если дверные петли, защелки или уплотнители не повреждены.Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) рекомендует внимательно осмотреть вашу духовку и не использовать ее, если дверца неплотно закрывается, согнута, деформирована или иным образом повреждена.
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) также контролирует приборы на предмет радиационной безопасности и получило отчеты о микроволновых печах, которые остаются включенными и работают, пока дверца открыта. При работе по назначению микроволновые печи имеют функции безопасности, предотвращающие дальнейшее генерирование микроволн, если дверца открыта. Однако, если духовка продолжает работать с открытой дверцей, потребители не могут быть на 100 % уверены, что микроволновое излучение не испускается.Таким образом, если это произойдет, FDA рекомендует немедленно прекратить использование печи.
Как сообщить о проблемах радиационной безопасности микроволновой печи
Если вы подозреваете, что микроволновая печь имеет проблемы с радиационной безопасностью, вы можете обратиться к ее производителю. Производители, которые обнаружат, что какие-либо микроволновые печи, произведенные, собранные или импортированные ими, имеют дефект или не соответствуют применимому федеральному стандарту, должны немедленно уведомить об этом FDA.Кроме того, производители/импортеры обязаны сообщать FDA обо всех случаях аварийного излучения, если только инцидент не связан с дефектом или несоответствием, о котором сообщалось ранее (21 CFR 1002.20).
Вы также можете сообщить в FDA о любых предполагаемых проблемах или травмах, связанных с радиацией, заполнив и отправив по почте форму Отчета о случайном радиационном происшествии.
Советы по безопасной эксплуатации микроволновой печи
- Следуйте инструкциям производителя по рекомендуемым процедурам эксплуатации и мерам предосторожности для вашей модели печи. №
- Используйте безопасную для использования в микроволновой печи посуду, специально изготовленную для использования в микроволновой печи.
- Не используйте микроволновую печь, если дверца неплотно закрывается, согнута, деформирована или имеет другие повреждения.
- Прекратите использование микроволновой печи, если она продолжает работать при открытой дверце.
- В качестве дополнительной меры предосторожности не стойте прямо напротив печи (и не позволяйте делать это детям) в течение длительного времени во время ее работы.
- Не нагревайте воду или жидкости в микроволновой печи дольше, чем это рекомендовано в инструкциях производителя.
- Некоторые духовки не должны работать, когда они пусты. Обратитесь к инструкции по эксплуатации вашей духовки.
- Регулярно очищайте камеру духового шкафа, внешний край камеры и дверцу водой с мягким моющим средством. Специальное чистящее средство для микроволновой печи не требуется. Убедитесь, что , а не , используют губки для мытья посуды, стальную мочалку или другие абразивы.
Для получения дополнительной информации для потребителей об излучении микроволновых печей свяжитесь с персоналом отдела образования потребителей и промышленности (DICE) по электронной почте [email protected].
Дополнительная информация от отдела информации о здоровье потребителей FDA
Отношения Ангустии | СЕЛБСТ
Компакт-диск Relatos de Angustia
Компакт-диск (CD) + цифровой альбом
ВАЖНЫЙ ! ! ! Перед заказом ВНИМАТЕЛЬНО ПРОЧИТАЙТЕ:
Доставка осуществляется из Чили, поэтому Я МОГУ ОТПРАВИТЬ ТОЛЬКО ЗАРЕГИСТРИРОВАННЫЕ ПОСЫЛКИ В СЛЕДУЮЩИЕ СТРАНЫ: США, Германию, Австрию, Бельгию, Китай, Испанию, Финляндию, Францию, Грецию, Голландию, Гонконг, Израиль, Италия, Япония, Норвегия, Польша, Португалия, Чехия, Доминиканская Республика, Мексика, Канада, Гватемала, Коста-Рика, Гондурас, Сальвадор, Швейцария, Германия, Дания, Великобритания, Индия, Япония, Корея, Швеция, Сингапур , Тайвань и Южная Африка.
Поставляется в 6-панельном дигипаке.
Компакт-диск из черного поликарбоната
Выпускается Debemur Morti Productions
Компакт-диски могут быть подписаны по запросу
Включает неограниченную потоковую передачу Relatos De Angustia через бесплатное приложение Bandcamp, а также высококачественную загрузку в форматах MP3, FLAC и других форматах.
отправляется в течение 7 дней
Купить компакт-диск 13 долларов
Отправить в подарок
ОбзорWild Tales (Relatos Salvajes) – захватывающий аргентинский чемодан мести | Дикие сказки
Вот фантастически скабрезная коллекция киносказок из темного сердца Аргентины.Повсюду присутствует освежающе высокий стандарт цинизма и ужаса, хотя, вероятно, ничто не может сравниться с тем роскошным завершением первого приключения. Он заканчивается в пригородном саду, где пожилая пара безмятежно читает газеты. Я смотрел этот фильм дважды, и каждый раз концовка этой сцены заставляла всех зрителей, включая меня, подносить кулаки ко рту с тихим травмированным взвизгом.
В своем первоначальном заявлении на прошлогоднем Каннском кинофестивале я использовал аргентинское сленговое слово bronca , означающее «взбешенный».Это настоящие сказки нации bronca , и экран пульсирует жаром и дурным характером. Как говорит один персонаж: «Я повсюду вижу насилие». «Дикие сказки» — это гнев на самодовольство и посредственность правящих классов Аргентины. Я также изначально употребил термин «яйцо священника» (в его традиционном, ложном смысле), хотя сборник короткометражных фильмов, скорее всего, будет смешанным пакетом не более, чем обычное отдельное повествование, и соотношение успеха/неудачи для этого фильма равно ужасно много выше, чем для большинства других.Оно намного превосходит яйцо викария: это яйцо епископа, яйцо кардинала, хотя нужно сказать, что к финальному расширенному рассказу уровни энергии снижаются. Первоначально установив тон такой изысканной гадости, более поздние намеки на счастье в фильме ослабляют остроту на десятую долю микрометра. Это по-прежнему смертельно острый фильм.
Съемочная группа пересматривает Wild Tales GuardianНекоторые авиапассажиры понимают, что у них общего. Официантка узнает клиента из своего прошлого.Дорожный инцидент обостряется. Инженер чувствует себя обиженным из-за штрафа за парковку. Состоятельный человек покрывает преступление своего сына. Жених и невеста поссорились на свадьбе. В этих захватывающих кошмарах есть что-то от Роальда Даля, Квентина Тарантино или Педро Альмодовара, сопродюсера фильма. Они об одном: о мести. Сценарист и режиссер Дамиан Сифрон допускает тошнотворную иронию. На заставках в начальных титрах изображен ряд диких животных: ястреб, медведь, тигр. Подразумевается, что мы увидим что-то действительно дикое, звериное.И так мы делаем. Но животные не заинтересованы в мести. Этот тип эгоистичной дикости предназначен только для людей.
Моя любимая сцена с самолетом. Растущая тревога среди потрясенных пассажиров действительно одновременно забавна и пугающа, почти невозможная уловка. Но леденящая кровь агрессия между двумя гонщиками тоже очень хороша — как продолжение «Дуэли» Спилберга. Возможно, в «Диких сказках 2» будет рассказ о трех англичанах, которые едут по Аргентине и снимают телепрограмму об автомобилях, хотя, кстати, следует сказать, что Сифрона не интересует поведение неаргентинцев.
Рикардо Дарин — главная звезда фильма: инженер-взрывник, доведенный до предела — или точки детонации — системой штрафов за парковку, цинично спроектированной для получения муниципального дохода. (Лондонским зрителям это понравится.) В кульминационный момент истории, несмотря на мою предыдущую оговорку, лицо Дарина действительно похоже на лицо свирепого дикого зверя.
Мне немного меньше понравилась история о богатом человеке, который должен найти способ уберечь своего избалованного сына от тюрьмы, после того как мальчик сделал что-то ужасное.Сюжетная линия на самом деле такая же, как в фильме Нури Бильге Джейлана «Три обезьяны» 2008 года, хотя только при втором просмотре я оценил хитрую шутку Сифрона: богатую мать мальчика играет Мария Онетто, которая сыграла главную роль в кавере Лукреции Мартель. драма «Женщина без головы».
Подобно шекспировской комедии, «Дикие сказки» заканчиваются свадьбой: свирепой свадьбой, в которой сексуальные проступки усугубляются классовой ненавистью. Это более длинная история, чем другие, и в моем упрощенном и подлом смысле я предпочел бы, чтобы она закончилась полным оргиастическим смятением, а не более сложной нотой, чем фильм (гениально) находит.Но это великолепная коллекция с мельчайшими деталями: образец наращивания волос, сердито брошенный на пол, дергающиеся руки умирающего человека. Вкусная шоколадная коробка гадости.
Как превратить ваши презентации в истории — мультимедиа
В соответствии с действующими правилами защиты данных ISGlobal информирует вас о следующем:
Когда вас просят предоставить личные данные для предоставления услуг, вы будете проинформированы о том, какие данные вы должны предоставить.
Если вы не предоставите эти необходимые данные, мы не сможем предоставить вам услуги. Персональные данные, которые вы предоставляете или которые ISGlobal получает в результате вашего просмотра, запросов или запросов через нашу веб-страницу по адресу www.isglobal.org (« веб-сайт »), будут включены в файл, принадлежащий ISGlobal, для управления, хранения и отслеживание ваших запросов на информацию и/или заключение контрактов на товары или услуги, предлагаемые через веб-сайт. Информация, полученная от вас ISGlobal с веб-сайта, когда вы подписываетесь на рекламное мероприятие или отправляете форму, обрабатывается с максимальной конфиденциальностью, чтобы помочь вам принять участие в рассматриваемом мероприятии или, во втором случае, отправить вам информацию. вы запросили.Полученная информация не используется для каких-либо других целей. Предоставленные персональные данные не будут разглашены или переданы третьим лицам без вашего согласия.
Когда запрашивается заполнение формы, пользователь будет проинформирован о личности и данных контроллера данных и сотрудника по защите данных, целях и правовой основе обработки, получателях данных, а также, где соответствующие, международная передача данных, периоды хранения данных и возможность пользователя осуществлять свои права на доступ, исправление, удаление, переносимость, ограничение и / или противодействие обращению, право жалобы в контролирующий орган и наличие автоматизированных решений.Собранные персональные данные будут обрабатываться и / или передаваться только для явной цели и всегда с согласия пользователя.
Информация отправляется только через форму (формы) веб-сайта после того, как вы выразили свое согласие, выбрав кнопку «ПРИНЯТЬ/ОТПРАВИТЬ» (или аналогичную), с помощью которой ISGlobal получает подтверждение того, что вы дали свое согласие на обработку ваших данных. личные данные.
Во всех случаях вы гарантируете, что предоставленные вами данные являются достоверными, точными, полными и актуальными.ISGlobal может отказать в предоставлении информации или услуг, запрошенных любому пользователю, предоставившем ложные данные, без ущерба для любого другого судебного иска, открытого для него.
В соответствии со статьей 22 Закона Испании 34/2002 от 11 июля об услугах информационного общества и электронной коммерции, ISGlobal может хранить и извлекать «куки» (данные в текстовом файле) с вашего компьютера при условии, что вы предоставили согласия и после того, как мы предоставили вам четкую и полную информацию об использовании этих файлов cookie.Вы можете получить полную информацию о целях установки этих файлов cookie и о том, для чего они используются, в Политике использования файлов cookie ISGlobal.
Это не препятствует любому техническому хранению или доступу с единственной целью осуществления или облегчения передачи сообщения по сети электронной связи или в случае крайней необходимости для предоставления услуги информационного общества, явно запрошенной вами.
Вы можете воспользоваться своими правами на доступ, исправление, удаление, возражение, переносимость и ограничение обработки, отправив запрос сотруднику по защите данных по электронной почте ([email protected]) или почтовый адрес ISGlobal: c/Rosselló, 132, 08036 Barcelona, Spain. Запрос должен включать ваше полное имя, адрес для уведомлений, ксерокопию вашего документа, удостоверяющего личность, или паспорта, а также указание на право, которым вы хотите воспользоваться.
Если вы недовольны обработкой данных ISGlobal или считаете, что ваши права были нарушены, вы можете в любое время подать жалобу в Испанское агентство по защите данных (www.



 Если лекарственный препарат в ампуле, влить во вскрытую ампулу также 2—2,5 мл растворителя.
Если лекарственный препарат в ампуле, влить во вскрытую ампулу также 2—2,5 мл растворителя.